氨法脱硫脱碳富液解析CO2研究
蒋绍坚,彭锐,钟伟,张军, 潘智豪,谭建平, 姚晓莉,赵启成
(中南大学 能源科学与工程学院,湖南 长沙,410083)
摘要:基于氨溶液能同时吸收烟气中CO2和SO2可以降低烟气净化成本,对氨溶液吸收CO2和SO2后的富液CO2进行解析研究,以了解其解析特性。研究结果表明:富液中存在的高浓度硫酸铵对CO2解析有抑制作用,与碳酸氢铵溶液解析率相比降低18%以上;将碳酸氢钠作为添加剂加入溶液中解析时,能够显著提高解析率并且可以抵消硫酸铵的抑制作用;解析气中逸氨含量为9.5%左右,解析化学反应能耗约为30.8 kJ/mol。
关键词:氨法解析;再生能耗;分解热;CO2解析;脱硫脱碳
中图分类号:TK09 文献标志码:A 文章编号:1672-7207(2013)01-0367-05
Regeneration study on rich solution of SO2 and CO2 absorption by ammonia method
JIANG Shaojian, PENG Rui, ZHONG Wei, ZHANG Jun, PAN Zhihao, TAN Jianping, YAO Xiaoli, ZHAO Qicheng
(School of Energy Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Considering that absorbing SO2 and CO2 simultaneously with ammonia solution can reduce the cost of flue gas purification, the decomposition of the rich solution was studied to find out the desorption character. The results show that the high concentration of ammonium sulfate in the rich solution restrains the CO2 desorption. Compared to the desorption rate of ammonium bicarbonate solution, the desorption rate of the high concentration of ammonium sulfate decreases by 18%. Adding sodium bicarbonate to the solution as an additive in the desorption process can significantly improve the desorption rate. The ammonia accounts for about 9.5% in the desorbed gas and the heat of decomposition is about 30.8 kJ/mol.
Key words: ammonia regeneration; heat of regeneration; decomposition heat; CO2 desorption; SO2 and CO2 capture
CO2是大气中最主要的温室气体之一,由于其排放量大,对全球温室效应的影响最大。现有技术捕获工业烟气中CO2的成本较高,目前较为成熟的以乙醇胺(MEA)作为吸收剂的化学吸收方法在捕获燃煤电厂烟气中CO2时将会使电厂发电效率下降10%甚至更多[1]。采用MEA工艺捕捉烟气中CO2时对烟气中SO2以及O2体积分数要求比较严格,这2种气体体积分数过高会使MEA溶剂产生降解损耗,这无疑增加了该工艺的应用难度以及经济成本。而氨溶液做为碱性吸收剂可以吸收SO2,NOx和CO2等所有酸性气体[2-3]。一些实验和研究结果也证明:氨溶液吸收能力比MEA的大,并且再生能耗也比MEA的低[4]。吸收实验证实了氨法脱除CO2的脱除率可以达到90%以上[5-7],因而,Yeh等[8]提出氨溶液吸收工艺有望取代MEA 工艺用于吸收烟气中3种主要酸性气体(SO2,NOx和CO2)以及HCl和HF等,采用一套装置即可同时吸收所有酸性气体的工艺可以大大降低烟气净化成本。以氨溶液吸收烟气中CO2,反应主要产物为NH4HCO3和(NH4)2CO3。并且由于整个吸收反应是可逆的,通过对吸收CO2后的富液进行加热解析,就可以使得氨溶液吸收剂吸收CO2的能力再生,实现吸收剂的循环利用。很多学者对氨溶液解析再生过程进行了实验研究,指出溶液解析能耗较大,CO2解析率不高导致解析不完全,并且溶液再生后吸收CO2能力下降。以质量分数7.5%氨水溶液作为吸收剂为例,富液1次再生后的吸收能力仅为新鲜溶液的18.7%[9]。而对于氨法脱硫脱碳富液的解析研究很少。现有的氨法脱硫工艺采用的循环吸收液中含有高质量分数的硫酸铵,因此,氨法脱硫脱碳富液主要是高质量分数的硫酸铵以及碳酸氢铵组成的混合溶液。受碳酸氢铵溶解度的限制,低浓度无结晶再生氨法脱碳技术应采用浓度为2 mol/L以下氨吸收剂[10]。研究表明:质量分数2%氨吸收剂即可以实现CO2脱除率在90%以上[11],而且高浓度的氨吸收剂容易造成氨损失增加[12]以及吸收产物结晶析出堵塞系统[13]。为此,本文作者解析研究氨法脱硫脱碳富液为高浓度的硫酸铵及浓度在2 mol/L以下碳酸氢铵溶液混合液。通过实验对比研究高浓度硫酸铵对解析液再生的影响以及碳酸氢钠用作添加剂对解析过程的促进作用,并通过实验测定解析过程化学反应能耗,以便为氨法脱硫脱碳技术的进一步研究提供依据。
1 实验
在对富液加热解析的过程中主要发生的反应为式(1),(2)和(3)[8]:
2NH4HCO3(aq)→(NH4)2CO3(aq)+CO2(g)+H2O(l),△H=27.51 kJ/mol (1)
NH4HCO3(aq)→NH3(aq)+CO2(g)+H2O(l),△H=64.87 kJ/mol (2)
(NH4)2CO3(aq)→2NH3(aq)+CO2(g)+H2O(l),△H=102.23 kJ/mol (3)
其中又以反应(1)起主导作用。在加热再生过程中,溶液释放出来的气体主要为CO2,只有少部分NH3和H2O在气液相平衡作用下进入气相,随生成的CO2气体离开溶液[10]。受碳酸氢铵溶解度的限制(见表1),本实验所有解析溶液中碳酸氢铵的浓度均为1 mol/L。
实验系统如图1所示。由于碳酸氢铵溶液在室温下即可分解,为了避免实验误差,实验所用到的溶液都是由分析纯样品与蒸馏水在5 ℃下配制而成。开始试验前,先用CO2气体吹扫整个系统,待系统中充满CO2后,将溶液注入系统中并打开恒温水浴系统以及磁力搅拌器开始试验。在实验中,解析出来的气体先经过装有硫酸钙的干燥管脱去水分后,进入浓硫酸洗气瓶吸收NH3,最后由CO2流量传感器测量解析出来的CO2流量。浓硫酸洗气瓶放置在电子天平上用于测量实验过程中释放出来的NH3的质量。测量中使用的CO2流量传感器量程为0~500 mL/min,电子天平测量精度精确到1 mg。
表1 碳酸氢铵溶解度及饱和浓度[14]
Table 1 Solubility and saturation concentration of ammonium bicarbonate solution
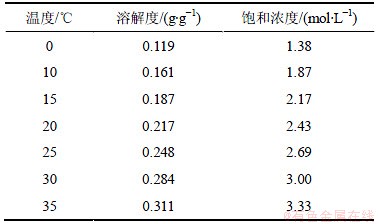
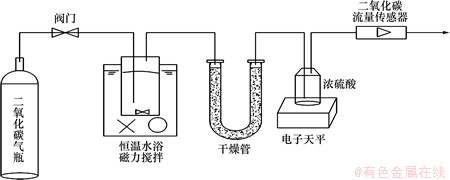
图1 CO2解析实验系统示意图
Fig.1 Diagram of apparatus to measure CO2 desorption
2 结果与讨论
2.1 硫酸铵对溶液解析的影响
实验分别以100 mL 浓度为1 mol/L的碳酸氢铵溶液和1 mol/L碳酸氢铵及4 mol/L硫酸铵组成的混合溶液为解析对象。碳酸氢铵溶液在60 ℃即开始缓慢分解。本实验将恒温水浴温度依次控制在70,80和90 ℃,并分别保持解析时间15 min后测量其CO2解析率。碳酸氢铵溶液和碳酸氢铵及硫酸铵混合溶液随温度变化的解析规律如图2所示,其1 mol/L碳酸氢铵溶液的解析规律与刘芳等[10]的实验结果相似。从图2可以看出:这2种溶液在温度较低时解析率较低,随温度升高,解析率也相应提高。
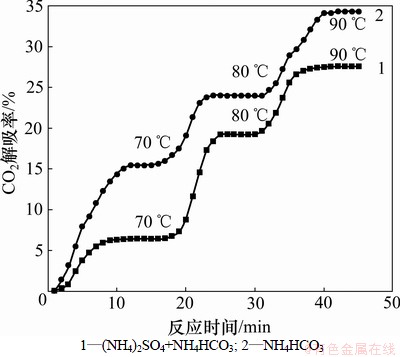
图2 CO2解析率与加热温度的关系
Fig.2 Relationship between CO2 desorption ratio and temperature
对比图2中2条解析曲线可以发现:在70,80和90 ℃时含硫酸铵的混合溶液解析率比纯净的碳酸氢铵溶液分别降低9.0%,4.4%和6.7%,减少率分别为58%,18%和19%。这说明高浓度的硫酸铵溶液对碳酸氢铵溶液解析CO2有抑制作用。氨法脱碳技术自身存在的一个很大问题就在于吸收液再生解析率低,导致溶液循环吸收能力下降,工艺成本升高,实验表明硫酸铵的存在更加凸显了这一问题。而硫酸铵来自于烟气中含有的SO2,说明烟气中SO2的存在将会影响氨法脱碳富液的解析,增加脱碳成本。
2.2 碳酸氢钠对碳酸氢铵溶液解析的影响
实验中发现碳酸氢钠对碳酸氢铵溶液解析有明显促进作用。在吸收液中添加碳酸氢钠并不影响原有溶液吸收CO2的能力,并且碳酸氢钠溶液在加热时几乎不会分解放出CO2,因此,可以认为在整个吸收以及再生过程中碳酸氢钠并不参与反应,总量保持不变。在解析温度为80 ℃时,分别对含碳酸氢钠1.0,0.8,0.6和0.4 mol/L的碳酸氢铵溶液进行解析研究。浓度为1 mol/L的碳酸氢铵溶液中碳酸氢钠浓度对解析率的影响如图3所示。
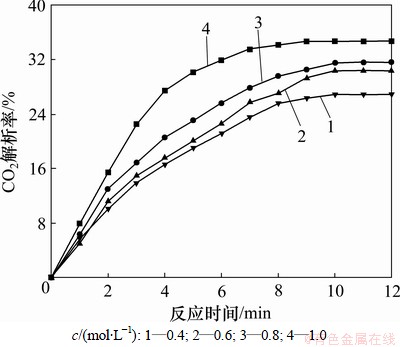
图3 碳酸氢钠对碳酸氢铵溶液解析率的影响
Fig.3 Effect of sodium bicarbonate concentration on desorption ratio of ammonium bicarbonate solution
对比图2和图3可以看出:随着碳酸氢钠浓度的增大,溶液CO2解析率也显著增大;当溶液中碳酸氢钠浓度为1 mol/L时,在80 ℃时的解析率接近于纯净碳酸氢铵溶液90 ℃时的解析率,达到34%;与80 ℃时相比,90 ℃时纯净碳酸氢铵溶液解析率提高率为40%。由化学反应动力学分析可知:以碳酸氢钠作为添加剂增加了HCO3-浓度,有利于促使解析反应正向进行,解析率增加。由此说明以碳酸氢钠作为添加剂在不影响溶液吸收能力的情况下,能够大幅度提高富液CO2的解析率,甚至在温度相对较低的条件下也能获得较高的解析率。降低富液解析CO2温度有利于降低NH3的逸出,同时也能降低解析能耗。
2.3 碳酸氢钠对碳酸氢铵和硫酸铵混合溶液解析的影响
在80 ℃时,分析以浓度为1 mol/L碳酸氢钠作为添加剂对碳酸氢铵和硫酸铵混合溶液CO2解析率的影响,结果如图4所示。从图4可见:由于硫酸铵的存在,碳酸氢铵和硫酸铵混合溶液的解析率只有15%左右,低于纯净碳酸氢铵溶液的23%;含碳酸氢钠的混合溶液解析率为28%,与纯净碳酸氢铵溶液相比解析率提高了24%,与碳酸氢铵和硫酸铵混合溶液相比解析率提高了67%。这说明碳酸氢钠的存在不但可以抵消硫酸铵带来的对解析过程的抑制作用,而且可以增加解析率。
碳酸氢钠的加入增加了HCO3-的浓度,而硫酸铵的加入则增加了NH4+的浓度,这样,就相当于增加了溶液中碳酸氢铵的整体浓度,促使解析反应式(1)和(2)的化学平衡向右移动,促进溶液的解析作用,增加溶液CO2的解析率。由于烟气中存在SO2,SO2被吸收后转化为硫酸铵,存在于溶液中,将会抑制脱碳富液CO2的解析。研究表明:在溶液中添加碳酸氢钠不仅可以消除硫酸铵带来的抑制作用,同时可以促进CO2的解析。
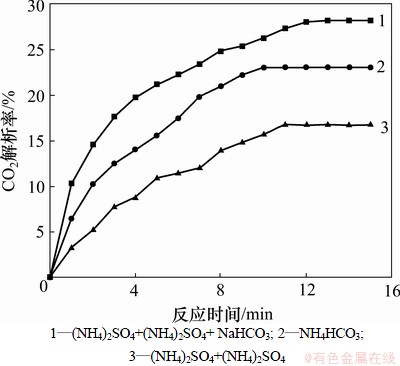
图4 碳酸氢钠对CO2解析率的影响
Fig.4 Effect of sodium bicarbonate concentration on desorption ratio
2.4 解析过程中氨的逸出及能耗分析
碳酸氢铵溶液解析能耗由反应热和溶液显热组 成,本实验仅对化学反应热进行分析。在碳酸氢铵加热解析过程中,发生的主要反应为式(1),而式(2)和(3)中分解产生的NH3一部分以游离状态存在于溶液中,一部分在气液相平衡作用下随CO2进入解析气中。从式(1)~(3)可以看出:每释放1 mol CO2需要吸收热量26.88 kJ,每释放1 mol CO2+1 mol NH3则需吸收热量64.26 kJ。这里认为解析能耗不包括溶液中游离的NH3,因为这部分NH3仍然在水溶液系统中,并没有逸散出去。因此,只计算随CO2逃逸出的那部分NH3所消耗的能量,这样,根据实验中测量得到的CO2流量以及逸出NH3的质量可以依据式(4)计算碳酸氢铵解析CO2的化学反应能耗:
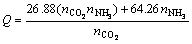 (4)
(4)
式中: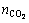 和
和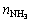 分别为解析气中CO2和NH3的物质的量,mol。
分别为解析气中CO2和NH3的物质的量,mol。
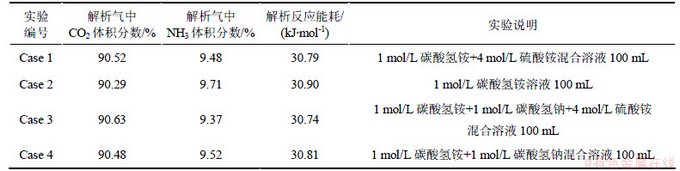
在解析温度为80 ℃时进行4组解析实验,试验中产生的解析气中CO2及NH3流量及化学反应能耗如图5和表2所示。从图5和表2可见:这4组实验解析气中CO2体积分数为90.5%左右,逸氨体积分数为9.5%左右。计算解析过程化学反应能耗约为30.8 kJ/mol,与MEA等方法所得的80 kJ/mol[8]相比,能耗要小得多。
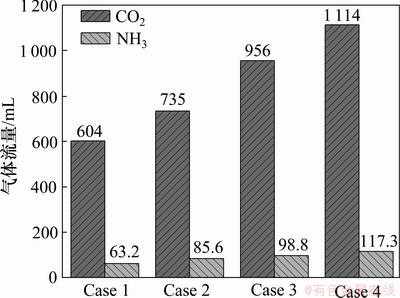
图5 解析气中CO2及NH3体积
Fig.5 Volume of CO2 and NH3 in desorbed gas
表2 解析气中CO2与NH3含量及反应能耗
Table 2 Percentage content of CO2 and NH3 in desorbed gas and reaction energy
3 结论
(1) 氨法脱硫脱碳富液CO2解析率随温度升高而上升。
(2) 氨法脱硫脱碳富液中存在的高浓度硫酸铵对解析液再生有明显抑制作用。
(3) 在解析液中添加碳酸氢钠不但可以抵消硫酸铵的抑制作用,还可以提高溶液的CO2解析率。
(4) 将碳酸氢钠作为添加剂加入到氨法脱硫脱碳吸收液中有助于提高溶液再生解析率,降低再生能耗。
参考文献:
[1] 秦锋, 王淑娟, 陈昌和, 等. 氨法脱碳系统再生能耗的研究[J]. 化工学报, 2010, 61(5): 1233-1240.
QIN Feng, WANG Shujuan, CHEN Changhe, et al. Research on heat requirement of aqua ammonia regeneration for CO2 capture[J]. Journal of Chemical Industry and Engineering, 2010, 61(5): 1233-1240.
[2] Resink K P, Yeh J T, Pennline H W. Aqua ammonia process for simultaneous removal of CO2, SO2 and NOx[J]. Int J Environ Technol Manag, 2004, 4(1/2): 89-104.
[3] Steeneveldt R, Berger B, Torp T A. CO2 capture and storage closing the knowing-doing gap[J]. Chemical Engineering Research and Design, 2006, 84(A9): 739-763.
[4] DIAO Yongfa, ZHENG Xianyu, HE Boshu, et al. Experimental study on capturing CO2 greenhouse gas by ammonia scrubbing[J]. Energy Conversion and Management, 2004, 45(13/14): 2283-2296.
[5] Yeh A C, Bai H. Comparison of ammonia and monoethanolamine solvents to reduce CO2 greenhouse gas emissions[J]. The Science of the Total Environment, 1999, 228(2/3): 121-133.
[6] RESNIK K P, GARBER W, HREHA D C, et al. A parametric scan for regenerative ammonia-based scrubbing for the capture of CO2[C]//Proceedings of the 23rd Annual International Pittsburgh coal Conference. Pittsburgh, US, 2006.
[7] Kim Y J, You J K, Hong W H, et al. Characteristics of CO2 absorption into aqueous ammonia[J]. Separation Science and Technology, 2008, 43(4): 766-777.
[8] Yeh J, Resnik K, Rygle K, et al. Semi-batch absorption and regeneration studies for CO2 capture by aqueous ammonia[J]. Fuel Processing Technology, 2005, 86(14/15): 1533-1546.
[9] SHI Yao, LI Wei. Capture and separation of CO2 from flue gas by coupling free and immobilized amines[J]. Journal of Environmental Sciences, 2002, 14(4): 451-456.
[10] 刘芳, 王淑娟, 张曦, 等. 碳酸氢铵溶液解析二氧化碳研究[J]. 环境科学学报, 2009, 29(9): 1886-1890.
LIU Fang, WANG Shujuan, ZHANG Xi, et al. Study on ammonium bicarbonate decomposition after CO2 sequestration by ammonia method[J]. Acta Scientiae Circumstantiae, 2009, 29(9): 1886-1890.
[11] ZHU Dechen, FANG Mengxiang, ZHONG Lü, et al. Semi-batch experimental study on CO2 absorption characteristic of aqueous ammonia[J]. Energy Procedia, 2011, 4: 156-163.
[12] Kim J, Han K, Chun H. CO2 absorption with low concentration ammonia liquor[J]. Energy Procedia, 2009, 1(1): 757-762.
[13] Darde V, Thomsen K, Willy J M, et al. Chilled ammonia process for CO2 capture[C]//9th International Conference on Greenhouse Gas Control Technologies. Washington D C, 2008: 1-8.
[14] 刘光启, 马连湘, 刘杰. 化学化工物性数据手册: 无机卷[M]. 北京: 化学化工出版社, 2002: 324-329.
LIU Guangqi, MA Lianxiang, LIU Jie. Handbook of data on properties of chemistry and chemical industry: Inorganic volume[M]. Beijing: Chemical Engineering Press, 2002: 324-329.
(编辑 陈灿华)
收稿日期:2012-03-10;修回日期:2012-05-22
基金项目:国家科技部科技型中小企业创新基金资助项目(08C26214302185)
通信作者:蒋绍坚(1963-),男,湖南邵阳人,教授,从事高效低污染燃烧、生物质能源利用研究;电话:13974870633;E-mail: sjjiang@csu.edu.cn