���Er-TiO2��Ĥ���Ʊ�����������
��Դ�ڿ����й���ɫ����ѧ��2017���8��
�������ߣ������� ���� ������ ��ΰ ������
����ҳ�룺1621 - 1632
�ؼ��ʣ�ˮ���ԿǾ��ǣ�����ӣ��������ѱ�Ĥ�������ģ��ɼ���
Key words��water-soluble chitosan; erbium-doped; titanium dioxide film; photocatalysis; simulated solar light
ժ Ҫ����ˮ���ԿǾ���(WSC)Ϊ���Ӽ�����ˮ������Ϊ��Դ�����ñ��������з��Ľ���/��ת����ʯӢ����Ƭ���Ʊ�һϵ��Er-TiO2��ױ�Ĥ������ͿĤ����(1~4)�������¶�(550~650 ��)������ʱ��(0.5~3 h)�Լ�WSC����(0~0.05% (��������))�Ա�Ĥ�ṹ�����ʵ�Ӱ�죬������XRD��SEM��EDX��TG-DTG��BET�ȼ����Ա�Ĥ�Ľṹ���б�����ͨ��������Һ�Ĺ�����ⷴӦ�����������ܡ�������������ܽ���WSC��������Ϊ0.04%(��������)��ͿĤ����Ϊ3�㣬�����¶�Ϊ550 �棬����ʱ��Ϊ1 hʱ����ģ��ɼ����£���Ĥ��7.8 mg/L�ļ�����Һ�����Ӧ����6 h���������ʿɴﵽ64.6%��
Abstract: The porous Er-TiO2 films were prepared using water-soluble chitosan (WSC) as addictive, Er(NO3)3��5H2O as source of Er element we created by dip/spin-coating method. The effects of the preparation parameters, including the number of coating layers (1-4), calcination temperature (550-650 ��), calcination time (0.5-3 h) and the content of WSC in sol (0-0.05% (mass fraction)) on the structure and performance of the films were investigated. The films were characterized by X-ray diffraction (XRD), scanning electron microscopy (SEM), energy dispersive X-ray spectroscopy (EDX), thermal analysis (TG-DTG) and nitrogen adsorption method (BET). The photocatalytic degradation reaction of methyl orange was chosen to evaluate the photocatalytic performance. The results show that the highest quality film is obtained by sol with 0.04% (mass fraction) of WSC, 3 layers, the calcination temperature of 550 ��, and calcination time of 1 h. With this film, the degradation rate of 7.8 mg/L methyl orange solution reaches up to 64.6% under simulated solar light after 6h photocatalytic reaction.
DOI��10.19476/j.ysxb.1004.0609.2017.08.11
������1������1��������1���� ΰ1��������1, 2
(1. ̫ԭ������ѧ ú��ѧ�뼼����������ɽ��ʡ�ص�ʵ���ң�̫ԭ 030024��
2. ����¬��ѧ ����ϵ������¬ N2L3G1�����ô�)
ժ Ҫ����ˮ���ԿǾ���(WSC)Ϊ���Ӽ�����ˮ������Ϊ��Դ�����ñ��������з��Ľ���/��ת����ʯӢ����Ƭ���Ʊ�һϵ��Er-TiO2��ױ�Ĥ������ͿĤ����(1~4)�������¶�(550~650 ��)������ʱ��(0.5~3 h)�Լ�WSC����(0~0.05% (��������))�Ա�Ĥ�ṹ�����ʵ�Ӱ�죬������XRD��SEM��EDX��TG-DTG��BET�ȼ����Ա�Ĥ�Ľṹ���б�����ͨ��������Һ�Ĺ�����ⷴӦ�����������ܡ�������������ܽ���WSC��������Ϊ0.04%(��������)��ͿĤ����Ϊ3�㣬�����¶�Ϊ550 �棬����ʱ��Ϊ1 hʱ����ģ��ɼ����£���Ĥ��7.8 mg/L�ļ�����Һ�����Ӧ����6 h���������ʿɴﵽ64.6%��
�ؼ��ʣ�ˮ���ԿǾ��ǣ�����ӣ��������ѱ�Ĥ�������ģ��ɼ���
���±�ţ�1004-0609(2017)-08-1621-11���� ��ͼ����ţ�O643���� ���ױ�־�룺A
TiO2��Ϊ����������仯ѧ�����ȶ��������Ըߡ�������Ⱦ���������۵��ŵ㱻���ڽ��з�ˮ�ͷ����Ĵ���[1-3]������TiO2������ԽϿ��Ĵ�϶��ֻ�ܱ�����⼤�����Ӷ��������̫����������ʡ������о�������ϡ����������������4f���ӽṹ�ͷḻ���ܼ����ܹ���չTiO2�Ĺ����շ�Χ���ɼ��⣬����˶�̫�����������[4-8]���������߿������Er���ӵ�TiO2��Ĥ���е��о�����[9]��Er-TiO2�����ڿɼ������������Ƚϸߣ�����һ���̶��ϸ���������������ʵ͵�ȱ�ݣ����������ӵ�������Ч�ٽ���e��h+�ķ��룬���������Ч�ʣ��������������ߡ�ͬʱ����TiO2�������������壬�Ʊ��ɱ�Ĥ�����Կ˷���ĩ״TiO2������ʹ��֮�����ڷ�����յ����⡣
���Ա�Ĥ�����������ʱ������ֻ�ܵ��ﱡĤ��һ����ȣ�ʹ�ÿ����õ���Ч��������½������¹�����Բ���[10]�����Ƴɶ�ṹ�ı�Ĥ�������ʹ���ߵ����������ӣ������õĴ������ࡣ�������Ӽ�������ֹ���ӵ��žۣ��õ���ϸС������������߲��ϵıȱ��������ǿ�������[11-13]���ڲ����ܽ�-�������Ŀ���·���Ʊ�TiO2��Ĥʱ�������ںϳɱ�Ĥ�������м������Ӽ��ǻ�ö�ױ�Ĥ����Ч�ֶΣ��Ծ���ϩ��(PVA)[14]�����Ҷ���(PEG)[15-16]�ͼ���ά��(MC)[17]��Ϊ���Ӽ��Ʊ���ṹ��Ĥ���ϡ��������߿�����������ˮ���ԿǾ���Ϊ���Ӽ��Ʊ���TiO2/Al2O3��Ĥ�����������������������Ĥ���������[18]��
Ŀǰ�����й���Er-TiO2��Ĥ�ı���[19-20]�����Ƕ�ṹ��Er-TiO2��Ĥ��δ���������������߿��������Span 80Ϊ���Ӽ��Ʊ��˶��Er-TiO2��Ĥ���о��������ñ�Ĥ�������ÿɼ���ʵ�ֹ�������л���Ⱦ���������Ը������ܵ�Er-TiO2��Ĥ[21]��ˮ���ԿǾ�����������������Ӽ������и���İ������ǻ����������ӵ���������ǿ����ˣ�����������ˮ���ԿǾ���Ϊ���Ӽ����ڲ����������Ʊ���ϸС������ɵĶ��Er-TiO2��Ĥ��������Լ�����Һ��ģ��ɼ����µĴ����ܣ�����ϸ�о�ͿĤ�����������¶ȡ�����ʱ�估ˮ���ԿǾ���(WSC)���������Ա�Ĥ�Ľṹ��������ܵ�Ӱ�졣
1 ʵ��
1.1 ʵ���Լ�
�����Ķ���(Ti(OC4H9)4��TBOT���ɶ��п��������Լ���������98%)��������(C2H4O2�����ŷ������������˾������99.5%)����ˮ�Ҵ�(C2H6O������п���ŷ��ѧ�Լ�����˾������99.7%)����ˮ������(Er(NO3)3��5H2O��Aladdin������99.9%)��ˮ���ԿǾ���(ɽ���¿�����Ƽ�����˾������081223WT)����������ˮ(����)��
1.2 �ܽ����Ʊ�
��3.4 mL���ᶡ���ܽ���10.0 mL��ˮ�Ҵ��У�������ȣ���Ϊ���ҺA���ֱ��ȡ7.6��11.4��15.2��19 mgˮ���ԿǾ��ǣ�����1.0 mL��������ˮ�У�����WSC��ˮ��Һ��2.0 mL��ˮ�Ҵ���1.0 mL�������ϣ���е������ȣ���Ϊ���ҺB�������ҺA�����μӵ����ҺB�У�����10 h�õ����ҺC����0.0446 g(1.0%(Ħ������)�������������о�Er�������������)��ˮ�������ܽ���1 mL��ˮ�Ҵ��к���μӵ����ҺC�У���������3 h���õ������ܽ�����ͿĤҺ��ˮ���ԿǾ��Ǻ����ֱ�Ϊ0.02%��0.03%��0.04%��0.05%(��������)��
1.3 ��Ĥ���Ʊ�
��Ĥ���Ʊ����̲��ñ����������������Ľ���-��תͿĤ��[22]���Ƚ������õ�ʯӢ��������(ֱ��18 mm����2 mm������ʯӢ��������˾����)�̶������Ƶ���תװ���ϣ������崹ֱ�����ܽ�����30 s���뿪�ܽ�����ת�õ�ʪĤ����ʪĤ��һ��ʪ����(70%)����2 h[23]��Ȼ���ظ�����ͿĤ����ֱ���õ��걸Ĥ(1~4��)����������Ĥ��1 ��/min����/��������������¯�����պɵõ������Er-TiO2��Ĥ�����µ��ܽ�����ͬ���ĸ�������չ����Ƶ�Er-TiO2���塣
1.4 �ṹ�����ܼ��
����DX-2700��X���������Dz�����Ʒ�ľ��ͣ�Cu K�����䣬�ܵ�ѹΪ36 kV���ܵ���Ϊ30 mA��ɨ�跶ΧΪ20��~70�㣬ɨ������Ϊ8 (��)/min������Ϊ0.01�㡣���ú���Philips��˾�������䱸�е���HKL��˾HKLC I�ͱ�ɢ����������ǵ�XL30ESEM�ͻ���ɨ���������(SEM)���۲��������Ĥ��Ʒ�ı�����ò��������С����Ϣ�����ٵ�ѹΪ10 kV��Ϊ��ȷ��WSC�������л������ȫ�ֽ��¶ȣ��������߲����˵¹�NETZSCH��˾������STA409C�����ط����Ƕ�����WSC�ĸ�������ĩ���з�������������Ϊ���������գ������¶ȷ�ΧΪ������800 �棬��������Ϊ10 ��/min������NOVA 2000e�ͱȱ���Ϳ������ǶԴ����ıȱ�����Ϳṹ���вⶨ��
1.5 ���ʵ��
��������[22]�������Ƚ�Ĥ���������Һ�У��ܹ����30 min��ʹ������Һ�ڱ�Ĥ�������ӱ���ﵽ����-�Ѹ�ƽ�⡣ȡ����Ĥ������ڹ����Ӧ���У�����30 mLŨ��Ϊ7.8 mg/L�ļ�����Һ�����裬�̶���Դ���Ա�Ĥ����Դ���������ҺҺ��20 cm����ԴΪ500 W믵�(���ײ���Ϊ200~1100 nm)��ģ��̫���⡣ÿ��10 min�ӷ�Ӧ����ȡ��5 mL��������-�ɼ��ֹ��ȼƷ���������ͨ�����¹�ʽ�������ʱ���¼��Ƚ�����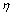 ��
��
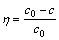 (1)
(1)
ʽ�У�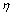 Ϊ��������ʣ�c0Ϊ���ȳ�ʼŨ�ȣ�cΪ������6 h�����Ũ�ȡ�
Ϊ��������ʣ�c0Ϊ���ȳ�ʼŨ�ȣ�cΪ������6 h�����Ũ�ȡ�
2 ���������
2.1 ��ͬͿĤ�����Ա�Ĥ�ṹ���������ܵ�Ӱ��
2.1.1 XRD����
ͼ1��ʾΪ����ˮ���ԿǾ��Ǻ���Ϊ0.04%(��������)���ܽ���ͿĤ1~4�Σ���550 ��������1 h�Ƶõı�Ĥ�������XRD�ס���ͼ1�ɼ�����2��Ϊ25.1�㴦������������壬������TiO2�����ѿ���(101)���������塣δ�۲쵽Er���ֵ�����壬�������Er��ɢ���ȣ�Ҳ����������Er3+��ʽ������TiO2�����У���������Er2O3�������ʽ��������[19]��EDX���������ʾErԪ����Ĥ���еĺ���Ϊ1.0%(Ħ������)��ͿĤ3�����µ������ʮ������˵�������ϳ��صĴ������١�ͿĤ������һ�����ӵ�4�㣬�����ǿ��������ǿ��˵����Ĥ��Er-TiO2���������ࡣ
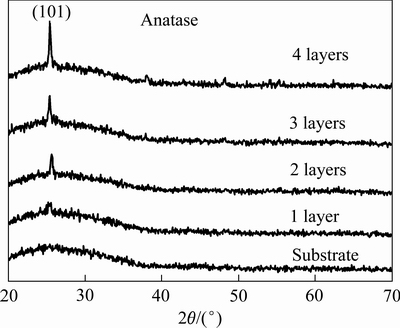
ͼ1 ��ͬͿĤ�����Ƶõ�Er-TiO2��Ĥ������XRD��
Fig. 1 XRD patterns of Er-TiO2 thin films with different coating layers and substrate
2.1.2 SEM����
ͼ2��ʾΪͿĤ������ͬ���ñ�Ĥ��SEM����ͼ2�ɿ�����ͿĤΪһ��ʱ����Ĥ����TiO2������С����һ������������ͿĤ����Ϊ����ʱ����Ĥ��������ߣ��������н�Ϊ���ܣ������������Ȼ���ͿĤ���ӵ�3�㣬Ĥ���������걸������û����������������ͿĤ��4��ʱ�������ߴ�����
2.1.3 �����Ӧ
ͼ3��ʾΪ��ͬͿĤ������Ĥ��Ӧ6 h�����������ʱ��ı仯����ͼ3�ɿ�������ͿĤ��һ�����ӵ�4��ʱ�������������ߺ�(32.67%��44.49%��63.24%��53.90%)��ͿĤ3��õ���Ĥ�㽵������ߡ�����Span80���ܽ��Ƶõı�Ĥ��ͿĤ����Ϊ4��ʱ���õ��ı�Ĥ���������ߣ�Ϊ55.2%[21]��������ˮ���ԿǾ���Ϊ���Ӽ��Ƶõı�Ĥ�Ĺ������63.24%���ɼ�����ˮ���ԿǾ���Ϊ���Ӽ��Ƶñ�Ĥ�Ĺ�����ܸ��š������ʵı仯�뱡Ĥ����TiO2������أ�����ͿĤ�������ӣ�Ĥ����TiO2�������ӣ�������λ�����ࣻ��ͿĤ�������ӵ�4��ʱ�������������ᵼ�±ȱ������С��ʹ��������½����ʵ����ͿĤ����Ϊ3�㡣
2.2 ��ͬ�����¶ȶԱ�Ĥ�ṹ���������ܵ�Ӱ��
2.2.1 TG����
ͼ4��ʾΪ��ˮ���ԿǾ���Ϊ0.04%(��������)����������֮�����÷�ĩ��TG-DTGͼ���������ĸ���������Ĥ����ͬ����ͼ4��֪����Ʒ�ķֽ���̿��Դ����Ϊ4���Σ���һ��(20~167 ��)������ʧ9.74%(��������)����ӦΪ��������������ˮ���Լ��л��ܼ����Ҵ���������ȵ��Ѹ�[24]���ڶ���(167~280 ��)������ʧ5.52%(��������)��Ϊ��������ǰ���������л�����ȷֽ����[25]��������(280~380 ��)������ʧ11.05%(��������)��Ϊ�������ѿ���֮�����������õĻ��ŵȵĶ��Ѽ��ֽ�ȥ������[26]�����Ľ�(380~520 ��)������ʧ1.57%(��������)��Ϊˮ���ԿǾ��ǵķֽ⡣520~800 ����Ʒ��������������ʧ��˵��520 ��ʱˮ���ԿǾ����ѷֽ���ȫ��
2.2.2 XRD����
���������ϵĴ������٣�Ϊ�˸������ع۲��侧��ṹ���ռ�����Ĥ��ͬ�����Ʊ��ķ�ĩ��XRD������ͼ5��ʾΪˮ���ԿǾ��Ǻ���Ϊ0.04%(��������)���ܽ�����ͬ�¶��¾�1 h�����Ƶõ�Er-TiO2��ĩ��XRD�ס���ͼ5�п��Կ������������¶ȴ�550 �����ߵ�650 ��ʱ����Ʒֻ�������ѿ������壬�������¶ȵ����ߣ���Ʒ�����������ǿ����������Ľᾧ������ߡ�����л�ֹ�ʽ��������ӳߴ�ֱ�Ϊ9.2 nm��13.1 nm��15.8 nm����������

ͼ2 ��ͬͿĤ�����Ƶõ�Er-TiO2��Ĥ��SEM��
Fig. 2 SEM images of Er-TiO2 thin films with different coating layers
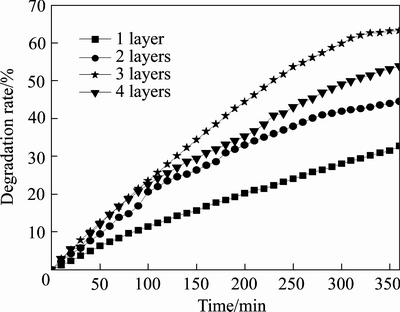
ͼ3 ��ͬͿĤ������Er-TiO2��Ĥ��������ʵ�Ӱ��
Fig. 3 Effect of different coating layers on photocatalytic degradation rate of Er-TiO2 films

ͼ4 Er-TiO2��������TG-DTGͼ
Fig. 4 TG-DTG analysis of Er-TiO2 gel powder
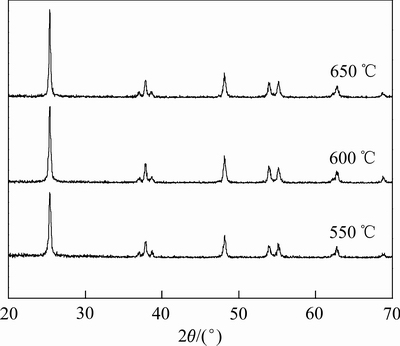
ͼ5 ��ͬ�����¶��µ�Er-TiO2������XRD��
Fig. 5 XRD patterns of Er-TiO2 catalysts at different calcination temperatures
2.2.3 SEM����
ͼ6��ʾΪ�ڲ�ͬ�����¶�������1 h�Ƶõı�Ĥ��SEM����ͼ6�ɿ������������¶�Ϊ550 ��ʱ����Ĥ����������ƽ��������ϸС�����ȣ�����С����϶�ʽϸߣ��������¶����ߵ�600 ��ʱ��������������϶�ʽ��͡�������������¶ȣ���������Ѹ��������һ������϶�ʽ��͡�

ͼ6 ��ͬ�����¶���Er-TiO2��Ĥ��SEM��
Fig. 6 SEM images of Er-TiO2 films at different calcination temperatures
2.2.4 �����Ӧ
ͼ7��ʾΪ��ͬ�����¶�����Er-TiO2��Ĥ�Ĺ����������ʱ��ı仯����ͼ7�ɿ������������¶���550 �����ߵ�650 ��ʱ�������������60.87%�����½���54.38%��48.51%�����¶�Ϊ550 ��ʱ����Ĥ��TiO2������С����϶����ߣ���ʹ�ñȱ������������λ����࣬�ʹ����������ߣ��������������¶ȣ�TiO2����������������Խ��͡����Ƚᾧ�����¶ȵ���߶����ߣ�ʹ�����еĸ���ȱ�ݼ��٣��Ӷ����ٹ������ӿ�Ѩ�ĸ������ģ��ӳ�������������ͬʱ�������¶����ߣ�������������������µ������Ѩ�ĸ��ϼ���������������������[27-29]�����о�����������¶�Ϊ550 �档
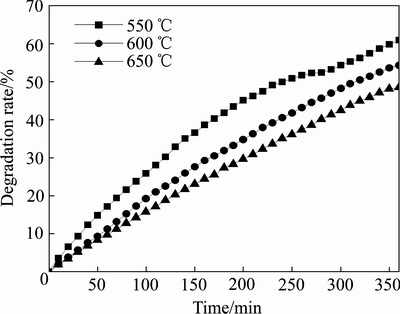
ͼ7 �����¶ȶ�Er-TiO2��Ĥ��������ʵ�Ӱ��
Fig. 7 Effect of calcination temperature on photocatalytic degradation rate of Er-TiO2 films
2.3 ��ͬ����ʱ��Ա�Ĥ�ṹ���������ܵ�Ӱ��
2.3.1 XRD����
ͼ8��ʾΪ������ˮ���ԿǾ���0.04%���ܽ���550 ���·ֱ�����0.5 h��1 h��2 h��3 h�ƵõĴ�����XRD�ס���ͼ8�ɿ����������Աȱ�PDF��Ƭ(JCPDS 21-1272)��4����ͬ�ȴ���ʱ��Ĵ�������������������Ϊ���ѿ���TiO2���������¶ȴ� 0.5 h�����ӵ�2 hʱ�������ǿ������ǿ��������ʱ������ӳ���3 hʱ�������ǿ�������Ա仯������л�ֹ�ʽ�������Ʒ��ƽ������Ϊ8.76 nm��9.01 nm��11.02 nm��15.66 nm�������ߴ�������

ͼ8 ��ͬ����ʱ���Er-TiO2�������XRD��
Fig. 8 XRD patterns of Er-TiO2 catalyst at different calcination time

ͼ9 ��ͬ����ʱ���Er-TiO2��Ĥ��SEM��
Fig. 9 SEM images of Er-TiO2 catalyst at different calcination time
2.3.2 SEM����
ͼ9��ʾΪ��ͬ����ʱ���±�Ĥ��SEM��ͼ9�п�֪��������ʱ��Ϊ0.5 hʱ��Ĥ�㾧�������Խϲ�ӳ�����ʱ����1 h��Ĥ���о���ϸС�����ȡ�������������ʱ�䣬����������������϶�ʽ��͡�
2.3.3 �����Ӧ
ͼ10��ʾΪ��ͬ�����¶����Ƶñ�Ĥ�Ĺ����������ʱ��ı仯����ͼ10�ɿ���������ʱ��Ϊ0.5��1��2��3 hʱ�������ʷֱ�Ϊ30.64%��59.99%��45.12%��40.86%�����������ߺ����ƣ�����ʱ��Ϊ1 hʱ����������ߡ�������������ʱ��̫�̣��л���û����ȫȥ����������TiO2���Ծ��͵��γɣ���������ʱ����������¿����ߴ��ȱ�������ͣ�ͬʱĤ��Ŀ�϶�ʽ��ͣ��Թ�Ĵ����������������������ԡ�
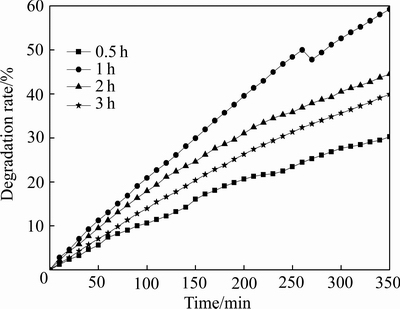
ͼ10 ����ʱ���Er-TiO2��Ĥ��������ʵ�Ӱ��
Fig. 10 Effect of calcination time on photocatalytic degradation rate of Er-TiO2 films
2.4 ��ͬˮ���ԿǾ����������Ա�Ĥ��Ӱ��
2.4.1 XRD����
ˮ���ԿǾ��Ǻ���Ϊ0.03%~0.05%���ܽ�(��������)����550 ��������1 h�Ƶõ�Er-TiO2������ĩ��XRD����ͼ11��ʾ����ͼ11��֪����Ʒ����2����25.1�㡢37.8�㡢48.1�㡢54.1�㡢55.2���62.9�㴦�������ѿ���TiO2�������(JCPDS No. 21��1272)�����ʯ�Ͱ��ѿ��������֣�˵��ˮ���ԿǾ��ǵļ��벢��Ӱ��TiO2�������͡�����л�ֹ�ʽ����ò�ͬˮ���ԿǾ��Ǻ���(0��0.02%��0.03%��0.04%��0.05%(��������))�ܽ��Ƶõ�Er-TiO2������ĩ�������ֱ�Ϊ12.1��10.2��9.3��8.2��14.4 nm����ˮ���ԿǾ��ǵļ���ʹ�ô����������Լ�С�����京��Ϊ0.04%(��������)ʱ�����þ���������С��Ϊ8.2 nm���ﵽ���ӻ�ЧӦ��Χ�����ӳߴ�ЧӦʹTiO2�۴��ܼ��͵����ܼ���ɷ������ܼ�����϶�����������λ�������۴���λ�������Ӷ���ǿ�˹������ӺͿ�Ѩ��������ԭ������ͬʱ������ЧӦҲʹTiO2�ĵ��Ǩ���������ռ��ɲ��ȴ���TiO2������ʱ������������ͨ����ɢ����Դ������ڲ�Ǩ�Ƶ����棬�Ӷ��������ӺͿ�Ѩ����ɢ�ٶ����[30]�������Ƶ��Ʊ������£�����Span80Ϊ���Ӽ�ʱ�����ô�����С����Ϊ13.2 nm������ˮ���ԿǾ���Ϊ���Ӽ��ƵõĴ�����С����8.2 nm[21]�������������Span80�������������������õ��ǻ�����ˮ���ԿǾ��Dz��������ǻ������Һ��а�����ˮ���ԿǾ����������ӵ���������ǿ���������ӵķ�ɢ�Ը��ã�ʹ��������С����С���������������ıȱ�������ߵĴ����ԡ�
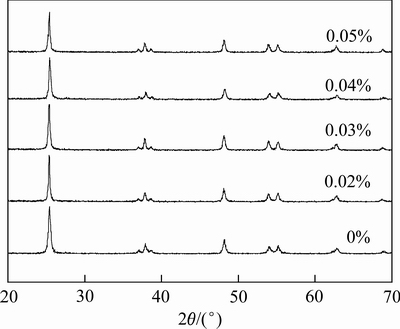
ͼ11 ��ͬˮ���ԿǾ��Ǻ����ܽ��Ƶô�����XRD��
Fig. 11 XRD patterns of Er-TiO2 catalysts prepared from sol with different amount of water-soluble chitosan and pure TiO2 catalysts

ͼ12 ��ͬˮ���ԿǾ����������ܽ��Ƶõ�Er-TiO2��Ĥ��SEM��
Fig. 12 SEM images of Er-TiO2 films prepared from sol with different amounts of water-soluble chitosan
2.4.2 SEM����
ͼ12��ʾΪ��ͬˮ���ԿǾ��Ǻ������ܽ�ͿĤ3�κ�550 ������1 h�Ƶõ�Er-TiO2��Ĥ��SEM����ͼ12��֪���������Ӽ����ܽ��Ƶõı�Ĥ�����������С�����ȣ���ˮ���ԿǾ��ǵĺ����ϵ�ʱ (��0.04%(��������))����Ĥ�п�������ϸС����ˮ���ԿǾ���������Ϊ0.05%(��������)ʱ��������С��һ�������ž����۲쵽�ϴ�Ŀ������ɴ˿ɼ������˺�����ˮ���ԿǾ��������ڵ���TiO2������������С��ʹ���һ��ϸС����Ĥ��ƽ�������ȡ�

ͼ13 ˮ���ԿǾ��Ǻ���Ϊ0��0.04%�ܽ��Ƶõ�Er-TiO2������N2����-�Ѹ�������ͼ�����ֲ�ͼ
Fig. 13 N2 absorption-desorption isotherms and pore size distribution of Er-TiO2 catalysts prepared with 0 and 0.04% water-soluble chitosan
2.4.3 BET����
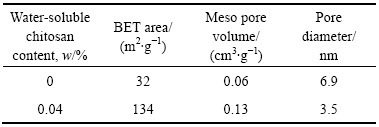
��Ʒ��N2����-�Ѹ����������ֲ���ͼ13��ʾ���ܽ��к���0.04% ˮ���ԿǾ����Ƶ���Ʒ�벻��ˮ���ԿǾ����Ƶ���Ʒ�����������߾����ڢ��ͣ� P/P0Ϊ0.4~1.0ʱ���е��͵��ͺ������ò��Ͼ��н�����벻�������Ӽ����(3~12 nm)������ˮ���ԿǾ���(0.04%)ʹĤ����(3~6 nm)����С���ҿ��ֲ���խ�����������Ľṹ��������1������ˮ���ԿǾ�����Ʒ��BET�ȱ����Ϊ143 m2/g�������Ϊ0.13 cm3/g����������û�����Ӽ����ܽ��Ʊ�����Ʒ(32 m2/g��0.06 cm3/g)���������Span80Ϊ���Ӽ��Ʊ�����Ʒ�ıȱ����(99 m2g-1)�ͽ����(0.1 cm3/g)[20]��
��1 ˮ���ԿǾ��Ǻ���Ϊ0��0.04%�ܽ��Ƶõ�Er-TiO2�����Ľṹ����
Table 1 Textural parameters of Er-TiO2 catalysts modified by 0 and 0.04% water-soluble chitosan
2.4.4 ���������
ͼ14��ʾΪˮ���ԿǾ��Ǻ����ֱ�Ϊ0��0.02%��0.03%��0.04%��0.05%���ܽ��Ʊ��ı�Ĥ�Ĺ����������ʱ��ı仯����ͼ14��֪��6 h�Ĺ������������Ϊ38.2%��41.8%��47.4%��64.6%��56.7%����ˮ���ԿǾ���������Ϊ0.04%ʱ����Ĥ�Ĺ�����������Ϊ64.6%������������Span80Ϊ���Ӽ��Ʊ��Ķ��Er-TiO2��Ĥ���뱾�о���ͬ��ʵ��������Ĥ���254 mm2��ģ��ɼ���Ϊ��Դ��30 mLŨ��Ϊ7.8 mg/L�ļ�����Һ��6 h�Ĺ����Ӧ�����ȵĽ�����Ϊ55.23%[20]��WANG��[18]�Ʊ�����Er-TiO2��Ĥ��Ĥ���Ϊ1935 mm2��5�������Ϊ��Դ��250 mLŨ��Ϊ8 mg/L�ļ�����Һ��1 h�Ĺ����Ӧ�����ȵĽ�����Ϊ22.65%�����о������Ӧ����1 hʱ�����ȵĽ�����Ϊ14.7%���ɴ˿ɼ�����ˮ���ԿǾ���Ϊ���Ӽ��Ʊ��Ķ��Er-TiO2��Ĥ���нϸߵĹ�����ԡ���������ˮ���ԿǾ���Ϊ���Ӽ�����ʹ���������ߴ�ﵽ8.2 nm���������ӳߴ�ЧӦ���������ӺͿ�Ѩ����ɢ�ٶ���ߣ�������ԭ������ǿ�����⣬TiO2������С��ʹ��Ĥ�ıȱ����������λ�����ࡣ
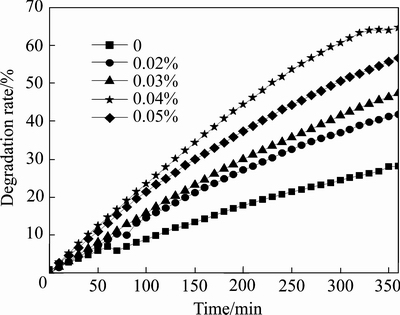
ͼ14 ˮ���ԿǾ��Ǻ�����Er-TiO2��Ĥ�Ĺ�������ʵ�Ӱ��
Fig. 14 Effect of water-soluble chitosan content on photocatalytic degradation rate
3 �����Ӧ�Ķ���ѧģ��
���ܲ���Er-TiO2���������������ɼ����¹��������ȵķ�Ӧ�Ѿ��������о������Ǹ÷�Ӧ������Ȼ����ȷ�������о���������TiO2Ϊ�������������ϵĹ�������������ʷ���Langmuir- Hinshelwood����ѧģ�ͣ���ģ�����£�
 (2)
(2)
ʽ�У�r�Ǽ��ȵĽ�������(mol/(L��min))��c�Ǽ��ȵ�Ũ��(mol/L)��t�ǹ�����ʱ�䣻kr�Ƿ�Ӧ���ʳ���(mol/(L��min))��Ka�Ƿ�Ӧ�������ϵ����
������(2)���ֵõ�����ʽ(3)��
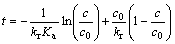 (3)
(3)
ʽ�У�c/c0��δ����ļ���ռ�ܵļ��ȵķ�����������ʱ����ء�
�������ּ��������1) ����ʼ����Ũ���㹻�ͻ������ڴ����ϵ������㹻��(��Kac<< 1)������ʽ(2)�ɽ���һ����Ӧ���̣������ʽ���£�
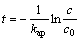 (4)
(4)
kap=krKa��һ����Ӧ�ı������ʳ�����
2) ����ʼ����Ũ�Ƚϸ�ʱ���������ڴ����ϵ��������ý�ǿ(Kac>>1)�����ȵĽ�������Ϊ����������(2)�Ļ�����ʽ���£�
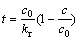 (5)
(5)
�����Ӧ��Ͳ����ڴ����ϴ��ھ�������������(2)�Ļ�����ʽ�ɱ�ʾ���£�
 (6)
(6)
ʽ�У�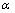 �����ڴ����Ͼ��������IJ�������Ȼ��������������ﲻ�ڴ�������������
�����ڴ����Ͼ��������IJ�������Ȼ��������������ﲻ�ڴ�������������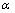 = 0[21]��
= 0[21]��
��Ĥ���������ȵĶ���ѧģ������ͼ15��ʾ��ģ�ʽ����������2���������Ӽ������ܱ�Ĥ�����������ʱ��Ķ���ѧģ��������ʽ(4)��˵����Ӧ���ڴ����ϵ���������������ṹ�ı�Ĥ�����������ʱ��Ķ���ѧģ��������ʽ(6)˵����Ӧ�P�����ڴ����ϴ��ھ�����������ױ�Ĥ�ķ�Ӧ���ʳ���Զ�������ܱ�Ĥ�ķ�Ӧ���ʳ�����
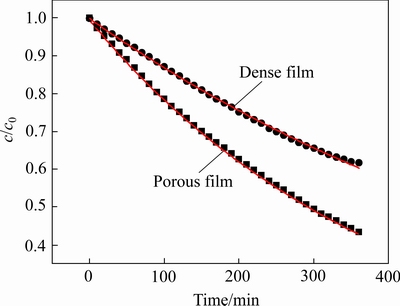
ͼ15 c/c0��ʱ��ı仯ͼ
Fig. 15 Change of c/c0 with time
��2 ģ�ʽ������
Table 2 Model equations and parameters

4 ����
1) ͿĤ����Ϊ��������ʱ���ɵõ��������걸�ı�Ĥ��Ϳ��3��ʱ�õ���Ĥ����ϸС���ֲ����ȣ�������õĴ����ԡ�
2) �����¶ȸ���550 ��ſ���ȷ���л���ȫ�����ճ�ȥ����ʱ�õ���Ĥ������ߵĹ�����ԡ����������¶ȵ����ߣ�TiO2����Ѹ��������������͡�
3) ��������ʱ����ӳ����ᾧ�������ӣ�����������������1 hʱ�õ���Ĥ���������á�
4) ˮ���ԿǾ��ǿ�ʹ�������������Լ�С���ȱ������������ˮ���ԿǾ��Ǻ���Ϊ0.04%(��������)ʱ����С�����ﵽ8.2 nm�������������ߣ��ﵽ64.6%��
REFERENCES
[1] ������, ����ͮ, �� ��, ������, ����, ������. �������ѹ��Ч��Ӱ�����ص��о�[J]. ���ֻ���ѧԺѧ��, 2009, 26(4): 44-48.
ZHANG Wei-hua, LI Xiao-tong, XU Song, WANG Wei-dong, XU Hong-jun, LI Zhong-yu. Study on the influence factors of photocatalysis efficiency of titanium dioxide[J]. Journal of Jilin Institute of Chemical Technology, 2009, 26(4): 44-48.
[2] ZHAO Zhen, SONG Ji-ling, ZHENG Jia-hong, LIAN Jian-she. Optical properties and photocatalytic activity of Nd-doped ZnO powders[J]. Transactions of Nonferrous Metals Society of China, 2014, 24(5): 1434-1439.
[3] MI Qian, CHEN Dai-quan, HU Jun-cheng, HUANG Zheng-xi, LI Jin-lin. Nitrogen doped graphene/CdS hollow spheres nanocomposite with enhanced photocatalytic performance[J]. Chinese Journal of Catalysis, 2013, 34: 2138-2145.
[4] MIGNOTTE C. EXAFS studies on erbium-doped TiO2 and ZrO2 sol-gel thin films[J]. Journal of Non-Crystalline Solids, 2001, 291: 56-77.
[5] DEUK Y L, JINTAE K, JUHYUN P. Effect of Er doping on optical band gap energy of TiO2 thin films prepared by spin coating[J]. Current Applied Physics, 2013, 13: 1301-1305.
[6] FANG Q, MEIER M, YU J J, WANG Z M, ZHANG J Y, WU J X, KENYON A, HOFFMANN P. FTIR and XPS investigation of Er-doped SiO2-TiO2 films[J]. Materials Science and Engineering B, 2003, 105: 209-213.
[7] LIANG Chun-hua, HOU Mei-fang, ZHOU Shun-gui. The effect of erbium on the adsorption and photodegradation of orange I in aqueous Er3+-TiO2 suspension[J]. Journal of Hazardous Materials, 2006, 138: 471-478.
[8] DU Jun, GU Xin, WU Qi. Hydrophilic and photocatalytic activities of Nd-doped titanium dioxide thin films[J]. Transactions of Nonferrous Metals Society of China, 2015, 25(8): 2601-2607.
[9] ������. ����Ӷ�������Ĥ���Ʊ������������о�[D]. ̫ԭ: ̫ԭ������ѧ, 2014.
LI Shao-ni. Preparation of Er-doped TiO2 films and the study of their photocatalytic activity[D]. Taiyuan: Taiyuan University and Technology, 2014.
[10] CHOI H, STATHATOS E, DIONYSIOS D. Sol-gel preparation of mesoporous photocatalytic TiO2 films and TiO2/Al2O3 composite membranes for environmental applications[J]. Applied Catalysis B: Environmental, 2006, 63: 60-67.
[11] HYEOK C, ELIAS S, DIONYSIOS D. Synthesis of nanocrystalline photocatalytic TiO2 thin films and particles using sol-gel method modified with nonionic surfactants[J]. Thin Solid Films, 2006, 510: 107-114
[12] LUMINITA A, ANCA D. TiO2 thin films for dyes photodegradation[J]. Thin Solid Films 2007, 515: 6294-6297.
[13] LIU Kun, ZHU Lian-jie, LI Nai-xuan, SUN You-guang, LI Hong-bin, ZHU Xu-chen. Solvothermal synthesis of mesoporous slabstone-like TiO2 and its photodegradation preference in a methyl orange-rhodamine B mixture solution[J]. Cryst Res Technol, 2012, 47(10): 1088-1094.
[14] CHANG C H, GOPALAN R, LIN Y S. A comparative study on thermal and hydrothermal stability of alumina, titania and zirconia membranes[J]. Membrane Science, 1994, 91(1/2): 27-45.
[15] PETERSON R A, ANDERSON M A, HILL C G. Development of TiO2 membranes for gas phase nanofiltration[J]. Membrane Science, 1994, 94: 103-109.
[16] �� ϼ, ½����, �� ��, �ƾ���. PEG�Զ������ѱ�Ĥ�۽ṹ������ܵ�Ӱ��[J]. ������ѧ��, 2016, 35(1): 302-309.
CHEN Xia, LU Gai-ling, ZHOU Yun, JI Jing-jing. Effect of PEG on the microstructure and photocatalytic activity of TiO2 films[J]. Bulletin of the Chinese Ceramic Society, 2016, 35(1): 302-309.
[17] AUST U, BENFER B, DIETZE M. Development of microporous ceramic membranes in the system TiO2/ZrO2[J]. Journal of Membrane Science, 2006, 281(1/2): 463-471.
[18] WANG Xiao-dong, SHI Fang, HUANG Wei, FAN Cai-mei. Synthesis of high quality TiO2 membranes on alumina supports and their photocatalytic activity[J]. Thin Solid Films, 2012, 520: 2488-2492.
[19] LEE D Y, KIM J, PARK J, KIM Y, LEE I K, LEE M H , KIM B Y. Effect of Er doping on optical band gap energy of TiO2 thin films prepared by spin coating[J]. Current Applied Physics, 2013, 13: 1301-1305.
[20] �� ��, ���û�, ������, �ֽ���. ����ӶԲ�������TiO2��Ĥ������ܵ�Ӱ��[J]. �й���ɫ����ѧ��, 2009, 19(10): 1866-1871.
WANG Ru, XU Yue-hua, CHEN Ming-jie, JIA Jin-liang. Effect of erbium doping on photocatalytic properties of TiO2 films on glass surface[J]. The Chinese Journal of Nonferrous Metals, 2009, 19(10): 1866-1871.
[21] ������. ����Ӷ�������Ĥ���Ʊ������������о�[D]. ̫ԭ: ̫ԭ������ѧ, 2014.
LI Shao-ni. Preparation of Er-doped TiO2 films and the study of their photocatalytic activity[D]. Taiyuan: Taiyuan University and Technology, 2014.
[22] WANG Xiao-dong, SHI Fang, GAO Xiao-xia, FAN Cai-mei, HUANG Wei, FENG Xian-she. A sol-gel dip/spin coating method to prepare titanium oxide films[J]. Thin Solid Films, 2013, 548: 34-39.
[23] ������, �� ǫ, �����. ����ѧʵ���е�ʪ�ȿ��ƣ�������װ�ü�����ԭ��[J]. Ӧ����̬ѧ��, 1999, 10(3): 357-361.
FENG Ming-guang, XU Qian, XU Jun-huan. Humidity control in biological experiments: modified device and methodology[J]. Chinese Journal of Applied Ecology, 1999, 10(3): 357-361.
[24] BLANCO E, GONZA J M, RAMI M. Photocatalytic TiO2 sol-gel thin films: Optical and morphological characterization[J]. Solar Energy, 2015, 122: 11-23.
[25] LEAUSTIC A, BABONNEAU F, LIVAGE J. Structural investigation of the hydrolysis-condensation process of titanium alkoxides Ti(OR)4 (OR=OPr-iso, OEt) modified by acetylacetone. 1. Study of the alkoxide modification[J]. Journal of Materials Chemistry, 1989, 1: 240-247.
[26] ACIK I O,  POKOL G,
POKOL G,  L. Titanium(��) acetylaceonate xerogels for processing titania films[J]. Journal of Thermal Analysis and Calorimetry, 2009, 97 (1): 39-45.
L. Titanium(��) acetylaceonate xerogels for processing titania films[J]. Journal of Thermal Analysis and Calorimetry, 2009, 97 (1): 39-45.
[27] ������, Ǯ�廪, �� ��, ��ѩ��, �� ��, ½С��. �����¶ȶ�K2Ti6O3��Ĥ��绯ѧ�����Ӱ��[J]. �й���ɫ����ѧ��, 2007, 17(10): 1711-1717.
HU Yu-yan, QIAN Qing-hua, LIU Chang, ZHOU Xue-feng, FENG Xin, LU Xian-hua. Effect of calcined temperature on photoelectrochemical and photocatalytic properties of K2Ti6013 thin films[J]. The Chinese Journal of Nonferrous Metals, 2007, 17(10): 1711-1717.
[28] �����. ���յ�P-25TiO2�ṹ�����������[J]. ������ѧѧ��, 1999, 15(1): 82-86.
LI Yu-guang. Microstructure characteristics and photoreactivity of calcined P-25 TiO2[J]. Journal of Physical Chemistry, 1999, 15(1): 82-86.
[29] KOZLOV D V, PATTKSLMS E A, SAVNIOV E N. The comparative studies of titanium dioxide in gas-phase ethanol photocatalytic oxidation by the FTIR in situ method[J]. Appl Catal B-Euvrion, 2000, 24(1): L7-L12.
[30] ZHANG Z, WANG C C, ZAKARIA R, YING J Y. Role of particle size in nanocrystalline TiO2-based photocatalysts[J]. Journal of Physical Chemistry B, 1998, 102(52): 10871-10878.
WANG Xiao-dong1, HUANG Yu-jiao1, LI Shao-ni1, HUANG Wei1, FENG Xian-she1, 2
(1. Key Laboratory of Coal Science and Technology of Ministry of Education and Shanxi Province, Taiyuan University of Technology, Taiyuan 030024, China;
2. Department of Chemical Engineering, University of Waterloo, Waterloo Ontario N2L3G1, Canada)
Abstract: The porous Er-TiO2 films were prepared using water-soluble chitosan (WSC) as addictive, Er(NO3)3��5H2O as source of Er element we created by dip/spin-coating method. The effects of the preparation parameters, including the number of coating layers (1-4), calcination temperature (550-650 ��), calcination time (0.5-3 h) and the content of WSC in sol (0-0.05% (mass fraction)) on the structure and performance of the films were investigated. The films were characterized by X-ray diffraction (XRD), scanning electron microscopy (SEM), energy dispersive X-ray spectroscopy (EDX), thermal analysis (TG-DTG) and nitrogen adsorption method (BET). The photocatalytic degradation reaction of methyl orange was chosen to evaluate the photocatalytic performance. The results show that the highest quality film is obtained by sol with 0.04% (mass fraction) of WSC, 3 layers, the calcination temperature of 550 ��, and calcination time of 1 h. With this film, the degradation rate of 7.8 mg/L methyl orange solution reaches up to 64.6% under simulated solar light after 6h photocatalytic reaction.
Key words: water-soluble chitosan; erbium-doped; titanium dioxide film; photocatalysis; simulated solar light
Foundation item: Project(21201130) supported by the National Natural Science Foundation of China
Received date: 2016-06-28; Accepted date: 2016-11-30
Corresponding author: HUANG Wei; Tel: +86-351-6018073; E-mail: huangwei@tyut.edu.cn
(�༭ ����)
������Ŀ��������Ȼ��ѧ����������Ŀ(21201130)
�ո����ڣ�2016-06-28�������ڣ�2016-11-30
ͨ�����ߣ��� ΰ�����ڣ���ʿ���绰��0351-6018073��E-mail: huangwei@tyut.edu.cn

