DOI:10.11817/j.ysxb.1004.0609.2020-35718
双膜三室电沉积金属锰联产EMD的离子传输过程
徐 祺1,王三反1,孙百超2,周 键1
(1. 兰州交通大学 寒旱地区水资源综合利用教育部工程研究中心,兰州 730070;
2. 中建钢构有限公司,四平 136000)
摘 要:针对传统单槽电解金属锰或二氧化锰存在能耗高、资源利用率低、环境污染严重等问题,提出双膜三室电解法实现阴极电沉积锰同时阳极联产电解二氧化锰,中隔室电化学再生硫酸。通过分析各隔室离子浓度变化,探究双膜三室电解法技术可行性,并对比三种离子交换膜对电沉积效果的影响。结果表明:双膜三室电解法电沉积金属锰同时联产电解二氧化锰可以实现,并且阴极电流效率可达80%以上,阳极电流效率可达60%以上,中隔室酸回收率高于65%;与Ionsep-HC、LANRAN-AM相比,TRJM-10W均相膜槽压最低,电解12 h后,阴极电流效率为86.25%,阳极电流效率为70.6%,中隔室酸回收率可达73.08%,但阴极液pH增幅最大,中间液Mn2+浓度最高。
关键词:金属锰;电解二氧化锰;双膜三室;电流效率;离子传输
文章编号:1004-0609(2020)-01-0194-09 中图分类号:TF792 文献标志码:A
锰是一种灰白色、有光泽的过渡金属元素,金属锰质坚而脆、化学性质活泼。全球90%以上的锰被用于钢铁工业,主要用于提高钢的硬度、强度、耐磨和耐腐蚀性等[1-2]。电解二氧化锰(EMD)呈黑色或棕黑色,一般用于锌锰、碱锰和锂锰电池阴极,增大放电容量,是电池工业中一种优良的去极化剂[3-4]。除在电池工业领域的使用外,EMD还广泛应用于玻璃脱色、陶瓷的釉药、织物印染、废水处理[5]等方面。
电解制备金属锰或EMD根据电解液成分可分为氯盐体系[6]和硫酸盐体系[7-9],氯盐体系较硫酸盐体系相比具有导电性好、槽压低、能耗少等优点,但由于盐酸易挥发且电解过程中阳极有Cl2释放,严重污染环境且操作不便,目前国内外企业大多用MnSO4溶液电解。
在单独电解金属锰过程中,阴极析出锰,阳极则放空不用,阳极电压主要耗于发生析氧反应,同时还会产生锰阳极污泥,其含锰量高、成分复杂,不仅浪费资源且污染环境[10]。针对这一问题,郑凡等[11]提出用阴离子交换膜代替传统布袋隔膜,将锰离子限制在阴极区,避免锰在阳极沉积;牛莎莎等[12]、严浩等[13]分别用桔子皮、葡萄糖做还原剂还原浸出锰阳极渣,有效实现锰铅分离。在单独电解二氧化锰过程中,阳极析出EMD,而阴极放空不用,阴极电压主要耗于发生析氢反应,气体带出酸雾腐蚀设备,严重污染操作环境。可见,无论是单独电解金属锰还是二氧化锰,均有一极放空不用消耗电能,造成能源浪费[14-15]。因此,为提高电能利用率,减少环境污染,迫切需要一种清洁节能工艺,在电沉积金属锰同时联产电解二氧化锰,既能实现节能生产又能避免锰阳极污泥带来的环境污染问题。目前,由于电沉积锰和EMD的实验条件相差较大,有关同槽电解方面的研究甚少。
本研究采用双膜三室电解槽从MnSO4体系中电沉积金属锰,同时阳极联产电解二氧化锰,中隔室回收硫酸,回收的硫酸用于锰矿酸浸过程。通过测定电解槽的中间液、阴极液、阳极液成分变化研究离子传输过程,探究双膜三室电解法的技术可行性,为同槽电解条件的选择提供理论基础,并对三种离子交换膜的电解效果进行了对比研究。
1 实验
1.1 试剂与材料
实验所用3种离子交换膜如表1所示。阴极液为某制锰厂提供锰矿浸出液(Mn2+浓度约为40 g/L,(NH4)2SO4约为110 g/L),阳极液为40 g/L MnSO4+150 g/L H2SO4混合溶液,中隔室为0.5%稀硫酸溶液。所有试剂均为分析纯,溶剂为蒸馏水。
1.2 装置与仪器
实验装置由自制双膜三室电解槽[16]、直流稳压稳流电源、循环液槽、蠕动泵、数显恒温水浴锅等组成。双膜三室电解槽由抗腐蚀性能好、耐高温的聚甲基丙烯酸甲酯材料制成,用一张阴离子交换膜和一张阳离子交换膜将电解槽依次分为阴极室、中隔室和阳极室,每个隔室尺寸相同。三个隔室溶液均由蠕动泵驱动循环流动,电解槽外对应设置循环液槽,数显恒温水浴锅将槽内温度统一控制在45 ℃。阴极为不锈钢板(尺寸为14 cm×16 cm),阳极为Dimensionally stable anode(DSA)电极(尺寸为5 cm×10 cm),膜有效尺寸为17 cm×17.5 cm,阴阳极间距为90 mm。实验装置示意图如图1所示。
1.3 实验方法
通电前,阴阳极室分别注入阴阳极电解液;中隔室注入0.5%稀硫酸。将阴极板一面用环氧树脂胶进行绝缘;另一面先用金相砂纸打磨,后用40 g/L稀硫酸溶液清洗5~20 min,再置于硅酸钠溶液中浸泡备用。开启蠕动泵将各室流速控制在70~80 mL/min。通电后,在阴极电流密度为400 A/m2、阳极电流密度为500 A/m2、温度均为45 ℃条件下电解,记录槽电压并定时取样检测分析。实验结束后,小心剥离阴极板上沉积的锰片,烘干称重,阳极溶液中的电解二氧化锰用0.22 μm滤膜抽滤,蒸馏水冲洗4~5次后烘干称重。
表1 实验用离子交换膜的性能参数
Table 1 Performance parameters of experimental ion exchange membranes
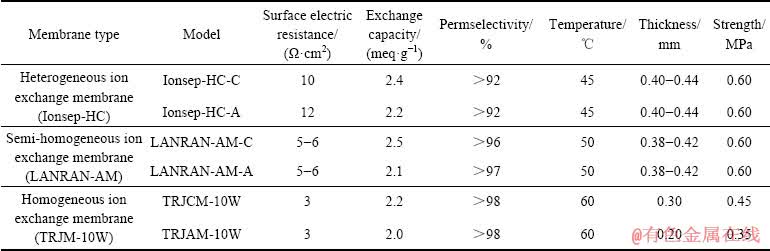

图1 实验装置示意图
Fig. 1 Schematic diagram of experimental device
1.4 分析及计算方法
实验中Mn2+浓度采用高锰酸钾滴定法测定;H+浓度用酸碱滴定法测定,甲基红-次甲基蓝为指示剂;电解锰纯度采用电感耦合等离子体原子发射光谱法(ICP-AES)测定; 浓度用硫酸钡重量法测定;基于产品质量和纯度计算电流效率,根据法拉第电解第一定律,电流效率的计算如式(1)所示
浓度用硫酸钡重量法测定;基于产品质量和纯度计算电流效率,根据法拉第电解第一定律,电流效率的计算如式(1)所示
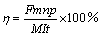 (1)
(1)
式中:η为电流效率,%;F为法拉第常数,96485.33 C/mol;m为电沉积产品质量增量,g;n为电子数,阴阳极均有n=2;p为电积产品纯度,%;M为摩尔质量,M(Mn)=55 g/mol,M(MnO2)=87 g/mol;I为电流强度,A;t为电解时间,s。
根据实际富集酸的量占理论富集量的百分比计算中隔室酸回收率[17],如式(2)所示:
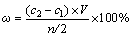 (2)
(2)
式中: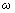 为酸回收率,%;c2为终时硫酸浓度,mol/L;c1为初时硫酸浓度,mol/L;V为溶液体积,L;n为电子转移量,mol。
为酸回收率,%;c2为终时硫酸浓度,mol/L;c1为初时硫酸浓度,mol/L;V为溶液体积,L;n为电子转移量,mol。
2 结果与讨论
2.1 双膜三室电解槽中电沉积过程的离子传输行为
将离子交换膜选择透过机理与金属电沉积理论相结合,构成双膜三室电解法同时电沉积锰和EMD的理论基础。双膜三室电沉积金属锰联产EMD过程中,外加直流电形成电场,离子运输主要推动力以电场力为主,此外还可能会受到因浓度梯度引起的浓差扩散、水分子渗透等作用[18-19]。
双膜三室电解槽中可能发生的离子传输过程如图2所示。在电场力作用下,阴极室中的Mn2+受阴极吸引,经过氨电催化作用在阴极板上还原成锰单质,同时发生析氢副反应,与金属锰析出形成竞争,但由于在不锈钢电极上析氢具有较高过电位[20-21],在阴极上发生的还原反应仍然以析锰为主。阴极液中的SO42-经电场力作用透过阴膜进入中隔室,并被阳膜阻隔留在中隔室。
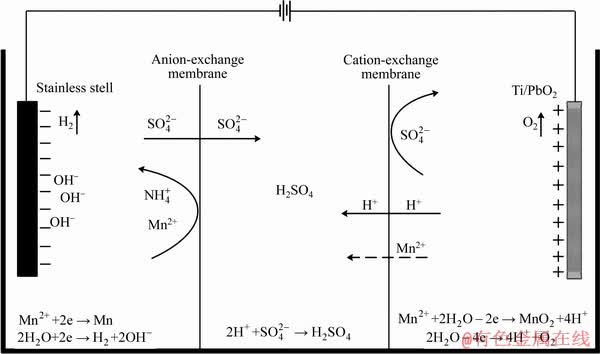
图2 双膜三室电解槽中离子传输示意图
Fig. 2 Schematic diagram of ion transport in double-membrane three-chamber electrolysis cell
阳极室发生Mn2+的氧化反应和水电解反应,Mn2+在阳极被氧化成Mn4+生成MnO2,水电解生成H+和O2,阳极液中的H+和水电解生成的H+经电场力作用穿过阳膜进入中隔室,与从阴极迁移过来的 结合生成H2SO4。随着反应进行,
结合生成H2SO4。随着反应进行, 和H+不断从阴阳
和H+不断从阴阳
极室迁移进入中隔室,中隔室内H2SO4浓度将随时间增长而升高。各隔室发生的电化学反应方程式如式(3)~(7)所示。
阴极:
Mn2++2e→Mn↓ (3)
2H2O+2e→H2↑+2OH- (4)
中隔室:
2H++ →H 2SO4 (5)
→H 2SO4 (5)
阳极:
Mn2++2H2O-2e→MnO2↓+4H+ (6)
2H2O-4e→4H++O2↑ (7)
本研究通过测定阴极液、阳极液、中间液的离子浓度变化验证上述离子传输过程是否发生。
2.2 不同种类离子交换膜电沉积实验结果
如表2所示,为在双膜三室电解槽中用不同种类离子交换膜电沉积锰联产EMD的实验参数及结果。
可以看出,三种离子交换膜的电沉积实验中,阴极电流效率均大于80%,阳极联产EMD电流效率均大于60%,中隔室酸回收率均在65%以上。说明在该实验条件下,双膜三室同时电解金属锰和EMD能够实现。其中,TRJM-10W离子交换膜无论在阴极还是阳极电流效率均为最高,酸回收率可达73.08%。分析原因认为,TRJM-10W离子交换膜选择透过系数最高(>98%),阳极液中H+和阴极液中的 迁移进入中隔室最多,酸回收率达到最大。但由于阴极发生析氢反应,Mn2+无法沉积完全,根据电荷守恒原理,阴极液中
迁移进入中隔室最多,酸回收率达到最大。但由于阴极发生析氢反应,Mn2+无法沉积完全,根据电荷守恒原理,阴极液中 不会全部迁移进入中隔室,即使酸回收率最高,中隔室内酸富集量也无法达到理论富集量。根据阳极反应方程式(4)可知,H+的迁移有利于反应向正向进行,因此TRJM-10W离子交换膜电解MnO2产量最多,阳极电流效率最大。
不会全部迁移进入中隔室,即使酸回收率最高,中隔室内酸富集量也无法达到理论富集量。根据阳极反应方程式(4)可知,H+的迁移有利于反应向正向进行,因此TRJM-10W离子交换膜电解MnO2产量最多,阳极电流效率最大。
阴极电解过程主要分三步进行:Mn(NH3)2+在阴极上放电吸附,阴极上锰的还原和氨的脱附,脱附下来的NH3继续与Mn2+结合形成Mn(NH3)2+,其中氨在阴极电解过程中起到电催化作用[22]。在用TRJM-10W离子交换膜的实验中,由于阴极 向中隔室迁移量最多,根据电荷守恒原则,相应阳离子减少量也最多。阴极液中锰主要以Mn2+和锰氨络离子Mn(NH3)2+形式存在,两种阳离子的减少主要用于发生电化学还原反应,即金属锰析出,因此阴极电流效率也达到最大。
向中隔室迁移量最多,根据电荷守恒原则,相应阳离子减少量也最多。阴极液中锰主要以Mn2+和锰氨络离子Mn(NH3)2+形式存在,两种阳离子的减少主要用于发生电化学还原反应,即金属锰析出,因此阴极电流效率也达到最大。
三种离子交换膜的槽电压随时间变化趋势如图3所示,均随着时间增长而减小,前2 h内降幅明显,2 h以后趋于稳定,降幅在1.6 V左右。这主要是由于在电解初期中隔室硫酸浓度较低,中隔室和阴阳极室浓度差过大,浓度梯度在膜两侧引起电势差。随着H+和 迁移进入中隔室,中间液硫酸浓度增大,由浓度差产生的溶液电阻逐渐减小,导致槽压降低。由图3可知,三种膜的槽电压由大到小排序为Ionsep-HC>LANRAN-AM>TRJM-10W,这可由膜电阻差异解释。由表1可知,Ionsep-HC膜电阻最大,因此槽压最高。这也是离子膜电解法槽电压略高于常规无膜电解法的原因,但综合经济效益来看,槽电压增加量在可接受范围内。
迁移进入中隔室,中间液硫酸浓度增大,由浓度差产生的溶液电阻逐渐减小,导致槽压降低。由图3可知,三种膜的槽电压由大到小排序为Ionsep-HC>LANRAN-AM>TRJM-10W,这可由膜电阻差异解释。由表1可知,Ionsep-HC膜电阻最大,因此槽压最高。这也是离子膜电解法槽电压略高于常规无膜电解法的原因,但综合经济效益来看,槽电压增加量在可接受范围内。

图3 槽电压随时间变化
Fig. 3 Cell voltage changes over time
表2 双膜三室电沉积金属锰联产EMD的实验条件及结果
Table 2 Experimental conditions and results of dual-membrane three-chamber electrodeposition manganese co-production EMD

2.2.1 阴极室各离子浓度变化
阴极液pH值、Mn2+、 浓度变化趋势如图4~6所示。由图4可以看出,三种离子交换膜的实验中pH值均先逐渐上升后趋于稳定,增幅较小,在1.2左右。这可由水电解和H+扩散的共同作用解释。由式(2)可知,阴极在析锰的同时会有析氢副反应发生。析氢实质是水电解过程,水在阴极电解产生H2的同时会产生OH-,因此碱度增加,pH值升高,分析其增幅不大的原因在于H+的扩散作用[23]。虽然阴极液与中间液被阴离子交换膜隔开,但由于H+在中隔室与阴极室之间的浓差扩散方向与所受电场力方向相同,仍会有部分H+泄露进入阴极液,与水电解产生的OH-结合呈中性,因此电解过程中虽有OH-产生,但pH值增幅不大;尤其随着电解时间延长,中隔室和阴极室之间的H+浓差越来越大,H+的扩散作用越来越明显,电解后期pH值几乎趋于稳定。这表明使用TRJM-10W离子交换膜时pH值增幅最大的原因在于其选择透过系数最大,H+泄漏率最低,因此被中和的OH-量最少,pH值最高。
浓度变化趋势如图4~6所示。由图4可以看出,三种离子交换膜的实验中pH值均先逐渐上升后趋于稳定,增幅较小,在1.2左右。这可由水电解和H+扩散的共同作用解释。由式(2)可知,阴极在析锰的同时会有析氢副反应发生。析氢实质是水电解过程,水在阴极电解产生H2的同时会产生OH-,因此碱度增加,pH值升高,分析其增幅不大的原因在于H+的扩散作用[23]。虽然阴极液与中间液被阴离子交换膜隔开,但由于H+在中隔室与阴极室之间的浓差扩散方向与所受电场力方向相同,仍会有部分H+泄露进入阴极液,与水电解产生的OH-结合呈中性,因此电解过程中虽有OH-产生,但pH值增幅不大;尤其随着电解时间延长,中隔室和阴极室之间的H+浓差越来越大,H+的扩散作用越来越明显,电解后期pH值几乎趋于稳定。这表明使用TRJM-10W离子交换膜时pH值增幅最大的原因在于其选择透过系数最大,H+泄漏率最低,因此被中和的OH-量最少,pH值最高。
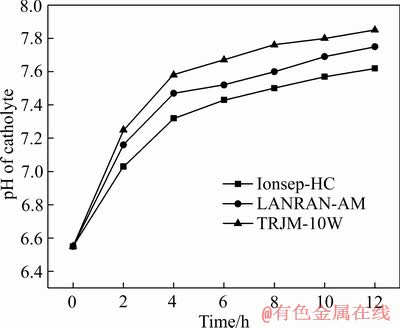
图4 阴极液pH值随时间变化
Fig. 4 pH value of catholyte changing over time
阴极液中Mn2+浓度变化趋势如图5所示。由图5可见,Mn2+浓度随电解时间的增加而迅速减少,这是由于除少量因浓差扩散泄露进入中隔室的Mn2+外,大量Mn2+在阴极被还原以金属单质的形态析出,同时,为维持电荷守恒,等量的 在电场力作用下迁移进入中隔室,如图6所示,
在电场力作用下迁移进入中隔室,如图6所示, 的变化趋势与Mn2+的大致相同。
的变化趋势与Mn2+的大致相同。
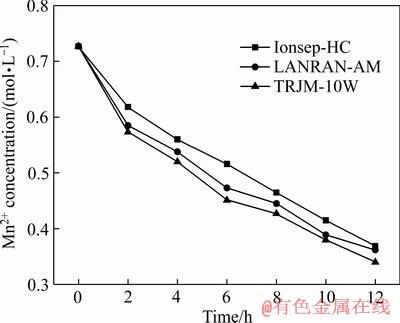
图5 阴极液Mn2+浓度随时间变化
Fig. 5 Concentration of Mn2+ in catholyte changing over time
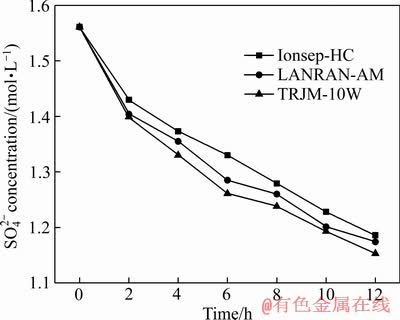
图6 阴极液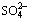 浓度随时间变化
浓度随时间变化
Fig. 6 Concentration of 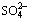 in catholyte changing over time
in catholyte changing over time
2.2.2 中隔室各离子浓度变化
考虑到阳极室与中隔室之间同时存在Mn2+浓度梯度和电场梯度,阳极液中的Mn2+有可能进入中隔室,所以对中隔室内Mn2+浓度增量进行了考察。如图7所示,为Mn2+浓度随时间的变化趋势,可以看出,三种离子交换膜的中隔室内Mn2+浓度均随时间缓慢增加,增加量小于0.04 mol/L,其中还有部分Mn2+来自于阴极液的浓差扩散作用。由此可知,阳极液中大部分Mn2+会参与氧化反应,不会迁移进入中隔室,这是由于Mn2+在MnSO4-H2SO4电解体系中,大多以[Mn2(SO4)3]2-形式存在[24],这种带负电的络离子在电场力作用下向阳极迁移,到达阳极附近再解离为Mn2+,接着Mn2+被氧化为MnO2。因此,进入中隔室内的Mn2+量很少,对电流效率的影响较小。其中TRJM-10W膜的中隔室Mn2+泄露最多,这是由于通过测定TRJM-10W膜电荷密度最大,活性基团最多,根据“空穴传导-双电层”理论[25],其膜表面活性基团越多,相应空穴数量越多,对反离子的选择透过性越好,因此在TRJM-10W离子交换膜的实验中,阳极室迁移进入中隔室内的Mn2+量最多。考虑到中隔室回收的酸用于锰矿浸出阶段,因此其中含有少量Mn2+可以接受。

图7 中隔室Mn2+浓度随时间变化
Fig. 7 Concentration of Mn2+ in middle cell changing over time
阴极室与中隔室之间主要依靠 迁移进行导电,阳极室和中隔室之间依靠H+迁移导电。如图8~9所示,可由中隔室内
迁移进行导电,阳极室和中隔室之间依靠H+迁移导电。如图8~9所示,可由中隔室内 和H+的浓度变化来证明。由图8可知,三种离子交换膜中隔室内
和H+的浓度变化来证明。由图8可知,三种离子交换膜中隔室内 浓度均随时间呈线性增加,其原因包括:一方面阴极液与中间液之间的
浓度均随时间呈线性增加,其原因包括:一方面阴极液与中间液之间的 浓差扩散作用与电场力作用方向相同,
浓差扩散作用与电场力作用方向相同, 向中隔室发生定向迁移。另一方面,由于阴极液中锰的析出,Mn2+浓度急剧减少,为维持阴极液电荷守恒
向中隔室发生定向迁移。另一方面,由于阴极液中锰的析出,Mn2+浓度急剧减少,为维持阴极液电荷守恒 受到同离子排斥也会穿过阴膜向中隔室移动。由图9可得,中隔室内H+浓度随时间增长而升高,说明不断有H+从阳极迁移进入中隔室,其推动力同样是阳极液与中间液的浓度梯度和电场梯度。阳极室中H+包括初始阳极液自带H+和电解水产生的H+。由图8~9可知,H+变化趋势与
受到同离子排斥也会穿过阴膜向中隔室移动。由图9可得,中隔室内H+浓度随时间增长而升高,说明不断有H+从阳极迁移进入中隔室,其推动力同样是阳极液与中间液的浓度梯度和电场梯度。阳极室中H+包括初始阳极液自带H+和电解水产生的H+。由图8~9可知,H+变化趋势与 相似,浓度约为
相似,浓度约为 的2倍。
的2倍。

图8 中隔室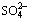 浓度随时间变化
浓度随时间变化
Fig. 8 Concentration of 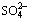 in middle cell changing over time
in middle cell changing over time
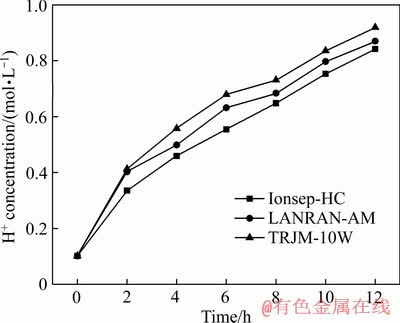
图9 中隔室H+浓度随时间变化
Fig. 9 Concentration of H+ in middle cell changing over time
2.2.3 阳极室各离子浓度变化

图10 阳极液Mn2+浓度随时间变化
Fig. 10 Concentration of Mn2+ in anolyte changing over time
阳极液中Mn2+浓度变化如图10所示,随着时间延长,Mn2+浓度呈线性降低。对比图5和10可知,阳极液Mn2+浓度变化趋势与阴极液相似,总减少量比阴极液少。这与表2所述相符,阴阳极电流效率相差明显,阳极析出EMD的电流效率始终比阴极析锰效率低。分析原因有:①在实验过程中,观察到随着电解进行,阳极液逐渐由淡粉色变为暗红色,是因为部分Mn2+在阳极发生了如下反应:
Mn2+-e→Mn3+ (8)
尽管Mn3+在酸性溶液中可歧化生成MnO2和Mn2+,但仍有部分Mn3+游离于阳极液中难以在阳极放电,造成损失。②阳极液中微量Mn2+穿过阳膜进入中隔室,造成Mn2+浓度降低。③由式(7)可知,阳极会发生水电解生成H+和O2,用于阳极电压部分耗于析出氧气,析氧反应与析EMD反应产生竞争,从而电流效率变低。
图11所示为阳极液H+浓度随时间变化趋势。由图11可知,三种离子交换膜的阳极液酸度均有所降低,这是由于在浓差扩散和电场力作用下H+迁移进入中隔室所致。尽管阳极在析氧过程中不断产生H+,但H+浓度总体呈下降趋势,说明H+向中隔室的迁移速度比在阳极析出速度快,酸度不断下降。TRJM-10W离子交换膜由于其选择透过性最好,H+迁移量最多,因而浓度降幅最大。
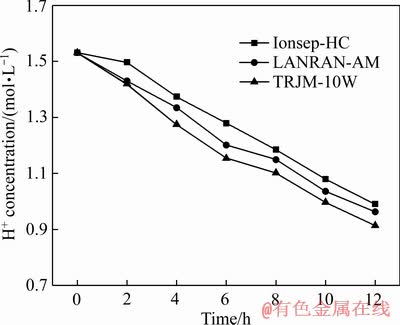
图11 阳极液H+浓度随时间变化
Fig. 11 Concentration of H+ in anolyte changing over time
3 结论
1) 采用双膜三室电解槽阴极电沉积金属锰同时阳极联产EMD是可行的,并在中隔室回收硫酸。三种离子交换膜电沉积实验结果表明:阴极电流效率均大于80%,阳极电流效率均大于60%,中隔室酸回收率在65%以上。与传统单槽电解相比,双膜三室电解法具有较高电流效率和较低能耗,中隔室回收硫酸实现资源高效利用,具有明显的经济效益。
2) 对双膜三室电解槽的离子传输过程研究表明,电沉积金属锰联产EMD过程中阴极pH逐渐上升但增幅不大,Mn2+浓度的减少量用于在阴极析出锰,SO42-迁移进入中隔室;阳极Mn2+浓度下降,减少量大部分用于在阳极放电析出EMD,部分转化成Mn3+,还有微量Mn2+进入中隔室,H+迁移进入中隔室;中隔室内H+和 结合生成H2SO4,电解12 h后酸回收率最高可达73.08%。
结合生成H2SO4,电解12 h后酸回收率最高可达73.08%。
3) 三种离子交换膜电流效率从大到小顺序依次为TRJM-10W>LANRAN-AM>Ionsep-HC。其中TRJM-10W均相膜槽压最低,阴极电流效率可达86.25%,阳极电流效率可达70.6%,但阴极pH增幅最大,中隔室Mn2+浓度最高。因此,在使用双膜三室电解法应用于规模化锰电积生产时,应结合具体需求选择合适离子交换膜。
REFERENCES
[1] ZHANG D S, MA Z, SPASOVA M, YELSUKOVA A E, LU S W, FARLE M. Formation mechanism of laser-synthesized iron-manganese alloy nanoparticles, manganese oxide nanosheets and nanofibers[J]. Particle & Particle Systems Characterization, 2017, 34(3): 1-12.
[2] BANERJEE A, ZIV B, LUSKI S, AURBACH D, HALALAY I C. Increasing the durability of Li-ion batteries by means of manganese ion trapping materials with nitrogen functionalities[J]. Journal of Power Sources, 2017, 341: 457-465.
[3] DOSE W M, DONNE S W. Heat treated electrolytic manganese dioxide for primary Li/MnO2 batteries: Effect of manganese dioxide properties on electrochemical performance[J]. Electrochimica Acta, 2013, 105: 305-313.
[4] BISWAL A, TRIPATHY B C, SANJAY K, SUBBAIAH T, MINAKSHI M. Electrolytic manganese dioxide (EMD): A perspective on worldwide production, reserves and its role in electrochemistry[J]. RSC Advances, 2015, 5: 58255-58283.
[5] LIU R P, LIU H J, ZHAO X, QU J H, ZHANG R. Treatment of dye wastewater with permanganate oxidation and in situ formed manganese dioxides adsorption: Cation blue as model pollutant[J]. Journal of Hazardous Materials, 2010, 176(1/3): 926-931.
[6] YIN W X, HAN Y X, LIU Y, SHU F X. Electrowinning of manganese dioxide using Ti-Ru anode from chloride solution[J]. Journal of Northeastern University, 2007, 28(6): 855-858.
[7] TSURTSUMIA G S, KOIAVA N S, GOGISHVILI N S, ZARIDZE I T, KAKHNIASHVILI I B, GORELISHVILI G G, KVESELAVA V M, NIKOLEISHVILI P N. Simultaneous production of electrolytic metallic manganese and electrolytic manganese dioxide in an AMI 7001S anion exchange membrane electrochemical reactor[J]. Journal of the Electrochemical Society, 2015, 162(8): 96-103.
[8] 冯雅丽, 杜云龙, 李 辉, 周宇照, 王维大. 用离子膜电解槽无硒电沉积金属锰[J]. 湿法冶金, 2014, 33(3): 203-207.
FENG Ya-li, DU Yun-long, LI Hui, ZHOU Yu-zhao, WANG Wei-da. Non-selenium electrodeposition of metal manganese using ion membrane electrolyzer[J]. Hydrometallurgy of China, 2014, 33(3): 203-207.
[9] LLEA P, POPESCU I C, URDA M, ONICIU L. The electrodeposition of manganese from aqueous solutions of MnSO 4. Ⅳ: Electrowinning by galvanostatic electrolysis[J]. Hydrometallurgy, 1997, 46(1): 149-156.
[10] 黄齐茂, 王春平, 周 红, 胡学雷, 潘志权. 锰阳极泥回收制备硫酸锰工艺研究[J]. 有色金属(冶炼部分), 2010(6): 6-8.
HUANG Qi-mao, WANG Chun-ping, ZHOU Hong, HU Xue-lei, PAN Zhi-quan. The research on manganese anode slime recycled to produce manganese sulfate[J]. Nonferrous Metals(Extractive Metallurgy), 2010(6): 6-8.
[11] 郑 凡, 黄炳行, 闭伟宁, 朱 华. 阴离子交换膜无硒电解金属锰工艺及工业可行性探索[J]. 中国锰业, 2016, 34(5): 75-78.
ZHENG Fan, HUANG Bing-xing, BI Wei-ning, ZHU Hua. A study on non-selenium electrolytic process with anion exchange membrane electrolyzer[J]. China’s Manganese Industry, 2016, 34(5): 75-78.
[12] 牛莎莎, 王志兴, 郭华军, 李新海, 彭文杰, 胡启阳, 张云河. 电解锰阳极渣还原浸出锰[J]. 中国有色金属学报, 2012, 22(9): 2662-2666.
NIU Sha-sha, WANG Zhi-xing, GUO Hua-jun, LI Xin-hai, PENG Wen-jie, HU Qi-yang, ZHANG Yun-he. Reductive leaching of manganese from manganese anode slag[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(9): 2662-2666.
[13] 严 浩, 彭文杰, 王志兴, 李新海, 郭华军, 胡启阳. 响应曲面法优化电解锰阳极渣还原浸出工艺[J]. 中国有色金属学报, 2013, 23(2): 528-534.
YAN Hao, PENG Wen-jie, WANG Zhi-xing, LI Xin-hai, GUO Hua-jun, HU Qi-yang. Reductive leaching technology of manganese anode slag optimized byresponse surface methodology[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(2): 528-534.
[14] GONG J, ZHANGRI G. Electrodeposition and characterization of manganese coatings[J]. Journal of the Electrochemical Society, 2002, 149(4): 209-217.
[15] DUAN N, DAN Z G, WANG F, PAN C X, ZHOU C B, JIANG L H. Electrolytic manganese metal industry experience based China’s new model for cleaner production promotion[J]. Journal of Cleaner Production, 2011, 19(17/18): 2082-2087.
[16] 王三反, 周 键, 王 挺, 赵红晶, 张学敏, 李乐卓. 一种用于金属氯化物精炼的膜电积槽: 中国, CN202925116[P]. 2013-05-08.
WANG San-fan, ZHOU Jian, WANG Ting, ZHAO Hong-jing, ZHANG Xue-min, LI Le-zhuo. Electrowinning of metal chlorides in the membrane electrolytic cell: China, CN 202925116[P]. 2013-05-08.
[17] 李 韬, 王三反, 周 键. 离子膜电解法电沉积回收硫酸镍体系中金属镍的实验研究[J]. 材料导报, 2016, 30(S2): 432-435, 439.
LI Tao, WANG San-fan, ZHOU Jian. Experimental study of ion-exchange membrane electrolysis nickel sulfate electrowinning of nickel metal system[J]. Materials Review, 2016, 30(S2): 432-435, 439.
[18] TANAKA Y. Mass transport and energy consumption in ion-exchange membrane electrodialysis of seawater[J]. Journal of Membrane Science, 2003, 215(1): 265-279.
[19] SATA T. Studies on anion exchange membranes having permselectivity for specificanions in electrodialysis-effect of hydrophilicity of anion exchange membranes on permselectivity of anions[J]. Journal of Membrane Science, 2000, 167(1): 1-31.
[20] LEONARD K C, TEJEDOR-ANDERSON M L, ANDERSON M A. Nanoporous oxide coatings on stainless steel to enable water splitting and reduce the hydrogen evolution overpotential[J]. International Journal of Hydrogen Energy, 2012, 37(24): 18654-18660.
[21] ZHOU Jian, WANG San-fan, SONG Xiao-san. Electrodeposition of cobalt in double-membrane three- compartment electrolytic reactor[J]. Transactions of Nonferrous Metals Society of China, 2016, 26(6): 1706-1713.
[22] 王敬民. 电解金属锰阴极过程初探[J]. 中国锰业, 1994(1): 47-49.
WANG Jing-min. Approach on the cathode process of electolyte metal manganese[J]. China’s Manganese Industry, 1994(1): 47-49.
[23] 周 键, 王三反, 宋小三, 张学敏. 双膜三室电解槽中电沉积钴的离子传输[J]. 中国有色金属学报, 2016, 26(11): 2426-2432.
ZHOU Jian, WANG San-fan, SONG Xiao-san, ZHANG Xue-min. Ion transport for electrodeposition of cobalt in double-membrane three-compartment electrolytic cell[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(11): 2426-2432.
[24] 连锦明, 朱则善, 张其昕. 电解二氧化锰时电解液体系中间粒子的考察[J]. 福建师范大学学报(自然科学版), 1986, 2(4): 53-56.
LIAN Jin-ming, ZHU Ze-shan, ZHANG Qi-xin. A investigate of internzediates in depositing electrolytic manganese dioxide[J]. Journal of Fujian Normal University(Natural Science Edition), 1986, 2(4): 53-56.
[25] 孟 洪, 彭昌盛, 卢寿慈. 离子交换膜的选择透过性机 理[J]. 北京科技大学学报, 2002, 24(6): 656-659.
MENG Hong, PENG Chang-sheng, LU Shou-ci. Permselectivity mechanism of ion exchange membranes[J]. Journal of University of Science and Technology Beijing, 2002, 24(6): 656-659.
Ion transport process of double-membrane three-chamber electrodeposited metal-manganese co-production EMD
XU Qi1, WANG San-fan1, SUN Bai-chao2, ZHOU Jian1
(1. Engineering Research Center of Water Resources Utilization in Cold and Drought Region, Ministry of Education, School of Environmental and Municipal Engineering, Lanzhou Jiaotong University, Lanzhou 730070, China;
2. China Construction Steel Structure Co., Ltd., Siping 136000, China)
Abstract: In view of the problems of high energy consumption, low resource utilization and serious environmental pollution in the traditional single-slot electrolytic manganese or manganese dioxide, this work proposed a double-membrane three-chamber electrolysis method to achieve cathode electrodeposition of manganese while the anode was co-produced with electrolytic manganese dioxide, and the intermediate compartment electrochemically regenerated sulfuric acid. By analyzing the changes of ion concentration in each compartment, the feasibility of double-membrane three-chamber electrolysis was explored, and the effects of three ion exchange membranes on electrodeposition were compared. The results show that the double-membrane three-chamber electrolysis method can realize the electrodeposition of manganese metal and the simultaneous production of electrolytic manganese dioxide, and the cathode current efficiency can reach more than 80%, the anode current efficiency can reach more than 60%, and the acid recovery rate in the middle compartment is higher than 65%. Compared with Ionsep-HC and LANRAN-AM, the TRJM-10W homogeneous membrane has the lowest cell voltage. After 12 hours of electrolysis, the cathode current efficiency is 86.25%, the anode current efficiency is 70.6%, and the intermediate compartment acid recovery rate is 73.08%. However, the pH value of the catholyte increases the most, and the concentration of Mn2+ in the middle compartment is the highest.
Key words: electrolytic manganese dioxide; double-membrane three-chamber; current efficiency; ion transport
Foundation item: Project(21466019) by the National Natural Science Foundation of China; Project(LZJTU 201606) supported by the Excellent Platform Foundation of Lanzhou Jiaotong University, China
Received date: 2018-12-23; Accepted date: 2019-04-18
Corresponding author: WANG San-fan; Tel: +86-13150016917; E-mail: sfwang1612@163.com
(编辑 何学锋)
基金项目:国家自然科学基金资助项目(21466019);兰州交通大学优秀平台基金资助项目(LZJTU201606)
收稿日期:2018-12-23;修订日期:2019-04-18
通信作者:王三反,教授;电话:13150016917;E-mail:sfwang1612@163.com