Fe3+, Ce3+共掺杂纳米TiO2的相变及其降解水中CHCl3的催化性能
许金生1, 余润兰2, 冯泳兰1, 匡云飞1
(1. 衡阳师范学院 化学与材料科学系, 衡阳 421008;
2. 中南大学 资源加工与生物工程学院, 长沙 410083)
摘 要: 制备一系列Fe3+, Ce3+共掺杂的纳米TiO2, 并用X射线衍射仪进行表征。 与单一金属离子掺杂相比, 当x(Fe3+)=0.020和x(Ce3+)≈0.010时, Fe3+, Ce3+共掺杂不仅显著抑制纳米晶TiO2的相转化, 而且大大提高了其热稳定性。 在紫外灯辐照下, 用Fe3+, Ce3+共掺杂的纳米晶TiO2可降解水中的三氯甲烷, 表现出强的催化活性。 随着掺杂Fe3+的摩尔分数增大, x(Fe3+)=0.020时, CHCl3的降解率存在一个最佳值, 而随着掺杂Ce3+的摩尔分数增大, CHCl3的降解率先是急剧上升, 而x(Ce3+)>0.020时, 其增势趋缓。
关键词: 纳米二氧化钛; 稀土; 三氯甲烷; 过渡金属离子; 共掺杂; 光催化 中图分类号: O614
文献标识码: A
Phase transition of Fe3+, Ce3+ co-doped nanosized titania and its photocatalytic performance for degradation of CHCl3 in water
XU Jin-sheng1, YU Run-lan2, FENG Yong-lan1, KUANG Yun-fei1
(1. Department of Chemistry and Materials Science,Hengyang Normal University, Hengyang 421008, China;
2. School of Minerals Processing and Bioengineering,Central South University, Changsha 410083, China)
Abstract: A series of Fe3+, Ce3+ co-doped nano-TiO2 were prepared and characterized by XRD. Compared with one of Fe3+ or Ce3+ ions doping, co-dopants not only inhibit the phase transition of nanocrystalline TiO2 significantly, but also improve its thermal stability remarkably at x(Fe3+)=0. 020 and x(Ce3+)≈0. 010. Strong photocatalytic activity shows for the degradation of trichloromethane in water by the nano-TiO2 under irradiation of UV light. There is an optimum degradation of trichloromethane at x(Fe3+)=0.020. But the degradation of trichloromethane firstly increases rapidly, then it rises slowly when the mole fraction of Ce3+ is over 0.020.
Key words: nanosized titania; rare earth; trichloromethane; transition metal ions; co-doping; photocatalysis
氯化消毒以其工艺简单、 经济实用、 杀菌效果好而成为一般水厂净化水质的主要手段。 但是饮用水氯化后会产生以三氯甲烷为主的有机氯化物[1]。 这些物质大多具有致癌性, 故饮用水的氯化对人体健康的影响越来越被人们所关注[2]。
TiO2光催化氧化法可将有机物直接氧化分解成无毒的二氧化碳, 其光催化性质在环境治理及太阳能转化等领域有重要应用前景, 因而其制备及光催化性质的研究一直受到人们的广泛关注。 金属离子掺杂, 非金属氮、 碳、 硫、 硼等掺杂, 半导体复合或用光敏染料进行表面敏化, 可以扩展TiO2的光响应范围, 减少光生空穴和电子复合, 提高太阳光的吸收效率, 改善光催化性能[3-18]。 金属离子的单一掺杂的报道较多, 其中以Fe3+或稀土离子的掺杂效果比较好[5-6, 12, 14-15]。 Ce3+和Ce4+间容易发生氧化还原价态改变, 在体相和表面积累可变的氧空位, CeO2也被广泛用作催化剂的结构助剂和电子助剂, 以提高催化剂的催化活性、 选择性和热稳定性[7-8]。
本文作者采用Fe3+和稀土离子Ce3+对TiO2进行双金属离子同时掺杂, 制备一系列TiO2纳米材料, 系统研究这两种金属离子同时掺杂对二氧化钛纳米材料的影响, 探讨其对光催化降解水中CHCl3活性的影响。
1 实验
1.1 Fe3+, Ce3+双金属离子共掺杂的纳米二氧化钛的合成及表征
称取计算量的CeO2, 加入过量的H2O2和少量稀硝酸, 使CeO2还原为Ce3+, 徐徐蒸干, 然后加入适量异丙醇使其完全溶解; 称取一定量Fe(NO)3・9H2O, 用一定量的异丙醇溶解, 二者混合成溶液。 向上述混合溶液中加入一定量的聚乙二醇作分散剂, 在不断搅拌下加入钛酸丁酯至完全均匀透明, 置于60℃烘箱中得透明固体凝胶, 再在105℃继续加热24h后得透明干凝胶. 用高温控温炉在设定温度下煅烧1h后得到掺杂双金属离子的二氧化钛纳米材料样品。
首先固定Ce3+的摩尔分数为0.020, 依次改变Fe3+的摩尔分数, 样品编号分别为TFC1, TFC2, TFC3和TFC4, 对应于Fe3+的摩尔分数分别为0.0054, 0.011, 0.020和0.070, 然后再固定Fe3+的摩尔分数为0.020, 依次改变Ce3+的摩尔分数, 样品编号分别为TFC5, TFC6, TFC3和TFC7, 分别对应于Ce3+的摩尔分数分别为0.0050, 0.010, 0.020和0.070。 将样品TFC1至TFC7分别在650℃和800℃烧结, 以考察双金属离子配比对物相、 组成和晶粒的影响。 将Fe3+, Ce3+的摩尔分数都为0.020的TFC3样品分别在480, 550, 650, 800℃烧结, 以考察配比相同时, 温度对相变、 热稳定性和晶粒的影响。 采用Rigaku Dmax/2550VB+18kW转靶X射线粉末衍射仪测定物相和组成, 通过对Kα1和Kα2剥离, Scherrer方法校正, 测晶粒大小。 通过(101)和(200)面计算锐钛矿的晶格参数。
1.2 降解水中CHCl3的催化活性
将TFC1, TFC2, TFC3, TFC4, TFC5, TFC6和TFC7分别在500℃烧结, 用于研究不同的Fe3+, Ce3+配比掺杂的TiO2光催化分解CHCl3的活性。
在30cm×25cm×20cm的密闭容器的顶部, 装有一只30W ZSZD直管型石英紫外线低压汞灯, 辐射波长为253.7nm。 玻璃血清瓶中加入CHCl3浓度为6.17g/L的水溶液15mL, 再加入0.10g的催化剂, 立即用塞子塞紧并用蜡密封, 以防三氯甲烷挥发。 超声5min后, 置于该密闭容器中, 辐照0.5h。 用HP-GC气相色谱仪进行测量, 以峰面积计算CHCl3的含量。 根据下式计算CHCl3的降解率η:
η=100×(A 0-A)/A0
式中 A0和A分别为在相同条件下未加催化剂和加催化剂时紫外灯辐照后样品的峰面积。
2 结果与讨论
2.1 Fe3+, Ce3+双金属离子共掺杂的纳米二氧化钛的相变及热稳定性
2.1.1 掺杂离子组成固定时不同温度下纳米二氧化钛的热稳定性
]图1所示为Fe3+, Ce3+掺杂量皆为0.020(摩尔分数)时(样品TFC3)纳米TiO2在不同温度下的变化。

图1 Fe3+, Ce3+掺杂的TiO2在不同温度下的X射线衍射谱
Fig.1 XRD patterns of co-doped TiO2 with both Fe3+ and Ce3+ calcined at different temperatures for 1h in air
TiO2的锐钛矿为亚稳态, 随着温度的升高, 衍射峰的半峰宽变窄, 逐步向稳态金红石型转化, 粒径逐渐增大, 并在650℃开始出现金红石相。
当温度≤650℃时, 在2θ大约为30.7°处出现非常弱而宽的无定形板钛矿相的衍射峰, 没有观测到CeO2晶相。 Ce3+和Ce4+的离子半径分别为0.103nm和0.097nm, 比Ti4+离子半径(0.068nm) 大得多, Ce4+或Ce3+离子不能进入TiO2晶格形成CeO2-TiO2固溶体[7-8]。 这个板钛矿是Ti4+离子进入CeO2 并晶格取代而形成的无定形TiO2-CeO2固溶体[7-8]。
800℃时全部转化为金红石相, 粒径急剧增大, 并在2θ=28.38°, 33.08°和47.48°处出现新相CeO2, 而2θ大约为30.7°处非常弱而宽的无定形相衍射峰(板钛矿)消失。 这个峰位(2θ=28.38°)比与文献[7]报道的CeO2相(2θ=28.65°)稍小。 这是CeO2相中存在少量Ce3+的缘故, 这个TiO2-CeO2实际上是无定形TiO2-CeO2-x固溶体[7]。
2.1.2 Fe3+离子浓度对纳米二氧化钛相变及热稳定性的影响
图2所示为固定Ce3+掺杂量为0.020而改变Fe3+的摩尔分数时, 共掺杂纳米TiO2在不同温度下的变化。
纯的无定形TiO2完全晶化的温度一般约为400℃[10, 12, 17], 500℃时TiO2金红石相明显[12, 17], 600℃时完全为TiO2金红石相[12]。 从图2可以看出: 当焙烧温度为650℃时, Fe3+的摩尔分数小于0.020时(TFC1和TFC2), TiO2全为锐钛矿相; 当Fe3+的摩尔分数等于0.020时(TFC3), 出现金红石相, 此时锐钛矿相为91.8%, 金红石相为8.2%; 当Fe3+的摩尔分数达0.070时(TFC4), 锐钛矿相为39.6%, 金红石相为68.1%; 从TFC1到TFC4的(101)面的2θ(分别为25.36°, 25.30°, 25.24°, 25.18°)逐渐减小, Fe3+离子进入了TiO2的晶格中并发生了晶格取代[17]。 800℃时TFC1和TFC2仍含相当量的锐钛矿相。 很明显, Ce3+掺杂量为0.020而改变Fe3+的摩尔分数时, TiO2的相转变温度及热稳定性提高了, Fe3+离子的掺杂量也提高了, 总的金属离子掺杂量提高了。 这主要是TiO2表面的TiO2-CeO2-x固溶体抑制了锐钛矿TiO2向金红石TiO2的成核过程[17, 18], 双金属离子掺杂产生了协同效应。
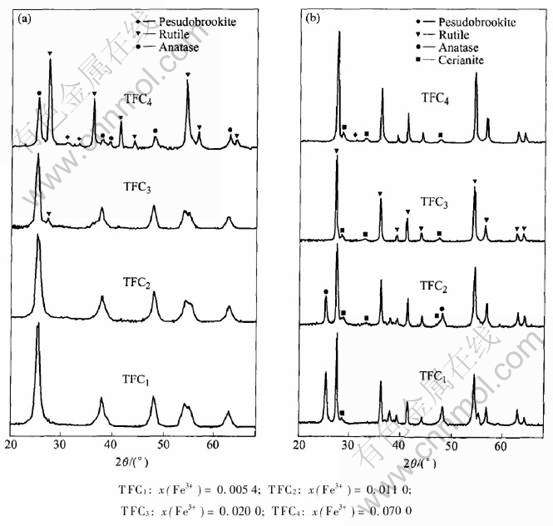
图2 在650℃和800℃煅烧1h后x(Ce3+)=0.020时不同铁掺杂浓度TiO2材料的X射线衍射谱
Fig.2 XRD patterns of co-doped titania samples with both Ce3+(x=0.020)and different amount of Fe3+ calcined at 650℃(a) and 800℃(b) for 1 h in air respectively
从图2可以看出: 无论是650℃还是800℃, Fe3+的摩尔分数达0.070时(TFC4)皆出现Fe2TiO5相[12]; 当焙烧温度为650℃时, Fe3+为各种掺杂浓度下, Ce高度分散在TiO2上, 而焙烧温度为800℃时, 皆出现CeO2相。 可见, 当掺杂量x(Ce3+)≥0.020时, Ti4+离子晶格取代Ce而形成的TiO2-CeO2-x无定形固溶体, 并在800℃时完全氧化结晶为CeO2相, 这是它的固有特性。
2.1.3 Ce3+离子浓度对纳米二氧化钛相变及热稳定性的影响
图3所示为固定Fe3+掺杂量为0.020而改变Ce3+的摩尔分数时, 共掺杂纳米TiO2在不同温度下的变化。
从图3可以看出, 掺杂的铈离子浓度变化比铁离子浓度变化对TiO2的影响更复杂些。 当温度为650℃时, 随着Ce/Ti比的增大, 锐钛矿相逐渐减少, 并在2θ大约为30°和52°处出现宽的无定形相衍射峰, 当x(Ce3+)=0.070时, 出现宽而弱的板钛矿峰(2θ=30.7410), 未见CeO2峰。 这与Ce3+单掺杂TiO2的结果一致[8]; 而TiO2的晶胞体积分别为0.1394, 0.1354, 0.1358和0.1386nm3。 这却与n(Ce)/n(Ti)=0.20时达到最大值的报道不一致[8]。 这种差异与双金属离子共掺杂有关: 由于存在x=0.020的Fe3+离子掺杂, 扩展了TiO2的晶格, 以致x〈0.0050的低浓度Ce3+离子能在TiO2的晶格中填隙[18]; 随着Ce3+离子掺杂浓度增大, 部分出现TiO2的晶格取代, Ti4+离子同时进入CeO2 晶格形成了brookite固溶体, 抑制了TiO2的晶核的生长。
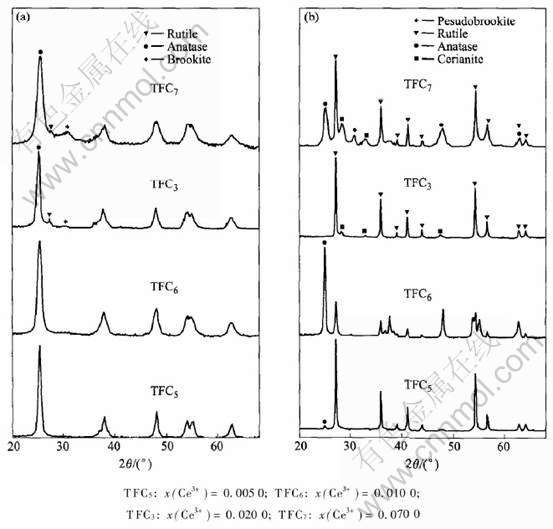
图3 在650℃和800℃煅烧1h后x(Fe3+)=0.020时不同铈掺杂浓度TiO2材料的X射线衍射谱
Fig.3 XRD patterns of co-doped titania samples with x(Fe3+)=0.020 and different amounts of cerium calcined at 650℃(a) and 800℃(b) for 1h in air, respectively
800℃时Ce3+氧化成CeO2是它的固有特性, 填隙在TiO2晶格内的极少量Ce3+反而造成了TiO2锐钛矿相向金红石相的转变(TFC5); 随着Ce3+的摩尔分数增加, TiO2晶格的部分取代和表面brookite固溶体的形成, 抑制了TiO2锐钛矿相向金红石相的转变(TFC6); 当x(Ce3+)≥0.020, 界面CeO2晶相出现, TiO2锐钛矿相转化为金红石相(TFC3); x(Ce3+)=0.070时出现了4个晶相(TFC7), 这与大量的CeO2氧化析出并造成了TiO2崩溃重组以及CeO2包覆等原因有关, 同时与样品制备中的凝胶、 干燥过程有关[8]。
因此, Fe3+, Ce3+共掺杂不仅明显抑制了纳米TiO2的A-R相转化, 而且显著提高了它的热稳定性。 最佳的掺杂配比是摩尔分数x(Fe3+)为 0.020和x(Ce3+)大约为0.010。 其掺杂机制有待更深入的研究。
2.2 降解水中CHCl3的催化活性
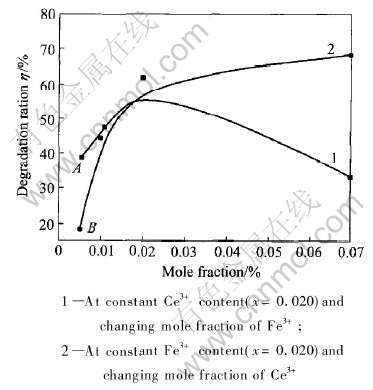
图4 不同配比的Fe3+, Ce3+共掺杂样品在500℃煅烧1 h 后光催化降水中CHCl3的降解率
Fig.4 Degradation rate of CHCl3 in water by co-doped titania with different proportion of Fe3+ and Ce3+ calcined at 500℃for 1 h in air
从图4可以看出, 固定Ce3+(x=0.020)的掺杂量而改变Fe3+掺杂量时(曲线1), 随着掺杂Fe3+的摩尔分数增大, TiO2对水中CHCl3的降解率先上升后下降。 这是因为掺杂量过低, 捕获电子或空穴的浅势阱数量不够, 光生电子-空穴不能有效分离; 掺杂量过大, 使得金属粒子可能成为电子-空穴的复合中心, 增大电子与空穴的符合几率[6, 9]。 由于Fe3+, Ce3+掺杂引起TiO2晶格膨胀, 有利于更多的Fe3+掺入TiO2中, 这个最佳值为x(Fe3+)=0.020, 比Choi等[3]报道的单一Fe3+最佳掺杂量0.5%(摩尔分数)大。 固定Fe3+(x=0.020)的掺杂量而改变Ce3+掺杂量时(曲线2), 随着掺杂Ce3+的摩尔分数增大, TiO2对水中CHCl3的降解率先是急剧上升的, 然后增势趋缓。 稀土掺杂二氧化钛光催化活性的提高是由于稀土f 轨道与被降解底物的配位作用而使得TiO2材料表面被降解物的浓度提高所致, 掺杂稀土离子的浓度越大, 其光催化效率提高的程度应越高[4, 7]。 Ce3+掺杂浓度的升高主要是增强了与H2O中O的配位作用, 增加了半导体光生自由基的有效浓度, 从而提高了催化活性[6, 9]。
图4中A点(x(Ce3+)=0.02, x(Fe3+)=0.0054)的催化活性比B点(x(Fe3+)=0.02, x(Ce3+)=0.0050)的催化活性要高得多, 就是因为B点的Ce3+掺杂浓度很低, 铈离子主要是晶隙内填充, 几乎没有Ce3+/Ce3+的配位中心; 而A点掺杂的Ce3+浓度较高, 铈离子与铁离子的协同作用, 形成了晶格取代并在TiO2表面形成了TiO2-CeO2-x固溶体, 稀土离子的配位中心增多, Ce3+和Ce4+间容易发生氧化还原价态改变, 在体相和表面积累可变的氧空位, 有利于光生电子的迁移[7-8]。 高Ce3+浓度掺杂的C点(c(Fe3+)=0.02, x(Ce3+)=0.070 )的催化活性增势变缓, 这与晶体表面吸附趋于饱和, 半导体光生自由基的表观复合几率增大有关[6, 9]。
REFERENCES
[1]RooK J J. Formation of haloforms during chlorination of natural waters[J]. J Water Treament Exam, 1974, 23: 234-238.
[2]Black B D, Harrington G W, Singer P C. Reducing cancer risks by improving organic carbon removal[J]. J Awaa, 1996, 88(6): 40-43.
[3]Choi W, Termin A, Hoffmann M R. The role of metal ion dopants in quantum-sized TiO2: correction between photo reactivity and charge carrier recombination dynamics[J]. J Phys Chem, 1994, 9: 13669-13679.
[4]张华星, 张玉红, 徐永熙, 等. 铽( Ⅲ) 掺杂TiO2 纳米材料相转移和光催化性质研究[J]. 化学学报, 2003, 61(11): 1813-1818.
ZHANG H X, ZHANG Y H, XU Y X, et al. Phase transition and photocatalytic properties of terbium doped nanosized titanium dioxide[J]. Acta Chimica Sinica, 2003, 61(11): 1813-1818.
[5]张玉红, 徐永熙, 王彦广. Fe3+, Si4+掺杂TiO2纳米材料相变和热稳定性研究[J]. 无机化学学报, 2003, 19(10): 1099-1103.
ZHANG Yu-hong, XU Yong-xi, WANG Yan-guang. Effect of Fe3+, Si4+ dopants on the phase transformation and thermal stability of nanocrystalline TiO2[J]. Chinese Journal of Inorganic Chemistry, 2003, 19(10): 1099-1103.
[6]赵德明, 金宁人. 过渡金属Fe3+离子掺杂改性TiO2的光催化性能研究进展[J]. 浙江工业大学学报, 2005, 33(2): 165-168.
ZHAO De-ming, JIN Ning-ren. Photocatalytic performance of TiO2 modified by doped transition metal Fe3+ ion[J]. Journal of Zhejiang University of Technonogy, 2005, 33(2): 165-168.
[7]Reddy B M, Khan A. Nanosized CeO2-SiO2, CeO2-TiO2, and CeO2-ZrO2 mixed oxides: influence of supporting oxide on thermal stability and oxygen storage properties of ceria[J]. Catalysis Surveys from Asia, 2005, 9(3): 155-160.
[8]朱华青, 秦张峰, 王建国. CeO2/TiO2混合氧化物及Pd/ CeO2/TiO2催化剂的氧化还原性能[J]. 催化学报, 2005, 26(5): 377-382.
ZHU Hua-qing, QIN Zhang-feng, WANG Jian-guo. Redox property of CeO2-TiO2 mixed oxide and Pd/ CeO2/TiO2 catalyst[J]. Chinese Journal of Catalysis, 2005, 26(5): 377-382.
[9]姜月顺, 李铁津. 光化学[M]. 北京: 化学工业出版社, 2005: 97-114.
JIANG Yue-shun, LI Tie-jing. Photochemistry[M]. Beijing: Chemical Industry Press, 2005: 97-114.
[10]Chang C C, Lin C K, Chan C C, et al. Photocatalytic properties of nano-crystalline TiO2 thin film with Ag additions[J]. Thin Solid Films, 2006, 494: 274-278.
[11]Yoon K H, Noha J S, Kwon C H. Photocatalytic behavior of TiO2 thin films prepared by sol-gel process[J]. Materials Chemistry and Physics, 2006, 95: 79-83.
[12]Vujii N S, Music G. Synthesis and microstructural properties of Fe-TiO2 nanocrystalline particles obtained by a modified sol-gel method[J]. Journal of Sol-Gel Science and Technology, 2004, 30: 5-19.
[13]Yoon K H, Noha J S, Kwon C H, et al. Photocatalytic behavior of TiO2 thin films prepared by sol-gel process[J]. Materials Chemistry and Physics, 2006, 95: 79-83.
[14]Yu J G, Yu H G, Ao C H, et al. Preparation, characterization and photocatalytic activity of in situ Fe-doped TiO2 thin films[J]. Thin Solid Films, 2006, 496: 273-280.
[15]肖美群, 杨建纯, 沈嘉年, 等. 添加Fe3+对二氧化钛薄膜吸收光谱及光催化活性的影响[J]. 材料科学与工程学报, 2005, 23(1): 48-52.
XIAO Mei-qun, YANG Jian-chun, SHEN Jia-nian, et al. Effect of Fe3+ dopen of titanium dioxide film on absorption spectra and photo catalysis[J]. Journal of Materials Science and Engineering, 2005, 23(1): 48-52.
[16]Wong M S, Chou H P, Yang T S. Reactively sputtered N-doped titanium oxide films as visible-light photocatalyst[J]. Thin Solid Films, 2006, 494: 244 -249.
[17]Wu X H, Wei Q, Jiang Z H. Influence of Fe3+ ions on the photocatalytic activity of TiO2 films prepared by micro-plasma oxidation method[J]. Thin Solid Films, 2006, 496: 288-292.
[18]West A R. 固体化学及其应用[M]. 苏勉曾, 等译. 上海: 复旦大学出版社, 1989: 272-278.
West A R. Solid State Chemistry and Its Applications[M]. Su Mian-zeng, et al, transl. Shanghai: Fudan University Press, 1989: 272-278.
(编辑陈爱华)
基金项目: 湖南省自然科学基金资助项目(05JJ30015)
收稿日期: 2006-05-08; 修订日期: 2006-09-11
通讯作者: 余润兰, 教授;电话: 0731-8836943; E-mail: YRL715@sina.com