稀有金属 2014,38(06),1030-1034 DOI:10.13373/j.cnki.cjrm.2014.06.015
异丙醇协助Al2O3包覆LiMn2O4合成及高温电化学性能研究
张雁南 张英杰 董鹏 夏书标 杨瑞明
昆明理工大学材料科学与工程学院
摘 要:
采用溶胶凝胶法, 以硫酸铝、异丙醇 (IPA) 为原料对Li Mn2O4进行包覆。合成了含2% (质量分数) Al2O3表面包覆的Li Mn2O4电极材料。利用场发射扫描电镜 (FESEM) 对制备材料的形貌进行表征。结果显示, 异丙醇协助包覆后材料表面呈现均匀分布的Al2O3颗粒。在55℃, 3.0~4.5 V, 1C充放电测试表明, IPA协助包覆可以显著提高Li Mn2O4正极材料高温下的循环稳定性。以异丙醇协助的Al2O3包覆Li Mn2O4材料作为正极, 100次循环容量保持率为87.3%, 而未加异丙醇包覆后的Li Mn2O4材料100次循环容量保持率为82.2%, 未经过包覆的材料只有74.1%。不同倍率恒流充放电测试结果表明, 异丙醇协助包覆能够改善Li Mn2O4的倍率性能, 在5C和10C的放电倍率下的放电比容量分别达到了102.1和91.0 m Ah・g-1。通过电感耦合等离子体质谱仪 (ICP) 测试样品在电解液中Mn的溶解浓度。结果显示, 高温 (55℃) 储存20 d后, 异丙醇协助包覆的Li Mn2O4材料中Mn在电解液中的浓度仅为58.7×10-6, 远远低于未加异丙醇包覆的和未经过包覆的。
关键词:
异丙醇;尖晶石锰酸锂;包覆;容量保持率;
中图分类号: O611.4;O646
作者简介:张雁南 (1985-) , 男, 云南昆明人, 博士研究生, 研究方向:锂电材料;E-mail:zyn_legolas@163.com;;张英杰, 教授;电话:0871-65152692;E-mail:yingjie@kmust.edu.cn;
收稿日期:2013-11-15
基金:国家自然科学基金项目 (51264016);云南省教育厅项目 (2010[493]) 资助;
Synthesis and Electrochemical Performance of Isopropyl Alchol ( IPA) Assisted Al2O3 Coated LiMn2O4 at Elevated Temperature
Zhang Yannan Zhang Yingjie Dong Peng Xia Shubiao Yang Ruiming
Faculty of Materials Science and Engineering, Kunming University of Science and Technology
Abstract:
A series of spinel Li Mn2O4 coated with 2% Al2O3 were synthesized by Al2 ( SO4) 3and isopropyl alcohol ( IPA) assisted sol-gel process. The morphologies of the as-prepared materials were characterized by field emission scanning electron microscopy ( FESEM) . The results showed that Al2O3 particles uniformly distributed on the surface of the spinel Li Mn2O4 prepared by IPA assisted process. Galvanostatic charge-discharge test indicated that the IPA-assisted coating could significantly improve the cycle stability of spinel Li Mn2O4 at elevated temperature. The capacity retention of the Al2O3-IPA-coated Li Mn2O4 as cathode material was 87. 3% after100 cycles ( condition: 3. 0 ~ 4. 5 V, 1C, 55 ℃) , Which was considerably higher than the value of 82. 2% for the coated Li Mn2O4 prepared without IPA assisted process and 74. 1% for the uncoated one. Tests with different discharge rates showed that the Al2O3-IPA-coated Li Mn2O4 produced excellent rate capability: 102. 1 m Ah・g- 1at 5C and 91. 0 m Ah・g- 1at 10 C. After the storage at 55 ℃for 20 d, the Mn dissolution from the spinel samples was tested by inductive coupled plasma emission spectrometer ( ICP) . The solubility of Mn for Al2O3-IPA-coated Li Mn2O4 was only 58. 71 × 10- 6, which was much lower than that for the ones without IPA assisted process and uncoated.
Keyword:
isopropyl alcohol; spinel LiMn2O4; coating; capacity retention;
Received: 2013-11-15
自Goodenough等首次提出尖晶石化合物Li Mn2O4以来[1], Li Mn2O4作为一种极具潜力的正极材料被广泛研究。尖晶石Li Mn2O4作为锂离子电池正极活性材料具有成本低廉、原材料丰富、常温循环性能好, 安全性能优异等优点[2,3,4,5]。但随着电动工具在不同环境下使用, 特别在高温下循环使用, Li Mn2O4中的Mn3+会发生歧化反应, 生成的Mn2+溶解于电解液中使电极中的活性物质丧失, 这是使电池容量衰减的重要原因[6,7,8]。据研究发现, 通过对材料进行表面包覆处理可以改善Li Mn2O4的高温循环稳定性[9,10,11,12,13,14]。
通过表面包覆提高Li Mn2O4的循环稳定性, 必须改善尖晶石与电解液之间的界面关系[15], 氧化铝因为其良好的成膜性能, 及在电解液中稳定性能佳, 电催化活性低, 价格便宜, 被认为是一种适合产业化应用的Li Mn2O4包覆材料。本文没有采用传统昂贵的有机溶剂和金属醇盐作为介质和反应前驱体[16,17], 而是采用水作溶剂, 硫酸铝作为包覆盐, 异丙醇作为添加剂, 采用水溶胶法对Li Mn2O4进行表面包覆Al2O3处理。基本原理是利用了异丙醇分子结构中含有羟基 (-OH) 可以作为很好的锚固官能团[18,19], 与水解后的铝盐形成牢固氢键结合, 避免了成膜过程中龟裂或颗粒团聚现象的产生, 显著提高了材料在高温中充放电循环的容量保持率, 同时抑制了Mn的溶解。
1 实验
选取Al2 (SO4) 3・18H2O (与Li Mn2O4按质量比2∶100) 与2.5 g异丙醇溶解于200 ml去离子水中, 用稀氨水调p H值至8.0, 充分搅拌下, 缓慢加入50 g Li Mn2O4, 持续搅拌加热升温至75℃, 保温12h至大部分溶剂蒸干, 将形成的凝胶放入120℃干燥箱中干燥, 烘干后于700℃下进行热处理6 h, 得到异丙醇协助的Al2O3包覆Li Mn2O4的最终样品C。按照上述相似步骤, 在未加入异丙醇的条件下制备Al2O3包覆Li Mn2O4材料, 定义为样品B。将未包覆的Li Mn2O4材料定义为样品A。
采用S-4700场发射扫描电镜观察粉末颗粒的表面形貌。样品在电解液中Mn的溶解用 (Thermo-6000) ICP进行定量测试。将5 g样品在真空手套箱内存储于50 ml电解液内, 并用塑封机密封后在55℃下分别储存10, 20 d后测试。
正极材料的电化学性能测试选用2025扣式电池。正极材料, 粘接剂PVDF, 导电乙炔黑以质量比85∶9∶6, 制浆涂膜, 在100℃下真空干燥后得到电池正极;采用锂片做负极;选取电解液EC+DMC+DEC (1∶1∶1) , 在充满氩气的手套箱中组装成2025式扣式电池。在3.0~4.5 V之间、60℃下做循环充放电测试。电池测试系统为LAND-CT2001A。
2 结果与讨论
图1为包覆前后材料的扫描电镜图, 图1 (c) 为在异丙醇协助条件下, 采用溶胶凝胶法对Li Mn2O4进行氧化铝包覆材料的SEM图;图1 (b) 为未加入异丙醇情况下, 以硫酸铝为原料在水溶液体系对Li Mn2O4进行氧化铝包覆材料 (样品B) 的SEM图, 图1 (a) 为未包覆材料的SEM图。从图1中可以看出, 异丙醇协助溶胶凝胶法包覆的材料, 其包覆层更加均匀。

图1 样品的扫描电镜 (SEM) 图Fig.1 SEM images of samples
(a) Sample A; (b) Sample B; (c) Sample C
从图2中可以看出, 未经包覆处理的材料 (样品A) 在55℃, 3.0~4.5 V, 1.0C充放电条件下, 100次循环后, 容量由最初的114.22降至84.59 m Ah・g-1, 容量保持率仅有74.1%。样品B经过包覆后, 在3.0~4.5 V, 1.0C充放电条件下, 100次循环后, 容量由最初的113.93降至93.91 m Ah・g-1, 容量保持率提高到82.2%。样品C经过异丙醇协助包覆后, 循环稳定性最好, 在3.0~4.5 V, 1.0C充放电条件下, 100次循环容量保持率达到87.3%。
图3是在55℃不同倍率下充放电得到的放电容量与循环次数的关系图。对于未包覆样品A、Al2O3-和IPA协助Al2O3包覆样品B和C 3种材料在50次充放电循环后的容量保持率分别为85.8%, 91.1%和93.4%, 其中IPA协助包覆样品C在5.0C和10.0C的放电倍率下的放电比容量分别达到了102.1和91.0 m Ah・g-1, 明显高于没有IPA协助包覆和未包覆的样品。充放电测试表明, 循环性能和倍率性能的提高与包覆作用分不开, 其中异丙醇的加入使Al2O3在材料表面形成了更加致密的离子传导膜, 能够改善电极材料与电解液的界面性质, 增加材料的倍率性能和循环寿命。
根据图4可以看出, 55℃储存条件下所有样品中Mn在电解液中的溶解都随时间的增加而增大。储存20 d后, 未包覆的样品A在电解液中Mn浓度最高, 达到219.7×10-6。这与Blyr等[20]对Li1.05Mn2O4在55℃电解液中0%SOC储存后的研究结论一致, 长时间储存下离子交换反应导致锰的溶解并形成低电位的缺陷尖晶石相, 不同于锂离子电化学脱嵌反应形成的Mn O2, 这种缺陷尖晶石相没有脱/嵌锂活性, 从而造成材料的容量损失。通过溶胶凝胶法包覆后样品B中Mn在电解液中的溶解量大大降低。以异丙醇协助条件下包覆后的样品C, Mn在电解液中的浓度仅为58.7×10-6。原因是样品表面由于包覆了保护膜, 减轻了样品与电解液之间的相互作用, 进而可以减少Mn的溶解量。而异丙醇的加入, 其中羟基 (-OH) 作为锚固官能团与铝盐形成牢固的化学键结合, 在尖晶石表面形成均一稳定的分子包覆层, 更好地抑制Li Mn2O4颗粒表面与电解液直接接触。
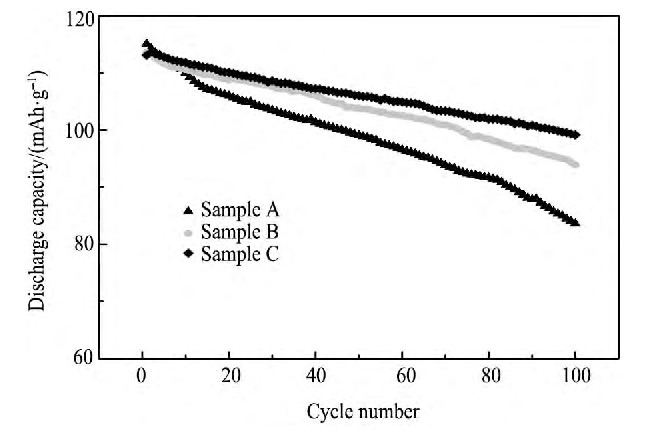
图2 不同样品在55℃, 1.0C充放电循环的容量/循环次数图Fig.2Cycling performance of bare and IPA assisted coated Li Mn2O4at 55℃and 1.0C charge and discharge rate
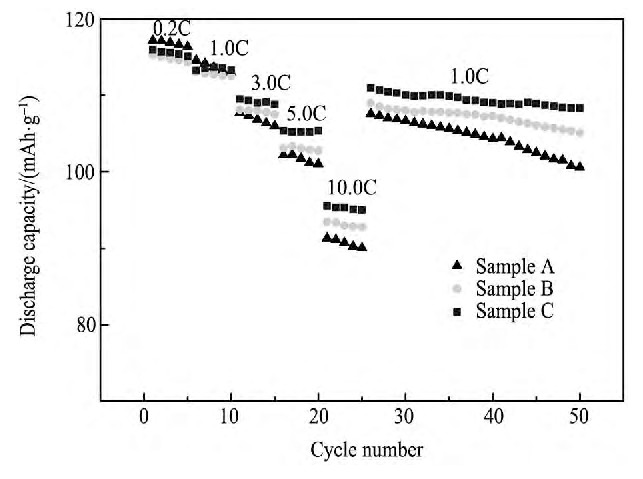
图3 不同样品在55℃, 不同倍率下充放电循环的容量/循环次数图Fig.3Cycling performance of bare and IPA assisted coated Li Mn2O4at different charge and discharge rates
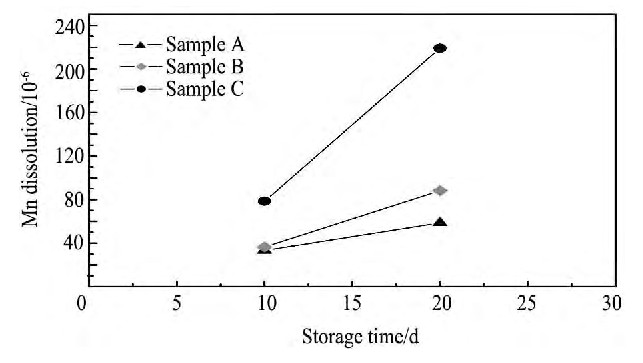
图4 55℃下不同工艺包覆后样品储存后锰元素的溶解量与储存时间的关系Fig.4 Relation of storage time and Mn dissolution for different samples at 55℃
3 结论
采用异丙醇协助溶胶凝胶法对Li Mn2O4进行Al2O3包覆, 发现包覆后的材料比未包覆的材料循环稳定性明显提高。异丙醇协助包覆的材料, 在55℃, 1C充放电条件下, 100次循环后, 容量保持率为90.1%;ICP的测试结果显示, 高温储存后, 异丙醇协助包覆的Li Mn2O4材料中Mn的溶解量低于未加异丙醇和未经过包覆的。该方法可以应用于尖晶石锰酸锂正极材料改性的工业生产中。
参考文献
[1] Thackeray M M, David W I F, Bruce P G, Goodenough J B.Lithium insertion into manganese spinels[J].Mater.Res.Bull., 1983, 18 (4) :461.
[2] Kim Daesoo, Park Sangjin, Chae Oh-B, Ryu Ji-Heon, Kim Young-Ugk, Yin Ri-Zhu, Seung M-Oh.Re-deposition of manganese species on spinel Li Mn2O4electrode after Mn dissolution[J].J.Electrochimica Soc., 2012, 159 (3) :A193.
[3] Tarascon J M, Armand M.Issues and challenges facing rechargeable lithium batteries[J].Nature, 2001, 414:359.
[4] Hassoum J, Lee K S, Sun Y K, Scrosati B.An advanced lithium ion battery based on high performance electrode materials[J].J.Am.Chem.Soc., 2011, 133:3139.
[5] Ma P P, Liu Z J, Xia J H, Chen Y, Hu P, Lu Z C.Synthesis with spray-dry method and study on compounds of x Li Fe PO4-y Li3V2 (PO4) 3as cathode material for lithium battery[J].Chinese Journal of Rare Metals, 2012, 36 (1) :105. (马平平, 刘志坚, 夏建华, 陈宇, 胡朴, 卢志超.喷雾干燥法合成锂离子电池复合正极材料x Li Fe PO4-y Li3V2 (PO4) 3及性能研究[J].稀有金属, 2012, 36 (1) :105.)
[6] Song M Y, Ahn D S, Park H R.Capacity fading of spinel phase Li Mn2O4with cycling[J].Journal of Power Sources, 1999, 83 (1-2) :57.
[7] Cho J.Correlation of capacity fading of Li Mn2O4cathode material on 55℃cycling with their surface area measured by a methylene blue adsorption[J].Solid State Ionics, 2001, 138 (3-4) :267.
[8] Wu H C, Guo Z Z, Wen H P, Yang M H.Study the fading mechanism of Li Mn2O4battery with spherical and flake type graphite as anode materials[J].Journal of Power Sources, 2005, 146 (1-2) :736.
[9] Cao J, Cao G, Yu H, Xie J, Zhao X.Synthesis and electrochemical performance of YF3-coated Li Mn2O4cathode materials for Li-ion batteries[J].Rare Metals, 2011, 30 (1) :39.
[10] Liu Y, Guo H, Li X, Wang Z.Improving the electrochemical performance of Li Mn2O4/graphite batteries using Li F additive during fabrication[J].Rare Metals, 2011, 30 (2) :120.
[11] Fey G T K, Lu C Z, Kumar T P.Solid-state synthesis and electrochemical characterization of Li MyCr0.5-yMn1.5O4 (M=Fe or Al;0.0<y<0.4) spinels[J].Mater.Chem.Phys., 2003, 80:309.
[12] Singhal R, Das S R, Tomar M S, Osbert Ovideo, Santander Nieto, Ricardo E, Melgarejo, Katiyar Ram-S.Synthesis and characterization of Nd doped Li Mn2O4cathode for Li-ion rechargeable batteries[J].Journal of Power Sources, 2007, 164 (2) :857.
[13] Yu L, Qiu X, Xi J, Zhu W, Chen L.Enhanced highpotential and elevated-temperature cycling stability of Li Mn2O4cathode by Ti O2modification for Li-ion battery[J].Eletrochim.Acta, 2006, 51 (28) :6406.
[14] Hu G R, Deng X R, Peng Z D, Du K.Comparison of Al PO4and Co3 (PO4) 2coated Li Ni0.8Co0.2O2cathode materials for Li-ion battery[J].Electrochimica Acta, 2008, 53 (5) :2567.
[15] K Edstrom K, Gustafsson T, Thomas J O.The cathode-electrolyte interface in the Li-ion battery[J].Electrochimica Acta, 2004, 50 (2-3) :397.
[16] Lee S W, Kim K S, Moon H S, Kim H J, Cho B W, Cho W, Ju J B, Park J W.Electrochemical characteristics of Al2O3-coated lithium manganese spinel as a cathode material for a lithium secondary battery[J].Journal of Power Sources, 2004, 126 (1-2) :150.
[17] Park S B, Shin H C, Lee W G, Cho W I, Jang H.Improvement of capacity fading resistance of Li Mn2O4by amphoteric oxides[J].Journal of Power Sources, 2008, 180 (1) :597.
[18] Sequeira S, Casanova C, Cabrita E J.Deacidificaiton of paper using dispersions of Ca (OH) 2nanoparticles in isopropanol.Study of efficiency[J].Journal of Cultural Heritage, 2006, 7 (4) :264.
[19] Li W, Yang Z H, Zhang G, Qin M.Heat-treated polyacrylonitrile (PAN) hollow fiber strctured packings in isopropanol (IPA) /water distillation with improved thermal and chemical stability[J].Ind.Eng.Chem.Res., 2013, 52:6492.
[20] Blyr A, Sigala C, Amatucci G, Guyomard D, Chabre Y, Tarascon J M.Self-discharge of Li Mn2O4/C Li-ion cells in their discharged state[J].Journal of Electrochemical Society, 1998, 145 (1) :194.