文章编号:1004-0609(2008)02-0349-07
Acidithiobacillus ferrooxidans菌株的分离及阴离子对其亚铁氧化活性的影响
吴学玲,蒋 莹,邱冠周,刘新星,翁文筠
(中南大学 资源加工与生物工程学院,长沙 410083)
摘 要:采用连续稀释法分别从江西德兴铜矿、湖北大冶铜矿和广西大厂这3处酸性矿坑水样品中分离得到三株嗜酸性短杆状细菌,其形态及生理特征与嗜酸性氧化亚铁硫杆菌相似,16S rRNA系统学分析进一步证实这种细菌属于硫杆菌属的嗜酸性氧化亚铁硫杆菌。研究表明:阴离子对嗜酸氧化亚铁硫杆菌的Fe2+氧化能力具有一定影响,其影响顺序由大到小依次为: >Cl->
>Cl-> ;不同菌株对阴离子的耐受能力存在明显的差异。
;不同菌株对阴离子的耐受能力存在明显的差异。
关键词:嗜酸氧化亚铁硫杆菌; ;Cl-;
;Cl-;
中图分类号:Q 939.97 文献标识码:A
Isolation of Acidithiobacillus ferrooxidans strains and effect of anions on their ferrous ions oxidation capacities
WU Xue-ling, JIANG Ying, QIU Guan-zhou, LIU Xin-xing, WENG Wen-yun
(School of Resources Processing and Bioengineering, Central South University, Changsha 410083, China)
Abstract: By successive diluting method three acidicbacillus strains were isolated from the samples of acid mine drainage taken from Dexing Copper Mine in Jiangxi province, Daye Copper Mine in Hubei province and Dachang Copper Mine in Guangxi province. The three Acidithiobacillus strains are similar to Acidithiobacillus ferrooxidans in shapes and biological characters. 16S rRNA gene sequence analysis further confirms that the three bacteria strains are Acidithiobacillus ferrooxidans. The results show that anions obviously impact the oxidation capacity of ferrous ions of these bacteria with an effect order as:  >Cl->
>Cl-> . And their tolerances to anions are obviously different from each other.
. And their tolerances to anions are obviously different from each other.
Key words: Acidithiobacillus ferrooxidans;  ; Cl-;
; Cl-; 
自1947年Temple和Colmer发现氧化亚铁硫杆菌以来,嗜酸氧化亚铁硫杆菌(Acidithiobacillus ferrooxidans,以前叫氧化亚铁硫杆菌[1],简称A. ferrooxidans菌)已经成为工业生物浸出各种有价金属的主要菌种之一,广泛应用在煤炭脱硫、工业废气、石油废气的处理和生活污水净化等领域[2-3]。研究人员对其生理生化性质,分子遗传性能及能量代谢机制等各方面都展开深入的研究[1-3]。但是,从自然界分离得到的嗜酸氧化亚铁硫杆菌往往存在对亚铁氧化活性低、对重金属离子敏感等缺点,因而限制了其应用。目前,研究各种离子对嗜酸氧化亚铁硫杆菌的活性的影响主要集中在3类金属离子上[4],即:1) 嗜酸氧化亚铁硫杆菌生长所需的营养离子,如Fe2+和Mg2+ 等[5-6];2) 对嗜酸氧化亚铁硫杆菌浸出硫化矿起抑制作用的重金属离子,如Cu2+、Ni2+和Co2+等[7-8];3) 对氧化亚铁硫杆菌浸出硫化矿起催化作用的重金属离子,如Ag+和Hg2+等[9-10]。然而研究人员在研究这些金属阳离子对嗜酸氧化亚铁硫杆菌活性的影响时,往往忽略了阴离子的影响。
本文作者采用连续稀释法从江西德兴铜矿和湖北大冶铜矿、广西大厂这3处酸性矿坑水样品中分离得到三株菌并对其进行鉴定,研究了这三株菌对重金属离子的耐受能力及不同锌盐中阴离子对细菌的影响,了解各种因素对浸矿细菌氧化性能的影响,为获得浸矿细菌的最优生长条件提供依据。
1 实验
1.1 菌种来源和分离纯化
实验样品分别来自江西德兴、湖北大冶和广西大厂的酸性矿坑水。
样品富集和纯化采用改进的9 K培养基 [11-12],其成分组成如下(g/L):(NH4)2SO4 3.0,KCl 0.1,K2HPO4 0.5,MgSO4?7H2O 0.5,Ca(NO3)2 0.01,FeSO4?7H2O 22.4,蒸馏水1 000 mL,pH 2.0~2.5。
菌种的分离纯化采用液体稀释分离法[13]。取42支试管分3组编号,每支试管中加入9 K培养基9 mL,分别接种来自3个矿区的矿坑水样本1 mL于1号管,摇匀后从1号管取1 mL菌液到对应的2号管中,摇匀后取1 mL菌液到对应的3号管,如此依次到对应的13号管。14号管中加入1 mL无菌水。所有试管置于温度为30 ℃、转速为160 r/min的恒温震荡器中培养12 d。从已变色的接种浓度最低的试管中取1 mL菌液作为原始菌液,再次稀释、培养。如此稀释培养6次得到纯化细菌。
1.2 菌种对亚铁及硫的氧化活性研究
配制9 K培养基[12],调节pH=2.0,置于30 ℃,160 r/min的摇床中培养,通过溶液颜色变化情况来判断菌种氧化亚铁的活性。另外配置9 K培养基,用1.0 g/L升华硫代替9 K培养基中的硫酸亚铁,调节pH=2.0,置于30 ℃,160 r/min的摇床中培养,通过测定培养液pH值的变化来判断细菌氧化硫的情况。
1.3 纯化菌株的16SrDNA鉴定
将菌种扩大培养后收集菌体,提取细菌DNA,通过16S rDNA PCR后,纯化PCR产物,委托北京三博远志生物技术有限责任公司完成序列测定。
1.4 不同金属盐对细菌Fe2+氧化活性的影响
在250 m L容量的锥形瓶中加入95 mL灭菌的9 K培养基,菌液接种量为5%,接种菌液浓度为1×108/mL。每种盐按照表1中浓度配比分别加入不同的锥形瓶中,分别以不接菌的正常9 K培养基作为空白对照。
表1 锌离子浓度配比
Table 1 Concentration gradient of zinc ions(g/L)

锥形瓶置于30 ℃, 160 r/min条件下振荡培养,定期取出0.1 mL培养液,用重铬酸钾滴定法测定培养液中Fe2+的含量变化[14]。
通过测定培养液中Fe2+氧化率,研究上述锌盐中金属离子及不同阴离子对细菌亚铁氧化能力的影响。实验过程中取样减少的培养液用9 K基本盐溶液补充,蒸发的水分用灭菌蒸馏水补充。
2 实验结果
2.1 菌种富集及分离纯化
从江西德兴、湖北大冶和广西大厂这3处的矿坑水中稀释分离获得的3株纯化菌株分别命名为:DX、DY和DC。
2.2 实验菌株对亚铁和硫的氧化
实验中所用培养基为9 K培养基,pH=2.0,温度为30 ℃,摇床转速为160 r/min,接种量为5%,接种菌液浓度为1×108/mL。在相同条件下,培养液颜色变成桔红色的先后顺序依次是DC、DY和DX。从菌液颜色的变化可以看出,3株菌均能氧化Fe2+生成Fe3+ ,其氧化能力DC菌的活性最高,DX菌的活性相对较低。
配制9 K培养基,用1.0 g/L升华硫代替9 K培养基中的硫酸亚铁,调节pH=2.0,置于30 ℃,160 r/min的摇床中培养,通过测定培养液pH值的变化来判断细菌氧化硫的情况。在相同培养条件下,3株菌的pH值均有所降低。 培养11 d后,DX、DY和DC的pH值分别下降到1.47、1.71和1.51,说明这3株菌均能氧化硫,其氧化硫能力由大到小的顺序为:DX>DC>DY。
2.3 菌种鉴定
将分离得到的菌株制样进行微观形貌观察,其形貌如见图1所示。由图可知:这3株菌都呈短杆状,长度约为1.0~1.5 μm,宽度约为0.4~0.5 μm,单个或多个连成链状,与嗜酸氧化亚铁硫杆菌的形态相同[13]。

图1 菌株的SEM照片
Fig.1 SEM photographs of strains: (a) DC strain; (b) DX strain; (c) DY strain
采用这3株菌的16S rDNA序列数据在GenBank核酸序列数据库中进行同源序列搜索(BLAST search),比较供试菌株与已知嗜酸氧化亚铁硫杆菌属其它菌株相应序列的相似程度[15]。结果表明,DX与Acidithiobacillus ferrooxidans strain ATCC23270的16S rDNA的同源性为99%,DY与Acidithiobacillus ferrooxidans strain YN 的16S rDNA的同源性为98%,DC与Acidithiobacillus ferrooxidans strain TF-49的16S rDNA的同源性为99%。结合分离菌株的生理生化特性和16S rDNA序列比对分析结果,可以确定该3株菌均为嗜酸氧化亚铁硫杆菌(Acidithiobacillus ferrooxidans,简称A. ferrooxidans菌)。
2.4 A. ferrooxidans菌在不同阴离子锌盐条件下的生长活性
2.4.1 A. ferrooxidans DX菌在不同阴离子锌盐条件下的生长活性
不同浓度的硫酸锌、氯化锌和硝酸锌对DX A. ferrooxidans菌氧化Fe2+活性的影响分别见图2、3和4。由图2可见,当硫酸锌浓度小于12 g/L时, 对细菌氧化Fe2+的能力基本无影响,细菌在41 h内完全氧化9 K培养基中的Fe2+;当硫酸锌浓度范围为12~48 g/L时细菌对Fe2+氧化能力受到抑制,硫酸锌浓度为24 g/L时,在62 h内完全氧化9 K培养基中的Fe2+,而硫酸锌浓度达到48 g/L 时,细菌经过158 h的停滞期后,迅速氧化Fe2+。
对细菌氧化Fe2+的能力基本无影响,细菌在41 h内完全氧化9 K培养基中的Fe2+;当硫酸锌浓度范围为12~48 g/L时细菌对Fe2+氧化能力受到抑制,硫酸锌浓度为24 g/L时,在62 h内完全氧化9 K培养基中的Fe2+,而硫酸锌浓度达到48 g/L 时,细菌经过158 h的停滞期后,迅速氧化Fe2+。

图2 A. ferrooxidans DX 菌作用下含不同浓度硫酸锌9 K培养基中的亚铁氧化率
Fig.2 Ferrous ions microbial oxidation rate in 9 K medium containing different concentrations of zinc sulfate by A. ferrooxidans strain DX
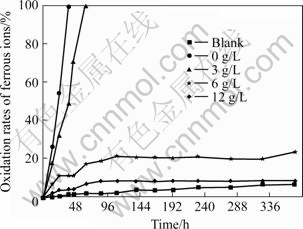
图3 A. ferrooxidans DX 菌作用下含不同浓度氯化锌9 K培养基中的亚铁氧化率
Fig.3 Ferrous ions microbial oxidation rate in 9 K medium containing different concentrations of zinc chlorate by A. ferrooxidans strain DX

图4 A. ferrooxidans DX 菌作用下含不同浓度硝酸锌的9 K培养基中的亚铁氧化率
Fig.4 Ferrous ions microbial oxidation rate in 9 K medium containing different concentrations of zinc nitrate by A. ferrooxidans strain DX
由图3可知:当氯化锌浓度小于3 g/L时,Cl-对细菌氧化Fe2+的能力无明显影响,细菌在64 h内完全氧化9K培养基中的Fe2+;当氯化锌浓度大于3 g/L时,细菌生长受到抑制,对Fe2+的氧化能力下降,随氯化锌浓度的增加,对Fe2+氧化速率急剧下降,当氯化锌浓度为6 g/L时,培养374 h时Fe2+氧化率仅为23.8%。
由图4可知,当硝酸锌浓度小于3 g/L时,细菌对Fe2+氧化所受影响较小,在97 h内完全氧化9 K培养基中的Fe2+;当硝酸锌浓度为6 g/L时,细菌生长受抑制,Fe2+氧化率几乎为零。
2.4.2 A. ferrooxidans DY菌在不同阴离子锌盐条件下的生长活性
不同浓度的硫酸锌、氯化锌和硝酸锌对A. ferrooxidans DY菌亚铁氧化活性的影响分别见图5、6和7。由图5可见,当硫酸锌浓度小于12 g/L时,细菌对Fe2+氧化基本不受影响,在46 h内完全氧化9 K培养基中的Fe2+;当硫酸锌浓度约为12~48 g/L时,Fe2+氧化速率随锌盐浓度上升而减缓,当硫酸锌浓度为48 g/L时,细菌在134 h内完全氧化9 K培养基中的Fe2+。

图5 A. ferrooxidans DY 菌作用下含不同浓度硫酸锌的9 K培养基中的亚铁氧化率
Fig.5 Ferrous ions microbial oxidation rate in 9 K medium containing different concentrations of zinc sulfate by A. ferrooxidans strain DY

图6 A. ferrooxidans DY菌作用下含不同浓度氯化锌的9 K培养基中的亚铁氧化率
Fig.6 Ferrous ions microbial oxidation rate in 9 K medium containing different concentrations of zinc chlorate by A. ferrooxidans strain DY
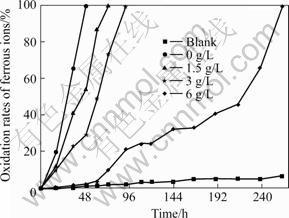
图7 A. ferrooxidans DY菌作用下含不同浓度硝酸锌的9 K培养基中的亚铁氧化率
Fig.7 Ferrous ions microbial oxidation rate in 9 K medium containing different concentrations of zinc nitrate by A. ferrooxidans strain DY
由图6可知:在氯化锌中,锌盐浓度小于3 g/L时,Cl-对细菌氧化Fe2+速率影响较小,细菌在50 h内完全氧化9 K培养基中的Fe2+;锌盐浓度为6 g/L时,细菌生长受到抑制,Fe2+氧化没有对数期,氧化速率缓慢,后期几乎不再氧化Fe2+,培养203 h后Fe2+氧化率达到67.41%;锌盐浓度为12 g/L时,细菌生长基本完全被抑制,Fe2+氧化率几乎为零。
由图7可知,当硝酸锌浓度小于3 g/L时, 对细菌氧化Fe2+的速率影响较小,细菌在92 h内完全氧化9 K培养基中的Fe2+;当硝酸锌浓度为6 g/L时,细菌经过214 h的延滞期后,迅速氧化Fe2+,262 h内完全氧化9 K培养基中的Fe2+。
对细菌氧化Fe2+的速率影响较小,细菌在92 h内完全氧化9 K培养基中的Fe2+;当硝酸锌浓度为6 g/L时,细菌经过214 h的延滞期后,迅速氧化Fe2+,262 h内完全氧化9 K培养基中的Fe2+。
2.4.3 A. ferrooxidans DC菌在不同阴离子锌盐条件下的生长活性
不同浓度的硫酸锌、氯化锌和硝酸锌对A. ferrooxidans DC菌氧化Fe2+活性的影响分别见图8、9和10。由图8可见:当硫酸锌浓度小于12 g/L时, 对细菌氧化Fe2+的速率影响较小,细菌在61 h内完全氧化9 K培养基中的Fe2+;当硫酸锌浓度约为12~48 g/L时,亚铁氧化速率随锌盐浓度上升而减缓,硫酸锌浓度为24 g/L时,细菌在85 h内完全氧化9 K培养基中的Fe2+,而当硫酸锌浓度达到48 g/L,经过278 h延滞期后,在306 h内完全氧化9 K培养基中的Fe2+。
对细菌氧化Fe2+的速率影响较小,细菌在61 h内完全氧化9 K培养基中的Fe2+;当硫酸锌浓度约为12~48 g/L时,亚铁氧化速率随锌盐浓度上升而减缓,硫酸锌浓度为24 g/L时,细菌在85 h内完全氧化9 K培养基中的Fe2+,而当硫酸锌浓度达到48 g/L,经过278 h延滞期后,在306 h内完全氧化9 K培养基中的Fe2+。

图8 A. ferrooxidans DC菌作用下含不同浓度硫酸锌的9 K培养基中的亚铁氧化率
Fig.8 Ferrous ions microbial oxidation rate in 9 K medium containing different concentrations of zinc sulfate by A. ferrooxidans strain DC
由图9可知:氯化锌浓度小于3 g/L时,Cl-对细菌氧化Fe2+的影响较小,细菌在86 h内完全氧化9 K培养基中的Fe2+;氯化锌浓度为6 g/L时,细菌生长受到抑制,亚铁氧化没有对数期,亚铁氧化速率缓慢,后期几乎不再氧化Fe2+,培养336 h后Fe2+氧化率达到65.73%;氯化锌浓度达到12 g/L时,细菌生长基本完全抑制,Fe2+氧化率几乎为零。

图9 A. ferrooxidans DC菌作用下含不同浓度氯化锌的9 K培养基中的亚铁氧化率
Fig.9 Ferrous ions microbial oxidation rate in 9 K medium containing different concentrations of zinc chlorate by A. ferrooxidans strain DC
从图10可得知,硝酸锌浓度小于3 g/L时, 对细菌氧化Fe2+速率影响较小,细菌在97 h内完全氧化9 K培养基中的Fe2+;随硝酸锌浓度的增加,细菌氧化Fe2+速率逐渐减小;当硝酸锌浓度等于6 g/L时,细菌经过214 h的延滞期后,迅速氧化Fe2+,在336 h内完全氧化9 K培养基中的Fe2+。
对细菌氧化Fe2+速率影响较小,细菌在97 h内完全氧化9 K培养基中的Fe2+;随硝酸锌浓度的增加,细菌氧化Fe2+速率逐渐减小;当硝酸锌浓度等于6 g/L时,细菌经过214 h的延滞期后,迅速氧化Fe2+,在336 h内完全氧化9 K培养基中的Fe2+。

图10 A. ferrooxidans DC菌作用下含不同浓度硝酸锌的9K培养基中的亚铁氧化率
Fig.10 Ferrous ions microbial oxidation rate in 9 K medium containing different concentrations of zinc nitrate by A. ferrooxidans strain DC
3 结果与分析
硫酸根离子是一种常见的阴离子,广泛存在于矿山酸性矿坑水中。氧化亚铁硫杆菌在有氧和酸性条件下,能将亚铁氧化成高铁、元素硫氧化成硫酸,或将金属硫化物直接氧化成硫酸盐。硫酸根离子最初被认为是一个连接亚铁离子和细菌的配合体,进一步研究发现在铁氧化中从铁硫团到铜离子的电子传递链中起作用。从图2、5和8可以看出,A. ferrooxidans DX、DY、DC 菌都能在浓度为48 g/L的ZnSO4环境中生长并氧化Fe2+。其中,A. ferrooxidans DX菌完全氧化Fe2+时间约为217 h,停滞期约为182 h;A. ferrooxidans DY菌完全氧化Fe2+时间约为134 h,停滞期约为109 h;A. ferrooxidans DC菌完全氧化Fe2+时间约为306 h,停滞期约为230 h。由此可知,三株菌耐受 能力由大到小的顺序为:DY>DX>DC。
能力由大到小的顺序为:DY>DX>DC。
较高浓度的氯化物是一个已知的细胞生长和铁氧化抑制剂。它是一个细胞色素c还原酶的抑制剂。1963年有报告指出当氯化物浓度达到0.14 mol/L就会对细菌产生毒害作用。在本实验中,A. ferrooxidans DX、DY、DC菌在3 g/L的ZnCl2中都能正常生长并氧化Fe2+,当ZnCl2浓度达到6 g/L时,三株菌的生长受到不同程度的影响,培养基中的Fe2+也没有完全被氧化。当ZnCl2浓度为3 g/L时,A. ferrooxidans DX 、DY、 DC菌完全氧化Fe2+时间分别约为64、50、85 h;当ZnCl2浓度为6 g/L时,A. ferrooxidans DX菌培养374 h后Fe2+氧化率为23.76%,A. ferrooxidans DY菌培养203 h后Fe2+氧化率达67.41%,A. ferrooxidans DC菌培养336 h后亚铁氧化率为65.73%。这些数据说明,在相同培养条件下,三株菌耐受Cl-能力为:DY>DC>DX。
较高浓度的硝酸根也是一种能抑制A. ferrooxidans菌氧化亚铁的阴离子。A. ferrooxidans菌株对低浓度的硝酸盐也很敏感。增加硝酸盐浓度将完全抑制Fe2+氧化。在3 g/L的Zn(NO3)2环境中,A. ferrooxidans DX 、DY和DC菌完全氧化Fe2+时间分别约为97、92和97 h,相差不大;而在6 g/L的Zn(NO3)2环境中,A. ferrooxidans DX菌的生长完全被抑制,Fe2+几乎不被氧化,A. ferrooxidans DY、DC菌能生长并将Fe2+完全氧化,Fe2+完全被氧化时间分别为262 h和336 h,停滞期分别为166 h和214 h。实验说明,A. ferrooxidans DX菌耐受硝酸锌能力较弱,A. ferrooxidans DC、DY菌较强。
分析3株细菌对阴离子的耐受能力发现,3株菌对ZnSO4的最大耐受浓度都可以达到48 g/L,而对ZnCl2、Zn(NO3)2的耐受浓度仅为3 g/L或6 g/L,说明了A. ferrooxidans DX、DY和DC菌对ZnSO4的抗性比ZnCl2、Zn(NO3)2强。在6 g/L的ZnCl2环境中,三株菌都没有正常生长,Fe2+也没有完全被氧化;而在相同浓度的Zn(NO3)2环境中,A. ferrooxidans DC、DY菌能完全氧化Fe2+,A. ferrooxidans DX菌的生长完全被抑制。另外,在3 g/L的锌盐溶液中,加入ZnCl2时Fe2+完全氧化时间比相同情况下加入Zn(NO3)2的短。因此,ZnCl2比Zn(NO3)2对这3株A. ferrooxidans 菌的影响相对较大。
以上结果表明,阴离子对A. ferrooxidans菌的生长动力学有很大影响,在 、Cl-和
、Cl-和 这3种阴离子中,
这3种阴离子中, 的影响相对较小,Cl-和
的影响相对较小,Cl-和 的影响相对较大。而且不同的菌株对这3种阴离子的抗性也有差异,A. ferrooxidans DY菌抗3种阴离子的能力较强。
的影响相对较大。而且不同的菌株对这3种阴离子的抗性也有差异,A. ferrooxidans DY菌抗3种阴离子的能力较强。
4 结论
1) 不同的阴离子对嗜酸氧化亚铁硫杆菌生长动力学有明显影响,其影响弱到强的顺序为: <Cl-<
<Cl-< 。
。
2) 对A. ferrooxidans DX、DY和DC这3株菌,在9 K培养基中细菌活性由大到小的顺序为:DC>DY>DX,其中DY菌抗 、Cl-及
、Cl-及 离子能力相对较强,其次为DC和DX。
离子能力相对较强,其次为DC和DX。
REFERENCES
[1] Kelly D P, Wood A P. Reclassification of some species of Thibacillus to the newly designated genera Acidithiobacillus gen.nov. ,Halothibacillus gen.nov. and Thermithiobacillus gen.nov.[J]. International Journal of Systematic and Evolutionary Microbiology, 2000, 50: 511-516.
[2] 耿 冰, 郑宇, 邸进申. 氧化亚铁硫杆菌的生物学特性研究进展[J]. 生物技术, 2004, 14(2): 71-74.
GENG Bing, ZHENG Yu, DI Jin-shen. The biological characteristics of Thiobacillus ferrooxidans progress[J]. Biotechnology, 2004, 14(2): 71-74.
[3] 邓恩建, 杨朝晖, 曾光明, 徐峥勇. 氧化亚铁硫杆菌的研究概况[J]. 黄金科学技术, 2005, 13(5): 8-12.
DENG En-jian, YANG Zhao-hui, ZENG Guang-ming, XU Zheng-yong. General situation in Thiobacillus ferrooxidans[J]. Gold science and Technology, 2005, 13(5): 8-12.
[4] 刘 清, 徐伟昌, 张 宇. 重金属离子对氧化亚铁硫杆菌活性的影响[J]. 铀矿冶, 2004, 23(3): 155-157.
LIU Qing, XU Wei-chang, ZHANG Yu. Effect of heavy metal ions the activity of Thiobacillus ferrooxidans[J]. Uranium Mining and Metallurgy, 2004, 23(3): 155-157.
[5] 何良菊, 李秀艳, 周建民, 魏德洲. Fe2+、NH4+对氧化亚铁硫杆菌氧化黄铁矿的影响[J]. 黄金学报, 1999, 1(4): 278-280.
HE Liang-ju, LI Xiu-yan, ZHOU Jian-ming, WEI De-zhou. The effects of Fe2+,  on the oxidation of pyrite by Thiobacillus ferrooxidans[J]. Gold Journal, 1999, 1(4): 278-280.
on the oxidation of pyrite by Thiobacillus ferrooxidans[J]. Gold Journal, 1999, 1(4): 278-280.
[6] 李洪枚, 柯家骏. Mg2 +对氧化亚铁硫杆菌生长活性的影响[J] . 中国有色金属学报, 2000, 4(10): 576-578.
LI Hong-mei, KE Jia-jun. Effect of Mg2 + on the growth and activity of Thiobacillus ferrooxidans[J]. The Chinese Journal of Nonferrous Metal, 2000, 4(10): 576-578.
[7] 李洪枚, 柯家骏. Cu2+对氧化亚铁硫杆菌生长活性的影响[J] . 黄金, 2000, 21(6): 27-29.
LI Hong-mei, KE Jia-jun. Effect of Cu2 + on the growth and activity of Thiobacillus ferrooxidans[J]. Gold, 2000, 21(6): 27-29.
[8] 李洪枚, 柯家骏. Ni2+和Co2+对氧化亚铁硫杆菌活性的影响[J] . 有色金属, 2000, 52(1): 49-54.
LI Hong-mei, KE Jia-jun. Effect of Ni2+ and Co2+ on activity of Thiobacillus ferrooxidans[J]. Nonferrous Metals, 2000, 52(1): 49-54.
[9] 汪模辉, 谭龙华, 王 俊, 缪 辉, 陈昌荣. 金属离子在细菌浸取金属硫化矿中的催化作用[J]. 应用化学, 1997, 14(5): 55-58.
WANG Mo-hui, TANG Long-hua, WANG Jun, MIAO Hui, CHENG Chang-rong. Catalysis of metal ions in bacterial leaching of metal sulphide minerals[J]. Chinese Journal of Applied Chemistry, 1997, 14(5): 55-58.
[10] 胡岳华, 张在海, 邱冠周, 王淀佐. Ag+在细菌浸出中的催化作用研究[J]. 矿冶工程, 2001, 21(1): 24-28.
HU Yue-hua, ZHANG Zai-hai, QIU Guan-zhou, WANG Dian-zuo. Catalystic effect of Ag+ on bacterial laching―A study[J]. Mining and Metallurgical Engineering, 2001, 21(1): 24-28.
[11] Das A, Modak J M, Natarajan K A. Studies on multi-metal ion tolerance of Thiobacillus ferrooxidans [J]. Minerals Engineering, 1997, 10(7): 743-749.
[12] WU Xue-ling, DING Jian-nan, GAO Jian, LIU Xin-xing, QIU Guan-zhou. Isolation and identification of metal-resistant iron-oxidizing bacteria[J]. Minerals & Metallurgical Processing, 2007, 24(1): 57-60.
[13] 胡岳华, 康自珍. 氧化亚铁硫杆菌的细菌学描述[J]. 湿法冶金, 1996(4): 36-39.
HU Yue-hua, KANG Zi-zhen. The bacteria Thiobacillus ferrooxidans description[J]. Hydrometallurgy, 1996(4): 36-39.
[14] 张在海. 铜硫化矿生物浸出高效菌种选育及浸出机理[D]. 长沙: 中南大学, 2002.
ZHANG Zai-hai. The screening and breeding of high effective bacteria for bioleaching of copper sulfide minerals and its leaching mechanism[D]. Changsha: Central South University, 2002.
[15] Stephen F A, Engene V K. Iterated profile searches with PSI-BLAST―a tool for discovery in protein databases[J]. Trends in Biochemical Science, 1998, 23(11): 444-447.
基金项目:国家自然科学基金创新群体研究基金资助项目(50321402);中南大学研究生教育创新工程基金资助项目(040113 )
收稿日期:2007-05-07;修订日期:2007-07-06
通讯作者:邱冠周,教授,博士;电话:0731-8836944; E-mail: xueling0714@yahoo.com.cn
(编辑 龙怀中)