难处理铜钴合金的氧化酸浸出
王多冬,赵中伟,陈爱良,陈星宇,霍广生,李洪桂
(中南大学 冶金科学与工程学院,湖南 长沙,410083)
摘 要:采用硫酸和盐酸的混合酸在有氧化剂存在的常压条件下对磨细后的铜钴合金进行浸出。试验结果表明:在溶液初始酸度为5.0~6.5 mol/L,硫酸与盐酸摩尔比较低,酸过量系数φH为1.2,氧化剂加入量ψn为理论量的1.2倍,反应温度为80 ℃,反应时间为70 min,搅拌速度为200~300 r/min的条件下,铜钴浸出率均能达到97%以上,浸出过程中不会有硅胶产生,过滤性能良好,实验重现性好。
关键词:铜钴合金;氧化浸出;浸出率;氧化剂;硫酸;盐酸
中图分类号:TF111.31, TF235.212 文献标识码:A 文章编号:1672-7207(2009)05-1188-06
Oxidative leaching of refractory Cu-Co white alloy in acid solution
WANG Duo-dong, ZHAO Zhong-wei, CHEN Ai-liang, CHEN Xing-yu, HUO Guang-sheng, LI Hong-gui
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: The atmospheric pressure leaching tests for milled Cu-Co alloy from Africa were studied by the mixed acid solution of sulfuric acid and hydrochloric acid with oxidant. The experimental results show that more than 97% of Cu and Co can be reached under the following condition that initial acidity is 5.0-6.5 mol/L, excessive acid coefficient φH and oxidant quality ψn are 1.2 times as the theoretic quality, reaction time is 70 min, and stirring rate is 200-300 r/min at the lower mole ratio of sulfuric acid to hydrochloric acid and at 80 ℃. The formation of silica gel can be prevented under modified experimental condition. Slurry can be easily filtrated and there is no silica gel produced. The experiments can be repeated well.
Key words: Cu-Co white alloy; oxidative leaching; leaching recovery; oxidant; sulfuric acid; hydrochloric acid
世界钴资源较丰富,据2005 年统计,储量达到700 万t,储量基础为1 300万t。世界钴储量集中分布于刚果(金)、澳大利亚、古巴、赞比亚、新喀里多尼亚、俄罗斯和加拿大等国,这些国家的钴储量总和约占世界总储量的95%以上[1-2]。中国是钴资源贫乏国家,一般含钴品位平均仅0.02%左右,个别为0.05%~0.08%。世界上最主要的钴资源国家刚果(金)和赞比亚的铜钴矿,一般含钴品位为0.1%~0.5%,高的达到2%~3%,比我国高十几倍到几十倍。我国由于含钴品位偏低,回收工艺比较复杂,导致钴精矿回收率低且生产成本高[3]。近年来,我国经济保持稳定、快速发展的态势,带动了镍、铜、钴消费的大幅度增长,但是,受矿产资源条件制约,我国铜、钴矿山的原料生产增长速度缓慢,铜、钴矿产品进口量逐步上升,例如,2004年我国共进口钴精矿143.594 kt,比2003年增加72%,供不应求的矛盾日益突出,成为目前钴消费量最大的国家,导致国内钴矿产品产量远不能满足要求,大部分依赖进口。铜钴合金是目前刚果(金)钴铜矿石深加工产品的主要形式之一[3],因而它将是我国今后从非洲进口的主要钴原料之一。研究合理处理铜钴合金的工艺和方法显得日益紧迫和重要。铜钴合金基本上是钴、铜、铁的三元合金。自铜钴合金中提取分离铜、钴的难度很大,主要表现在合金的溶解过程中。国外多采用硫酸加压浸出工艺或电溶处理铜钴合金[4-5]。芬兰的OMG公司是世界上最早处理铜钴合金的钴生产公司;另一家处理铜钴合金的公司是赞比亚的谦比西钴冶炼厂,采用硫酸加压浸出,产出CuSO4和CoSO4溶液,然后,分别进入电铜、电钴生产流程[6-8]。由于加压浸出产量小、对设备要求苛刻,因此,采用的厂家少。彭忠东等[9-10]利用“造渣熔炼―浸出”方法处理Cu-Co-Fe 合金,在1 300 ℃添加CaCO3 造渣焙烧,用H2SO4 溶液高温浸出,钴的浸出率为95%,在此基础上添加Na2SO3造渣焙烧后,再用浓硫酸高温浸出,钴浸出率升高到97%。尽管CaCO3和Na2SO3均为工业常用原料,钴浸出率能达到97%,但要,经过火法处理,工艺繁琐。张忠平等[11-13]用硫酸、硝酸、盐酸将钴原料中金属溶成混合盐溶液或者在进行稀硫酸浸出时,往溶液中通入氯气,强化合金的浸出,但是硝酸容易分解、氯气容易溢出,造成环境污染。喻正军等[15-17]采用硫酸介质作电解液,将合金作阳极,铜板作阴极,当电流通过电解槽时,阳极中的金属和金属硫化物溶解,铜离子将会在阴极得到电子而形成电铜。由于铜在阴极上沉积,溶液中含铜量一般很少,因此,在很大程度上减轻了以后硫酸盐的净化作业,但是,此法耗电量大。微生物浸出 法[17-18]是利用某些微生物或其代谢物对某些矿物进行氧化、还原、溶解、吸附等,从矿石浸出金属或从水中回收金属。采用此法所得的钴浸出率低,一般只有76%左右。本文作者为了寻求一种浸出效率高,经济合理且对环境无污染的浸出工艺,提出采用混酸(硫酸加盐酸混合酸)加氧化剂法的方案对铜钴合金进行浸出。
1 实 验
1.1 实验原料
本实验所用原料为刚果(金)进口的铜钴合金,是一种黄褐色带金属光泽的粉末。其含量,激光粒度分析和物相分析结果分别如表1、表2和图1所示。
表1 铜钴合金成分
Table 1 Component of Cu-Co white alloy
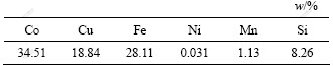
表2 铜钴合金物质组成分析结果
Table 2 Chemical phase analysis of Cu-Co white alloy

从表 2 可以看出,铜钴合金各元素基本上均是以金属单质相存在。可溶性金属离子、金属氧化物及其硫化物含量均低于1%。从XRD分析[3, 7]可知,合金中铜、钴、铁的主要存在形式为:CoxSiy,FexSiy,CoxFeyOz,Fe-Co-Cu固溶体,Cu单质。
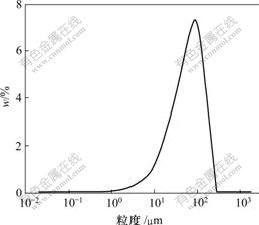
图1 铜钴合金粉激光粒度分布
Fig.1 Laser particle size analysis of Cu-Co white alloy powder
从图1可以看出:粒度呈正态分布,粒径D50 = 75 μm。(D50表示样品的累计粒度分布百分数达到50%时所对应的粒径)。
1.2 实验方法
将水、硫酸和盐酸按照一定摩尔比混合,再将已经破碎好的铜钴合金粉末50 g加入其中,机械搅拌(转速为400 r/min),加入一定量的氧化剂,在水浴中维持一定的反应温度,待反应一段时间后,将料浆过滤、洗涤,浸出渣烘干,最后分析渣中铜、钴、铁金属含量。
按照以下公式计算铜、钴、铁金属浸出率:
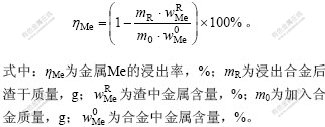
1.3 分析检测
将铜钴合金浸出渣通过王水溶解,再稀释,利用原子吸收(3510-a型)分析渣中各金属(铜、钴、铁)含量,从而得到金属的浸出率。在中速滤纸下,研究料浆过滤性能。
2 结果与讨论
试探性直接酸浸试验结果表明,钴的浸出率在50%以下。其主要原因是:反应过程生成硅酸胶体包裹于合金颗粒表面,阻碍了液固反应界面层氢离子和金属阳离子的扩散,即使再延长反应时间,也很难实现钴的完全浸出;另外,Fe-Co-Cu金属固溶体与其单质或氧化物具有比较稳定的结构,在热酸条件下,其溶解速度也相当缓慢。
因此,针对铜钴合金的特点,对氧化剂进行选择,并对初始溶液酸度、硫酸与盐酸的比例、氧化剂加入量、酸过量系数、浸出时间、反应温度等条件进行了条件实验研究。实验表明,适合的氧化剂为过氧化氢、氯酸钠、次氯酸钠。
2.1 初始酸度
在盐酸与硫酸摩尔比为8?2,氧化剂加入量倍数ψn=1.2,酸过量系数φH=1.2,反应温度为80 ℃,反应时间为1 h的条件下,改变初始酸度(液固比也相应地改变),其试验结果如图2所示。
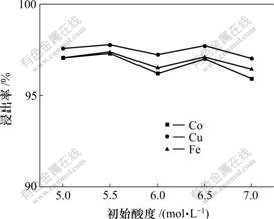
图2 初始酸度对浸出率的影响
Fig.2 Effect of initial acidity on leaching recovery
从图2可知,当溶液初始酸度为5.0~6.5 mol/L时,钴、铜、铁浸出率均为97%左右,当溶液初始酸度达到7 mol/L后,由于液固比太小,不利于扩散,钴、铁浸出率明显下降,而且酸度升高(高于7 mol/L)后,合金中硅浸出,溶液变得黏稠且难于过滤。因此,应该将浸出液初始酸度控制在5.0~6.5 mol/L。
2.2 硫酸与盐酸摩尔比对浸出率的影响
在初始酸度为6.5 mol/L,氧化剂为理论量的1.2倍,酸过量系数为1.2,液固比为10?1,反应温度为80 ℃,反应时间为1 h的条件下,改变硫酸与盐酸摩尔配比,铜钴合金浸出率如图3所示。
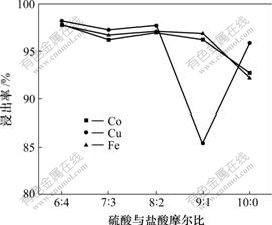
图3 硫酸与盐酸摩尔比对浸出率的影响
Fig.3 Effect of mole ratio of sulfuric acid to hydrochloric on leaching recovery
从图3可见,在盐酸含量较高时,2种酸的配比对浸出率的影响不显著,随着硫酸比例的加大和氯离子含量的减少,浸出率呈降低的趋势。当硫酸与盐酸摩尔比从6?4增至9?1时,金属阳离子以 [Cu(Cl)4]2-,[Co(Cl)4]2-和[Fe(Cl)4]2-的形式存在,降低了体系中Cu2+,Co2+和Fe2+的浓度,有利于浸出的进行,钴、铁浸出率可达到97% 左右;当硫酸与盐酸摩尔比加大到接近10?0时,由于溶液中无Cl-,[Cu(Cl)4]2-,[Co(Cl)4]2-和[Fe(Cl)4]2-配位络合物全部离解为简单的Cu2+,Co2+和Fe2+[17],在一定程度上阻碍了浸出的进行,钴、铁浸出率明显下降,只有92%。可见,提高盐酸含量,有利于浸出的进行,但是,当盐酸太高甚至于无硫酸的情况下,浸出液中含有大量的铁,对于下一步工序,无法采用比较经济有效的铁矾法除铁。
2.3 酸过量系数对浸出率的影响
在硫酸与盐酸摩尔比为8?2,初始酸度为6.5 mol/L,氧化剂加入量为理论量的1.2倍,反应温度为80 ℃,反应时间为1 h的条件下,改变酸过量系数,铜钴合金的浸出率如表3所示。
表3 酸过量系数对铜钴合金浸出的影响
Table 3 Effect of excessive acid coefficient on leaching of Cu-Co alloy

从表3可见,随着酸过量系数增加,钴、铜、铁浸出率逐步增加,当酸过量系数为1.2时,钴、铜、铁浸出率均达到最大。随着酸过量系数进一步加大到1.4时,开始有硅胶产生,产出的硅胶使合金颗粒表面形成硅胶膜,阻碍了反应的进行,浸出率开始下降,当酸过量系数达到1.6时,有大量的硅胶胶体产生,浸出液难于过滤。
2.4 氧化剂加入量对浸出率的影响
在硫酸与盐酸摩尔比为8?2,初始酸度为6.5 mol/L,酸过量系数为1.2,液固比为10?1,反应温度为80 ℃,反应时间为1 h的条件下,考察氧化剂加入量ψn(理论量倍数)对浸出的影响,其试验结果如图4所示。
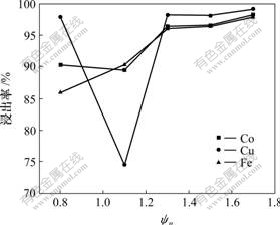
图4 氧化剂加入量ψn 对浸出率的影响
Fig.4 Effect of oxidant quality on leaching recovery
从图4可知,随着氧化剂加入量的增加,钴铜铁浸出率均增加,当氧化剂加入量为理论量的1.7倍时,钴浸出率达到98%,铜浸出率达到99%。在氧化剂用量为理论量的1.1倍时,Cu浸出率突然降低,这是 因为:
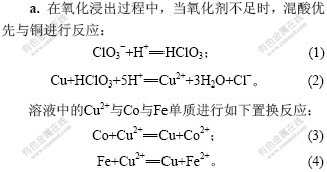
Cu2+又形成单质Cu,使其浸出率下降。
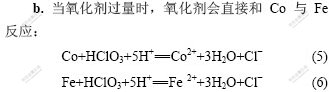
因此,在反应的初始阶段,氧化剂优先与铜进行反应,Cu的浸出率明显高于Co和Fe浸出率,随着氧化剂的增加,Co和Fe浸出率逐步升高。在浸出过程中,已经被浸出的铜离子与溶液中的钴铁离子发生置换反应,当铜的浸出速率低于被置换的速率时,铜的浸出率开始降低[18-19]。
2.5 反应时间对浸出率的影响
在硫酸与盐酸摩尔比为8?2,初始酸度为6.5 mol/L,液固比为10?1,氧化剂加入量为理论量的1.2倍,酸过量系数为1.2,反应温度为80 ℃的条件 下,考察反应时间对铜钴合金浸出的影响,结果如图5所示。

图5 反应时间对钴铜铁浸出率的影响
Fig.5 Effect of leaching time on leaching recovery
从图5可知,随着时间的延长,钴、铁浸出率增加,但是铜的浸出率先降低,在90 min后增加,这是因为在反应的初始阶段,氧化剂优先与铜进行反应,所以Cu的浸出率明显高于Co与Fe的浸出率。随着反应时间的延长,铁、钴的浸出率逐步升高,而由于铜与Co与Fe置换反应的影响,铜的浸出率呈降低趋势。到反应的末期(90 min后),随着Co与Fe总量的减少,铜的置换反应速率逐步降低,氧化剂主要作用于Cu的氧化浸出,铜的浸出率迅速升高[19]。而且浸出后,浸出液均容易过滤。
2.6 温度对浸出率的影响
在硫酸与盐酸摩尔比为8?2,初始酸度为6.5 mol/L,液固比为10?1,氧化剂加入量为理论量的1.2倍,酸过量系数为1.2,反应时间为1 h的条件下,反应温度对铜钴合金浸出率的影响如表4所示。
表4 反应温度对铜钴合金浸出率影响
Table 4 Effect of reaction temperature on leaching of Cu-Co alloy
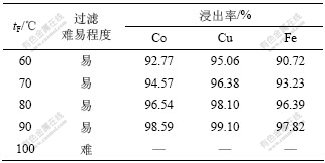
从表4可知,随着反应温度的升高,钴、铜、铁的浸出率均增加,但是,当反应温度达到90 ℃后,开始有硅胶产生,当达到100 ℃以上时,硅胶明显增多,浸出液难于过滤。因此,反应温度控制在80 ℃为最佳。
2.7 搅拌速度对金属浸出率的影响
在硫酸与盐酸摩尔比为8?2,初始酸度为6.5 mol/L,液固比为10?1,氧化剂加入量为理论量的1.2 倍,反应温度为80 ℃,反应时间为1 h,酸过量系数为1.2的条件下,改变搅拌速度,铜钴合金浸出率如表5所示。
从动力学的角度考虑,搅拌速度大,有利于加快扩散速度,使液固相混合均匀,在反应器中处于理想的全混状态,使液体保持充分湍流状态,有利于浸出反应的进行。表 5 所示结果表明,搅拌速度对金属的浸出率影响不大,当搅拌速度达到200 r/min,金属的浸出率即达99%左右,转速大于200 r/min,转速对浸出速率没有明显影响,说明转速大于200 r/min时外扩散已不是过程的控制步骤。因此,选取的搅拌速度以200~300 r/min为宜。
表5 搅拌速度与金属浸出率的关系
Table 5 Effect of stirring rate on leaching recovery Cu and Co

2.8 综合试验
根据上述条件试验,取各种参数的最佳值,即硫酸与盐酸摩尔比为8?2,初始酸度为6.5 mol/L,液固比为10?1,氧化剂加入量为理论量的1.2倍,反应温度为80 ℃,反应时间为1 h,酸过量系数为1.2,搅拌速度为250 r/min,得到的铜钴合金的浸出率如表6所示。
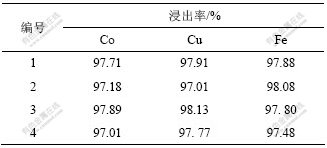
从表6可以看出,在最佳条件下,铜钴浸出率均能达到97%以上,浸出过程中不会有硅胶产生,过滤性能良好,实验重现性良好。
表6 铜钴合金的浸出率
Table 6 Leaching recovery of Cu-Co alloy
3 结 论
a. 浸出过程存在合金的直接氧化浸出与铜的置换2种反应,在反应的初始阶段或者当氧化剂的加入量较小时,氧化剂优先与铜进行反应,Cu的浸出率明显高于Co与Fe浸出率,当铜的浸出速率低于被置换速率时,铜的浸出率开始降低。
b. 溶液初始酸度为5.0~6.5 mol/L,钴、铜、铁浸出率均为97%左右,当溶液初始酸度达到7 mol/L后,合金中硅浸出,溶液变得粘稠且难于过滤。
c. 硫酸与盐酸摩尔比为6?4至10?0(全是硫酸,无盐酸)时,浸出后液均容易过滤。硫酸与盐酸摩尔比为6?4至9?1时,钴、铁浸出率均为97%左右。
d. 随着酸过量系数的增加,钴、铜、铁浸出率先增加后降低。当酸过量系数为1.2时,钴、铜、铁浸出率均达到最大,当酸过量系数达到1.6时,难以 过滤。
e. 随着氧化剂加入量的增加,钴铜铁浸出率均增加,当氧化剂加入量为理论量的1.7倍(试验设定的最大值)时,浸出率最高,钴浸出率达到98%,铜浸出率达到99%。
f. 随着反应温度升高,钴铜铁浸出率均增加,但是,当温度达到90 ℃以上时,浸出液难于过滤,故将反应温度控制在80 ℃。
g. 随着反应时间的延长,钴、铁浸出率增加,在反应时间为70 min时,各金属浸出率能达到97%以上。
h. 搅拌速度对金属的浸出率影响不大,当搅拌速度达到200 r/min时,金属Cu和Co的浸出率即达97%以上,当转速大于200 r/min时,转速对浸出速率没有明显影响。
参考文献:
[1] 何焕华, 蔡乔方. 中国镍钴冶金[M] . 北京: 冶金工业出版社, 2000.
HE Huan-hua, CAI Qiao-fang. Metallurgy of nickel and cobalt in China[M]. Beijing: Metallurgical Industry Press, 2000.
[2] 邓 彤, 凌云汉. 含钴铜转炉渣的工艺矿物学[J]. 中国有色金属学报, 2001, 11(5): 882-885.
DENG Tong, LING Yun-han. Process mineralogy of cobalt- bearing copper converter slag[J]. The Chinese Journal of Nonferrous Metals, 2001, 11(5): 882-885.
[3] 夏文堂, 史海燕. 采用无污染氧化剂浸出钴铜钴合金中钴铜的试验研究[J]. 矿冶, 2006, 15(3): 27-30.
XIA Wen-tang, SHI Hai-yan. A novel process for extracting Co and Cu from cobalt white alloy in hydrochloric acid solution with pollution-free oxidant[J]. Mining & Metallurgy, 2006, 15(3): 27-30.
[4] Jones R T, Deney A C. Using a direct current arc furnace to recover cobalt from slag[J]. Matals, 1998, 50(10): 57-61.
[5] 董春艳, 李碧乐, 孙丰月, 等. 难选多金属矿石中提取钴、镍、铜和金的试验研究[J]. 矿产综合利用, 2003, 4(2): 12-15.
DONG Chun-yan, LI Bi-le, SUN Feng-yue, et al. Experimental research on extraction of cobalt, nickel, copper and gold from a refractory polymetallic ore[J]. Multipurpose Utilization of Mineral Resources, 2003, 4(2): 12-15.
[6] 陈敬阳. 锌湿法冶炼中高钴矿的处理[J]. 材料研究与应用, 2007, 1(1): 69-71.
CHEN Jing-yang. Handling of high-cobalt mine in zinc hydrometallurgy[J]. Materials Research and Application, 2007, 1(1): 69-71.
[7] 龚燕春, 张启修, 温俊杰. 从钴白合金的酸性浸出液中选择性萃取铁[J]. 湿法冶金, 2006, 25(1): 26-29.
GONG Yan-chun, ZHANG Qi-xiu, WEN Jun-jie. Selectivity solvent extraction of Fe from acidic leaching solution of Co white alloy containing Fe, Cu and Co[J]. Hydrometallurgy of China, 2006, 25(1): 26-29.
[8] Jone P, Hayman D, Denton G M. Recovery of cobalt, nickel and copper from slages using DC arc furnace technology[C]//The International Symposium on Challenges of Process Intensification. Mont real: CIM, 1996: 89-108.
[9] 彭忠东, 万文治, 胡国荣, 等. 造渣熔炼―浸出方法处理Cu-Co-Fe合金的研究[J]. 有色矿冶, 2007, 23(1): 30-33.
PENG Zhong-dong, WAN Wen-zhi, HU Guo-rong, et al. Study of pre-process slag roasting during leaching Cu-Co-Fe alloy for cobalt[J]. Nonferrous Mining and Metallurgy, 2007, 23(1): 30-33.
[10] 王永利, 赵丽霞. 从含钴废料中提取钴的研究进展[J]. 再生资源研究, 2005(2): 29-32.
WANG Yong-li, ZHAO Li-xia. The research progress of drawing the cobalt[J]. Regeneration Resource Research, 2005(2): 29-32.
[11] 张忠平, 王 新, 万新军. 氯化物浸出黄铜矿的试验研究[J]. 中国有色冶金, 2006, 8(4): 35-37, 46.
ZHANG Zhong-ping, WANG Xin, WAN Xin-jun. Experimental investigation on chloride leaching of chalcopyrite[J]. Nonferrous Metallurgy of China, 2006, 8(4): 35-37, 46.
[12] WANG Wen-zhen, JIN Tao, ZHAO Nai-ren, et al. Effect of cobalt on chemical segregation and solution process in re-containing single crystal superalloys[J]. Trans Nonferrous Met Soc China, 2006, 16(S3): 1978-1981.
[13] ZHENG Ya-jie, XIAO Fa-xin, WANG Yong, et al. Industrial experiment of copper electrolyte purification by copper arsenite[J]. Journal of Central South University: Science and Technology, 2008, 15(2): 204-208.
[14] 喻正军, 冯其明, 欧乐明, 等. 常压下硫酸体系中钴冰铜的浸出[J]. 中南大学学报: 自然科学版[J]. 2006, 37(4): 675-679.
YU Zheng-jun, FENG Qi-ming, OU Le-ming, et al. Leaching of cobalt bearing metallic matte in sulphuric acid at normal pressure[J]. Journal of Central South University: Science and Technology, 2006, 37(4): 675-679.
[15] Arslan C. Recovery of copper, cobalt, and zinc from copper smelter and converter slags[J]. Hydrometallurgy, 2002, 67(1): 1-7.
[16] YANG You-ping, LIU Ren-sheng, HUANG Ke-long, et al. Preparation and electrochemical performance of nanosize Co3O4 via hydrothermal method[J]. Trans Nonferrous Met Soc China, 2007, 17(6): 1334-1338.
[17] 梁建龙, 刘惠娟, 史文革, 等. 某含钴、铜尾矿的浸出研究[J]. 矿冶工程, 2006, 26(5): 37-39.
LIANG Jian-long, LIU Hui-juan, SHI Wen-ge, et al. Parameters influencing the leaching effect of a tailing containing cobalt and copper[J]. Mining and Metallurgical Engineering, 2006, 26(5): 37-39.
[18] 谌可颂. 从废弃炉渣中回收钴、镍、铜的研究[J]. 湖南有色金属, 2006, 22(6): 24-29.
CHEN Ke-song. Study on separating and recovering cobalt, nickel and copper from waste slag[J]. Hunan Nonferrous Metals, 2006, 22(6): 24-29.
[19] 杨显万, 邱定蕃. 湿法冶金[M]. 北京: 冶金工业出版社, 1998.
YANG Xian-wan, QIU Ding-bo. Hydrometallurgy[M]. Beijing: Metallurgy and Technology Press, 1998.
收稿日期:2008-11-06;修回日期:2009-03-10
基金项目:国家重点基础研究发展计划项目(2007CB613603);教育部“新世纪优秀人才支持计划”项目(NCET-05-0692)
通信作者:赵中伟(1966-),男,河北邯郸人,教授,博士生导师,从事有色金属冶金提取、相似元素分离及冶金材料的制备研究;电话:0731-88830476;E-mail: zhaozw@mail.csu.edu.cn