文章编号:1004-0609(2014)02-0569-08
RAPD用于20株嗜酸氧化亚铁硫杆菌菌株亲缘性研究
吴学玲,范宏伟,段 红,张真真,刘莉莉,刘新星
(中南大学 资源加工与生物工程学院,长沙 410083)
摘 要:为研究中国20株嗜酸氧化亚铁硫杆菌菌株的基因多样性,以及基因指纹技术分类与嗜酸氧化亚铁硫杆菌生理生化特性的相关性,使用20种随机引物,通过PCR扩增20株菌株的基因组DNA,并分析凝胶电泳条带的有无,使用Jaccard系数和UPGMA分析菌株间相关性。20种引物产生的条带将20株菌株分成了5组,菌株间相关性系数最小为35.1%(YTW与DXS),而相似系数最大为96.9%(BY-0502与DXS,DY26与DY30)。结果表明:20株来自不同地区的嗜酸氧化亚铁硫杆菌株具有较高的多样性,并且亲缘性分类与各菌株取样地以及最大铜离子耐受能力分类,有较高的分类相似性,说明RAPD技术拥有在嗜酸氧化亚铁硫杆菌内分类鉴定菌株的能力。
关键词:嗜酸氧化亚铁硫杆菌;RAPD;多样性
中图分类号:Q751 文献标志码:A
RAPD to study relatedness of 20 Acidithiobacillus ferrooxidans strains
WU Xue-ling, FAN Hong-wei, DUAN Hong, ZHANG Zhen-zhen, LIU Li-li, LIU Xin-xing
(School of Minerals Processing and Bioengineering, Central South University, Changsha 410083, China)
Abstract: To study the genome diversity of 20 Acidithiobacillus ferrooxidans strains in China, and the relationship between the genome classification and physiological-biochemical characteristic of Acidithiobacillus ferrooxidans, DNA was amplified by PCR and twenty random primers, amplification products were separated by gel electrophoresis and photographed under UV light. The RAPD (Randomly Amplified Polymorphic DNA) profiles were compared on the basis of the presence or absence of each DNA band, and strain diversity was calculated using the Jaccard’s coefficient and UPGMA (Unweighted Pair-Group Arithmetic Average Clustering) cluster analysis. The primers used in this study grouped the 20 strains into five major groups. Similarities between the strains ranged from 35.1%(YTW and DXS) to 96.9%(BY-0502 and DXS,DY26 and DY30). These results indicate that the 20 strains have a high degree of genomic diversity and the RAPD markers related to characteristics, such as metal resistance and geographical locations. The RAPD procedure is a powerful technique to assess strain variability in Acidithiobacillus ferrooxidans.
Key words: Acidithiobacillus ferrooxidans; RAPD; diversity
随着生物冶金的逐步发展,许多与生物冶金相关的微生物菌株被分离鉴定,并用于各种条件下的金属矿石预处理与浸出过程[1]。嗜酸氧化亚铁硫杆菌(Acidithiobacillus ferrooxidans)是最早被分离鉴定出用于生物浸出的微生物之一[2],而其菌种内不同菌株间的生理生化特性千差万别[3]。吴学玲等[4]对3株A. ferrooxidans菌株进行比较后发现,三者Cu2+抗性与浸矿能力均存在较大差异,而16s rRNA DNA序列差异很小。随着诸多菌株逐步被分离出,一个快速、有效、辨识率高的分子生物学鉴定方法的构建,对于研究不同菌株之间的差异性,以及快速分类筛选出特殊能力菌株有着十分重要的意义。
RAPD(Random amplification of polymorphic DNA)于1990年由WILIAMS[5]和WELSH[6]分别提出,是一种利用随机引物对细菌基因组进行扩增并分析其多态性的分子生物学技术。RAPD操作简便,且用于鉴定菌种不同菌株时多样性比较明显,但是RAPD技术的影响因素较多,因此对不同实验中反应条件的掌握以及改良是目前该技术的难点[7],如果能标准化实验操作,并构建相关数据库,RAPD技术将拥有快速鉴定A. ferrooxidans菌株的潜力[8]。
RAPD方法是分析全基因组的一种基因指纹技术,这种分子生物学方法利用合成寡核苷酸随机产生基因组DNA扩增片段,从而产生样品条带的多样性特性[9]。DNA指纹技术和RAPD是分类学与流行病学强有力的工具[10],可以用于各种细菌以及真菌的DNA指纹鉴定,而且可以用于同种菌不同菌株间的区分[11]。由于引物的随机性,RAPD方法无需预知基因组DNA的相关信息,可以直接使用基因组DNA进行实验。
WALTENBURY等[12]对分别取样自加拿大、美国和英国的12株A. ferrooxidans菌株进行了RAPD基因指纹分析,得出RAPD对于A. ferrooxidans有着区分度高的优势,是一种有效可靠的分析该菌种多样性的基因指纹技术。PAULINO等[13]利用RAPD与rep-PCR(repetitive extragenic palindromic PCR)两种基因指纹技术,研究了巴西矿物废弃物中浸矿菌的基因多样性,得出基于PCR的基因指纹技术比核糖分型技术更为灵敏快捷,但未发现基因亲缘性与菌株的理化特性有任何相关。
本文作者采用RAPD基因指纹分析技术对来自甘肃、江西、广西、湖北、新疆等各地分离的共20株A. ferrooxidans菌株进行了实验,并对结果进行了分析,首次对中国各地分离得到的不同的A. ferrooxidans菌株进行了基因多样性以及亲缘性研究,就其亲缘性与菌株理化特性进行了比对分析,并就RAPD技术在A. ferrooxidans中作为菌株鉴定手段的可能性进行了讨论。
1 实验
1.1 A. ferrooxidans菌株
本研究使用了包括来自甘肃、江西、广西、湖北、新疆等各地分离的共20株A. ferrooxidans菌株(见表1)。所有菌株均由教育部中南大学生物冶金重点实验室分离和保藏。
1.2 菌株的活化培养以及铜离子最大耐受能力测定
菌种从保藏库中拿出后常规复苏[14],之后分别接种至121 ℃高压蒸汽灭菌的30 mL 9K基础培养基中培养4~7 d。9K培养基配方[15]为:(NH4)2SO4 3.0 g/L,K2HPO4 0.5 g/L,KCl 0.1 g/L,MgSO4・7H2O 0.5 g/L,Ca(NO3)2 0.01 g/L。高温灭菌后,加入30 g/L紫外灭菌30 min的FeSO4・7H2O混匀,使用浓度为70%的 H2SO4调整pH至2.0。培养条件如下:温度为30 ℃,转速为175 r/min。20株菌分别传代4~5次之后,活性达到正常水平。
先通过预实验了解20株A. ferrooxidans菌的铜离子最大耐受浓度(MTC, Maximum talerated concentration)范围,之后按照预实验结果,设定不同铜离子浓度梯度进行试验。根据设定的铜离子浓度梯度,配置加入对应浓度CuSO4・5H2O的9K基础培养基,分别接种5×106浓度的A. ferrooxidans菌种,每12 h取样,使用重铬酸钾滴定法测定溶液剩余亚铁离子浓度,使用血细胞计数法测定菌液细菌浓度,培养7 d。每种菌设置空白组,每个梯度设置对照组。
1.3 DNA提取制备
20株菌株分别转接至150 mL培养基于30 ℃、 175 r/min条件下进行扩大培养3~5 d。培养基pH使用70%的硫酸调整至2.0。使用滤纸过滤去除黄钾铁矾后,使用Beckman Avanti J-E离心机在10 000 r/min,4 ℃条件下离心15 min收集菌体。离心后除去上清液,菌斑使用70%的硫酸配置的pH 2.0的无菌水进行冲洗,并转移到EP离心管中,12 000 r/min转速离心15 min后,除去上清液,再用无菌水吸打均匀。
收集后的菌液使用天根生化科技(北京)的细菌基因组提取试剂盒对20株A.f菌进行基因组DNA的提取纯化。DNA保存在-20 ℃条件下。
1.4 随机引物扩增(RAPD)及电泳
RAPD的PCR过程采用20个10b长度的DNA单链引物(A1-A20,见表1),购自北京鼎国生物公司。
使用DNA master mix(天根生化科技,包含0.1U Taq Polymerase/μL、500 μmol/L dNTPs each、20 mmol/L Tris-HCl(pH8.3)、100 mmol/L KCl、3 mmol/L MgCl2)与引物和模板构成PCR体系,25 μL的PCR总体系中包含:DNA master mix 12.5 μL,ddH2O 10.5 μL,单链引物1 μL,模板1 μL。
表1 20种引物序列(A1-A20为随机引物)
Table 1 Sequences of random primers(A1-A20)

RAPD的PCR过程为:94 ℃下解链10 min后,进行42个循环(94 ℃变性1 min,37 ℃退火1 min,72 ℃延展2 min),最后72 ℃下延展10 min后,在-20 ℃冰箱进行保存。
所有扩增产物使用1.5%琼脂糖凝胶和1×TAE缓冲液[16],加入1 μg/mL的溴乙锭,在60 V电压下电泳4 h。电泳完成后,使用Molecular Imager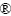 Gel DocTM XR System对电泳凝胶进行成像分析。
Gel DocTM XR System对电泳凝胶进行成像分析。
1.5 电泳条带分析及数据处理
RAPD结果通过对比每条DNA条带的有(1)或无(0),构建n×t数据矩阵,t代表归类的OTU(operational taxonomic unit),n代表条带数。如果条带存在,则记为1;不存在,则记为0。数据矩阵使用Jaccard系数(Jaccard's coefficient)检测不同菌株间的相似性。Jaccard系数方程为Sj=n11/(n11+n01+n10),其中,n11代表在两个OTU中条带都存在时的n值,n01代表第一个OTU中不存在,但另一个存在条带时的n值,n10代表第一个OTU中存在,但另一个不存在条带时的n值[12]。使用Ntsys 2.1软件进行非加权组平均法(unweighted pair group method with arithmetic mean,UPGMA)归类分析构建树形图,并检测共性分类相关系数。
2 结果与讨论
2.1 Acidithiobacillus ferrooxidans菌株铜离子耐受能力
20株A. ferrooxidans菌株的铜离子耐受能力通过绘制生长曲线与亚铁离子氧化曲线进行分析。本实验就20株菌株的铜离子耐受能力高低进行了实验分析,以将其按照生理特性进行归类。20株A. ferrooxidans菌的铜离子耐受能力如表2所列。
铜离子耐受能力较高的菌株从高到低为DY26、DY30、DY32、GF、BY-01、BY-0502、GD-A、GD-B、GD-9、DXS、DY15、DY18、JYC-2、JYC-3,最大铜离子耐受浓度为200~160 mmol/L;耐受能力较低的菌株从高到低为DX5、YTW、JYC-1、BY-03、DC、GD-0,最大铜离子耐受浓度为120~60 mmol/L。
2.2 RAPD实验结果
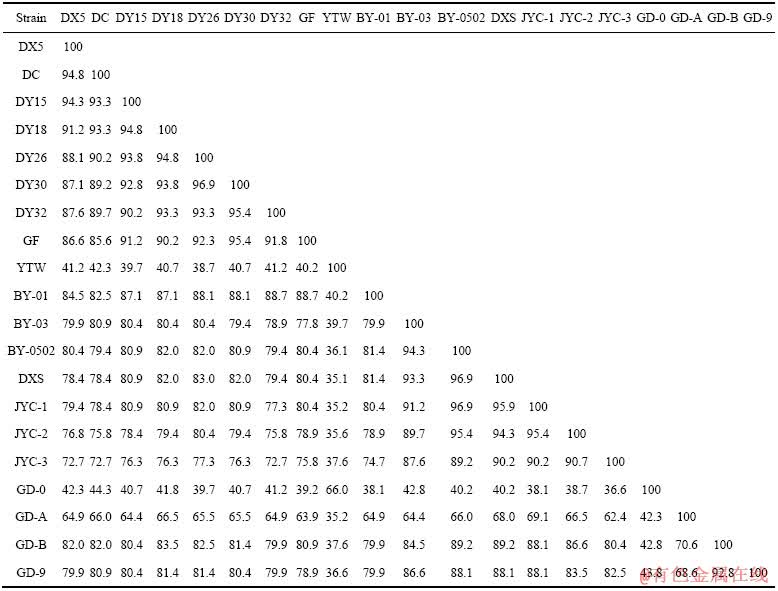
本次RAPD实验中,部分条带由于可重复性较差,因此不将这些条带进行统计分析。20个随机引物共产生194个不同长度的可重复条带,其中,20株菌共有条带有7条,分别是由引物A3(1.0 kb,1.5 kb)、A6(0.9 kb)、A12(2.0 kb)、A17(2.0 kb)、A19(1.2 kb)、A20(0.5 kb)产生,单条引物产生最多的条带数为14个条带(A4,A13),产生最少条带数为7个条带(A3,A7,A8),产生条带长度最大为4.5 kb左右(A7),最短长度为0.2 kb左右(A18)。根据表格2可知,20株菌种间相似系数最小为35.1%(YTW与DXS),而相似系数最大为96.9%(BY-0502与DXS,DY26与DY30)。
RAPD方法使用的是10碱基长度的引物,因此PCR扩增过程中的退火时必须使用较低退火温度,而低退火温度很可能导致识别率低以及不可重复的条 带[17]。本研究中,通过重复实验, 建立最佳的反应条件和反应体系,在一定程度上确保了实验数据的可信度。
本研究中使用到的20株A. ferrooxidans菌株按照相关性树形图(见图1),可以被分为5组,第一组为菌株DX5、DC、DY15、DY18、DY26、DY30、DY32、GF和BY-01,相似系数在82.5%(BY-01与DC)至96.9% (DY26与DY30)之间;第二组为菌株BY-03、BY-0502、DXS、JYC-1、JYC-2、JYC-3、GD-B和GD-9,相似系数在80.4%(JYC-3与GD-B)至96.9% (BY-0502与DXS)之间,而菌株GD-A、YTW、GD-0各单独归类为一组。
表2 A. ferrooxidans菌株的GenBank登录号以及取样地
Table 2 Sources and GenBank accession numbers of A. ferrooxidans strains
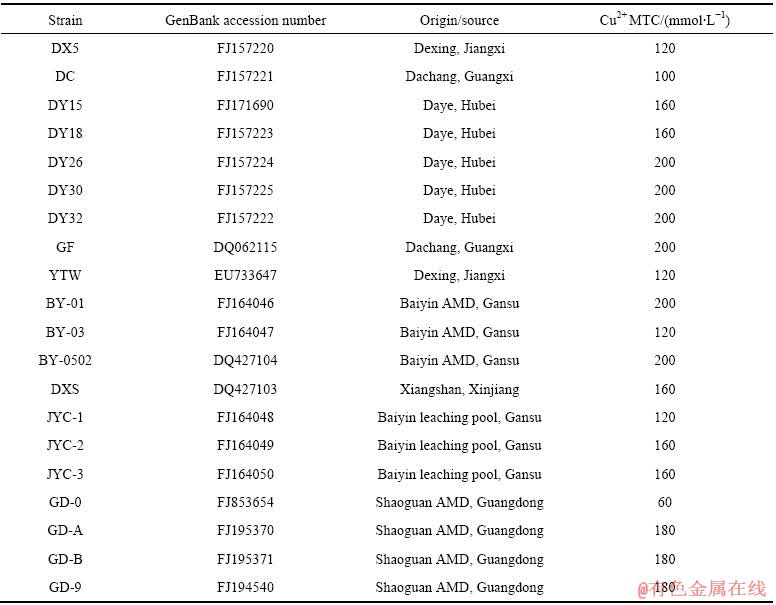
图1 基于RAPD指纹构建20株菌株间的相关性树形图(不同条带的相关性(%)使用Jaccard相关性系数计算得出(数据使用UPGMA分类法进行分类处理)
Fig. 1 Dendrogram representing relationships between strains of A. ferrooxidans based on RAPD fingerprints (Similarity (%) between patterns was calculated by using the Jaccard’s coefficient. The data were sorted by using the UPGMA clustering method)
表3 RAPD获得的20株A. ferrooxidans菌的Jaccard相似系数(%)矩阵
Table 3 Similarity matrix for Jaccard’s coefficient(%) of different A. ferrooxidans obtained from RAPD markers
2.3 菌株表型分类与基因型分类相关性
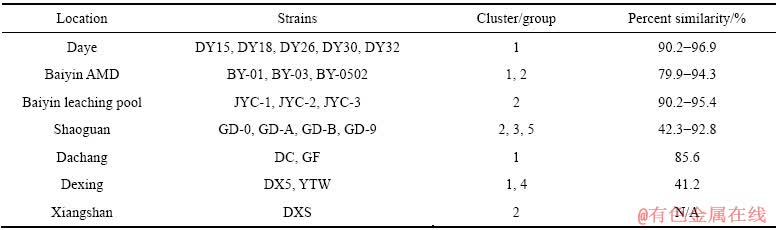
如表4中所列,菌株DY15、DY18、DY26、DY30、DY32均分离自湖北大冶铜矿山,这5株菌均在第一组中,相似系数在90.2%(DY15与DY32)至96.9% (DY26与DY30)之间;菌株BY-01、BY-03、BY-0502、JYC-1、JYC-2、JYC-3分离自甘肃白银,其中除BY-01在第一组外,其他菌株均在第二组,6株菌相似系数在74.7%(BY-01与JYC-3)至96.8%(BY0502与JYC-1)之间;菌株GD-0、GD-A、GD-B、GD-9均取样自广东韶关矿坑AMD,其中GD-B和GD-9在第二组,而GD-0和GD-A各为一组,4株菌相似系数在42.3% (GD-0与GD-A)至92.8%(GD-B与GD-9)之间;菌株DC和GF取样自广西大厂,两株菌均在第一组,相似系数为85.6%;菌株DX5和YTW取样自江西德兴铜矿,其中DX5在第一组,而YTW在第四组,两株菌相似系数为41.2%;菌株DXS取样自新疆哈密东香山水样,归为第二组。
由表4可知,来自同一地区的菌株,亲缘性部分较高(大冶,大厂),而部分较低(白银,韶关,德兴)。通过菌株相关性系数可以区分主要的地理取样地(城市,矿区)[18],白银地区的6株菌株取样自两个不同的取样点(酸性矿坑水与矿山积液池),两个取样点的理化条件有较大差异,而相同取样点的菌株间亲缘性较高。德兴地区的两株菌株相似系数也较低(41.2%,YTW与DX5),这可能是因为菌株YTW与DX5虽然都来自江西德兴铜矿,但YTW取样自德兴铜矿的杨桃坞酸性矿坑水,杨桃坞是主要的废弃物存放地,包括废石与酸性废水[19],pH值多在2.5~4.5,且含多种重金属离子,而DX5取样自德兴铜矿山,因此,该亲缘性差异可能是外部环境造成。而韶关的部分菌株(GD-0、GD-A)与同取样地其他菌株的相似系数较低,这可能是由于这些菌株是不同时期从其他环境中进入AMD开放环境中,故该菌株与其他菌株的亲缘性较低。由以上数据可知,来自同一地区的菌株,大多数相似系数较高,这说明了菌株的地理特性与亲缘性有一定程度的相关。
表4 20株A. ferrooxidans菌株取样地分组
Table 4 Source grouping of 20 A. ferrooxidans strains
冯敏等[20]研究了在部分微生物中RAPD基因指纹与菌株起源地的相关性。GANTER等[21]利用RAPD技术研究了40株毕赤酵母属菌株的群落结构。结果表明:在研究的每个菌种中,RAPD的分类结果与地理取样地相关。PATHANIA等[22]运用RAPD、通用报告引物(universal rice primers,URP)、简单序列重复区间扩增多态性(inter-simple sequence repeat,ISSR) 和delta分型这4种方法,对43株酵母菌进行鉴定分析,不仅在菌株水平存在差异,它们的地理起源也有所不同。此外,他还采用UPGMA对9 个RAPD 标记的分析结果构树,43个菌株共分为为6组,结果显示除了少数个例,大多数菌株可依照其地理起源分类。这印证了RAPD 指纹变异与菌株的起源地息息相关[22]。
铜离子耐受能力较高的14株菌株中,相似系数最高为96.9%(BY-0502与DXS,DY26与DY30),相似系数最低为62.4%(GD-A与JYC-3),铜离子耐受能力较低的6株菌株中,相似系数最高为94.8%(DX5与DC),而相似系数最低为35.2%(YTW与JYC-1)。本次试验期望通过铜离子耐受能力试验以及RAPD试验得出A. ferrooxidans菌株表型与RAPD基因型的相关性。实验结果表明,耐受能力较高的14株菌株间亲缘性较高,而耐受能力较低的菌株中部分菌株间的相似系数较低,这可能是由于高耐受能力菌株拥有类似的铜抗性基因,而低耐受能力菌株缺少相关基因,因此,部分菌株基因型差异较明显。CHEN等[23]在通过研究4株A. ferrooxidans菌株的重金属离子耐受能力、最适温度、pH等表型以及RAPD基因型之后,发现菌株AF2与其他菌株的表型与基因型菌差异较大,且表型分类与基因型分类相关,并发现在该菌株中缺少两种其他菌株共有的重金属抗性基因,该结果佐证了本实验中的结论。
2.4 RAPD技术与其他基因分类技术比较
本次研究中,RAPD的结果分析表明了20株A. ferrooxidans菌株有较高的基因多样性。AKBAR等[24]也同样使用RAPD方法对6株A. ferrooxidans以及3株Acidithiobacillus thiooxidans进行了分析,得到了类似的相关性结果。相对于其他分子生物学方法,RAPD使用全基因组作为扩增模板,因此相比较于RFLP等方法有明显优势[25]。POWELL等[26]通过利用RAPD,RFLP (Restriction fragment length polymorphism)、AFLP (Amplified fragment length polymorphism)和SSR (Simple sequence repeat, microsatellite) 4不同的基因分类技术比较大豆的基因亲缘性[26],发现基于RFLP,AFLP和SSR分析得出驯化与野生大豆的相关性较高,而通过RAPD技术得出了较低的相关性,并得出了RAPD在种内相关性比较时更有优势。而相对于rep-PCR技术,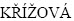 等[27]使用了RAPD与rep-PCR技术研究了Bifidobacteriu菌属内菌株的基因相关性,rep-PCR (84%和93 %)产生条带的多样性相比RAPD(53%)较低,而RAPD在亲缘性较近的菌株中,表现出较高的基因多样性。
等[27]使用了RAPD与rep-PCR技术研究了Bifidobacteriu菌属内菌株的基因相关性,rep-PCR (84%和93 %)产生条带的多样性相比RAPD(53%)较低,而RAPD在亲缘性较近的菌株中,表现出较高的基因多样性。
3 结论
1) RAPD技术适用于本文中的20株A. ferrooxidans菌菌株的亲缘性分析,通过条带分析得到的结果说明20株菌株拥有较高的基因多样性。
2) 通过对比RAPD凝胶电泳条带的有无得出,该20种随机引物对于20株菌株均能产生较好的可重复条带,且引物产生的条带特异性良好,均可以应用于RAPD实验。
3) 通过分析RAPD条带得到的分类结果显示出,20株菌株的亲缘性分类与各菌株取样地以及最大铜离子耐受能力分类,具有较高的分类相似性,说明RAPD技术拥有在A. ferrooxidans菌内分类鉴定菌株的能力。
REFERENCES
[1] BOSECKER K. Bioleaching: metal solubilization by microorganisms[J]. FEMS Microbiology Reviews, 2006, 20(3/4): 591-604.
[2] VESTAL J R, LUNDGREN D. The sulfite oxidase of Thiobacillus ferrooxidans (Ferrobacillus ferrooxidans)[J]. Canadian Journal of Biochemistry, 1971, 49(10): 1125-1130.
[3] KARAVAIKO G I, TAT'YANA P T, KONDRAT'EVA T F, LYSENKO A M, TAT'YANA V K, AGEEVA S N, MUNTYAN L N, TAT'YANA A P. Phylogenetic heterogeneity of the species Acidithiobacillus ferrooxidans[J]. International Journal of Systematic and Evolutionary Microbiology, 2003, 53(1): 113-119.
[4] 吴学玲, 袁 鹏, 胡 琪, 侯冬梅, 苗 博, 邱冠周. 不同嗜酸氧化亚铁硫杆菌(DY15, DY26, DC)对黄铜矿的浸出及其基因Afe0022的差异表达[J]. 中国有色金属学报, 2011, 21(4): 932-938.
WU Xue-ling, YUAN Peng, HU Qi, HOU Dong-mei, MIAO Bo, QIU Guan-zhou. Bioleaching of chalcopyrite by Acidithiobacillus ferrooxidans DY15, DY26 and DC and difference expressions of Gene Afeoozz[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(4): 932-938.
[5] WILLIAMS J G K, KUBELIK A R, LIVAK K J, RAFALSKI J A, TINGEY S V. DNA polymorphisms amplified by arbitrary primers are useful as genetic markers[J]. Nucleic Acids Research, 1990, 18(22): 6531-6535.
[6] WELSH J, McCLELLAND M. Fingerprinting genomes using PCR with arbitrary primers[J]. Nucleic Acids Research, 1990, 18(24): 7213-7218.
[7] 贺治国, 胡岳华, 胡维新, 钟 慧, 徐 兢, 朱 敏. 用 RAPD 分子标志方法研究氧化亚铁硫杆菌遗传多样性[J]. 遗传, 2004, 26(1): 69-74.
HE Zhi-guo, HU Yue-hua, HU Wei-xing, ZHONG Hui XU Jing, ZHU Min. Studies of polymorphisms of Thiobacillus ferrooxidans using RAPD[J]. HEREDITAS, 2004, 26(1): 69-74.
[8] 杨 坤, 张新明, 刘 平, 吕 波, 饶智宏, 王凤格, 赵久然, 史亚兴, 张 俊, 王世亮, 刘 鹏. 植物已知品种数据库构建方法的研究[J]. 中国农学通报, 2011, 27(33): 283-287.
YANG Kun, ZHANG Xin-ming, LIU Ping, 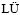 Bo, RAO Zhi-hong, WANG Feng-ge, ZHAO Jiu-ran, SHI Ya-xing, ZHANG Jun, WANG Shi-liang, LIU Peng. Study on construction of database of plants varieties of common knowledge[J]. Chinese Agriculture Science Bulletin, 2011, 27(33): 283-287.
Bo, RAO Zhi-hong, WANG Feng-ge, ZHAO Jiu-ran, SHI Ya-xing, ZHANG Jun, WANG Shi-liang, LIU Peng. Study on construction of database of plants varieties of common knowledge[J]. Chinese Agriculture Science Bulletin, 2011, 27(33): 283-287.
[9] JANSSEN P, COOPMAN R, HUYS G, SWINGS J, BLEEKER M, VOS P, ZABEAU M, KERSTERS K. Evaluation of the DNA fingerprinting method AFLP as a new tool in bacterial taxonomy[J]. Microbiology, 1996, 142(7): 1881-1893.
[10] ALBUFERA U, BHUGALOO-VIAL P, ISSACK M, JAUFEERALLY-FAKIM Y. Molecular characterization of Salmonella isolates by REP-PCR and RAPD analysis[J]. Infection, Genetics and Evolution, 2009, 9(3): 322-327.
[11] CALIGIORNE R B, RESENDE M A, PAIVA E, AZEVEDO V. Use of RAPD (random amplified polymorphic DNA) to analyse genetic diversity of dematiaceous fungal pathogens[J]. Canadian Journal of Microbiology, 1999, 45(5): 408-412.
[12] WALTENBURY D R, LEDUC L, FERRONI G. The use of RAPD genomic fingerprinting to study relatedness in strains of Acidithiobacillus ferrooxidans[J]. Journal of Microbiological Methods, 2005, 62(1): 103-112.
[13] PAULINO C L, BERGAMO R F, de MELLO M P, GARCIA O, MANFIO G P, OTTOBONI L M M. Molecular characterization of Acidithiobacillus ferrooxidans and A. thiooxidans strains isolated from mine wastes in Brazil[J]. Antonie van Leeuwenhoek, 2001, 80(1): 65-75.
[14] WU X L, XIN X H, JIANG Y, LIANG R X, YUAN P, FANG C X. Liquid-nitrogen cryopreservation of three kinds of autotrophicbioleaching bacteria[J]. Transactions of Nonferrous Metals Society of China, 2008, 18(6): 1386-1391.
[15] XIE M, YIN H Q, LIU Y, LIU J, LIU X D. Repetitive sequence based polymerase chain reaction to differentiate close bacteria strains in acidic sites[J]. Transactions of Nonferrous Metals Society of China, 2008, 18(6): 1392-1397.
[16] XIE X, LIANG J, PU T, XU F, YAO F, YANG Y, ZHAO Y L, YOU D, ZHOU X, DENG Z. Phosphorothioate DNA as an antioxidant in bacteria[J]. Nucleic Acids Research, 2012.
[17] HADRYS H, BALICK M, SCHIERWATER B. Applications of random amplified polymorphic DNA (RAPD) in molecular ecology[J]. Molecular Ecology, 2008, 1(1): 55-63.
[18] MARTINEZ C, COSGAYA P,  C, GAC S, GANGA A. High degree of correlation between molecular polymorphism and geographic origin of wine yeast strains[J]. Journal of Applied Microbiology, 2007, 103(6): 2185-2195.
C, GAC S, GANGA A. High degree of correlation between molecular polymorphism and geographic origin of wine yeast strains[J]. Journal of Applied Microbiology, 2007, 103(6): 2185-2195.
[19] 刘 成. 德兴铜矿酸性废水成因的研究[J]. 有色矿山, 2001, 30(4): 49-53.
LIU Cheng. Study on the cause of formation of acidic waste water in Dexing Copper Mine[J]. Nonferrous Mines, 2001, 30(4): 49-53.
[20] 冯 敏, 刘延琳. RAPD在酵母分类鉴定与育种研究中的应用[J]. 食品科学, 2012, 33(9): 267-270.
FENG Min, LIU Yan-lin. Application of RAPD in classification, identification and breeding of yeasts[J]. Food Scinece, 2012, 33(9): 267-270.
[21] GANTER P F, QUARLES B. Analysis of population structure of cactophilic yeast from the genus Pichia: P. cactophila and P. norvegensis[J]. Canadian Journal of Microbiology, 1997, 43(1): 35-44.
[22] PATHANIA N, KANWAR S, JHANG T, KOUNDAL K, SHARMA T. Application of different molecular techniques for deciphering genetic diversity among yeast isolates of traditional fermented food products of Western Himalayas[J]. World Journal of Microbiology and Biotechnology, 2010, 26(9): 1539-1547.
[23] CHEN H, YANG B, CHEN X. Identification and characterization of four strains of Acidithiobacillus ferrooxidans isolated from different sites in China[J]. Microbiological Research, 2009, 164(6): 613-623.
[24] AKBAR T, AKHTAR K, GHAURI M A, ANWAR M A, REHMAN M, REHMAN M, ZAFAR Y, KHALID A M. Relationship among acidophilic bacteria from diverse environments as determined by randomly amplified polymorphic DNA analysis (RAPD)[J]. World Journal of Microbiology and Biotechnology, 2005, 21(5): 645-648.
[25] RADEMAKER J, HOSTE B, LOUWS F J, KERSTERS K, SWINGS J, VAUTERIN L, VAUTERIN P, de BRUIJN F J. Comparison of AFLP and rep-PCR genomic fingerprinting with DNA-DNA homology studies: Xanthomonas as a model system[J]. International Journal of Systematic and Evolutionary Microbiology, 2000, 50(2): 665-677.
[26] POWELL W, MORGANTE M, ANDRE C, HANAFEY M, VOGEL J, TINGEY S, RAFALSKI A. The comparison of RFLP, RAPD, AFLP and SSR (microsatellite) markers for germplasm analysis[J]. Molecular Breeding, 1996, 2(3): 225-238.
[27] 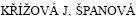 A, RITTICH B. RAPD and rep-PCR fingerprinting for characterization of Bifidobacterium species[J]. Folia Microbiologica, 2008, 53(2): 99-104.
A, RITTICH B. RAPD and rep-PCR fingerprinting for characterization of Bifidobacterium species[J]. Folia Microbiologica, 2008, 53(2): 99-104.
(编辑 何学锋)
收稿日期:2013-01-14;修订日期:2013-10-28
通信作者:刘新星,教授;电话:0731-88836944;E-mail: wxlcsu@csu.edu.cn