文章编号:1004-0609(2015)04-1109-07
铁泥溶剂热法制备磁性材料及其在水溶液中对亚甲基蓝的吸附性
方 帅1,刘志强1,陈 瑜1, 3,霍明昕1, 2,边德军1, 2,杨 霞1,耿 直1,朱遂一1, 3
(1. 东北师范大学 环境学院,长春 130117;
2. 长春工程学院 水利与环境工程学院,长春 130012;
3. 吉林省林业勘察设计研究院,长春 130022)
摘 要:以地下水厂含铁污泥为原料,利用一步溶剂热法制备出含有Fe3O4的磁性材料。采用磁学性质测量系统、X射线衍射仪、穆斯堡尔谱仪、X射线光电子能谱仪和扫描电镜对铁泥和磁性材料进行表征。结果表明:地下水厂铁泥含铁量较低(16.6%,质量分数),其杂质主要是硅和铝矿物,粒径约为70 nm,在磁场下不会迁移;经过溶剂热法处理后,生成含有Fe3O4的椭球形磁性材料,粒径达到1.5 μm,比饱和磁化强度(Ms)可达18.9 A・m2/kg,在磁场下可迅速向磁极迁移并聚集,体现了良好的磁响应特征。磁性材料对水中亚甲基蓝的吸附效果接近粉末活性炭,在5 min内对10 mg/L亚甲基蓝的吸附效率达到92.3%。本研究方法可以处理含铁量较低的铁泥,实现铁泥的资源化利用,制备的磁性材料在染料废水处理中具有潜在的应用价值。
关键词:四氧化三铁;亚甲基蓝;地下水厂;铁泥;溶剂热法
中图分类号:O614.8 文献标志码:A
Synthesis of magnetic materials by solvothermal method with iron-mud and adsorption of methylene blue in aqueous solution
FANG Shuai1, LIU Zhi-qiang1, CHEN Yu1, 3, HUO Ming-xin1, 2, BIAN De-jun1, 2, YANG Xia1, GENG Zhi1, ZHU Sui-yi1, 3
(1. School of Environment, Northeast Normal University, Changchun 130117, China;
2. College of Water Conservancy and Environmental Engineering,
Changchun Institute of Technology, Changchun 130012, China;
3. Jilin Institute of Forestry Survey and Design, Changchun 130022, China)
Abstract: Magnetic material with ferroferric oxide was synthesized by one-step solvothermal method using iron mud with low-iron-content as the raw material. The obtained magnetic material was characterized by magnetic property measurement system (MPMS), X-ray diffraction (XRD), M ssbauer spectroscopy, X-ray photoelectron spectroscopy (XPS) and scanning electron microscopy (SEM). The results show that the iron content in iron mud is only 16.6% (mass fraction), while the main impurities are silicon and aluminum oxides, iron mud with the average size of 70 nm does not have any magnetism. After solvothermal process, the obtained magnetic material contains ferroferric oxide and assumes a near-sphere shape with the average size of 1.5 μm. The material possesses well magnetic response, and the specific saturated magnetizing strength reaches 18.9 A・m2/kg, which can be easily magnetic separated from water. Dramatically, the adsorptivity of the material is nearly equivalent to powder active carbon, for example, the removal efficiency of methylene blue (10 mg/L) reaches to 92.3% in 5 min, which contributes to the chemical adsorption between the methylene blue and the material. Therefore, this facile solvothermal method can be applied to dispose iron mud with low-iron-content and make the mud into recoverable resource. Moreover, the prepared magnetic material has a potential application on the treatment of dye wastewater.
ssbauer spectroscopy, X-ray photoelectron spectroscopy (XPS) and scanning electron microscopy (SEM). The results show that the iron content in iron mud is only 16.6% (mass fraction), while the main impurities are silicon and aluminum oxides, iron mud with the average size of 70 nm does not have any magnetism. After solvothermal process, the obtained magnetic material contains ferroferric oxide and assumes a near-sphere shape with the average size of 1.5 μm. The material possesses well magnetic response, and the specific saturated magnetizing strength reaches 18.9 A・m2/kg, which can be easily magnetic separated from water. Dramatically, the adsorptivity of the material is nearly equivalent to powder active carbon, for example, the removal efficiency of methylene blue (10 mg/L) reaches to 92.3% in 5 min, which contributes to the chemical adsorption between the methylene blue and the material. Therefore, this facile solvothermal method can be applied to dispose iron mud with low-iron-content and make the mud into recoverable resource. Moreover, the prepared magnetic material has a potential application on the treatment of dye wastewater.
Key words: Fe3O4; methylene blue; groundwater treatment plant; iron mud; solvothermal synthesis
地下水厂铁泥是单级滤池反冲洗废水沉积后生成的污泥,成分复杂,包括脱落的铁锰滤膜和硅酸盐、泥砂、破碎滤料等杂质。这种铁泥含铁量相对较低,与传统二级曝气+二级过滤工艺的除铁滤池中高含铁污泥不同,不能直接用于制备氧化铁红。铁泥直接堆放会占用大量土地,在降水时金属离子容易析出并污染附近土壤和地表水[1-2]。为防止铁泥污染,水厂多采用浓缩、絮凝、压滤等方法将污泥脱水,处理步骤繁琐,费用较高,脱水污泥直接填埋而未能有效利用。
将地下水厂含铁污泥经处理后制备成磁性吸附剂,不仅可以减少水厂占地和污泥处理费用,而且能够用于环境污染治理,具有明显的经济效益和环境效益。一些利用铝厂赤泥[2-3]、电镀厂污泥[4]等为原料合成磁性材料的方法值得借鉴。如ILKER等[5]采用微波消解、强酸浸渍从铝厂红泥中提取Fe3+,再按照n(Fe2+):n(Fe3+)=1:1.75加入FeCl2・4H2O,碱性共沉淀法制备Fe3O4-NPs,能够有效吸附地下水中砷。在此基础上,一些学者提出了高温还原法处理含铁污泥,生成磁性材料来回收铁资源。刘万超等[6]以氧化铁质量分数为27.93%的拜耳法赤泥为原料,碳粉为还原剂直接还原焙烧后磁选制得铁精矿产品。ZHU等[7]以高含铁赤泥(w(Fe)=50.6%)为原料,无烟煤为还原剂,高温煅烧后通过磁分离达到94.1%的铁回收率。受铁泥中众多杂质影响,现行的方法应用于地下水厂铁泥原位合成磁性材料还存在不足。如强酸浸提虽然能获得高纯Fe3+,但浸提效率偏低、浸提后残留的酸性污泥会造成二级污染等;同样高温还原法对高含铁污泥具有良好效果,但在处理低铁含量(w(Fe)<20%)污泥时,会出现还原剂利用率低,且加入的褐煤、无烟煤等也会增大残留泥渣量。
溶剂热法作为一种简单、过程易于控制的合成方法,已广泛用于制备不同粒径和形貌的Fe3O4磁性材料[8]。在溶剂热法中,通过使用还原性多元醇和合适添加剂,可以获得水系中难以合成的目标产物[9]。为了研究溶剂热法是否对杂质众多的地下水厂铁泥也有相同的还原效果,本文作者采用溶剂热法,以乙二醇为溶剂和还原剂,首次在180 ℃条件下将低铁含量地下水厂铁泥(w(Fe)<20%)制备成含有Fe3O4的磁性材料(MMFO),并检测了其对水中亚甲基蓝的吸附效果。
1 实验
1.1 试剂与仪器
实验使用的无水乙酸钠、乙二醇、亚甲基蓝均为分析纯,购置于国药集团化学试剂有限公司。四氧化三铁为分析纯,购置于天津市光复精细化工研究所。分析纯级的粉末活性炭和颗粒活性炭购置于天津市福晨化学试剂厂。实验用水为二次蒸馏水。反冲洗废水取自亚泰水泥厂供水站。
1.2 材料的合成
将反冲洗废水静置8 h后,倾倒上清液,获得沉淀的铁泥,经过80 ℃干燥2 h后备用。
向烧杯中加入铁泥0.675 g,依次加入乙二醇20 mL和无水乙酸钠3.6 g,磁力搅拌30 min,在烧杯中形成悬浊液。将悬浊液转入50 mL反应釜中,放入干燥箱,以4 ℃/min升温至180 ℃,保温6 h。待反应釜冷却后,弃去上层清液,将底部黑色沉淀转移到烧杯中。
向装有黑色沉淀的烧杯中加入蒸馏水,超声清洗5 min,利用磁铁收集黑色沉淀。重复超声清洗处理5次后,将磁铁收集的黑色样品放于真空干燥箱中,40 ℃下真空干燥24 h,得到深黑色粉末(标记为MMFO)。
1.3 吸附效果评价
分别取MMFO样品、粉末活性炭和颗粒活性炭 20 mg置于3个50 mL三角瓶中,平行加入20 mL浓度为10 mg/L的亚甲基蓝溶液。将三角瓶置于室温摇床中,以200 r/min转速振荡吸附,间隔时间取样,用紫外可见分光光度法在665 nm波长下测定水中残留的亚甲基蓝浓度。每组实验做2次平行样,取均值为实验结果。
1.4 表征
采用磁学性质测量系统(MPMS-SQUID-VSM型,美国Quantum Design公司生产)测定样品的磁性。将在空气氛围下恒温300 ℃煅烧1 h后的泥渣和原泥渣、MMFO样品送到北京北达燕园微构分析测试中心,采用X射线粉末衍射仪(Dmax 12kW,日本Rigaku公司生产)对样品进行物相分析。采用X射线荧光光谱仪(ZSX Primus II,日本Rigaku公司生产)对煅烧前后的铁泥进行元素分析。MMFO样品经微波消解后,采用ICP-AES测定消解液中金属元素的含量。在室 温条件下,以α-Fe为参照采用穆斯堡尔谱仪(MS-500型,英国牛津公司生产)对MMFO样品中铁的化学形态进行了分析。进一步采用X射线光电子能谱仪(400型,英国VG-ADES公司生产)分析了样品表面铁的化合态。利用扫描电子显微镜(XL-30-ESEM型,美国FEI公司生产)分析样品的显微组织。采用全自动比表面及介孔微孔物理吸附仪(ASAP 2020M,美国Micromeritics公司生产)对MMFO样品的比表面积与孔径分布进行测定。采用傅立叶变换红外光谱仪(Nicolet 6700,美国Thermo fisher公司生产)在4000~ 400 cm-1范围内测定吸附亚甲基蓝前后MMFO样品的主要官能团。
2 结果与讨论
2.1 铁泥及MMFO样品的表征
地下水厂单级滤池的反冲洗水沉积后,形成的铁泥没有明显的磁响应特征,在磁场中不会发生移动。采用以乙二醇作还原剂的溶剂热法时,可以避免Fe2+的氧化,制备的MMFO样品呈深黑色,在磁场中迅速向磁极迁移并富集(见图1(a)),体现了良好的磁响应特性。当不加磁场时,MMFO样品短时间不会发生沉降,如图1(b)所示。

图1 磁分离前后MMFO样品溶液
Fig. 1 MMFO sample after(a) and before(b) magnetic separation
铁泥、MMFO样品和分析纯Fe3O4在室温下的磁化曲线如图2所示。由图2可以发现,MMFO样品的磁滞回线呈“S”型,没有明显的滞后环,具有软磁特性。MMFO样品的比饱和磁化强度(Ms)达到18.9 A・m2/kg,其剩余磁强度(Mr)仅为0.23 A・m2/kg。受溶剂热法制备的MMFO样品中杂质影响,其磁性低于分析纯Fe3O4的(Ms=68 A・m2/kg)。
铁泥和煅烧铁泥的XRD谱如图3(a)和(b)所示。对比图3(a)和(b)可以发现,铁泥的主要矿物成分为石英、斜长石、微斜长石、云母和高岭石,煅烧前后铁泥的XRD谱中并没有出现明显的Fe2O3衍射峰,可以推测铁泥中铁含量相对较低,且含铁矿物晶化性差而被基峰掩盖[10]。采用XRF分析了铁泥、煅烧铁泥中元素的质量分数,同时通过ICP-AES测定微波消解后MMFO样品中元素的质量分数(见表1),发现铁泥和煅烧铁泥中铁元素的质量分数分别为16.6%和18.5%,表明铁泥样品中存在含铁矿物。煅烧前后铁泥中SiO2质量分数超过40%,Al2O3质量分数也达到11%,此外还含有Ca、K、Mg、Na、Mn等元素。
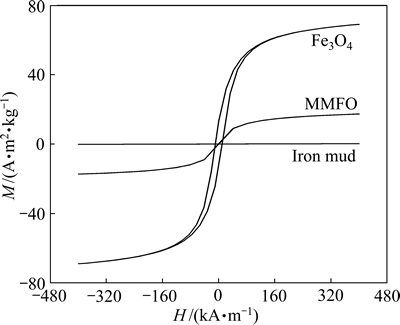
图2 铁泥、MMFO样品和分析纯Fe3O4在室温下的磁滞曲线
Fig. 2 Hysteresis loops of iron mud, MMFO sample and ferroferric oxide powder (AR)

图3 铁泥、煅烧铁泥和MMFO样品的XRD谱
Fig. 3 XRD patterns of iron mud(a), calcined iron mud(b) and MMFO sample(c)
表1 铁泥、煅烧后铁泥和MMFO样品中组分的质量分数
Table 1 Mass fraction of iron mud, calcined iron mud and MMFO sample
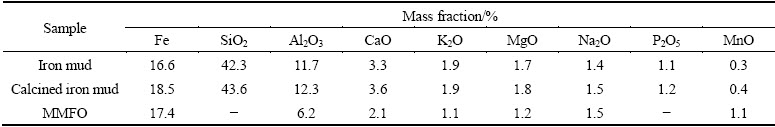
铁泥经过溶剂热法处理后,生成的MMFO样品中铁元素的质量分数为17.2%,其XRD谱中如图3(c)所示。与图3(a)相比,MMFO样品的XRD谱出现微弱的Fe3O4衍射峰,这表明在溶剂热条件下铁泥中含铁矿物发生了结构转变生成磁铁矿,经过多次磁分离纯化的MMFO样品中Al2O3的含量仍接近铁泥中的,结合图3(c)分析发现,MMFO样品中主要杂质为石英和含Al的斜长石、高岭石等矿物。结果表明这些杂质难以完全去除,但不影响其对亚甲基蓝分子的吸附效率和磁分离效果。
干燥后铁泥颗粒细小而分散,粒径约为70 nm(见图4(a))。这类细小颗粒容易穿透板框压滤机的滤膜,进入压滤水中,从而影响铁泥的正常脱水。铁泥经过溶剂热180 ℃处理6 h后,粒子团聚成椭球状(见图4(b)),表面粗糙,粒径约为1.5 μm。

图4 铁泥和MMFO样品的SEM像
Fig. 4 SEM images of iron mud(a) and MMFO sample(b)
图5所示为MMFO样品在室温下测量的穆斯堡尔谱。样品的室温谱可采用两组双线谱(Doublet1 和Doublet2)拟合。其中Doublet1双线谱占份额较高,分别对应高度弥散的Fe3+超顺磁物种和高自旋态的Fe2+物种[11-13]。
对室温谱进行参数分析(见表2),发现Doublet1谱的化学位移为0.34 mm/s,四极裂矩为0.78 mm/s,与文献[14]中报道的Fe3O4基本一致。而Doublet2谱峰形微弱,其化学位移与四极裂矩都较大,可以推测Fe处于高自旋二价铁的化合物中[15]。

图5 MMFO样品穆斯堡尔谱
Fig. 5 M ssbauer spectra of MMFO sample
ssbauer spectra of MMFO sample
表2 MMFO样品穆斯堡尔图参数
Table 2 M ssbauer parameters of MMFO sample
ssbauer parameters of MMFO sample

图6所示为MMFO样品的XPS谱。由图6可知,铁元素有2个分裂峰,结合能分别为711.8和725.6 eV,对应Fe的2p3/2和2p1/2轨道,属于Fe3O4中铁的特征电子结合能[16]。
2.2 MMFO样品的的吸附性能
在室温条件下,以粉末活性炭和颗粒活性炭作为参照,对比研究了MMFO样品对水中亚甲基蓝的吸附效果,如图7所示。在5 min内,等量的MMFO样品和粉末活性炭对水中亚甲基蓝吸附去除率分别达到92.3%和97.5%,在20 min内即可完全吸附水中的亚甲基蓝,由此可见MMFO样品的吸附效果接近粉末活性炭的。相比之下,颗粒活性炭对水中亚甲基蓝的吸附效果较弱,在90 min内吸附去除率仅为37.2%。
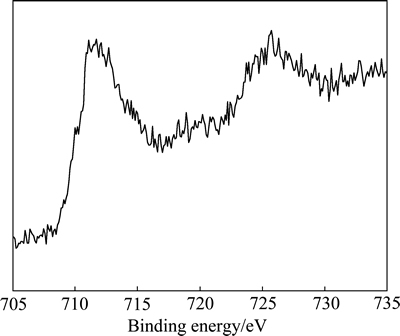
图6 MMFO样品的XPS谱
Fig. 6 XPS spectrum of MMFO sample

图7 MMFO样品、粉末活性炭及颗粒活性炭对亚甲基蓝的吸附去除率的影响
Fig. 7 Effect of MMFO sample, powder active carbon and granular active carbon on adsorption removal rate of methylene blue
分别采用准一级动力学模型和准二级动力学模 型[17]对亚甲基蓝的吸附过程进行拟合,其方程如下所示:
准一级动力学方程,
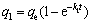 (1)
(1)
准二级动力学方程:
 (2)
(2)
式中:q1为准一级动力模型的吸附量,mg/g;q2为准二级动力学模型的吸附量,mg/g;qe为MMFO样品对亚甲基蓝的理论平衡吸附量,mg/g;k1为准一级动力学模型速率常数,min-1;k2为准二级动力学模型速率常数,g・mg-1・min-1;t为吸附时间,min。
动力学拟合参数如表3所列。由表3中拟合结果可知,准二级动力学模型的相关系数(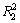 =0.9996)大于准一级动力学模型(
=0.9996)大于准一级动力学模型( =0.9993),且理论平衡吸附量qe (9.86 mg/g)与实验所得的平衡吸附量qe (9.87 mg/g)更接近。因此MMFO样品对亚甲基蓝的吸附符合准二级动力学模型。由于准二级动力学模型中反应速率控制步骤涉及吸附剂与吸附质之间电子交换、电子共享或者离子交换,因此推测MMFO对水中亚甲基蓝的吸附以化学吸附为主。
=0.9993),且理论平衡吸附量qe (9.86 mg/g)与实验所得的平衡吸附量qe (9.87 mg/g)更接近。因此MMFO样品对亚甲基蓝的吸附符合准二级动力学模型。由于准二级动力学模型中反应速率控制步骤涉及吸附剂与吸附质之间电子交换、电子共享或者离子交换,因此推测MMFO对水中亚甲基蓝的吸附以化学吸附为主。
表3 MMFO样品吸附亚甲基蓝的动力学参数
Table 3 Kinetics parameters of methylene blue adsorption on MMFO

MMFO样品的BJH孔径分布曲线和BET吸附-脱附等温线分别如图8和9所示。MMFO样品吸附-脱附等温线有明显的吸附滞后现象,相对压力p/p0在0.5~0.9范围时吸附明显增加,呈现出介孔材料的IV型吸附等温线和H1型滞后回线。样品的BJH孔径分布数据显示,其孔径具有高度一致性,平均值为4 nm;而且MMFO样品具有较高的比表面积(58.5 m2/g),这可能是纳米级二次粒子聚集,如图4(b)所示。而水中亚甲基蓝分子的大小为1.69 nm×0.74 nm×0.38 nm,最大截面积为1.25 nm2 [18-19],因而可以通过MMFO样品纳米孔道的纳米限域效应吸附亚甲基蓝分子。相比于分析纯级粉末活性炭的比表面积(1295.4 m2/g)和颗粒活性炭的比表面积(442.8 m2/g),MMFO样品具有更小的比表面积,但却表现出更强的亚甲基蓝吸附效果。

图8 MMFO样品的孔径分布曲线
Fig. 8 Pore size distribution curve of MMFO sample
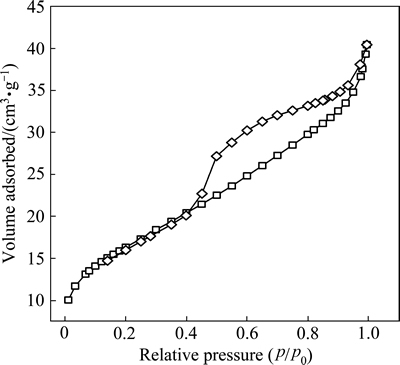
图9 MMFO样品的BET吸附-脱附等温线
Fig. 9 Nitrogen adsorption-desorption isotherms curves of MMFO sample
从经济学角度和效用角度考虑,与粉末活性炭和颗粒活性炭相比,MMFO样品可以通过外置磁场迅速从水中分离,其在废水处理中具有明显的优势。
图10所示为吸附亚甲基蓝前后MMFO样品的红外光谱。图10(a)中,在468、1031和1630 cm-1处的吸收峰值分别对应样品表面的Si―O、Si―O―Si和 ―OH基团。对比吸附亚甲基蓝后样品的红外光谱可知(见图10(b)),1031和468 cm-1在吸附前后并未发生显著变化,表明MMFO样品表面的Si离子并未结合生成新键。1630 cm-1处的吸收峰是MMFO样品表面羟基的弯曲振动引起的[20],在吸附后该吸收峰位移到1637 cm-1,并且强度也发生了变化,表明该羟基可能参与了亚甲基蓝吸附到MMFO表面的过程。亚甲基蓝的分子结构为对称分布,中间为两个苯环与N、S杂环共轭的大π体系,两边的苯环各接一个二甲胺基。在1500 cm-1处的吸收峰对应亚甲基蓝中苯环C=C键的骨架振动,1333和1400 cm-1处的吸附峰对应亚甲基蓝中的甲基峰,表明亚甲基蓝吸附到MMFO样品表面。同时受两侧甲基环境不同影响,与正电荷相连的甲基出现红移,由此推测亚甲基蓝的二甲基胺上氮原子共轭水中正电荷后,与MMFO样品表面羟基作用发生化学吸附。

图10 吸附亚甲基蓝前后MMFO样品的傅立叶红外光谱
Fig. 10 FT-IR spectra of MMFO sample
3 结论
1) 地下水厂含铁污泥颗粒细小,铁含量低且含铁矿物晶化性差,杂质主要为二氧化硅和含Al的矿物。铁泥经过溶剂热法处理后,生成含有Fe3O4的深黑色磁性材料,呈椭球状,粒径约1.5 μm,比饱和磁化强度达18.9 A・m2/kg,可以迅速从水中磁分离。
2) 该合成磁性材料可以迅速吸附水中亚甲基蓝,在5 min内对10 mg/L亚甲基蓝的吸附去除率达到92.3%,效果接近粉末活性炭;在20 min内可以完全吸附亚甲基蓝,其效果超过颗粒活性炭的。
REFERENCES
[1] YU Zhang-long, SHI Zhi-xia, CHEN Yong-mei, NIU Yin-jian, WANG Yong-xia, WAN Ping-yu. Red-mud treatment using oxalic acid by UV irradiation assistance[J]. Transactions of Nonferrous Metals Society of China, 2012, 22(2): 456-460.
[2] WANG S B, ANG H M, TADE M O. Novel applications of red mud as coagulant, adsorbent and catalyst for environmentally benign processes[J]. Chemosphere, 2008, 72(11): 1621-1635.
[3] LI Xiao-bin, XIAO Wei, LIU Wei, LIU Gui-hua, PENG Zhi-hong, ZHOU Qiu-sheng, QI Tian-gui. Recovery of alumina and ferric oxide from Bayer red mud rich in iron by reduction sintering[J]. Transactions of Nonferrous Metals Society of China, 2009, 19(5): 1342-1347.
[4] HILLS C D, KOE L, SOLLARS C J, PERRY R. Early heat of hydration during the solidification of a metal plating sludge[J]. Cement and Concrete Research, 1992, 22(5): 822-832.
[5] AKIN I, ARSLAN G, TOR A, ERSOZ M, CENGELOGLU Y. Arsenic(V) removal from underground water by magnetic nanoparticles synthesized from waste red mud[J]. Journal of Hazardous Materials, 2012, 235: 62-68.
[6] 刘万超, 杨家宽, 肖 波. 拜耳法赤泥中铁的提取及残渣制备建材[J]. 中国有色金属学报, 2008, 18(1): 187-192.
LIU Wan-chao, YANG Jia-kuan, XIAO Bo. Recovering iron and preparing building material with residues from Bayer red mud[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(1): 187-192.
[7] ZHU De-qing, CHUN Tie-jun, PAN Jian, HE Zhen. Recovery of iron from high-iron red mud by reduction roasting with adding sodium salt[J]. Journal of Iron and Steel Research, International, 2012, 19(8): 1-5.
[8] 颜爱国, 刘浩梅, 刘娉婷, 郝喜海, 刘跃军. Fe3O4和Zn2+掺杂型Zn1-xFe2+xO4纳米晶的溶剂热合成和电磁性能[J]. 高等学校化学学报, 2010(3): 447-451.
YAN Ai-guo, LIU Hao-mei, LIU Pin-ting, HAO Xi-hai, LIU Yue-jun. Solvothermal synthesis and electromagnetic properties of Fe3O4 and its Zn2+ substituted Zn1-xFe2+xO4 nanocrystallines[J]. Chemical Journal of Chinese University, 2010(3): 447-451.
[9] 段连峰, 张 雨, 王立民, 金松哲, 吴 化. 溶剂热法合成不同形貌MnFe2O4纳米颗粒及其在污水处理中的应用[J]. 无机材料学报, 2014, 29(7): 763-768.
DUAN Lian-feng, ZHANG Yu, WANG Li-min, JIN Song-zhe, WU Hua. Synthesis and characterization of MnFe2O4 with different morphologies and their application in water treatment[J]. Journal of Inorganic Materials, 2014, 29(7): 763-768.
[10] 陈汝芬, 邓 娟, 宋国强, 魏 雨, 侯登录. 不同晶化度γ-FeOOH的合成及其液相转化研究[J]. 化学学报, 2008, 66(21): 2348-2352.
CHEN Ru-fen, DENG Juan, SONG Guo-qiang, WEI Yu, HOU Deng-lu. Synthesis of different crystalline γ-FeOOH and their liquid phase transformation[J]. Acta Chimica Sinica, 2008, 66(21): 2348-2352.
[11] 李发伸, 王 涛, 王 颖. H2O2氧化法制备Fe3O4纳米颗粒及与共沉淀法制备该样品的比较[J]. 物理学报, 2005, 54(7): 3100-3105.
LI Fa-shen, WANG Tao, WANG Ying. Method for fabricating Fe3O4 nanoparticles using H2O2 and its comparison with coprecipitation method[J]. Acta Physica Sinica, 2005, 54(7): 3100-3105.
[12] SHYLESH S, SCHWEIZER J, ULBER R, THIEL W, SCHUNEMANN V. Mossbauer spectroscopy on super- paramagnetic nanoparticles used as catalyst supports for the production of fine chemicals[J]. Journal of Physics: Conference Series, 2010, 217: 12-24.
[13] RIVAS-SANCHEZ M L, ALVA-VALDIVIA L M, ARENAS- ALATORRE J, URRUTIA-FUCUGAUCHI J, PERRIN M, GOGUITCHAICHVILI A, RUIZ-SANDOVAL M, RAMOS- MOLINA M A. Natural magnetite nanoparticles from an iron-ore deposit: size dependence on magnetic properties[J]. Earth, Planets and Space, 2009, 61(1): 151-160.
[14] 吴卫芳. 穆斯堡尔谱仪及其对物质中Fe的分析应用[J]. 现代仪器, 2000(5): 39-43.
WU Wei-fang. Mossbauer spectroscopy and its application to analyse of Fe in the materials[J]. Modern Instruments, 2000(5): 39-43.
[15] 李爱国, 童永彭, 倪新伯, 王基庆, 郭盘林, 张桂林. 空气中含铁悬浮颗粒的穆斯堡尔研究[J]. 中国环境科学, 2001, 21(3): 198-202.
LI Ai-guo, DONG Yong-peng, NI Xin-bo, WANG Ji-qing, GUO Pan-lin, ZHANG Gui-lin. Mossbauer studies on iron-containing atmospheric suspended particles[J]. China Environmental Science, 2001, 21(3): 198-202.
[16] FAN Xiu-juan, LI Xin. Preparation and magnetic property of multiwalled carbon nanotubes decorated by Fe3O4 nanoparticles[J]. New Carbon Materials, 2012, 27(2): 111-116.
[17] KUMAR K V. Linear and non-linear regression analysis for the sorption kinetics of methylene blue onto activated carbon[J]. Journal of Hazardous Materials, 2006, 137(3): 1538-1544.
[18] 赵立艳, 王学恺, 郭玉国, 吴念祖, 谢有畅. 亚甲基蓝在云母表面吸附状态的研究[J]. 物理化学学报, 2003, 19(10): 896-901.
ZHAO Li-yan, WANG Xue-kai, GUO Yu-guo, WU Nian-zu, XIE You-chang. Adsorption of methylene blue on the muscovite[J]. Acta Physical Chimica Sinica, 2003, 19(10): 896-901.
[19] BRINDLEY G W, THOMPSON T D. Methylene blue absorption by montmorillonites: determinations of surface areas and exchange capacities with different initial cation saturations (clay-organic studies XIX)[J]. Israel Journal of Chemistry, 1970, 8(3): 409-415.
[20] RUSSELL J D. Infrared spectroscopy of ferrihydrite: Evidence for the presence of structural hydroxyl groups[J]. Clay Minerals, 1979, 14(2): 109-114.
(编辑 王 超)
基金项目:国家自然科学基金资助项目(51238001,51108069,51378098);吉林省自然科学基金资助项目(20130101038JC,20140520151JH)
收稿日期:2014-08-11;修订日期:2014-11-16
通信作者:朱遂一,副教授,博士;电话:18672919552;E-mail: zhusy812@nenu.edu.cn