�������Һ�ľ����о�
���1�����Ӣ2������1������1�����ֲ�1�����1
(1. ���������Ƽ���ѧ ұ��ѧԺ������ ������710055��
2. ������ѧ ������ұ��ѧԺ������ ������110004)
ժҪ���������������ӽ�������ij��Ʒλ�����⾫������������Һ���о����о����о�����������������ܹ���Ч�ij����������Һ�е�Cu2+��Fe2+��Pb2+��3���������ӵij����ʷֱ�ﵽ99.60%��99.24%��100.00%������717����֬�������������Һ������Ⱦ�������֬����Ķ�̬����������Ϊ125.28 g/Lʪ��֬������ʵ��ȷ�������ӽ�����Ѽ��������������£���ʼ��ҺpHΪ9~10��������Ũ��Ϊ11.46 g/L������Ϊ4 mL/min������������֬���������Ч����ѡ�����5 mol/L NH4Cl��4 mol/L NH3��OH �Ļ��Һ�Ը��������֬���н����������ʿɴ�99.85%������Һ��������Ũ�ȴ�167.72 g/L��
�ؼ��ʣ���Ʒλ�⾫������泥����γ��������ӽ���������
��ͼ����ţ�TF841.2 ���ױ�־�룺A ���±�ţ�1672-7207(2014)09-2959-07
Research on purification of ammonium molybdate solution
YU Juan1, YANG Hongying2, FANG Zhao1, WANG Bin1, LI Lingbo1, ZHU Jun1
(1. School of Metallurgy Engineering, Xi��an University of Architecture and Technology, Xi��an 710055, China;
2. School of Materials & Metallurgy, Northeastern University, Shenyang 110004, China)
Abstract: Sulfide precipitation and ion exchange method were used to purify the ammonium molybdate soiution obtained by ammonia leaching of a low-grade molybdnum concentration. The experimental results show that the sulfide precipitation method is effective to remove Cu2+, Fe2+ and Pb2+from ammonium molybdate solution, and the precipitation rates of these impurities reach 99.60%, 99.24% and 100.00%, respectively. 717 type anion resin was used to further purify the supernatant obtained from sulfide precipitation process. The dynamic saturation adsorption quantity of anion resin for molybdate is about 125.28 g/L. The optimum conditions of purification process were determined through condition test and list as follows: pH of initial solution is 9-10, the mass concentration of molybdate is 11.46 g/L, and the flow rate is 4 mL/min. The resin has best adsorption effect on molybdate under this conditions. A solution composed of 5 mol/L NH4Cl and 4 mol/L NH3��OH is used to desorbed molybdate from the loaded resin. The desorption rate is 99.85%. The content of molybdate in desorption solution reaches 167.72 g/L.
Key words: low grade molybdenum concentrates; ammonium molybdate; sulfide precipitation; ion exchange; purification
��������������淋���Ҫԭ��[1]�����Ÿ�Ʒλ��ѡ�����IJ��Ͽ��ɣ���Ʒλ��������ϵ���ӵ���ѡ�����Խ��Խ�ܵ����ǵĹ�ע������Ʒλ�ͣ��ҹ�����ϵ���ӣ������͵������ѡ�������⾫����Ʒλһ��Ϊ20%~40%����������ͭ������Ǧ��п���ơ�þ���ص����ʵĺ���Ҳ�ϸߣ�����Ʒλ�⾫��[2-3]�����������Ѵﵽ�⾫��Ĺ��ұ�[4]�������͵��⾫���ں����Ľ��������л��д�������������(Cu2+��Fe2+��Pb2+��Zn2+��Ca2+��Mg2+��K+��)�����������Һ��ʹ���������Һ����ɫ���ҽϻ��ǡ���ˣ����������Ṥ���У��������Һ�ľ�������dz��ؼ�����ֱ�Ӿ�����Ʒ����茶���������ȼ���Ϊ�˽�����什���Һ�е�����������Mo6+������������������(Cu2+��Fe2+��Pb2+��Zn2+)���룬һ����������������������ƻ���臨�����什�����Һ���г����־���[5-7]���÷����Ļ���ԭ�����£�������ˮ��Һ��ˮ����γ����⣬�������������Һ�еķ����������ӷ�Ӧ�����ܶȻ���С�Ľ�������������Ӷ��ﵽ��ȥ�����������ӵ�Ŀ��[8]���ھ��������У��������Һ�е�Cu2+��Pb2+��H2S(aq)�������
S2++2H2O=H2S(aq)+2OH- (1)
Me2++H2S(aq)=MeS(s)��+2H+ (2)
CuS��PbS���ܶȻ�Ksp��С���ֱ�Ϊ2.4��10-35��2.29��10-27[8]����ˣ���Һ�е�Cu2+��Pb2+����������ȫͨ��������ȥ����Һ�е�Fe2+��������������γ�FeS��Ksp�ϴ�Ϊ1.32��10-17[8]�����ȶ�������������������Һ��pH��10���ϣ�Fe2+���γ�����������������ˣ���Һ�е�Fe2+��������ȫ������ȥ��������Һ�е�Zn2+�����백����γɵ�Zn-NH3�������ȶ�����������Һ�е�H2S(aq)����γ�ZnS���ܶȻ��ϴ���ˣ����η�����Zn2+��ȥ���������ޡ���Zn2+�����������ﹲ����������Ч���Ϻ�[9]����������Һ����������������Ca2+��Mg2+��K+�ȣ�������������ȥ��Ч���ϲ���ӽ����������豸�����������ã����Է��롢�������ᴿ�������Һ[10-16]����ʹ�������Һ�е��������Ӽ�����ͣ��������ӽ�����֬����ѭ������������ʹ�óɱ��͡���ˣ��������߽�ϵ�Ʒλ�����⾫����Һ���������Ӻ����ߵ��ص㣬������������������������Һ���г����־��������������ӽ�����֬������Ⱦ������Ի�ô��Ƚϸߵ��������Һ��Ϊ����淋Ľᾧ�ṩ������
1 ʵ��
1.1 ԭ��
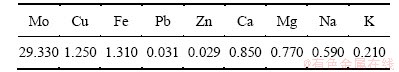
�ⱺɰ�������������������Һ��Ϊ������ʼ��Һ������Ҫ�ɷ����1��ʾ��
��1 �������Һ��Ҫ��ѧ�ɷ�(����Ũ��)
Table 1 Main chemical compositions of ammonium molybdate solution g/L
1.2 ʵ�鷽��
1.2.1 ������
ʵ����÷�����Na2S��9H2O��Ϊ�������ij�������ȡһ���������������������Һ�����ձ��У����ձ��������ˮԡ���в����н��裬���¶�35~40 ���±���1 h��Ȼ������ܽ����úõ�����(��������)��Һ��μ����ձ��У��۲��ձ�����Һ��ɫ�ı仯��ÿ��һ��ʱ�䣬ȡһ���ձ��е�����Һ�����Թ��кͿհ�����ˮ���бȶԣ�������Һ����ɫ��ʱ������������������ֹͣ����ͼ��ȣ�Ѹ�ٽ��ձ��е�Һ����й�����Һ���и����Ӻ����ⶨ��ת�����ӽ�����ʹ�á�(������Һ�ļ�����Ҫ���ϸ����й�������Һ�ʻ�ɫ�����е���ᷴӦ������������Σ���������ʧ)��
1.2.2 ���ӽ�����
ʵ����õ���֬��717��(����)ǿ���Ա���ϩϵ�����ӽ�����֬��ʵ��ǰ������֬װ����֬��������10%��NaCl��Һ����24 h��Ȼ������ˮƯϴ��ʹ�ų�ˮ������ɫ������4% NaOH��Һ����8 h��Ȼ��ž���Һ����ˮ��ϴ�����ԣ�֮������5% HCl����8 h��Ȼ��ž���Һ����ˮ��ϴ�����ԣ����ʹ��4% NaOH��Һ����8 h�ž���Һ������ˮϴ�����ԡ���Ԥ�����õ���֬װ����(ֱ������)Ϊ20 mm��450 mm���л��������д����ӽ���ʹ�á��������ռ�����Һ���������е��⺬������������֬������ˮϴ�Ӻ���һ��Ũ�ȵĽ���Һ���н����������������⺬����
��֬�Ķ�̬����������ʵ���У���Ķ�̬�������������㹫ʽ���£�
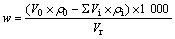
ʽ�У�wΪ������������g/L��V0Ϊ����茶�����ʼ��Һ�����L����0Ϊ��ʼ��Һ���������Ũ�ȣ�g/L��ViΪ������ȡ����Һ�����L����iΪ��ȡ����Һ���������Ũ�ȣ�g/L��VrΪ��֬�����90 mL��
2 ���������
2.1 ��������
��������������Һ�����������˺�õ�����Һ�и���������Ũ�����2��ʾ��
��2 ����������Һ�Ļ�ѧ�ɷ�(����Ũ��)
Table 2 Chemical compositions of supernatant obtained from sulfide precipitation process g/L
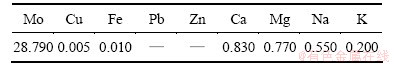
�ӱ�2���Կ�����������������Һ�е�ͭ��������Ũ���ɳ�ʼ��Һ�е�1.25 g/L���͵�0.005 g/L��������Ϊ99.6%�������ӵ�����Ũ����1.31 g/L����0.01 g/L��������Ϊ99.24%����Һ��δ��������Ǧ���Ӻ�п���ӣ�������2��������ȫ����Һ���ѳ�����������Һ�е�������Ca2+��Mg2+��Na+��K+������û�г�ȥ����ˣ������������ѳ��������Һ��Cu2+��Fe2+��Pb2+��Zn2+��Ч��������
2.2 ���ӽ�������
ȡ���������������Һ�������ӽ�����Ⱦ������ֱ���֬�ı�������������ʼ��Һ����Ũ�ȡ���ʼ��ҺpH����Һ���١�����Һ���༰����Һ����Ũ�ȶ����ӽ���Ч����Ӱ�졣
2.2.1 ��֬�Ķ�̬����������
ȡ����Ԥ��������֬���ж�̬����ʵ�飬ȷ����֬����ı�������������ʵ���������£���ʼ��Һ���⺬��Ϊ28.79 g/L����ҺpHΪ9����Һ����Ϊ3.5 mL/min��ʵ������з�����ȡ����Һ�����βⶨ����Һ���������Ũ�ȣ�������Һ��������Ũ�Ⱥ㶨ʱ��������֬�ﵽ������������ͼ1��ʾΪ����Һ��������Ũ�ȵı仯����ͼ1���Կ�������������Һ�������������Һ�������100 mL��������Ũ�ȳ�������������Һ����ﵽ685 mLʱ������Һ��������Ũ��Ϊ22.72 g/L��֮���ټ�������������Һ������Һ��������Ũ�Ȼ����ȶ���22.72~23.14 g/L���������ʱ��֬���������ѻ����ﵽ���͡����������֬��Ķ�̬����������Ϊ125.28 g/Lʪ��֬��
2.2.2 ��Һ������Ũ�ȶ�������Ч����Ӱ��
��ʼ��Һ������Ũ�ȶ���֬�������Ч���кܴ��Ӱ�죬��ˣ��о����������Һ���⺬������������ʵ�Ӱ�졣ʵ���������£���ҺpHΪ9����Һ����Ϊ3 mL/min���������Һ����Ũ�ȷֱ�Ϊ6.27��11.46��17.17��23.46��28.79 g/L�������ͼ2��ʾ����ͼ2���Կ��������ų�ʼ�������Һ��������Ũ�ȵIJ����������������Ѹ�ٽ��ͣ�����ʼ��Һ��������Ũ��Ϊ6.27 g/Lʱ�����������Ϊ99.01%������ʼ��Һ����Ũ������11.46 g/Lʱ�����������н��ͣ�Ϊ98.26%�����������ʼ��Һ���������Ũ�ȣ����������Ѹ���½�������ʼ��Һ��������Ũ��Ϊ����23.46��28.79 g/Lʱ�����������Ѹ�ٽ��͵�81.72%��66.39%�����Ͻ����������֬�����˴�������Ũ��̫�ߵij�ʼ��Һ�����ѡ����������ߵij�ʼ��Һ(������Ũ��6.27 g/L)�����ڰ�������������Һ����Ũ�Ƚϸߣ���Һ�ڽ������ӽ�����ǰ��Ҫ�ô�����ˮϡ�ͣ���Ӧ���ϲ���������ˣ������ӽ������������У���ʼ��Һ����淋�����Ũ��Ϊ11.46 g/L�Ϻ��ʡ�
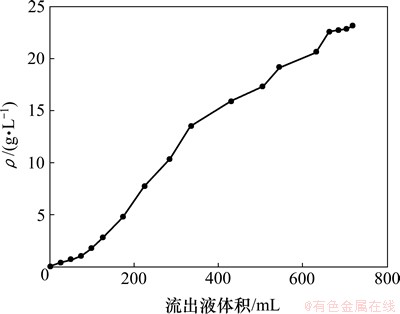
ͼ1 717������֬������������
Fig. 1 Adsorption curves of 717 type anion resin for Mo
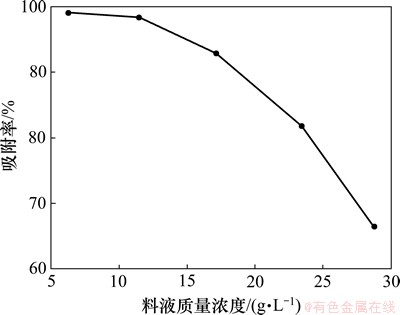
ͼ2 ��Һ����Ũ�ȶ��������ʵ�Ӱ��
Fig. 2 Effect of feed mass concentration on adsorption rate of Mo
2.2.3 ��ҺpH��������Ч����Ӱ��
��ʼ��Һ��pH����Ӱ����֬����ĵ�ɼ������ʵ����ӻ����̣���������֬�������Ч�������ܴ��Ӱ��[13-14]����ˣ��о��˳�ʼ��ҺpH�ֱ�Ϊ6��7��8��9��10ʱ����֬�������Ч����ʵ���������£��������Һ����Ũ��Ϊ11.46 g/L������Ϊ3 mL/min���������Һ��Һ��Ϊ150 mL��pH����֬�������Ӱ���ͼ3��
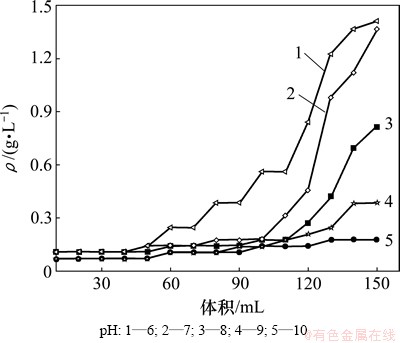
ͼ3 pH��������Ч����Ӱ��
Fig. 3 Effects of pH on adsorption of Mo
��ͼ3���Կ���������麟�ʼ��ҺpH���������Ч���кܴ��Ӱ�죬���ų�ʼ��ҺpH�IJ��ϼ�С������Һ����ĺ�����������ʼ��ҺpHΪ10����Һ��Ϊ150 mLʱ������Һ���������Ũ��Ϊ0.18 g/L������Һ��ʼpHΪ7����Һ����ﵽ100 mLʱ������Һ��������Ũ�ȿ�ʼ����������Һ���ﵽ150 mLʱ������Һ��������Ũ�ȴﵽ1.37 g/L������Һ��ʼpHΪ6����Һ����ﵽ60 mLʱ������Һ��������Ũ�ȿ�ʼ����������Һ���ﵽ150 mLʱ������Һ��������Ũ�ȴﵽ1.41 g/L���������ʼ�������ҺpH������������10ʱ����֬���������������á�
ͼ4��ʾΪ����麟�ʼ��ҺpH����֬�����������ʵ�Ӱ�졣��ͼ4���Կ��������ų�ʼ��ҺpH�IJ���������֬����Һ�������������������ʼ��ҺpHΪ6ʱ����֬����������ʽ�Ϊ69.76%����߳�ʼ��ҺpH��7�������������������Ϊ72.02%����������ҺpH�����������Ѹ��������ʼ��ҺpH����9ʱ���������������95.88%�����Ը�������pHʱ��Һ�������ʡ�����Ҫ��������ҺpH�ϸ�ʱ����Һ������Ҫ��MoO42-��ʽ���ڣ�����֬�������ã�����ʼ��ҺpH��ʱ����Һ�е����Ծۺ���������ʽ���ڣ����Ӱ뾶�ϴ�Ӱ����֬������Ч������ˣ����ӽ��������У���ʼ��Һ��pH������9~10�Ϻ��ʡ�
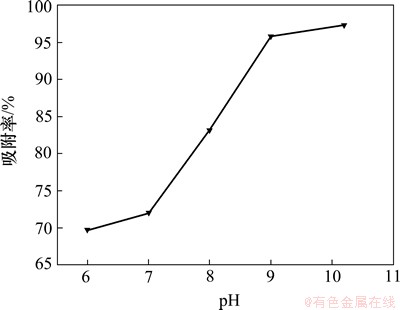
ͼ4 pH���������ʵ�Ӱ��
Fig. 4 Effect of pH on adsorption rate of Mo
2.2.4 ��Һ���ٶ�������Ч����Ӱ��
ͼ5��ʾΪ��Һ���ٶ���֬������Ч����Ӱ�졣ʵ���������£���ҺpHΪ10��������Ũ��Ϊ11.46 g/L�����ٷֱ�Ϊ2��4��7����10 mL/min���������Һ��Һ��Ϊ150 mL��
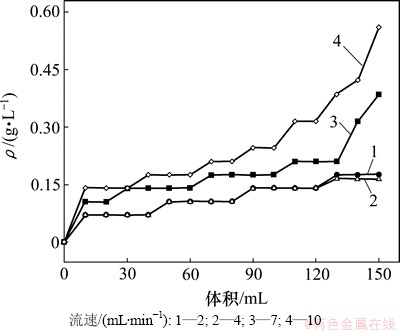
ͼ5 ��Һ���ٶ���֬�������Ӱ��
Fig. 5 Effects of feed velocity on adsorption of Mo by resin
��ͼ5���Կ������������Һ���ٶ���֬�������Ч���нϴ��Ӱ�졣�������ӽ�����������Һ���ٵIJ�����������Һ���������Ũ��Ѹ��������Һ����150 mL����Һ����Ϊ2��4 mL/minʱ������Һ���������Ũ�����Ե�����Һ����Ϊ7��10 mL/minʱ�������Ũ�ȣ�����������Һ����Ϊ7��10 mL/minʱ����Һ���ٹ���������ĵ�λ�����Һ�����еĶ���������Һ����ǿ�Ӷ������֬���ܳ��������Һ�е��⡣������Һ����Ϊ2 mL/minʱ��������Һ���ٹ�������ˮ�ӷ��������Һ��pH���ͣ���Ӱ����֬���������Ч����
ͼ6��ʾΪ��Һ���ٶ��������ʵ�Ӱ�졣��ͼ6���Կ������������������������Һ���ٵ��������С������Һ����Ϊ2��4 mL/minʱ����������ʷֱ�ﵽ95.38%��96.77%������Һ��������7 mL/minʱ�����������Ѹ�ٽ��͵�86.46%����������Һ���ٵ�10 mL/minʱ����������ʽ���Ϊ75.24%����ˣ����ӽ������������У���Һ���ٿ�����4 mL/min��������֬����ij��������
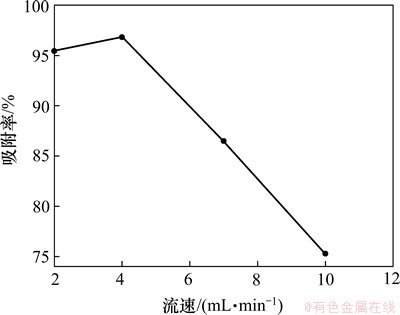
ͼ6 ��Һ���ٶ��������ʵ�Ӱ��
Fig. 6 Effect of feed velocity on adsorption rate of Mo
2.2.5 ����Һ����Ը�������֬����Ч����Ӱ��
���ڸ������717����������֬��ͨ�����ü���Һ����н�������ˣ���ʵ��ֱ����NH3��OH��NH4Cl��NaOH��NH4Cl��NH3��OH���Һ�Ը��������֬���н����������ͼ7��ʾ����ͼ7��֪������ʹ��3 mol/L NH3��OH ��3 mol/L NaOH�Ը��������֬�Ľ���Ч�������룬�����ʷֱ�Ϊ4.40%��22.43%����������NH4Cl������Һ����Ľ��������ֻ��79.40%��������3 mol/L NH4Cl��2 mol/L NH3��OH�Ļ��Һʱ�����������֬��������ʸ�����������Һ���ﵽ92.61%�����������NH4Cl��NH3��OH���Һ��Ϊ�������717��ǿ���������ӽ�����֬�Ľ���Һ����ʡ�
2.2.6 ����ҺŨ�ȶԸ�������֬����Ч����Ӱ��
����NH4Cl��NH3��OH���Һ��Ϊ�������717��ǿ���������ӽ�����֬�Ľ���Һ��ʵ���о���NH4Cl��NH4OH���Һ��Ũ�ȶ������Ч����Ӱ�죬ּ��ȷ������Һ�����Ũ�ȡ�
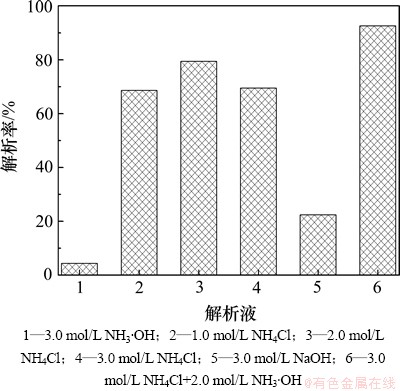
ͼ7 ��ͬ����Һ�и�������֬������
Fig. 7 Desorption rate of molybdate from loaded resin in various solutions
ʵ����õĽ���ҺŨ�ȷֱ�Ϊ��3 mol/L NH4Cl��2 mol/L NH3��OH���Һ��4 mol/L NH4Cl��3 mol/L NH3��OH���Һ��5 mol/L NH4Cl��4 mol/L NH3��OH���Һ��ʵ������У�������ȡϴ��Һ���ⶨ�����⺬������ϴ��Һ��������Ũ�Ƚ���0.1 g/Lʱ��ֹͣ����Һ�ļ��룬ϴ������ͼ8��
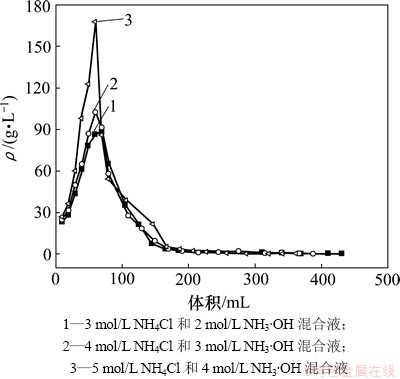
ͼ8 ����ҺŨ�ȶԸ�������֬����Ч����Ӱ��
Fig. 8 Effects of concentration of solution on desorption effect of molybdate from loaded resin
��ͼ8��֪���ڽ��������У�����3 mol/L NH4Cl��2 mol/L NH3��OH���Һ��������ϴ��Һ����ﵽ70 mLʱ������Һ��������Ũ�Ƚ�Ϊ87.82 g/L������4 mol/L NH4Cl��3 mol/L NH3��OH���Һ������������Һ���60 mLʱ������Һ���������Ũ�ȴﵽ102.02 g/L����һ����߽���ҺŨ�ȣ�����5 mol/L NH4Cl��4 mol/L NH3��OH���Һ������������Һ���Ϊ60 mLʱ������Һ���������Ũ�ȴﵽ167.72 g/L����˵����λ����Ľ���Һ��5 mol/L NH4Cl��4 mol/L NH3��OH����Һ�Ľ�������Ҫ��������2��Ũ�������Ľ���Һ��
��ͼ8�����Կ���������3 mol/L NH4Cl��2 mol/L NH3��OH���Һ������������Һ����ﵽ430 mLʱ������Һ��������Ũ�Ƚ���0.1 g/L������4 mol/L NH4Cl��3 mol/L NH3��OH���Һ������������Һ����ﵽ387 mLʱ������Һ��������Ũ�Ⱦ��ѽ���0.1 g/L��������5 mol/L NH4Cl��4 mol/L NH3��OH���Һ����ʱ�������ٶȿ죬������Һ����ﵽ361 mLʱ������Һ���������Ũ�Ƚ���0.1 g/L�����������5 mol/L NH4Cl ��4 mol/L NH3��OH��Ϊ����Һ�Ը��������֬����ʱ�������ٶȿ죬����Ч���á�
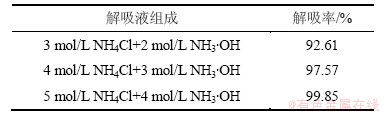
��3��ʾΪ3��Ũ�Ƚ���Һ�Ը�������֬�Ľ����ʵ�Ӱ�졣�ӱ�3���Կ��������Ż��Һ��NH4Cl��NH3��OHŨ�ȵ����ӣ����������֬�Ľ����ʲ�������Ũ��Ϊ5 mol/L NH4Cl��4 mol/L NH3��OH�Ľ���Һ����Ľ����ʴﵽ99.85%��������ϸ�Ũ�ȵ�NH4Cl��NH3��OH��Һ����Ľ���Ч���á�����ʵ��Ӧ���У�����ҺŨ�Ȳ���̫�ߣ���Ũ�ȹ���ʱ��һ���棬��ˮ���ӷ���ʧ���������ӣ���һ���棬��ʹ�Ͷ�����������֬�������ѡ���ˣ��ۺ����Ͻ�����Ը������717����֬����5 mol/L NH4Cl��4 mol/L NH3��OH�Ļ�Ͻ���Һ���н�����
��3 NH4Cl��NH3��OH���ҺŨ�ȶ�������ʵ�Ӱ��
Table 3 Effect of concentrations of NH4Cl and NH3��OH on desorption rate of Mo
3 ����
1) �������������������Һ�е�Cu2+��Fe2+��Pb2+���г����ѳ�������Ч���ã���Һ��ͭ������Ǧ�ij����ʷֱ�ﵽ99.6%��99.24%��100%��
2) ����717��ǿ���Ա���ϩϵ����֬�������������Һ������Ⱦ���������֬����������ٶȿ죬��̬����������Ϊ125.28 mg/mLʪ��֬�����ӽ�������Ѽ��������������£�����ǰ�������Һ��pHΪ9~10���������Ũ��Ϊ11.46 g/L������Ϊ4 mL/min������5 mol/L NH4Cl��4 mol/L NH3��OH�Ļ��Һ�Ը��������֬���н����������ٶȿ죬�����ʴ�99.85%������Һ������Ũ�ȴﵽ167.72 g/L��
�ο����ף�
[1] SHI Lihua, WANG Xuewen, WANG Mingyu, et al. Extraction of molybdenum from high-impurity ferromolybdenum by roasting with Na2CO3 and CaO and leaching with water[J]. Hydrometallurgy, 2011, 108(3): 214-219.
[2] Kumar M, Mankhand T R, Murthy D S R, et al. Refining of a low-grade molybdenite concentrate[J]. Hydrometallurgy, 2007, 86(1/2): 56-62.
[3] ��ѡ���ֲᡷ��ί��. ѡ���ֲ�: 8��1�ֲ�[M]. ����: ұ��ҵ������, 1990: 71-72.
Mineral Processing Handbook Editorial Board. Handbook of mineral processing: Part 1, volume 8[M]. Beijing: Metallurgical Industry Press, 1990: 71-72.
[4] ������, ��С��, ������, ��. ����-��̬�ݸ�ѡ����ѡij��ѡ���������о�[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2008, 39(2): 300-306.
LIU Jiongtian, LI Xiaobing, WANG Yongtian, et al. Experimental study on separating some molybdenum ore by using cyclonic-static micro-bubble flotation column[J]. Journal of Central South University (Science and Technology,) 2008, 39(2): 300-306.
[5] Shariat M H, Setoodeh N, Atash D R. Optimising conditions for hydrometallurgical production of purified molybdenum trioxide from roastedmolybdenite of Sarcheshmeh[J]. Minerals Engineering, 2001, 14(7): 815-820.
[6] ���ܷ�, ���, ʩ�Ѹ�. ������������������������м۽������ۺϻ���[J]. �й���ҵ, 2000, 24(5): 20-22.
HUANG Xianfa, ZOU Wei, SHI Youfu. The comprehensive recovery of valuable metals in the cleaning slag in ammonium molybdate production[J]. China Molybdenum Industry, 2000, 24(5): 20-22.
[7] ¬����, �Ժ�, ������. ���⾫����ȡ����淋������о�[J]. ʪ��ұ��, 2005, 24(1): 19-22.
LU Guojian, ZHAO Hong, LI Shourong. Study on producing ammonium molybdate using molybdenum concentrate[J]. Hydrometallurgy of China, 2005, 24(1): 19-22.
[8] ����˵. ��ɫұ��ԭ��[M]. ����: ұ��ҵ������, 2012: 192-195.
FU Chongshui. Non-ferrous metallurgical principle[M]. Beijing: Metallurgical Industry Press, 2012: 192-195.
[9] ������, ����, ����ϼ. ���ӽ����������Ʊ������[J]. �й���ҵ, 2011, 35(3): 33-35.
ZHOU Xinwen, WANG Lei, TANG Lixia. Preparation of ammonium molybdate by ion exchange exchange removing impurities[J]. China Molybdenum Industry, 2011, 35(3): 33-35.
[10] ������, Ф����, ���, ��. �ӷ�ʯ�ʹ����л��շ�����������о�[J]. ��ұ����, 2004, 24(3): 47-49.
CHEN Xinglong, XIAO Liansheng, XU Jie, et al. A study on recovering vanadium and molybdenum from spent catalyst[J]. Mining and Metallurgical Engineering, 2004, 24(3): 47-49.
[11] HU Jian, WANG Xuewen, XIAO Liansheng, et al. Removal of vanadium from molybdate solution by ion exchange[J]. Hydrometallurgy, 2009, 95(3): 203-206.
[12] ���ٿ�. ���ӽ�����ʪ��ұ���е�Ӧ��[M]. ����: ұ��ҵ������, 1991: 20-50.
MA Rongjun. Application of ion exchange in hydrometallurgy [M]. Beijing: Metallurgical Industry Press, 1991: 20-50.
[13] LI Qinggang, ZHANG Qixiu, ZENG Li, et al. Removal of vanadium from ammonium molybdate solution by ion exchange original research article[J]. Transactions of Nonferrous Metals Society of China, 2009, 19(3): 735-739.
[14] ���ݾ�, �ܴ���, Ҧ��Ƽ, ��. D201��4��֬������(��)�����ܼ�����[J]. ��ɫ����, 2006, 58(4): 29-32.
WANG Huijun, XIONG Chuhua, YAO Caiping, et al. Adsorption performance and mechanism of Mo(��) on D201��4 resin[J]. Nonferrous Metals, 2006, 58(4): 29-32.
[15] ����, ��ѧ��, Ф����, ��. ��������Һ���ӽ����ⷰ��������о�[J]. �й���ɫ����ѧ��, 2008, 18(1): 112-116.
HU Jian, WANG Xuewen, XIAO Liansheng, et al. Mechanism of vanadium removal from molybdate solution by ion-exchange[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(1): 112-116.
[16] �Ű�ʤ, ����ϲ, ������, ��. ��ȡ������������о���չ[J]. ��ɫ����, 2004, 56(4): 89-91.
ZHANG Bangsheng, JIANG Kaixi, WANG Haibei, et al. Process in W/M separation by solvent extraction[J]. Nonferrous Metals, 2004, 56(4): 89-91.
(�༭ �°���)
�ո����ڣ�2013-11-03�������ڣ�2014-03-22
������Ŀ��������Ȼ��ѧ����������Ŀ(51304151,51304152)�����Ҹ����о���չ�ƻ�(��863���ƻ�)��Ŀ(2012AA061502)�����������Ƽ���ѧ����Ƽ������ص�������Ŀ(QN1204)�����������Ƽ���ѧѧ�ƽ����˲���Ŀ(RC1227, RC1132)
ͨ�����ߣ����(1983-)��Ů������ػ��ˣ���ʿ����ʦ������ѡ��ʪ��ұ���о����绰��029-82202923��E-mail: neuyujuan@163.com