锂离子电池正极材料LiFe0.9Ni0.1PO4的合成与性能
王晓琼, 李新海, 王志兴, 郭华军, 彭文杰, 刘凤举
(中南大学 冶金科学与工程学院, 长沙 410083)
摘 要: 采用高温固相法合成锂离子电池正极材料LiFe0.9Ni0.1PO4, 研究了反应条件对合成产物的影响。 利用X射线衍射(XRD)和扫描电镜(SEM)对所得样品的晶体结构、 表面形貌等进行了表征。 结果表明: 反应温度和时间对LiFe0.9Ni0.1PO4晶体结构及材料性能均有较大影响, 其中650℃下焙烧20h合成出的样品电化学性能最佳; 在20mA/g 的电流密度下进行恒流充放电时, 首次放电比容量可达145mA・h/g, 循环30次后比容量仍为135mA・h/g, 容量衰减仅为6.9%。
关键词: LiFePO4; 锂离子电池; 正极材料; 镍掺杂; 固相反应; 电化学性能 中图分类号: TM912.9
文献标识码: A
Synthesis and performance of LiFe0.9Ni0.1PO4 as cathode material in lithium-ion battery
WANG Xiao-qiong, LI Xin-hai, WANG Zhi-xing, GUO Hua-jun,PENG Wen-jie, LIU Feng-ju
(School of Metallurgical Science and Engineering,Central South University, Changsha 410083, China)
Abstract: LiFe0.9Ni0.1PO4 for cathode materials of lithium-ion battery was synthesized by solid-state reaction. The effects of synthesis temperature and reaction time on the electrochemical performance were studied systematically. The crystalline structure and microstructures of resulting specimens were characterized by X-ray diffractometry (XRD) and scanning electromicroscopy (SEM). The results show that the reaction temperature and time have great effect on the structures and electrochemical performance of the obtained samples. Further electrochemical tests indicate that the material synthesized optimally at 650℃ for 20h possesses excellent electrochemical performance. The first discharge capacity of LiFe0.9Ni0.1PO4 on 20mA/g current density arrives at 145mA・h/g and after 30 times cycling the discharge capacity is still up to 135mA・h/g, only with about 6.9% capacity fade.
Key words: lithium iron phosphate; lithium-ion battery; cathode material; Ni-doping; solid-state reaction; electrochemical performance
-
在对锂离子电池正极材料的研究过程中, 用含铁物质代替含钴物质正逐渐引起人们的关注[1]。 可插入锂的含铁正极材料有很多, 其中LiFePO4由于无毒对环境友好, 稳定性好, 价格低廉, 还具有工作电位适中(3.45V vs Li/Li+)、 理论比容量高[CM(22](170mA・h/g)等优点, 被认为是最具有潜力的正[CM)]极材料之一。 LiFePO4属橄榄石型结构, 空间群为Pmmb[2], 其中锂离子占据的八面体相互共边, 它们在a-c平面沿着c轴方向延伸, 形成链状排列; 铁原子占据八面体相互共顶点, 它们在与锂原子相邻的a-c平面沿着c轴方向形成锯齿形排列, 在锂原子所在的a-c平面中, 包含有PO4四面体, 这样就限制了锂离子的移动空间, 因此它的电导比其他的层状化合物低[3]。 LiFePO4具有极低的电子导电率和离子扩散速度[4, 5], 这是其实用化的瓶颈, 因此如何提高LiFePO4的电子导电性是当前研究的热点。 提高LiFePO4的电导率主要有如下几种方法: 1) 包覆碳或纳米金属粒子形成中间导电体, 如: 乙炔黑[6]、 聚丙烯[7]、 碳凝胶[8]、 蔗糖[9]等都曾被用作碳源来制备碳处理(包覆)LiFePO4; Croce等[8]采用液相法直接将银、 铜等金属微粉掺入LiFePO4中; 2) 使合成物具有细小均匀的晶粒尺寸[10]; 3) 掺杂, 即掺杂少量金属离子合成缺陷半导体; Chung等[11]通过掺杂Mg2+、 Al3+、 Ti4+、 Zr4+、 Nb5+和W6+等离子, 将LiFePO4电子电导率提高了8个数量级, 这种通过制造晶格缺陷调节LiFePO4材料电性能的途径从本质上提高了晶体材料自身的导电性。 近年来, 国际上不同的研究小组对改性的LiFePO4进行了广泛的研究。 本文作者在前期实验中采用了固相烧结法在LiFePO4铁位掺镍合成LiFe1-xNixPO4(x=0.05~0.5)正极材料, 实验结果证明铁位掺镍对改善材料的自身导电性有一定的作用, 其中LiFe0.9Ni0.1PO4的材料的性能最佳。 因此, 本文作者进一步系统研究了反应温度、 时间对合成产物LiFe0.9Ni0.1PO4物相结构和电化学性质的影响。
1 实验
1.1 LiFe0.9Ni0.1PO4的合成
合成用反应物为分析纯的Li2CO3、 FeC2O4・2 H2O、 NH4H2PO4和Ni(CH3COO)2・4H2O, 以组成LiFe0.9Ni0.1PO4的化学计量比混合均匀, 在乙醇介质中球磨5h。 所得粉体在低温下烘干以除去乙醇, 然后将混合粉体转移至程序控温的管式炉内, 通高纯氩气保护, 升温至320℃, 预分解一段时间, 然后升温至指定温度, 保温一段时间后自然降至室温, 所得样品磨细备用。 未掺杂样品制备方式同上, 区别为不添加镍源。
1.2 材料的表征
本研究采用的仪器是日本Rigaku D/max2550VB+18kW转靶X射线衍射仪。 物相分析的条件是: Cu kα辐射, 40kV, 50mA, 步宽0.02°, 扫描速度2(°)/min, 扫描范围(2θ)为10°~90°; 用JEOL公司的JSM-5600LV扫描电子显微镜在20kV下分别以不同的放大倍数对样品的表面形貌进行观察。
合成材料的电导率通过直接伏安法进行初步测定[12]。 首先将粉末压成圆柱体, 成型压力为30MPa, 然后测出样品的厚度、 直径及电阻, 通过以下公式计算出样品的电导率:
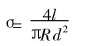
式中 l为样品的厚度; d为样品的直径; R为样品电阻。
1.3 电池组装和测试
通过组装CR2032型扣式电池测试材料的电化学性能。 LiFe0.9Ni0.1PO4、 乙炔黑(电池级, 广东省化工进出口公司)和PVDF(聚偏二氟乙烯, 法国阿托化学)按质量比8∶1∶1混合并研磨均匀后, 加入适量的有机溶剂NMP(N-甲基吡咯烷酮, 纯度99.9%, 南京京龙化工厂), 研磨成均匀糊状物涂于0.02mm厚的铝箔上, 在120℃下真空干燥12h得到正极片。 在充满高纯氩的手套箱内, 以金属锂片为负极, Celgard2400微孔聚丙烯膜(Celgard Inc. USA)为隔膜, 以溶于1∶1∶1(体积比)的EC(碳酸乙烯脂)/DMC(1, 2-二甲基碳酸脂)/EMC(碳酸甲乙脂)的1mol/L的LiPF6为电解液, 组装成CR2032型扣式电池。 在BTS-51二次电池性能检测仪(深圳新威尔多电子设备有限公司)上测试充放电性能。 采用恒流/恒压方式对电池充/放电。 恒流充电电流为20mA/g, 终止电压为4.1V; 恒流放电电流为20mA/g, 终止电压为2.3V。
2 结果及讨论
2.1 合成条件对LiFe0.9Ni0.1PO4物相结构的影响
图1所示为不同温度反应8h合成的LiFe0.9-Ni0.1PO4的X射线衍射谱。 对比500~750℃合成样品的X射线衍射谱可以发现, 在500℃就可以得到与LiFePO4相同的橄榄石晶型结构(标准JCPDS卡40-1499), 属正交晶系的Pnma空间群。 而随着温度的提高, 从图1中可以看出各晶面的衍射强度明显高于500℃合成的样品, 衍射峰逐渐尖锐清晰, 半高宽变窄。 根据X射线衍射理论, 衍射峰的宽化是由于晶体生长不完全、 结晶度不高、 晶体中存在较多的缺陷及晶粒细小引起的。 这一现象表明高温有利于晶体的生成, 形成完整的晶格与较大的晶粒。 但晶粒尺寸的提高并不是本研究所希望的, 因为对具有橄榄石结构的LiFePO4正极材料的锂离子扩散速度的研究表明, 锂离子在这类材料中的扩散系数为10-14~10-16 cm2/s[13], 较其他正极材料如LiMn2O4(10-9~10-10 cm2/s)[14]低5~7个数量级。 因此, 为了改善锂离子的扩散性能, 应尽量缩短锂离子的扩散距离, 即尽量减小晶粒尺寸, 或者说避免合成温度过高。
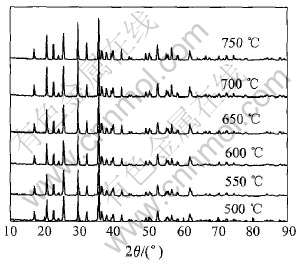
图1 不同温度反应8h合成的LiFe0.9Ni0.1PO4的X射线衍射谱
Fig.1 XRD patterns of LiFe0.9Ni0.1PO4 synthesized at different reaction temperatures for 8h
图2所示为在650℃不同反应时间合成的LiFe0.9Ni0.1PO4的X射线衍射谱。 从图中可以看出在650℃反应4h就已经可以得到结晶完整的LiFe0.9Ni0.1-PO4相。 随着合成时间的延长, 样品的衍射峰逐渐尖锐, 说明合成时间的延长对LiFe0.9Ni0.1PO4的生长有利, 在某一温度下适当延长反应时间会使反应更加完全, 得到较为理想的单相产物。
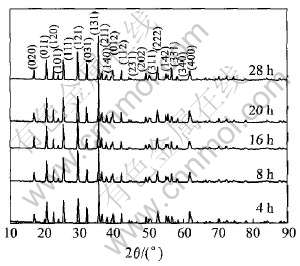
图2 在650℃反应不同时间合成的LiFe0.9Ni0.1PO4的X射线衍射谱
Fig.2 XRD patterns of LiFe0.9Ni0.1PO4 synthesized at 650℃ for different reaction time
2.2 合成条件对LiFe0.9Ni0.1PO4表面形貌的影响
电极材料的表面形貌对其电化学性能有很大的影响。 图3所示为不同温度反应8h合成的LiFe0.9-Ni0.1PO4的SEM形貌。 从图中可以看出合成温度对LiFe0.9Ni0.1PO4表面形貌影响显著。 在同一合成时间下, 500℃合成的样品颗粒细小, 明显存在小粒子团聚成大粒子的趋势(见图3(a)); 600℃合成的样品仍然保持团聚外形见图3(b); 当温度提高到650℃时, 可以看到样品晶体发育较完整, 颗粒均匀, 并且表面光滑(见图3(c)); 750℃合成的样品粒度明显增大, 颗粒表面光滑, 形状规则(见图3(d))。 这说明合成温度过高会强烈促进LiFe0.9Ni0.1-PO4晶体生长, 使其晶粒粗大, 晶格完整, 不利于锂离子在材料晶格中的扩散。
图4所示为在650℃不同反应时间合成的LiFe0.9Ni0.1PO4的SEM形貌。 从图中可以看出合成时间对LiFe0.9Ni0.1PO4表面形貌影响并不显著。 8h和20h合成的样品的形貌差别不大, 但当合成时间增加到28h时, 颗粒明显长大。
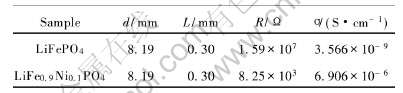
图5所示在650℃反应20h合成的LiFePO4和LiFe0.9Ni0.1PO4的SEM形貌。 由图可见, 纯相LiFePO4的晶体较粗大, 表面粗糙, 并且可以发现大部分一次粒子团聚形成大颗粒的二次粒子; 而掺杂后样品颗粒较均匀细小, 表面光滑, 表明Ni离子掺杂可改善LiFePO4的表面形态, 在一定程度上降低LiFePO4的粒径, 从而提高了Li离子在LiFePO4晶体中的扩散性能[15, 16]。 进一步对样品的电导率σ进行了初步测试, 结果表明, 掺Ni后的LiFePO4电导率较纯相的提高了3个数量级以上, 见表1。
表1 样品LiFePO4 和LiFe0.9Ni0.1PO4的电导率
Table 1 Conductivities of LiFePO4 and LiFe0.9Ni0.1PO4
2.3 合成条件对LiFe0.9Ni0.1PO4充放电性能的影响
LiFe0.9Ni0.1PO4/Li电池的充电过程对应于锂离子从LiFe0.9Ni0.1PO4电极中脱出过程, 放电过程对应于锂离子在LiFe0.9Ni0.1PO4电极中的嵌入过程。 不同温度反应8h合成的LiFe0.9Ni0.1PO4首次[CM(22]充放电曲线如图6所示。 从图中可看出, LiFe0.9- Ni0.1PO4样品的首次充放电容量随着合成温度的升高先增大, 然后又趋于减小, 650℃时达到最大值130mA・h/g。

图3 不同温度下反应8h合成的LiFe0.9Ni0.1PO4的SEM形貌
Fig.3 SEM morphologies of LiFe0.9Ni0.1PO4 synthesized at different reaction temperatures for 8h

图4 在650℃反应不同时间合成的LiFe0.9Ni0.1PO4的SEM形貌
Fig.4 SEM morphologies of LiFe0.9Ni0.1PO4 synthesized at 650℃ for different reaction time

图5 在650℃反应20h合成的LiFePO4和LiFe0.9Ni0.1PO4的SEM形貌
Fig.5 SEM morphologies of LiFePO4 and LiFe0.9Ni0.1PO4 synthesized at 650℃ for 20h
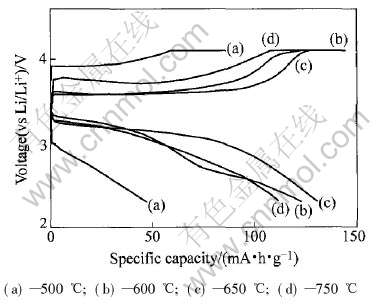
图6 不同温度反应8h合成的LiFe0.9Ni0.1PO4的首次充放电图
Fig.6 First charge-discharge curves of LiFe0.9Ni0.1PO4 synthesized at different reaction temperatures for 8h
图7所示为650℃不同反应时间合成的LiFe0.9-Ni0.1PO4样品的首次充放电曲线。 从图中可以看出, 不同的反应时间对LiFe0.9Ni0.1PO4样品的首次充放电比容量也有一定的影响, 但影响效果不如温度明显。 随着反应时间的增加, LiFe0.9Ni0.1PO4的首次放电比容量先增加后减小, 当时间为20h时, 放电比容量最大为145mA・h/g, 较文献上所提供的纯LiFePO4的一般放电比容量110mA・h/g[17], 要高出31.8%。 而且, 从图中还可以看出在该条件下合成的样品的充放电平台平稳, 电极极化小。
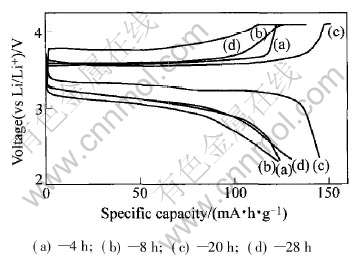
图7 650℃不同反应时间合成的LiFe0.9Ni0.1PO4的首次充放电图
Fig.7 First charge-discharge curves of LiFe0.9Ni0.1PO4 synthesized at 650℃ for different reaction time
2.4 样品循环性能测试
图8所示为650℃焙烧20h合成的LiFePO4和LiFe0.9Ni0.1PO4样品的循环性能曲线。 从图中可以看出, LiFePO4和LiFe0.9Ni0.1PO4的首次充放电容量分别为115和145mA・h/g, 经过30次循环后放电容量分别为94和135mA・h/g。 循环30次后LiFe0.9Ni0.1PO4的比容量衰减仅为6.9%, 而LiFePO4则达到了18.3%。 由此可见, 在该最优条件下合成的LiFe0.9Ni0.1PO4较LiFePO4而言, 不仅初次放电比容量有较大的提高, 而且循环性能也有一定的改善。
通过研究可知, 不同合成条件下得到的LiFe0.9-Ni0.1PO4的物理性质各不相同, 因而其电化学性能差异也很大。 Anderson等[18]研究了第一个循环的容量损失, 认为第一个循环容量损失的原因可能有两种, 一种称为半径模型(Radial model), 另一种称为马赛克模型(Mosaic model)。 他们认为两种模型共同作用的可能性更大, 即不活跃的磷酸亚铁锂(Inactive LiFePO4)区域的存在造成了容量损失[18]。 LiFe0.9Ni0.1PO4晶体的颗粒越大, Li离子在固相中扩散的路程就越长, 材料的电性能就越受Li离子扩散的限制, 所以减小粒径有助于材料体积比容量的提高。 由于Ni元素是在分子水平上掺入LiFePO4晶体中, 得到的是固溶体结构, 小晶体有相互聚集长大成晶体的趋势。 尽管一次粒子比较小, 但聚集成了更为细密的二次粒子, 有助于提高材料的振实密度和体积比容量。 因此通过改变烧结条件调控好LiFe0.9Ni0.1PO4晶体的粒径, 解决好电子导电性能、 离子扩散性能与材料的体积比容量之间的矛盾, 将进一步推动LiFe0.9Ni0.1PO4的实用化。
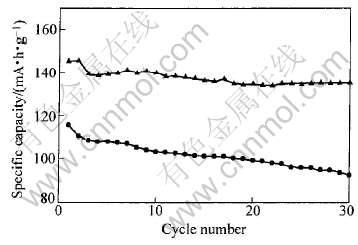
图8 LiFePO4 和LiFe0.9Ni0.1PO4的循环性能曲线
Fig.8 Cycle performance curves of LiFePO4 and LiFe0.9Ni0.1PO4
3 结论
研究了反应温度和时间对LiFe0.9Ni0.1PO4物理性能及电化学性能的影响。 实验结果表明, 在500℃下反应8h就可以得到与LiFePO4相同的橄榄石晶型结构, 随反应时间的延长, 反应温度的升高, LiFe0.9Ni0.1PO4结晶将更加完整, 晶粒将明显长大。 650℃下反应20h得到的LiFe0.9Ni0.1PO4样品, 结晶完整、 颗粒细小、 粒径相对均匀。 其电导率及电化学性能与相同条件下合成的LiFePO4相比有较大的改善, 以20mA/g电流放电, 其首次放电容量为145mA・h/g, 循环30次后比容量仍达到135mA・h/g, 衰减仅为6.9%。
REFERENCES
[1]Andersson A S, Kalska B, Haggstrom L, et al. Lithium extraction/insertion in LiFePO4: an X-ray diffraction and Moessbauer spectroscopy study[J]. Solid State Ionics, 2000, 130(1-2): 41-52.
[2]Padhi A K, Nanjundaswamy K S, Goodenough J B. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J]. Journal of Electrochemical Society, 1997, 144(4): 1188-1194.
[3]Yang S F, Song Y N, Zavalij P Y, et al. Reactivity, stability and electrochemical behavior of lithium iron phosphates[J]. Electrochemistry Communications, 2002, 4 (3): 239-2441.
[4]Tarascon J M, Armand M. Issues and challenges facing rechargeable lithium batteries[J]. Nature, 2001, 414(15): 359-367.
[5]Michael Thackeray. Lithium-ion batteries: an unexpected conductor[J]. Nature Materials, 2002, 1(2): 81-82.
[6]Kim H Y, Cho B W, Cho W I. Electronically conductive phospho-olivines as lithium storage electrodes[J]. Journal of Power Sources, 2004, 132(1-2): 235-239.
[7]Herstedt M, Stjerndahl M, Nyten A, et al. Surface chemistry of carbon-treated LiFePO4 particles for Li-ion battery cathodes studied by PES[J]. Electrochemical and Solid-State Letters, 2003, 6(9): 202-206.
[8]Yang S, Song Y, Zowalij P Y, et al. Reactivity, Stability and electrochemical behavior of lithium iron phosphates[J]. Electrochemistry Communications, 2002, 4(3) : 239-244.
[9]Ravet N, Chouinard Y, Magan J F. Electroactivity of natural and synthetic triphylite[J]. Journal of Power Sources, 2001, 97-98: 503-507.
[10]Franger S, Le C F, Bourbon C, et al. Comparison between different LiFePO4 synthesis routes and their influence on its physico-chemical properties[J]. J Power Sources, 2003, 119-121: 252-2571.
[11]Chung S Y, Bloking J T, Chiang Y M. Electronically conductive phospho-olivines as lithium storage electrodes[J]. Nature Materials, 2002, 1(2): 123-128.
[12]黄学杰. 锂离子电池正极材料磷酸铁锂研究进展[J]. 电池工业, 2004, 9(4): 174-180.
HUANG Xue-jie. Research progress in cathode material LiFePO4 for Li-ion battery[J]. Chinese Battery Industry, 2004, 9(4): 174-180.
[13]Prosini P P, Lisi M, Zane D, et al. Determination of the chemical diffusion coefficient of lithium in LiFePO4[J]. Solid State Ionics, 2002, 148(1-2): 45-51.
[14]Wakinara M, Li G H, Ikuta H, et al. Chemical diffusion coefficients of lithium in LiMyMn2-yO4(M=Co and Cr)[J]. Solid State Ionics, 1996, 86-88: 907-909.
[15]Huang H, Yin S C, Nazar L F. Approaching theoretical capacity of LiFePO4 at room temperature at high rates[J]. Electrochemical and Solid-State Letters, 2001, 4(10): A170-172.
[16]Prosini P P, Carewska M, Scaccia S, et al. A new synthetic route for preparing LiFePO4 with enhanced electrochemical performance[J]. Journal of the Electrochemical Society, 2002, 149(7): A886-890.
[17]Ravet N, Chouinard Y, Magan J F. Electroactivity of natural and synthetic triphylite[J]. J Power Sources, 2001, 97-98: 503-507.
[18]Andersson A S, Thomas J O. The source of first-cycle capacity loss in LiFePO4[J]. Journal of Power Sources, 2001, 97-98: 498-502.
(编辑何学锋)
基金项目: 国家自然科学基金资助项目(50302016)
收稿日期: 2005-05-23; 修订日期: 2005-09-22
通讯作者: 李新海, 教授; 电话0731-8836633, E-mail: zxwang@mail.csu.edu.cn