2, 5-���ϻ�-1, 3, 4������������ϵ��ϳɼ���绯ѧ����
�Ᵽ�����°��䣬Ф���£���ӵ����Ԭ ��
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ������ ��ɳ��410083)
ժ Ҫ����ˮ���¡�����̼Ϊԭ�ϣ����Ұ�Ϊ��������������Ϊת����������Ϊ�ữ������85 ����Һ�ۺϵõ�2, 5-���ϻ�-1, 3, 4�����(DMcT)���ú������������Ľṹ�����ý����迹���о�PAn��PMOT��CuC2O4��DMcT�ĵ�����ã�����PAn/DMcT�����������ϵij�ŵ����ܡ��о������������ѷ�Ӧ����Ϊ��n(����̼)?n(��������)?n(ˮ����)=3.5?1.5?1���ữpHֵ������0.6~1.0����ʱ�����ʴﵽ92%��PAn��DMcT�ĵ���������ԣ�ʹ���迹��1.28 k����С��270 ����PAn/DMcT�������������״ηŵ������Ϊ225 mA?h/g����DMcT��135 mA?h/g��ȣ��ŵ��������������ߡ�
�ؼ��ʣ�2, 5-���ϻ�-1, 3, 4�������Һ�ۺϣ������迹����ŵ�����
��ͼ����ţ�TQ252.5 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2009)02-0305-06
Synthesis and electrochemical properties of cathode material of 2, 5-dimercaptor-1, 3, 4-thiadiazole
WU Bao-an, CHEN Bai-zhen, XIAO Li-xin, HU Yong-jun, YUAN Yan
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: 2, 5-dimercaptor-1, 3, 4-thiadiazole was synthesized by emulsion polymerization method at 85 �� with triethylamine as the accelerating agent, sodium hydroxide as the convert agent, sulfuric acid as the acidulant. The structure of the product was analyzed by infrared spectrum. The AC impedance method was adopted to study the catalysis effect of PAn, PMOT, CuC2O4 and the charge �Cdischarge capacity of PAn/DMcT was tested. The results show that under the optimum reaction condition, i.e. n(CS2)?n(NaOH)?n(N2H4��H2O)=3.5?1.5?1 and the acidulant pH=0.6-1.0, the yield reaches up to 92%. The effect of PAn on the electrochemical activity of DMcT is very obvious, and the initial discharge capacity of PAn/DMcT reaches up to 225 mA?h/g, compared with 135 mA?h/g of DMcT.
Key words: 2, 5-dimercaptor-1, 3, 4-thiadiazole; emulsion polymerization; AC impedance; charge and discharge capacity
�л���������Ϊ﮶��ε�ص��������Բ��Ͼ��зdz��ߵı�����������Ϊ�����з�չǰ;�Ļ�������֮һ[1-3]��Liu��[4]��һϵ�еľ��л��������������Ͻ����о�����Ϊ���ڶ���л������У�2, 5-���ϻ�-1, 3, 4�����(���DMcT)�۵�ϵͣ�����ĵ�����Ҳ�ϸߣ����нϸߵ����۱����� (362 mA?h/g)����������[5]�������ºͶ���̼�ϳ�DMcT�������ʽϵ͡������ĵ�[6]��ˮ���ºͶ���̼�ϳ�DMcT�����ʽϸߡ����������������������µĵ绯ѧ������ԭ�dz����������û�еõ�ʵ��Ӧ��[7]����ˣ�Ѱ�Һ��ʵĵ���������DMcT��������ԭ��Ӧ�ٶȳ���Ŀǰ����Ҫ�о�����[8-9]����������ͨ����Һ�ۺϷ��ϳ�DMcT�����õ���ѷ�Ӧ��������DMcT���в��ӣ��о��佻���迹��̽�ֵ����������Ѱ�ҽϺõĵ���������������ŵ����ߡ�
1 ʵ ��
1.1 ʵ��ԭ�����Լ�
ʵ��ԭ�Ϻ��Լ��У�ˮ����(AR�����ϻ���Լ�����˾����)������̼(AR����ҩ���Ż�ѧ�Լ�����˾����)�����Ұ�(AR������д�ï��ѧ�Լ�������)���������� (AR������з紬��ѧ�Լ�����˾����)��PVDF(AR ElfAtochem, Kynar2801)��NMP(�Ͼ���������������)��Celgard 2400�۱�ϩĤ(Celgard Inc.USA����)��1 mol/L LiPF6/EC-DMC(��������ﻯ��������)��
1.2 ��Ӧ����
2������̼�����������Ұ����ڵ�����·ֱ�ȡ��ˮ�����е�2����ԭ�ӣ������м����{H(CS2)NN(CS2) H}2-��2��TEAH+���м��������ǿ���������������תλ������ϡ�����ữ����DMcT���ϳ�;�����£�

1.3 DMcT�ĺϳ�
��������ƿ�м���200 mL����ˮ��Ȼ���������¼���һ�������������ƣ������ܽ���ȴ��6~8 �棬����25 mL��ˮ���£�ҡ�ȡ��ټ���һ�������黯�������밴���Ϲ�ϵ�趨�Ķ���̼�����跴Ӧ֮����2 h���ں��´����������Ϸ������ȷ�Ӧ���¶ȿ�����75~85 �档��Ӧ3 h����Ӧֹͣ����ȴ�����£�����������ữ��pHֵ������0.6~1.0���»�2 h�����ˡ�ˮϴ����������ؽᾧ�ᴿ������ո��������� 85 ���ɵõ���״����ɫ��Ʒ��
1.4 �绯ѧ�������������
��DMcT��PAn/DMcT���ϲ��Ϸֱ�Ϊ������������Ȳ�ں�PVDF��������8?1?1��ϲ���ĥ���Ⱥ����������л��ܼ�NMP��ĥ�ɾ��Ⱥ�״���Ϳ�������ϣ���85 ����ո���12 h��Ȼ���Ƴ�����Ƭ���Խ����ƬΪ������1 mol/L LiPF6/EC-DMEΪ���Һ��Celgard 2400 �۱�ϩĤΪ��Ĥ�����������������װ��2032�Ϳ�ʽ��ء�
ʹ���Ϻ�����������˾��CHI660B�͵绯ѧ����վ���ڽ����ź����Ϊ5 mV��Ƶ��Ϊ10 mHz��100 kHz��������(25 ��)���н����迹���ԡ�ʹ��BTS-51�Ͷ��ε�����ܼ����(����������������豸����˾) ������(25 ��)���Գ�ŵ����ܡ�
������ײ�����WQF-310����Ҷ�任����������Ͻ��У�����Ϊ400~4 000 cm-1���ֱ���Ϊ2 cm-1��C��H��NԪ�ز���CHN-O-RAPIDԪ�ط�����(�¹�Heraeus��˾����)���з�����
2 ���������
2.1 �黯���Բ��ʵ�Ӱ��
��ͬ�黯���Է�Ӧ���ʵ�Ӱ�����1��ʾ���ɱ�1��֪����ͬ�黯���Է�Ӧ���ʾ��кܴ��Ӱ�죬�����Ұ��������黯����ȣ����黯��������ͬʱ����Ӧ����IJ��ʽϸߡ���ʵ������л����֣����Ұ��ڼ���ˮ��Һ���нϺõ��ܽ��ԣ��黯������ǿ���ܼ��ٷ�Ӧ������3 h����ɷ�Ӧ���ҷ�Ӧ�����ºͣ�������㡣���������Ұ����黯�����������Ƶ��������������٣�������Ϊ���Ұ��ܼ����м��������ɣ��Ӷ�ʹ�������תλ���ڽ���[10]��
��1 ��ͬ�黯���Է�Ӧ��Ӱ��
Table 1 Effects of different emulsifying agent on reaction

2.2 ���ϱ������ʵĹ�ϵ
�����Ұ����黯������85 ��ʱˮ���ºͶ���̼��Ӧ�ϳ�DMcT���ܷ�Ӧʱ��Ϊ3 h������̼��ˮ���µ�Ħ���������ʵĹ�ϵ��ͼ1��ʾ����ͼ1���Կ��������Ŷ���̼��ˮ����Ħ���ȵ����ӣ�������������������̼��ˮ���µ�Ħ����Ϊ3.5ʱ��������ߣ�Ħ���ȼ������ӣ�����ȴ�½����������ڶ���̼�ӷ����������̼��ˮ���µ�Ħ���ȣ�������ˮ���ºͶ���̼�ij�ַ�Ӧ�Ӷ�ʹ�������ӣ���Ħ���ȹ��ߣ����γɸ���������ʹ���ʷ����½��������Ħ����Ϊ3.5��
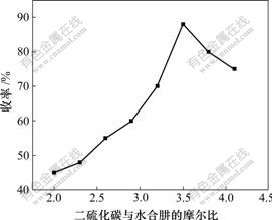
ͼ1 ����̼��ˮ���µ�Ħ���������ʵĹ�ϵ
Fig.1 Relationship between mole rate of CS2 to N2H4��H2O and yield
2.3 ��Ӧ�¶������ʵĹ�ϵ
�����Ұ����黯��������̼��ˮ����(3.5?1)��Ӧ�ϳ�DMcT����ʱ��Ϊ3 h���䷴Ӧ�¶������ʵĹ�ϵ��ͼ2��ʾ����ͼ2��֪�������¶ȵ����ߣ����������������¶ȴﵽ85 ��ʱ��������ߣ����������¶ȣ����ʷ����½����������ڷ�Ӧ�����ȼӳɷ�Ӧ���¶ȸ������ڷ�Ӧ�Ľ��У����¶ȹ����ֲ�������Ӧ��ʹ�����½����ʷ�Ӧ�¶���85 ��Ϊ�ˡ�

ͼ2 ��Ӧ�¶������ʵĹ�ϵ
Fig.2 Relationship between reaction temperature and yield
2.4 ��Ӧʱ�������ʵĹ�ϵ
�����Ұ����黯������85 ��ʱ����̼ˮ�����(3.5?1)��Ӧ�ϳ�DMcT���䷴Ӧʱ�������ʵĹ�ϵ��ͼ3��ʾ����ͼ3���Կ��������ŷ�Ӧʱ����� �ӣ�������������3.5 hʱ������ߣ�����ʱ���һ�����ӣ����ʷ����½���������������ʱ������ӣ�ˮ���������̼��Ӧ�Ӵ���֣�������ߣ�����ʱ�����������Ӧ���������ʷ����½����ʷ�Ӧʱ���� 3.5 hΪ�ˡ�

ͼ3 ʱ�������ʵĹ�ϵ
Fig.3 Relationship between time and yield
���Ͻ����������ѵķ�Ӧ����Ϊ�������Ұ����黯������Ӧ�¶�Ϊ85 �棬��Ӧʱ��Ϊ3.5 h��n(����̼)?n(ˮ����)=3.5?1��n(��������)?n(ˮ����)=1.5?1���ữpHֵΪ0.6~1.0����ʱ�������ȶ���92%��
2.5 DMCT��Ʒ�ĺ�����ײ��Խ��
������ײ�������KBrѹƬ�����б��ײ��ԡ�Ȼ��������Ʒ���ĥϸ��ȡ������ĩ��KBr���Ⱥ�ѹ��Ƭ����������ײɼ���������ײ��Խ����ͼ4��ʾ���ɱ�2��ͼ4��֪���ϳɲ�Ʒ������������λ�����ֵ����һ��[11]��
��2 DMcT�ĺ�����Ĺ���λ��(��ֵ)
Table 2 Affiliation position of IR spectrum of DMcT (standard value)


ͼ4 DMcT��Ʒ�ĺ������
Fig.4 IR spectrum of DMcT
2.6 DMcT��ƷԪ�ؽ��
DMcT��Ʒ��Ԫ�ط�����������ۼ���ֵ���3��ʾ���ɱ�3��֪��C��H��NԪ�ط��������麬��(������������ͬ)�����ۺ�������һ�¡�
��3 DMcT��Ԫ�ط���
Table 3 Elements analysis of DMcT w/%

2.7 DMCT��Ʒ������Ӻ����迹
ͼ5��ʾΪDMcT�зֱ����PAn��PMOT��CuC2O4�����������Ͻ����迹����ƽ��ͼ�����У�ZReΪʵ���迹��ZImΪ�鲿�迹����ͼ5��֪�� ��DMcT��Ʒ��DMcT�в���PAn��PMOT��CuC2O4����Ʒ���ڸ�Ƶ�γ���1�������Եİ�Բ���ڵ�Ƶ�γ���һ��ֱ�ߣ����Ӻ�绯ѧ�迹�����Լ�С���ر��Dz���PAn��绯ѧ�迹��ԭ����1.28 k����С�� 270 ����

1������PAn; 2������PMOT; 3������CuC2O4; 4����DMcT
ͼ5 ��ͬ����DMcT���������迹����ƽ��ͼ
Fig.5 A.C impedance plots of DMcT with different adulterations
DMcT�в���PMOT������������γɵ��Ӹ���-���帴����ٽ���DMcT��������ԭ��Ӧ����ʹ��DMcT�ĵ绯ѧ�迹��С[12]��
DMcT�в�������CuC2O4�����ɶ�����(DMcT)2�����У�Cu2+��ԭΪCu+��Cu+��DMcT�����ӵ������γ�һά��������ʹ��������ԭ��λ���ͣ��Ӷ��ӿ�绯ѧ��Ӧ[13]��
DMcT�в���PAn���γɵĸ��ϲ���PAn/DMcT �����ߴ��ڵ���ת��[14]�ȷ�Ӧ��PAn��Ϊ���Ӽ������ڳ��(����)�����У���ԭ̬��DMcT�ѵ��Ӵ�������̬��PAn�����������ۺϷ�Ӧ���ڷŵ�(��ԭ)�����У�����̬��DMcT(��DMcT�ۺ���)�ӻ�ԭ̬��PAn����õ����Ӷ�������ԭ��۷�Ӧ��������PAn��DMcT֮��ͨ�����ӻ���DMcT���ϻ���PAn���ǰ�����ö��������������֮��ĵ��ת�ƣ����ԣ����ӵĴ������ú�������������DMcT��PAn���Ӽ�������������ԭ��Ӧ�ӿ�[15-16]��
2.8 DMcT��PAn/DMcT��ŵ�����
DMcT-Li��ص��״γ�ŵ�������ͼ6��ʾ����ͼ6��֪��DMcT�״γ�ŵ�ı������ֱ�Ϊ250��135 mA��h/g���״γ�ŵ�Ч��Ϊ54%������PAn/DMcTΪ�������ϵ��״γ�ŵ��������ͼ7��ʾ����ͼ7��֪��PAn/DMcT�״γ�ŵ�ı������ֱ�Ϊ252��225 mA��h/g���״γ�ŵ�Ч��Ϊ89.3%������20��ѭ�����ŵ������˥����170 mA��h/g���ŵ������������״ηŵ������˥����24.4%����ʵ�ϣ��ڷŵ����DMcT����Щ���ŵĿ����ԱȽϲ������ȫ�ŵ磬�ʷŵ�������ϵͣ�������PAn��PAn��DMcT�ﵽ�˷���ˮƽ���ںϣ�PAn��DMcT�������Եĵ�����ã�ʹ����Щ���ŵĵ绯ѧ������ߣ��Ӷ������PAn/DMcT�����������ϵ�ѭ��������
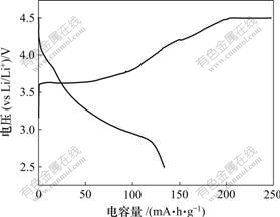
ͼ6 DMcT-Li��ص��״γ�ŵ�����(0.1C)
Fig.6 Initial charge/discharge curves of DMcT-Li battery
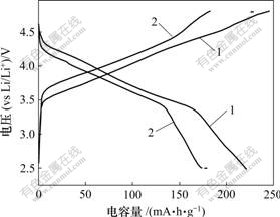
1����1��2����20��
ͼ7 PAn/DMcT-Li��صij�ŵ�����(0.1C)
Fig.7 Charge/discharge curves of PAn/DMcT-Li battery
ͼ8��ʾΪPAn/DMcT-Li��ʽ����ڲ�ͬ���ʷŵ��ٶ��µķŵ����ߡ���ͼ8��֪��PAn/DMcT-Li��ʽ��صķŵ���������ŷŵ��������������٣���0.1C��0.2C��0.3C�ı��ʷŵ�ʱ��PAn/DMcT-Li�ķŵ�������ֱ�Ϊ225��179��135 mA��h/g���������ڳ�ŵ��������ʱ���缫����Ҳ�������ڼ������õ�Ӱ�죬ʹ��س�ŵ粻��ȫ����ɷŵ���������١�

1��0.1C; 2��0.2C; 3��0.3C
ͼ8 PAn/DMcT-Li��صı��ʷŵ�����
Fig.8 Rate discharge curves of DMcT-Li battery
3 �� ��
a. ��ˮ���¡�����̼Ϊԭ�ϣ������Ұ�Ϊ��������������Ϊת����������Ħ����Ϊn(����̼)?n(ˮ����) =3.5?1��n(��������)?n(ˮ����)=1.5?1������Ϊ�ữ�����ữpHֵ������0.6~1.0����Һ�ۺϵõ���2, 5-���ϻ�-1, 3, 4�����(DMcT)�����ȶ���92%����Ʒ������������λ�����ֵ����һ�£�C��H��NԪ�ط���������ֵ������ֵ����һ�¡�
b. ��PMOT��CuC2O4��ȣ�PAn��DMCT�����õĵ�����ã�ʹ��绯ѧ�迹��С��ԭ����1/5��DMcT-Li��ʽ�����0.1C��ŵ�ʱ���״γ�ŵ������ֱ�Ϊ250��135 mA?h/g���״γ�ŵ�Ч��Ϊ54%��PAn/DMcT-Li��ʽ�����0.1C��ŵ�ʱ���״γ�ŵ������ֱ�Ϊ252��225 mA?h/g���״γ�ŵ�Ч��Ϊ89.3%������20��ѭ���ŵ������˥����170 mA?h/g, �ŵ������������״ηŵ������˥����24.4%���ɼ���PAn/DMcT-Li��ʽ��طŵ��������������ߣ�����ŵ籶���£����ڼ������ã��ŵ���������١�
�ο����ף�
[1] ����־. ���л������ﴢ�ܲ��ϵĵ绯ѧ�����о�[J]. ��ѧͨ��, 2001, 64(2): 295-298.
SU Yu-zhi. Studies of the electrochemical properties of organic disulfides and their polymer storage materials[J]. ChemistryOnline, 2001, 64(2): 295-298.
[2] Visco S J, Maihe C C, Jonghel C D, et al. A novel class of organo sulfur electrodes energy storage[J]. Electrochem Soc, 1989, 136(3): 661-664.
[3] Liu M, Visco S J, Jonghel C D. Electrode kinetics of organodisufide cathodes for storage batteries[J]. Electrochem Soc, 1990, 137(3): 750-759.
[4] Liu M, Viso S J, De Jonghe L C, et al. Electrochemical properties of organic disulfide/thiolate redox couples[J]. Electrochem Soc, 1989, 136(9): 2570-2575.
[5] ������, ���ξ�, ѦȺ��. ���������������Ʊ�[J]. ��ѧ�о�, 1997, 8(3): 60-63.
GAO Yong-jian, ZANG Zhi-jun, XUE Qun-ji. Synthesis of thiadiazole and ramification[J]. Chemical Study, 1997, 8(3): 60-63.
[6] ���ľ�, ��˳��, ¥̨��, ��. 2, 5-���ϻ�-1, 3, 4�����ϳɷ����Ľ�[J]. ��ѧ����ʦ, 2003, 98(5): 26-27.
L? Jun-wen, CAO Shun-an, LOU Tai-fang, et al. Animproved method for the synthesis of 2, 5-dimercapto-1, 3, 4-thiadiazole[J]. Chemical Engineer, 2003, 98(5): 26-27.
[7] Kaminaga A, Tatsuma T, Sotomura T, et al. Reactivation and reduction of electrochemically inactivated polyaniline by 2, 5-dimercapto-1, 3, 4-thiadiazole[J]. J Electrochem Soc, 1995, 142(4): 47-49.
[8] Oyama N, Tatsuma T, Satot T, et al. Dimercaptan-polyaniline composite electrodes for lithium batteries with high energy density[J]. Nature, 1995, 373(6515): 598-660.
[9] Oyama M, Pope J M, Sotomuta T. Effects of adding copper(��) salt to organosulfur cathodes for rechargeable lithium batteries[J]. J Electrochem Soc, 1997, 144(4): 47-51.
[10] �� ��, �� ��, Ǯ����. 2, 5-���ϻ�-1, 3, 4�����ĺϳ������о�[J]. ��������, 2004, 33(12): 695-696.
FU Lei, LIU Lin, QIAN Jian-hua. Study on the synthesis condition of 2, 5-dimercapto-1, 3, 4-thiadiazole[J]. Liaoning Chemical Industry, 2004, 33(12): 695-696.
[11] WANG Da-xi, LI Shu-yuan, YU Ying, et al. Theoretical and Experimental Studies of structure and inhibition efficiency of imidazoline derivatives[J]. Corrosion Science, 1999, 41(10): 1911-1919.
[12] �ž���, �� ³, �� ��, ��. ��3-��������ԶԶ��ϻ������ĵ绯ѧ�����о�[J]. ������ѧѧ��: ��Ȼ��ѧ��, 2006, 42(1): 19-21.
ZHANG Jing-hua, QI Lu, SHU Dong, et al. Study on the electrochemical performance of improvement 2, 5-dimercapto-1, 3, 4-thiadiazole(DMcT) by poly(3-methoxythiophene(PMOT)[J]. Acta Scientiarum Naturalium Universitatis Pekinensis, 2006, 42(1): 19-21.
[13] Chi Q, Tatsuma T, Ozaki M, et al. Electrochemical behavior and surface morphologic changes of copper substrates in the presence of 2, 5-dimercapto-1, 3, 4-thiadiazole[J]. Electrochem Soc, 1998, 145(7): 2369-2377.
[14] Tatsuma T, Matsui H, Shouji E, et al. Reversible electron transfer reation between polyanliline and thiol/disulfide couples[J]. Phys Chem, 1996, 100(33): 14016-14021.
[15] �����, ���º�, Ф����, ��. PAn/DMcT����Ĥ�缫�ĵ绯ѧ����[J]. ���ϵ���, 2004, 18(1): 89-90.
DENG Ling-feng, LI Xin-hai, XIAO Li-xin, et al. Electrochemical properties of PAn/DMcT compound film cathode[J]. Materials Review, 2004, 18(1): 89-90.
[16] Ф����, ������, �����j, ��. ����̼��DMcT-PAn�������ϵ绯ѧ���ܵ�Ӱ��[J]. ���ϴ�ѧѧ��: ��Ȼ��ѧ��, 2004, 35(5): 775-777.
XIAO Li-xin, HOU Tao-li, GUO Bing-kun, et al. Influence of nanocarbon on electrochemical properties of DMcT-PAn cathode[J]. Journal of Central South University: Science and Technology, 2004, 35(5): 775-777.
�ո����ڣ�2008-06-02�������ڣ�2008-09-11
������Ŀ������ʡ��Ȼ��ѧ����������Ŀ(06JJ2008)
ͨ�����ߣ��°���(1947-)��Ů�������人�ˣ����ڣ���ʿ����ʦ�����µ绯ѧ��������������о����绰��0371-8877352��E-mail: yhschen@mail.csu.edu.cn