���±�ţ�1004-0609(2014)08-2164-07
����-�������ƽ����Ѵ�������������ȶ���
��ϲ�ƣ������������ױ��� �գ�ʯ����
(���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083)
ժ Ҫ�����ø��±��ա�����-�������ƽ����Ѵ�������еĽ��о������¶ȡ���������Ũ�ȡ�����(Tu)Ũ�ȡ�Fe3+Ũ�ȡ�pHֵ�������¶Ⱥ�ʱ��Խ�����ʵ�Ӱ�죬�õ������ϵ������������������о������������������ƺ�������ȶ��ԡ������������Ľ����ʴﵽ93.1%��������ͬ�����µ�һ��ϵ�еĽ�����֮�ͣ���������������Ħ���ȶԽ�����ʺͽ�缫�ȶ���λӰ��ϴ���������ʹ������ȶ��Խ��ͣ�������ʹ�������Ƶ��ȶ�����ǿ��
�ؼ��ʣ��Ѵ���������壻�������ƣ�������
��ͼ����ţ�TF80 �� �� ���ױ�־�룺A
Leaching of Au from refractory gold ore in thiourea-thiocyanate solutions and stability of lixiviants
YANG Xi-yun, LIU Zheng-kun, GUO Kong-bin, XU Hui, SHI Xi-chang
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: Gold was extracted from refractory gold ore using a process of roasting followed by thiourea-thiocyanate leaching. The effects of roasting temperature, initial concentrations of thiocyanate, thiourea and ferric as well as pH value, leaching temperature and time on the leaching rate of gold were investigated. The results show that the gold leaching rate is 93.1% under the optimum conditions, and the leaching rate in mixed system is greater than the sum of leaching rate in solutions with each individual lixiviant. The mole ratio of thiourea to thiocyanate has significant influence on the leaching rate of gold and open potential. Thiocyanate accelerates the decomposition of thiourea whereas thiourea alleviates the decomposition of thiocyante.
Key words: refractory gold ore; thiourea; thiocyanate; lixiviant
���ŵر������Դ���ս��ľ�����IJ��Ͽ��ɣ���ѡұ�����Դ����ݽߣ��Ѵ������Ϊ���ƽ�ұ����ҵ����Ҫ��Դ[1-2]���Ѵ�������н�ͨ���Լ���ɢ����̬Ƕ���ڻ�����(FeS2)�Ͷ�ɰ(FeAsS)�ľ����У������������ڼ��ѷֽ����̿����ʹ���г�ϸĥҲ����ʹ������ȫ��¶�����½�������������Ӵ���ͬʱ�������������������������ã����Ĵ������Լ���Ӱ���Ľ����ʡ���ˣ��������Ѵ�������ڽ���֮ǰ��Ҫ����Ԥ������Ԥ����������Ҫ�б�����������ϸ���������ͼ�ѹ�����������б���������ϸ����������ҵӦ�ýϹ�[3-5]��
Ԥ��������������Ҫ�����軯���ͷ��軯��������[6-7]���軯�����������ʸߡ����ռ��������㡢�ɱ��ͼ��������������һֱ��Ϊ��Ҫ������������ھ綾�������ٶ�����ȱ�㡣��ˣ����衢��������Ⱦ�����������Ӧ�ý���Ϊ�Ժ�Ƽ����ص��ص㡣
Ŀǰ���Է��軯��������о���Ҫ���������巨[8-9]����������η�[10-11]����������[12-16]�ȡ���Щ���������ٶ�һ����軯���죬���ҶԻ�������Ⱦ�̶�ԶԶС���軯���ġ����ǣ����巨����������η�����ҩ���������ɱ��ߡ��ȶ��Բ��ȱ�ݣ��������ζ���С�������ȶ����������ٶ������������������ұ��ҵ�е��ƹ�Ӧ�á�һЩ�о���Աָ����������������ϵ�м����(�������)[17]����[18]����ɵĻ����ϵ���������ν����зdz����Եĸ��ơ��������������[19-21]�Խ�缫Ϊ����ϵͳ�о�������-�������ƻ����ϵ������Ĺ��ռ���ػ������о����֣���������������������������Һ�п������Ը������������ѧ���������������ƻ����ϵ�Ľ����ٶȴ�����ͬ�����µ�һ��ϵ������֮�ͣ���������������֮����һ��Эͬ���á������ϵ���Ѵ������Ľ���Ч����Σ����д���һ���о����ڴˣ������������Ѵ������Ϊ�����о�����-�������ƻ����ϵ�������գ���̽�ֽ��������ȶ��ԣ�Ϊ�����ϵ�Ĺ�ҵӦ�õ춨������
1 ʵ��
1.1 ԭ��
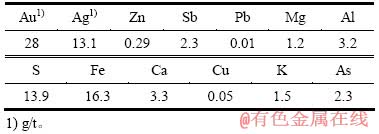
���Ϊ�Ĵ�ij��ҵ�ṩ�ĸ�Ʒλ������������������Ҫ�ɷ�ΪʯӢ(SiO2)��������(FeS2)���������(FeAsS)������ʯ(CaMg(CO3)2)��������(Fe(CO3))��dz������(Ag3AsS4)��KAl2Si3AlO10(OH)2 ����Ҫ��ѧԪ�صķ����������1������н϶����������ڵ��͵��Ѵ������
��1 ���Ļ�ѧ�ɷ�
Table 1 Composition of gold ore (mass fraction, %)
1.2 ʵ�����
����Ԥ�������Ⱦ����±���Ԥ���������ù�ʽ¯���գ����Ʊ����¶�600~800 �棬���պ�����SO2�Լ�As2O3���壬������ĩ�˽�����NaOH��Һ������SO2�Լ�As2O3��
��Ľ�����ȡ��������Ԥ�����ı�ɰ20 g����500 mL������ƿ�ڣ���ȡ200 mL Fe2(SO4)3������(Tu)�Լ�NaSCN��ɵĻ����Һ��Ȼ���Һ����������ƿ�뱺ɰ��ֻ�ϣ���ϡH2SO4��pHֵ�����½������һ��ʱ����ˣ�������Һ���Ũ�ȣ������Ľ����ʡ�
1.3 ��������
AuŨ�Ȳ���ICP-AES�������ϵ�������ԭ�ӷ�������м�⣬����Ϊ267.50 nm��
����Ũ�ȵIJⶨ���Ե���Ϊָʾ�������õ������Һ�ζ�����ɫ��
�������Ũ�ȵIJⶨ�������Խ�����Һ�м�������������������������������������������Ϊָʾ�������������Ʊ���Һ���ζ�����dz�غ�ɫ���������������������Ƶ����ʵ���֮�������������Ũ�ȡ�
1.4 ��·��λ�IJ���
����CHI660B�绯ѧ����վ���о��缫Ϊ��Pine Instrument��˾���õĽ�缫���αȵ缫Ϊ232�͵ı��ʹ��缫�����ô���ëϸ�ܵ�����������ͬ��Һ���Һ��ӽ���Ƽ�������Һ��ŷķ���裬��缫�ý���ɰֽ�⣬����ˮ��ϴ��Ȼ������ֽ���ɽ�缫�����ˮ����ֹ�ڱ������ˮĤ��Ӱ�췴Ӧ������ⶨ��
2 ���������
2.1 ���Ľ���ʵ��
2.1.1 �����¶ȶԽ�����ʵ�Ӱ��
���Ʊ���ʱ��2 h����ɰ�����Ĺ��ղ���ΪTu 0.01 mol/L��NaSCNŨ��0.05 mol/L��Fe3+ 0.01 mol/L��pH1.5�������¶�30 �桢����ʱ��Ϊ80 min�������¶ȶԽ�����ʵ�ʵ�������2���С�
��2 �����¶ȶԽ�����ʵ�Ӱ��
Table 2 Effect of roasting temperature on gold leaching rate
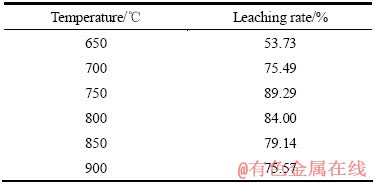
�ɱ�2���Կ��������ű����¶ȵ���ߣ�����������ӡ��������¶�����750 ��ʱ�����Ľ����ʴﵽ���ֵ89.29%�����������¶ȣ����Ľ����ʷ������ͣ�����������۹����������γ�����ֲ��ۻ����£���ˣ����Ͻ�飬�õ����ܵ�������������������½�Ľ���Ч���½�����750 �決�յı�ɰ��⣬��ɰ����Ϊ85.5%����ɰ��As����Ϊ0.21%��S����Ϊ0.17%����ĺ���Ϊ32.7 g/t�������As���ѳ���Ϊ92.2%������ѳ���Ϊ99.0%��˵�����������������Ѿ�ȫ����������û����ʧ����ˣ������ѱ����¶���750 �档
2.1.2 NaSCNŨ�ȶԽ�����ʵ�Ӱ��
�ڱ����¶�750 �桢TuŨ��0.01 mol/L��Fe3+Ũ��0.01 mol/L��pH1.5�������¶�30 ���Լ�����ʱ��80 min�������£��о�NaSCNŨ�ȶԽ�����ʵ�Ӱ�죬������ͼ1��ʾ��
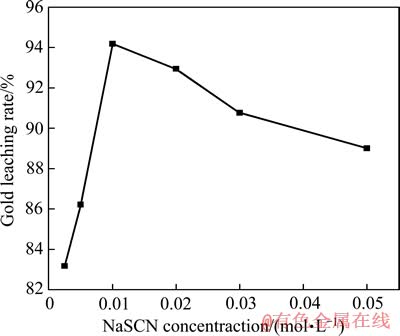
ͼ1 NaSCNŨ�ȶԽ�����ʵ�Ӱ��
Fig. 1 Effect of NaSCN concentration on gold leaching rate
��ͼ1���Կ�������NaSCNŨ�Ƚϵ�ʱ����Ľ���������NaSCNŨ�ȵ��������������NaSCNŨ�ȳ���0.01 mol/L��Ľ���������NaSCNŨ�ȵ�������½���������һ����������������ԭ��1) ��������Ũ��Ӱ����������������֮���Ħ���ȣ����˱���Ӱ�췴Ӧ���̡�YANG��[19-21]���о�������������/��������Ħ����Ϊ1:1��1:4ʱ���Ի����ϵ�����ķ�Ӧ����Ϊ������Ӧ����ʽ(1)���У�������/��������Ħ���ȴ���1:1ʱ�����������Ϊ������Ӧ��ʽ(2)���У�������/��������Ħ����С��1:5ʱ�����������ƽ���Ϊ������Ӧ��ʽ(3)���У��������Ƶķ�Ӧ����ѧ����������������������Ũ�ȴﵽһ��ֵ���������½���2) NaSCN��������ȶ�����Ӱ�죬�ϸߵ���������Ũ�ȵ�������ֽ⣬�����������ЧŨ�ȣ�������Ľ������ں������������ȶ��Խ������ۡ�
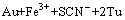 ��
�� (1)
(1)
 ��
�� (2)
(2)
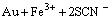
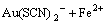 (3)
(3)
Ϊ���˽���������������Ħ���ȶԷ�Ӧ���̵�Ӱ�죬�Խ�缫Ϊ�о��缫���ʹ�Ϊ�αȵ缫���̶�TuŨ��Ϊ0.005 mol/L��Fe3+Ũ��0.055 mol/L��pH 1.5���¶�30 �棬�ı���������Ũ�ȣ�ʹ��������������Ħ���ȷֱ�Ϊ1:1��1:2��1:4��1:10�������˽�缫��·��λ��ʱ��ı仯��������ͼ2��ʾ��
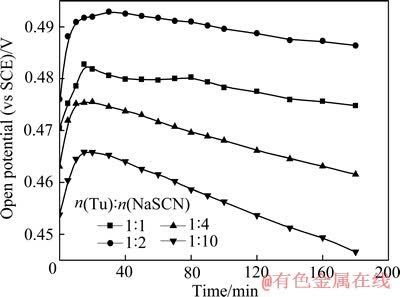
ͼ2 ��ͬ��������������Ħ����ʱ��缫��·��λ��ʱ��ı仯
Fig. 2 Changes of open potential of gold disk with time at different mole ratios of Tu to NaSCN
��ͼ2���Կ�����������������������Ħ������1:1��С��1:10����·��λ������������˹�ط��̣�����ʽ(1)��(3)����·��λӦ�ý��ͣ�˵����������������Ħ���ȶԷ�Ӧ������Ӱ�졣
2.1.3 TuŨ�ȶԽ�����ʵ�Ӱ��
��NaSCNŨ��0.01 mol/L��Fe3+Ũ��0.01 mol/L��pH 1.5�������¶�30 �桢����ʱ��80 min�������ٶȺ㶨�������£�TuŨ�ȶԽ�����ʵ�Ӱ���ͼ3��
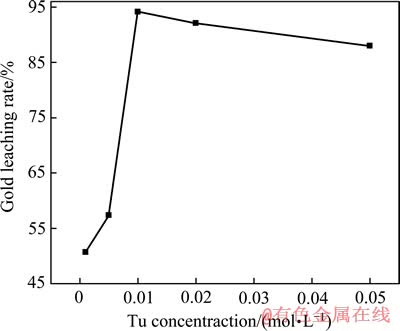
ͼ3 TuŨ�ȶԽ�����ʵ�Ӱ��
Fig. 3 Effect of thiourea concentration on gold leaching rate
��ͼ3���Կ�����TuŨ�ȶԽ�Ľ�����Ӱ���TuŨ�ȵ���0.01 mol/L������TuŨ�ȵ����ӣ����������50%���ӵ�94%����TuŨ�ȼ������ӣ����������н��͡�����Ҫ��������������Fe3+�����£����������������ʽ(2)���У�ͬʱ�����屾��Ҳ�ᱻFe3+�����ɶ�����ߣ�������߿ɽ�һ���ֽ�Ϊ���塢�������Ԫ����Ӧ�ֱ���ʽ(4)��(5)��ʾ��
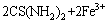

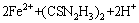 (4)
(4)
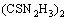

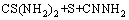 (5)
(5)
������߷ֽ������Ԫ����Ϊ�߶ȷ�ɢ(��ϸС)״�����װ����ڱ�ɰ���棬ʹ�����ۻ��Ӷ��ӻ�����ֹ��Ľ�����
��3 ��һ��ϵ�ͻ����ϵ��Ľ����ʶԱ�
Table 3 Comparison of gold leaching rate between single and mixed lixiviants
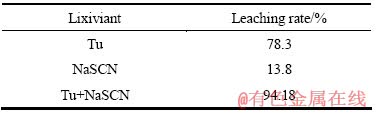
Ϊ�˶ԱȻ����ϵ�͵�һ��ϵ��Ľ����ʣ�����ͬ�����²����˽�Ľ����ʣ�������3���С��ɱ�3���Կ����������ϵ�н�����ʴ��ڵ�һ��ϵ���н�����֮�ͣ�˵�������ϵȷʵ����һ���Эͬ���á�
2.1.4 Fe3+Ũ�ȶԽ�����ʵ�Ӱ��
��pH 1.5�������¶�30 �桢NaSCNŨ��0.01 mol/L��TuŨ��0.01 mol/L������ʱ��80 min�������ٶȺ㶨�������£�Fe3+Ũ�ȶԽ�����ʵ�Ӱ���ͼ4��
��ͼ4���Կ�������Fe3+Ũ��Ϊ0.005 mol/L��0.01 mol/Lʱ����Ľ�������Fe3+Ũ�ȵ�������������Fe3+Ũ�ȴ���0.01 mol/L����Ľ�������Fe3+Ũ����������͡�Fe3+��Ϊ������ʹ��Һ��������λά����һ��ֵ���Ա�֤����нϸߵĽ������ʡ�ͬʱ�����������Fe3+�γ�һϵ��������Fe(NCS)4-��Fe(NCS)3��Fe(NCS)2+��Fe(NCS)2+����Fe3+Ũ��Ϊ0.005 mol/L���������������Fe(NCS)4-Ϊ������Fe3+Ũ��Ϊ0.05 mol/L�������������Fe(NCS)2+ռ����[13, 16]����Щ������ӵ������������ڲ��졣���ڵ�һ������ϵ��LI��[22]��Ϊ����Fe3+Ũ�ȵ���0.2 g/Lʱ����Ľ�������Fe3+Ũ�ȵ����Ӷ�����Fe3+Ũ�ȴ���0.2 g/Lʱ������ܽ��ܱ��淴Ӧ���ƣ�Fe3+Ũ�����ӣ�����ܽ��ٶȼ������䡣�����ĵ�[23]�о���Ϊ��������Ϊ�����������������Fe3+Ũ�ȵ�������������С����Ҫ����ΪFe3+Ũ������Au��������Au+�ij̶����ӣ���Ľ�����Ҳ����Fe3+Ũ�ȵ�������������Fe3+Ũ�ȳ���һ��ֵ��ʹAu������ͬʱҲʹ��������Ϊ��Ͷ�����ߣ�����Ũ�Ƚ��ͣ��������ɵ�Ԫ����Խ����жۻ����ã�����Au��������֮�½����ڵ�һ������������ϵ��BARBOSA-FILHO��[14-16]�о����֣�Fe3+Ũ�ȶԽ�����ʵ�Ӱ��С��Fe3+Ũ�ȵ����ӿ��Լ���SCN-����Ϊ(SCN)2��(SCN)3-��Fe2+�ۻ�ʹ��Ľ����ٶ������������ϵ��������������Ƶ��ۺ�Ӱ�죬���ԣ���Ľ�������Fe3+Ũ��������͡�

ͼ4 Fe3+Ũ�ȶԽ�����ʵ�Ӱ��
Fig. 4 Effect of ferric concentration on gold leaching rate
2.1.5 pHֵ�Խ�����ʵ�Ӱ��
��NaSCNŨ��0.01 mol/L��TuŨ��0.01 mol/L��Fe3+Ũ��0.01 mol/L���¶�30 �桢����ʱ��80 min�������ٶȺ㶨�������£������˲�ͬpHֵ�»����ϵ����Ч�ʣ�������ͼ5��ʾ��
��ͼ5���Կ�������Ľ�������pHֵ������һ�������Ĺ��̣���pH=1.5ʱ����������ߡ��Ե�һ�����������ϵ��pHֵ��1~2�ķ�Χ�ڣ���Ľ���������pHֵ���߶�����[22]���ڵ�һ������������ϵ�У��ϵ͵�pH ֵ����������������ȶ�[23]�����ڻ����ϵ�����������Խ���Ϊ�ڽϸ�pHֵʱ�������������ٶȼӿ죬��Tu�����ɶ������(SCN2H3)2���ٶȼӿ죬�������Ҳ�����ȶ������ԣ�����-��(��)-�������ƻ����ϵ��ȡ��ʱ,����Һ��pHֵΪ1.5��Ϊ���ʡ�
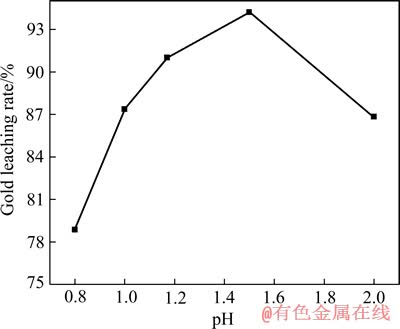
ͼ5 pHֵ�Խ�����ʵ�Ӱ��
Fig. 5 Effect of pH value on gold leaching rate
2.1.6 �¶ȶԽ������ʵ�Ӱ��
��NaSCNŨ��0.01 mol/L��TuŨ��0.01 mol/L��pH 1.5������ʱ��80 min�������ٶȺ㶨������£��������¶ȶԽ�����ʵ�Ӱ�죬�����ͼ6��
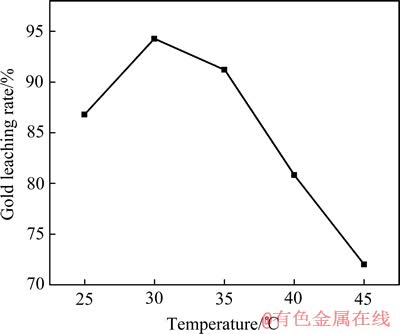
ͼ6 �¶ȶԽ�����ʵ�Ӱ��
Fig. 6 Effect of temperature on gold leaching rate
��ͼ6���Կ��������¶ȵ���30 �棬Au�Ľ��������¶����߶����ӣ����¶ȸ���30 ��ʱ��Au�Ľ��������¶����߶����͡���һ�������缫���ܽ��кܴ�ͬ�����������塢�������ƻ��ǻ����ϵ�У���缫�Ľ����ٶȾ����¶����߶����ӣ��ڵ�һ������������ϵ�У�Au�缫���ܽ��ܻ�ѧ������ƣ��ڵ�һ�����������ϵ�У���缫���ܽ��ܻ�ϲ������[19-22]�����ڽ��Ľ�������Ȼ���������������Ѿ����������Ѿ���¶��������Ȼ��ʯӢ������ʯ���������KAl2Si3AlO10(OH)2�����һ�𣬽���Һ��ɢ�������н������ٶȱȽ�缫Ҫ������ͬʱ�����е���ݼ�������ֽ⣬��Щ����ʹAu���������¶ȸ���30 �潵�͡�
2.1.7 ����ʱ��Խ������ʵ�Ӱ��
��NaSCNŨ��0.01 mol/L��TuŨ��0.01 mol/L��Fe3+Ũ��0.01 mol/L��pH=1.5�������¶�30 �桢�����ٶȺ㶨������£��о��˽���ʱ��Խ�����ʵ�Ӱ�죬�����ͼ7��ʾ��
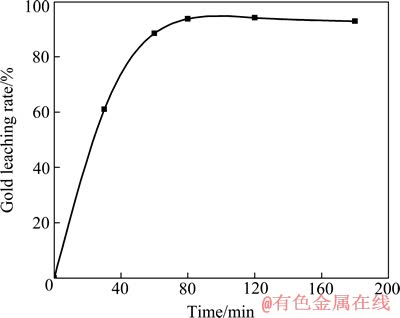
ͼ7 ʱ��Խ�����ʵ�Ӱ��
Fig. 7 Effect of time on gold leaching rate
��ͼ7�ɿ�������ʱ����ӳ�����Ľ������������ԣ�����ʱ��ﵽ80 minʱ��������Ϊ93.8%�������ӳ�ʱ�䣬���������ӻ�����
ȡ����750 �決��Ԥ�����ı�ɰ100 g����2500 mL������ƿ�ڣ���ȡ1000 mL����Һ������NaSCNŨ��0.01 mol/L��TuŨ��0.01 mol/L��Fe3+Ũ��0.01 mol/L��pH=1.5�������¶�30 �桢����ʱ��80 min�����ˣ�ϴ�ӣ���ɣ��õ�92.4 g�����Ըý��������л�ѧ���������ֽ���Ϊ2.54 g/t��S����Ϊ0.2%��As����Ϊ0.23%���������Ľ�����Ϊ93.1%��S�ĺ����ȱ�ɰ�е��Ըߣ��������������巢���ֽ����������⣬��ɰ�е������������Һ�е����ᷴӦ���������ν���������У����������������ӡ�
2.2 ���������ȶ���
��TuŨ��Ϊ0.01 mol/L��Fe3+Ũ��0.01 mol/L��pH=1.5�������¶�80 �桢����ʱ��80 min�������£���������������Ũ�ȶ�����ֽ��ʵ�Ӱ�죬�����ͼ8���������������Ũ����ʱ��ı仯��ͼ9��10��ʾ��Ϊ�˶Աȣ�����ͬŨ�ȵ����嵥һ��ϵ�еķֽ�����ʱ��ı仯Ҳ����ͼ9�С�

ͼ8 NaSCN�������ȶ��Ե�Ӱ��
Fig. 8 Effect of NaSCN concentration on thiourea stability
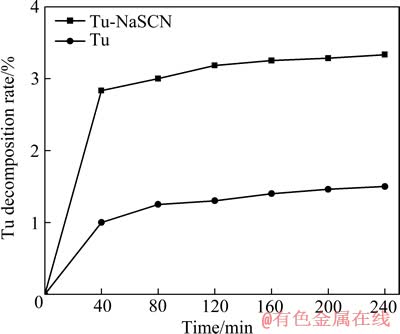
ͼ9 ����ֽ�����ʱ��Ĺ�ϵ
Fig. 9 Relationship between thiourea decomposition rate and time
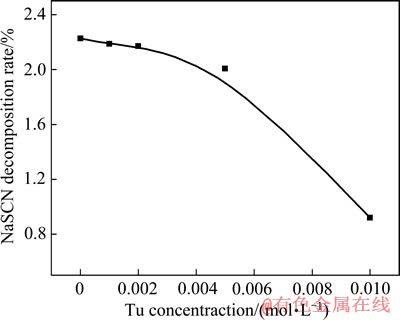
ͼ10 ����Ũ�ȶ��������Ʒֽ��ʵ�Ӱ��
Fig. 10 Effect of thiourea concentration on thiocyanate stability
����NaSCNŨ�ȵ����ӣ�Tu�ķֽ��������أ������������-�������ƻ����ϵ�У�NaSCN��Tu�ȶ���Ӱ��Ƚϴ�����������Χ������ķֽ��ʶ��ϵͣ�����4.0%�����������Ũ�ȵͣ��ֽ������١�ͼ8����������ķֽ���Ҫ���������40 min�ڣ������ֽ��ʻ������䣬��һ������ϵ������ϵ�У�������ʱ��仯�Ĺ�����ͬ�������������Ƶ����ã������ϵ����ֽ���ٶȿ�һЩ��
��ͼ10��֪������TuŨ���������������ȶ�����ǿ����TuŨ�ȴﵽ0.01mol/Lʱ���������Ƶķֽ���С��1.5%������������������Ƶķֽ⣬���������Ƽ���������ķֽ⣬˵����������������֮����ܷ������·�Ӧ��
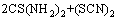 =
= (6)
(6)
3 ����
1) �Ժ��麬����Ѵ��������ø��±��գ�Ȼ��������-�������ƽ�����ɰ�еĽ𣬽����ѽ����ʴﵽ93.1%��
2) Ӱ�������ʵ������б����¶ȡ�����Ũ�ȡ���������Ũ�ȡ�������Ũ�ȡ�����ʱ����¶ȣ����б����¶Ⱥ�����Ũ�ȶԽ�����ʵ�Ӱ�����
3) ��·��λ���Ա���������-�������Ƶı��ʶԷ�Ӧ������Ӱ���
4) �������������ƻ����ϵ������Ľ����ʴ��ڵ�һ��ϵ������֮�ͣ���������������֮����һ��Эͬ���á�
5) ����Ũ�����ӣ��������Ʒֽ��ʽ��ͣ���ǿ�ȶ��ԡ���������Ũ����������ķֽ��������ȶ��Խ��͡�
REFERENCES
[1] ������, ������, ������. ���������ѹԤ����һ�軯������о�[J]. ����ۺ�����, 2011(6): 10-12.
DONG Bo-wen, LI Li-ting, LIU Sheng-ming. Research on the technology of high pressure preoxidation-cyanide leaching of gold for a high sulfur high arsenic gold concentrate[J]. Multipurpose Utilization of Mineral Resources, 2011(6): 10-12.
[2] ��ʯ, ��͢��, IJ����, �� ��, �� ��, ����־, ��Т��. �Ѵ���������Ԥ�������̵�FeS2-FeAsS-H2Oϵ��λ-pHͼ[J]. ������ұ��ѧ��, 2011, 10(2): 120-124.
KIM Chang-sok, ZHANG Ting-an, MU Wang-zhong, ZENG Yong, LIU Yan,  Guo-zhi, JIANG Xiao-di. E-pH diagram of FeS2-FeAsS-H2O system for leaching pretreatment of refractory gold ore[J]. Journal of Materials and Metallurgy, 2011, 10(2): 120-124.
Guo-zhi, JIANG Xiao-di. E-pH diagram of FeS2-FeAsS-H2O system for leaching pretreatment of refractory gold ore[J]. Journal of Materials and Metallurgy, 2011, 10(2): 120-124.
[3] ���Ԫ, ����ƽ, �� ��. ������������ձ�ɰ������������鱺ɰ����������о�[J]. �ƽ�, 2004, 25(10): 34-36.
WU Guo-yuan, WANG You-ping, CHEN Jing. Thiourea leach gold of bearing-high arsenic gold concentrates pretreated by vacuum evaporation and ordinary oxidation roasting[J]. Gold, 2004, 25(10): 34-36.
[4] ������, ���Ӣ. �Ѵ�������ѹ����Ԥ������������չ[J]. �ƽ�, 2008, 29(1): 56-59.
YIN Shu-yan, YANG Hong-ying. Technology and progress in high pressure oxidation from refractory gold ores[J]. Gold, 2008, 29(1): 56-59.
[5] ���Ӣ, �� ��, κ����. ����������˾�(SH-T)������ɰ�Ļ���[J]. �й���ɫ����ѧ��, 2001, 11(2): 323-327.
YANG Hong-ying, YANG Li, WEI Xu-jun. Mechanism on biooxidstion of arsenopyrite with Thiobacillus ferrooxidans strain SH-T[J]. The Chinese Journal of Nonferrous Metals, 2001, 11(2): 323-327.
[6] �� ��, ������, ����ǿ, ���ʳ�. �����Ѵ�����ϸ������-�軯���[J]. �й���ɫ����ѧ��, 2011, 21(5): 1151-1158.
YANG Wei, QIN Wen-qing, LIU Rui-qiang, REN Yun-chao. Extraction of Au from high arsenic refractory gold concentrate by bacterial oxidation-cyanidation[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(5): 1151-1158.
[7] �ι�, ������, �����. �������ճ���ѡ��-���巨��������о�[J]. ��ұ����, 2013, 33(5): 62-66.
HE Gui-chun, WU Yi-peng, HONG Jin-ni. Experimental study on gold extraction from gold-bearing pyrite concentrate by roasting for arsenic removal and thiourea leaching of gold[J]. Mining and Metallurgical Engineering, 2013, 33(5): 62-66.
[8] ZHANG H, RITCHIE I M, LA BROOY S R. Electrochemical oxidation of gold and thiourea in acidic thiourea solutions[J]. Journal of The Electrochemical Society, 2001, 148: D146-153.
[9] YANG X, MOATS M S, MILLER, J D. The interaction of thiourea and formamidine disulfide in the dissolution of gold in sulfuric acid solutions[J]. Minerals Engineering, 2010, 23: 698-704.
[10] BREUER P L, JEFFREY M I. An electrochemical study of gold leaching in thiosulfate solutions containing copper and ammonia[J]. Hydrometallurgy, 2002, 65: 145-157.
[11] FENG D, VAN DEVENTER J S J. Thiosulphate leaching of gold in the presence of orthophosphate and polyphosphate[J]. Hydrometallurgy, 2011, 106: 38-45.
[12] ���ε, �� ݼ, �ảƽ. ������立�������о�[J]. ��ұ����, 2013, 33(2): 84-87.
SONG Min-wei, LIU Jing, YU Hai-ping. Technical study on gold extraction by ammonium thiocyanate[J]. Mining and Metallurgical Engineering, 2013, 33(2): 84-87.
[13] BROADHURST J L, DU PREEZ J G H. Thermodynamic study of the dissolution of gold in an acidic aqueous thiocyanate medium using iron (��) sulphate as an oxidant[J]. Hydrometallurgy, 1993, 32: 317-334.
[14] BARBOSA-FILHO O, MONHEMIUS A J. Leaching of gold in thiocyanate solutions - part 1: chemistry and thermodynamics[J]. Transactions of the Institution of Mining and Metallurgy, Section C: Mineral Processing and Extractive Metallurgy, 1994, 103: C105-110.
[15] BARBOSA-FILHO O, MONHEMIUS A J. Leaching of gold in thiocyanate solutions-Part 2: Redox processes in iron(��)-thiocyanate solutions[J]. Transactions of the Institution of Mining and Metallurgy C, 1994, 103: C111-117.
[16] BARBOSA-FILHO O, MONHEMIUS A J. Leaching of gold in thiocyanate solutions-Part 3: Rates and mechanism of gold dissolution[J]. Transactions of the Institution of Mining and Metallurgy C, 1994, 103: C117-125.
[17] BARBOSA-FILHO O, MONHEMIUS A J. Iodide-thiocyanate leaching system for gold[J]. Hydrometallurgy, 1994, 94: 425-440.
[18] ���彭, �� Ρ. ��-����������ϵ��ȡ���еĽ�[J]. ����ʦ����ѧѧ��: ��Ȼ��ѧ��, 1996, 3: 72-73.
WANG Qing-jiang, ZONG Wei. Leaching of gold from sulfide ore by the system of Bromine and thiocyanate[J]. Journal of East China Normal University: Natural Science, 1996, 3: 72-73.
[19] YANG X, MOATS M S, MILLER J D. Gold dissolution in acidic thiourea and thiocyanate solutions[J]. Electrochimica Acta, 2010, 55: 3643-3649.
[20] YANG X, MOATS M S, MILLER J D. Using electrochemical impedance spectroscopy to investigate gold dissolution in thiourea and thiocyanate acid solutions[J]. ECS Transaction, 2010, 28: 213-221.
[21] YANG X, MOATS M S, MILLER J D, WANG X, SHI X, XU H. Thiourea�Cthiocyanate leaching system for gold[J]. Hydrometallurgy, 2011, 106: 58-63.
[22] LI J, MILLER J D. Reaction kinetics of gold dissolution in acid thiourea solution using ferric sulfate as oxidant[J]. Hydrometallurgy, 2007, 89: 279-288.
[23] ������, ��¶�, �Թ��. ����ʱ�䡢H2SO4��Fe3+Ũ�ȶ���������Ӱ��[J]. ������ѧ�����, 2008, 33(2): 49-52.
LI Yu-wen, WU De-dong, ZHAO Guang-nan. The impact of leaching gold of thiourea about time, sulfuric acid and ferric concentration[J]. Environmental Science and Management, 2008, 33(2): 49-52.
(�༭ ������)
������Ŀ������ʡ��Ȼ��ѧ����������Ŀ(13JJ3006)�����ϴ�ѧ��ʦ�о�����������Ŀ(2013JSJJ026)
�ո����ڣ�2013-09-20�������ڣ�2014-04-20
ͨ�����ߣ���ϲ�ƣ����ڣ���ʿ���绰��0731-88830869��E-mail: xiyun.yang@yahoo.com