DOI: 10.11817/j.ysxb.1004.0609.2020-37601
���ø����γ������Ӻ����ˮ�л������������鼰�����ε�ѭ������
�� ��1��֣�Ž�1���� ��1����ӳ��2���κ���1
(1. ���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083��
2. ���ϳ���ѧԺ �����뻯ѧ����ѧԺ������ 413000)
ժ Ҫ�����ø����γ��������������ˮ���о��˸���ȡ�ͭ��ȡ�����ȡ�п��ȶ����ѳ��ʵ�Ӱ�죬��������Ũ�ȡ�Һ�̱ȡ�����ʱ�䡢�����¶�Ϊ�������أ��Ժ�����������н������ӽ���Һ�л������������飬ͬʱ���������ĸҺ�������������n(Ca)/n(As)=1.05��n(Cu)/n(As)=0.45��n(Fe)/n(As)=1.20��n(Zn)/n(As)=1.20�ĸ���������£�������ʼAs(��)Ũ��Ϊ0.05~9.76 g/L�����ˮʱ�������Ũ�Ⱦ�����14 mg/L��ͨ�����Ӹ������������ж��������������Һ��ͭ��п����Ũ���ڡ���ˮ�ۺ��ŷű���(GB 8978��1996)��Χ�ڡ���Һ�̱�(mL:g)Ϊ3:1������ʱ��Ϊ0.5 h�������¶�Ϊ25 �桢����Ũ��0.87 mol/L�����¶Ժ��������н��������������������飬��ʹ������ʴﵽ72.38%�������պ�ĸҺ���ô�����ʼAs(��)Ũ��Ϊ50 mg/L�ĺ����ˮ����ʹ���ѳ��ʴ�83.65%�������������ʿɴ�80%���ϣ�������̬�뾭��˫��Ч�档
�ؼ��ʣ������Σ��������飻�����������ˮ��ѭ������
���±�ţ�1004-0609(2020)-07-1667-10���� ��ͼ����ţ�X756��X703���� ���ױ�־�룺A
����һ�ֶ����弰�����������ж������õ��°����ʡ��䶾�������ǵĻ�ѧ���ʺͼ�̬�йأ�ͨ�������黯������л��黯����Ķ��Դ�������Ķ��Ա������ĸ߳�Լ60��[1]���黯���ұ����������ɫ�����Ŀ���ұ���������Ի����ij�����Ⱦ�������黯����Ϊ�������Ƹ��֯�����ʵȹ�ҵ��ԭ���ϣ������˻����������Ⱦ��[2-3]�����й����������ܾ�ͳ�ƣ�2014�깤ҵ��ˮ�����ŷ���Ϊ109.2 t����������Ⱦ������ˮ�����У���ˮ�����������������Դ�����ԶԺ����ˮ����Ч�����̲��ݻ���
Ŀǰ���ں����ˮ��������Ҫ���û�ѧ����������Ҫ������������������η���ʯ���кͷ��ȡ�����Щ����Ҳ����һЩȱ�㣬�磺������������������ж����۸����η���������������̻���ſɶѷŴ��ã�ʯ���кͷ��г�������������ҳ������ȶ��Բ����ɶ�����Ⱦ��[1-5]����ˣ�Ҳ��ѧ���о���������Ƶ����������飬ʹ���������鲻���ܵõ���Ч���գ����ҳ���������ͭ��ѭ�����ã����Ǹ÷�������ͭ�ɱ��ϸߣ�����������ͭ����������[6]��Ϊ�˽���������⣬�����о����ø����γ����������Ȼ��ơ��Ȼ�п��������������ˮ����ͭ��Ϻ���Ϊ���������������ˮ���������ˮ����Ũ��С��0.4 mg/L�����ú��������������������ԭ��������������飬�������ĸҺ��ѭ�����ã��ҹ����ٶȿ죬ʵ���˺����ˮ���м۽����ĸ�Ч���գ���Ч�ļ�����������ʵ���˺����ˮ����Ⱦ��������Դ���գ����ƹ�Ӧ�õļ�ֵ��
1 ʵ��
1.1 ���鲽��
1.1.1 �����γ�����ʵ��
�����Ȼ��ơ��Ȼ�п��������������ˮ����ͭ(��Ϊ������)�����Ϊ������������2.34 g/L�����ˮ��(��������������������������Һ�У�ϡ�Ͳ������������pH=1.8~1.9���ƶ���)�������������£����ƽ����ٶ�250 r/min������10 min��������������Һ����pH=8.5~9.0�����跴Ӧ0.5 h������0.5 h����ˡ�
����������ó���Ѹ��������Ϊ����������ͬ���鲽�裬�о������ζԲ�ͬAs(��)Ũ�Ⱥ����ˮ������Ч�������������������ֱ�����5����10����20����40��������ͬʵ�鲽�裬�Ե�Ũ�Ⱥ�����Һ���ж�������ʵ�顣
1.1.2 �������������������Ļ���
������ȡ50 g������������������һ��Ũ�ȵ�������Һ�У�����ת��250 r/min����������������������Ż����飬��������ʼ�����Һ���ȷ�������˽���������
��ԭ�����������˺���Һ����������ƿ�У����ƻ�ԭ�¶�Ϊ25 �棬ת��250 r/min��SO2������0.4 L/min��ͨ��1 h��
����Ũ��������ԭ����Һ����Ũ����Լԭ���1/10����ȴ�����º��ˣ��������������顣
1.1.3 �ᾧĸҺ��ѭ������
�ⶨ�ᾧĸҺ�и���ֺ���������1.1.1�����鲽�輰���ø����������ȣ�ȡ����ĸҺ�������μ���4 LAs(��)Ũ��Ϊ50 mg/L�ĺ����ˮ�н��г�����
1.2 ��������
����X����ӫ�������(XRF��S4PIONEER)����ԭ����Ԫ�سɷ֣�����X���������� (XRD��Rigaku D/max-TTR III)������Ʒ���� (����ԴΪCu K���У���ѹΪ40 kV������Ϊ250 mA����=0.154056��10-10 m��2��Ϊ10.0��~80.0��)�����õ����ϵ������������(ICP-OES��IRIS Intrepid ��Thermo Eleetron Corporation)������Һ�е�Ԫ�غ�������ɨ��羵(SEM��FEIQuanta 200)�¹۲������Ʒ�ı�����ò�����ú��������(FT-IR, WQF-510A)�Գ��������и���Ҷ�任�����������
2 ���������
2.1 �����γ�����ʵ��
2.1.1 ��������ȶ����ѳ��ʵ�Ӱ��
�����ˮ�Ĵ���ͨ���������½��У��ҳ����ٶȽϿ죬�ʷ�ˮ�����ѳ�����Ҫ�ܸ�������ȵ�Ӱ�졣����̽��ʵ�飬�ڷ�ˮ��ʼAs(��)Ũ��Ϊ2.34 g/L�����������£��������շ�ӦpH=8.5~9.0������L9(34)���������о��˸�������ȶ�����Ч����Ӱ�죬�������������1��ʾ��
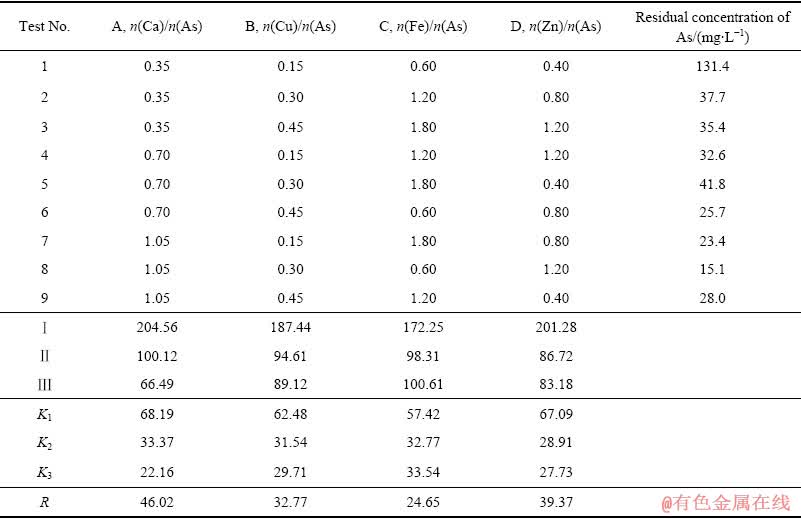
�ɱ�1��֪�������ض����ѳ���Ӱ���˳��ΪCa��Zn��Cu��Fe������������ΪA3B3C2D3����n(Ca)/n(As)=1.05��n(Cu)/n(As)=0.45��n(Fe)/n(As)=1.20��n(Zn)/n(As)=1.20���ڸ������¶�2.34 g/L��As(��)��ˮ��������ʵ�飬��������Һ�������Ũ��Ϊ12.14 mg/L�����ø��������Ϊ��ѳ�����ȡ�
��1 �������������������L9(34)
Table 1 Orthogonal test results of compound salt ratio
2.1.2 ��ʼAs(��)Ũ�ȶԸ���������Ч����Ӱ��
�����������γ���������A3B3C2D3���������£�����4 L��ͬ��ʼAs(��)Ũ�ȷ�ˮ�����츴���ζԲ�ͬAs(��)Ũ�Ⱥ����ˮ�Ĵ���Ч���������ζ����ѳ��ʵ�Ӱ����ͼ1��ʾ��

ͼ1 ��ʼAs(��)Ũ�ȶԸ����������Ӱ��
Fig. 1 Effect of initial As(��) concentration on arsenic removal rate by compound salt
��ͼ1��֪������ʼAs(��)Ũ����0.05 g/L���ӵ�9.76 g/Lʱ�����ѳ�����95.98%������99.87%���ڳ�ʼAs(��)Ũ��Ϊ0.05 g/Lʱ���ѳ��������������ƫ�ͣ��ɼ������������ڵ�As(��)Ũ��������Ч����Խϲ��Һ��As(��)��ʼŨ��Ϊ0.99~9.76 g/Lʱ������������Ч�����ȽϺã����ѳ��ʶ�����99%�������Ũ�Ⱦ�����14 mg/L���Դ�������Һ�и����β���Ũ�Ƚ��вⶨ��������2��ʾ��
��2 �����Һ�и����β���Ũ��
Table 2 Compound salt residual concentration in arsenic removal solution
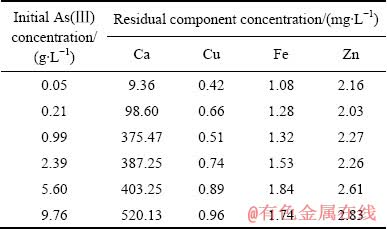
�ɱ�2��֪����Һ�и����θ����Ũ�����ʼAs(��)Ũ�ȵ������������Һ�и�������Ũ��Ϊ520.13 mg/L��ͭ������Ũ��Ϊ0.96 mg/L����������Ũ��Ϊ1.84 mg/L��п������Ũ��Ϊ2.83 mg/L��ͭ��пŨ�Ⱦ��ڡ���ˮ�ۺ��ŷű���(GB 8978��1996)��Χ�ڡ�������As(��)Ũ��Ϊ0.05��0.21��2.39��9.76 g/L�ĺ����ˮ���ó�������ɺ����XRD��⣬���XRD����ͼ2��ʾ��

ͼ2 ������ͬ��ʼAs(��)Ũ�Ⱥ����ˮ���ó������XRD��
Fig. 2 XRD patterns of precipitates obtained from arsenic-containing wastewater with different initial As(��) concentrations
��ͼ2���Կ���������As(��)Ũ�ȵ����ߣ�����������������ǿ���������ˮAs(��)Ũ��Ϊ0.05 g/Lʱ�����������Ϊ���ͣ�˵��������Ϊ�ǽᾧ�壻��As(��)Ũ��Ϊ0.21 g/Lʱ�����������Ҳ��ҪΪ���ͷ壻��As(��)Ũ��Ϊ2.36 g/Lʱ��������ǿ���ӣ���δ��ʶ������ʵ�������ࣻ��As(��)Ũ��Ϊ9.76 g/Lʱ�������������ǿ���ᾧ����ԽϺã�����������ʶ���Ca2Fe(AsO4)(OH)2H2O��Ca5H2(AsO4)4��5H2O�����ʣ���������Ȳ��䣬�Բ�ͬAs(��)Ũ�Ⱥ����ˮ���ܽ�����Ч������
As(��)�Ĵ����ǿ�����Fe3+��ͬ���õĽ��[7-8]���ں����ˮ��Fe2+�ױ�������Fe3+��
4Fe2++O2+4H+ 4Fe3++2H2O (1)
4Fe3++2H2O (1)
12Fe2++3O2+6H2O 8Fe3++4Fe(OH)3 (2)
8Fe3++4Fe(OH)3 (2)
��Fe3+�нϸߵĵ缫���ƣ�������ʾ[8]��
4H��+O2+4e=4H2O (a), ����=1.229 V (3)
Fe3++e=Fe2+, ����=0.77 V (4)
As3+�ĵ缫��Ӧ�����缫��������[8]��
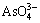 +3H2O+2e=
+3H2O+2e=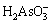 +4OH-, ����=-0.67 V (5)
+4OH-, ����=-0.67 V (5)
H3AsO4+2H++2e=H2AsO3+2H2O, ����=0.559 V (6)
���Կ�����Fe3+������pHֵ�������ܽ��ٲ���As3+������As5+���Ӷ������������������ͬʱ��ˮ��As3+Ҳ�ܺ����η�Ӧ���ɳ�������Ҫ��Ӧ����ʽ����[8-11]��
Fe3++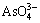 =FeAsO4�� (7)
=FeAsO4�� (7)
Fe3++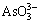 =FeAsO3�� (8)
=FeAsO3�� (8)
3Ca2++ =Ca3(AsO3)2�� (9)
=Ca3(AsO3)2�� (9)
3Ca2++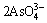 =Ca3(AsO4)2�� (10)
=Ca3(AsO4)2�� (10)
3Cu2++ =Cu3(AsO3)2�� (11)
=Cu3(AsO3)2�� (11)
3Zn2++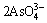 =Zn3(AsO4)2�� (12)
=Zn3(AsO4)2�� (12)
Cu2++ +H+=CuHAsO3�� (13)
+H+=CuHAsO3�� (13)
��Ӧ�������γɵ�������������Ҳ�������鼰���������[12]���ɴ˿ɵã������ζ�����ѳ��dz������������ù�ͬ�Ľ�������ڼ������ε����϶࣬��ˣ��������дֿ���������������������������̬��Ļ����[13]���ֱ�����ʼAs(��)Ũ��Ϊ0.05��0.21��2.36��9.76 g/L�ĺ����ˮ���ó�����SEM����ͼ3��ʾ��
��ͼ3�ɿ�������������״��������С��һ���������ӽ��ܣ��Ҵ��ΪС�����ž��壬���Ŵ�����ˮ����Ũ�ȵ�������������״��Ϊ��״��˵�����������Ч�ij�����������һ����������[14]���Դ���As(��)Ũ��Ϊ9.76 g/L�ĺ����ˮ���ó��������к����������������ͼ4��ʾ��
��ͼ4�пɿ�����3426 cm-1���ķ�Ϊˮ�������ǻ��������������ǻ��������壬��1617 cm-1�ʹ����ֵķ�Ϊˮ�������ǻ��������������ǻ���������[8]����798��597��659 cm-1������������ͬ�ķ壬��֤�������ǻ�������FeOOH��472 cm-1�������շ�ΪO��As��O����������[15-16]��As��O����������ΧΪ750~950 cm-1��������798 cm-1 �����ķ������Ϊ��������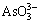 [17-19]��
[17-19]��
2.1.3 �����ˮ�Ķ��γ���
Ϊ��ʹ��ˮ�������ŷţ�����������Ѹ��������A3B3C2D3�������ε�������������һ�γ������ˮ��Ϻ�ȡ2 Lһ�γ��������ˮ���ж��γ�����ʵ�飬һ�γ������ˮ����ҪԪ�غ������3��ʾ�������ˮ���γ�����Ч�����4��ʾ��

ͼ3 ������ͬ��ʼAs(��)Ũ�ȵĺ����ˮ���ó������SEM��
Fig. 3 SEM images of precipitates obtained by treating arsenic-containing wastewater with different initial As(��) concentrations

ͼ4 ������ʼAs(��)Ũ��Ϊ9.76 g/L�ĺ����ˮ���ó�����ĺ������ͼ
Fig. 4 FT-IR spectra of precipitate obtained by treating arsenic- containing wastewater with initial As(��) concentration of 9.67 g/L
��3 һ�γ������ˮ����ҪԪ�غ���
Table 3 Main element content in wastewater after primary precipitation (mg/L)
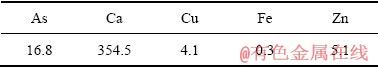
�ɱ�4��֪��ͨ����������������һ�γ������ˮ���ж������飬��ʹ��Һ����Ũ�ȴﵽ��0.5 mg/L���ŷű��������������ʹһ�γ������ˮ�����븴���η�����Ӧ���γɳ��������������������γ�����ˮ�ơ�����ͭ��пŨ�Ⱦ��ɴ���ŷš��Ը�������������20����Ӧ�����ó���������SEM��XRD��⡣��������SEM����ͼ5��ʾ����������XRD����ͼ6��ʾ��

ͼ5 ���γ�������SEM��
Fig. 5 SEM image of secondary precipitate slag

ͼ6 ���γ�������XRD��
Fig. 6 XRD pattern of secondary precipitate slag
��ͼ5���Կ��������γ������Դ�С�������εľ��������ɣ����ֳ�����״��Ƭ״����������ò������н�ǿ�������õ�ˮ��������������[14]�����ͼ6�������������к���CaSO4��Ca5H2(AsO4)4��5H2O��Ca2FeAsO4(OH)2��H2O�����ʡ�
��4 �����ˮ���γ�����Ч��
Table 4 Secondary arsenic precipitation effect of arsenic-containing wastewater

2.2 �����γ���������Ļ���
2.2.1 �����������������Ż�ʵ��
̽��ʵ�������������������������������ᣬ����̽��ʵ�������������L9(34)����������ʵ�飬�����ø���������������ϣ�����������ҪԪ�غ������5��ʾ���������ʵ�������6��ʾ��
�ɱ�6��֪�������ض��������Ӱ��˳��Ϊ��Һ�̱ȣ�����Ũ�ȣ������¶ȣ�����ʱ�䡣��������ΪA3B3C1D3����Һ�̱�(mL:g)Ϊ10:1ʱ��������ʾ�����99.5%��Ϊ�˼���Һ�̱ȡ���߽���Һ����Ũ�ȣ��ڴ˻����Ͻ����Ż�ʵ�顣�����¶�Ϊ25 �桢����ʱ��Ϊ0.5 h������Ũ��Ϊ0.87 mol/L�������䣬�о��˲�ͬҺ�̱ȶ�������ʵ�Ӱ�죬�������7��ʾ��
��5 ��ϳ���������ҪԪ�غ���
Table 5 Main element content in mixed precipitate (mass fraction,%)
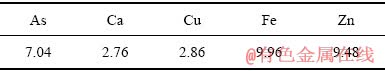
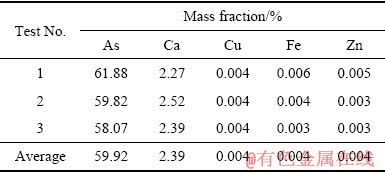
�ɱ�7���Կ�������Һ�̱�Ϊ10:1��6:1��5:1��3:1ʱ��������ʾ��ﵽ98%���ϣ�Ϊʹ������ʴﵽ�����ҽ���Һ�и�Ԫ�صõ��߶ȸ������Ա������ã�����ѡ��Һ�̱�3:1������Ũ��0.87 mol/L������ʱ��0.5 h�������¶�25 ��Ϊ���˵Ľ�����������������ɺ���������ܽ����ICP�ⶨ������ҪԪ�غ������8��ʾ��������SEM���XRD����ͼ7��8��ʾ��
��ͼ7��֪����������״Ϊ������Ƭ״�����ȴӼ����������ײ��ȣ��ҿ����ž����ء���ͼ8���Կ�����������������ɽϵ�һ����PDF��Ƭ��������������Ҫ�������Ϊ�����[20]��
2.2.2 ����������������Һ������������Ļ���
����Һ�̱�Ϊ3:1����������������ý���Һ3.25 L��AsT 20.56 g/L (As(��) 17.33 g/L)�����ý���Һ�ɷ����11��ʾ�������������£������Һ��ͨ��SO2��ԭ1h[21-22]������Һ��As(��)��2.98 g/L��Ϊ0.76 g/L��As(��)��ԭ�ʴﵽ74.28%������ԭ����ҺŨ����Լ�����1/10����ȴ�ᾧ���ˡ���ɣ��ýᾧ����90.13 g���ᾧ�����ܽ����з���������ҪԪ�غ������9��ʾ��
��6 �����������������L9(34)
Table 6 Orthogonal test results of sulfuric acid leaching

��7 ��ͬҺ�̱��½������������ֺ���
Table 7 Contents of related components in leaching residue under different liquid-solid ratio

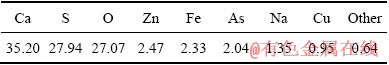
��8 ����������ҪԪ�غ���
Table 8 Main chemical components of leach residue (mass fraction,%)

ͼ7 ��������SEM��
Fig. 7 SEM image of leaching residue

ͼ8 ��������XRD��
Fig. 8 XRD pattern of leaching residue
��9 ���ղ�����ҪԪ�غ���
Table 9 Main chemical components of recycled product
�ɱ�9��֪����ԭ��Һ������Ũ����ԭ�����1/10��������ʿɴ�72.38%�����ղ����д����������ʡ����ղ����SEM���XRD����ͼ9��10��ʾ����ͼ9���Կ����������Ϸ�ɢ������Ƭ״������״����������״�IJ�����ͼ10 �е�XRD���Է�������һ�β�����ҪΪ����������[23]��ͨ������ɵã�����Ũ����ᾧ���������������麬��Ϊ71 g��

ͼ9 ���ղ����SEM��
Fig. 9 SEM images of recycled products
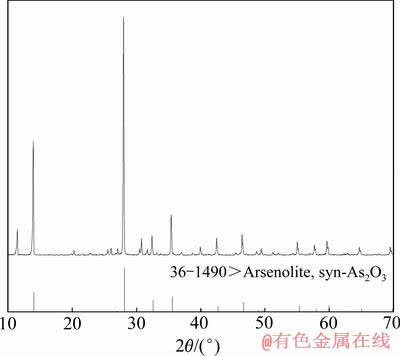
ͼ10 ���ղ����XRD��
Fig. 10 XRD pattern of recycled products
2.3 ĸҺ��ѭ������
�ԽᾧĸҺ����ѭ������ʵ�飬����4 L��ʼAs(��)Ũ��Ϊ50 mg/L�ĺ����ˮ������2.1.1�������������˸��������(n(Ca)/n(As)=1.05��n(Cu)/n(As)= 0.45��n(Fe)/n(As)=1.20��n(Zn)/n(As)=1.20)����������ĸҺ�����(��ĸҺ����Ũ��Ҳ��������)��ȡ5 mLĸҺ�����ˮ�У�������һ�����ĸ����Σ������������·�Ӧ������0.5 h������������ҺpH=8.5~9.0�����ú�ȡ����Һ���вⶨ����Һ�и�Ԫ��Ũ�����10��ʾ��
��10 �ᾧĸҺ��������ʵ����
Table 10 Results of reuse crystalline mother liquor for arsenic removal rate
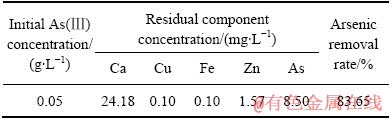
�ɱ�10 �ɿ��������ᾧĸҺ���ã�������As(��)Ũ�Ⱥ����ˮʱ�����ѳ��ʿɴ�83.65%���������������ж��δ������ˮ����Ũ�ȿɴ��ŷű������������ε������ʾ��ɴﵽ80%���ϣ�ʵ������Դ������ѭ�����á�
3 ����
1) ��n(Ca)/n(As)=1.05��n(Cu)/n(As)=0.45��n(Fe)/ n(As)=1.20��n(Zn)/n(As)=1.20Ϊ��Ѹ�������ȣ�������ʼAs(��)Ũ��Ϊ0.05~9.76 g/L�ķ�ˮ��ʹ��ˮ�������Ũ�Ⱦ�����14 mg/L������������������5��10��20��40�����ж������飬��Ӧ����Һ��ͭ��п����Ũ�Ⱦ��ڡ���ˮ�ۺ��ŷű���(GB 8978��1996)��Χ�ڡ�
2) ��Һ�̱�Ϊ3:1������ʱ��0.5 h�������¶�25 �桢����Ũ��Ϊ0.87 mol/L���������£��Գ�����������н���������Һ��ͨ��SO2��ԭ������Ũ������Ƶ������������Ʒ��������ʿɴ�72.38%��
3) ��һ�λ������ĸҺ���ã�����4 L��ʼAs(��)Ũ��Ϊ50 mg/L�ĺ����ˮ�����ѳ��ʿɴ�83.65%�����������ε������ʾ���80%���ϣ����δ������ʹ��ˮ����ŷš�
REFERENCES
[1] ׯ����, ����Ԫ, ��С��, �� ϼ. �����ˮ�����о���չ[J]. ��ҵˮ����, 2004, 24(7): 13-17.
ZHUANG Ming-long, CHAI Li-yuan, MIN Xiao-bo, YU Xia. Progress of the research on the treatment of As-containing wastewater[J]. Industrial Water Treatment, 2004, 24(7): 13-17.
[2] SONG S, LOPEZ-VALDIVIESO A, HERNANDEZ- CAMPOS D J, PENG C, MONROY-FERNANDEZ M G, RAZO-SOTO I. Arsenic removal from high-arsenic water by enhanced coagulation with ferric ions and coarse calcite[J]. Water Research, 2006, 40(2): 364-372.
[3] JIANG Q J. Removing arsenic from groundwater for the developing world��A review[J]. Water Science and Technology, 2001, 44(6): 89-98.
[4] �� ӱ, ��˹��, �� ��, ��Ӣ��. ȥ��ˮ��������о���չ��չ��[J]. ������ѧ�뼼��, 2010, 33(9): 102-107.
WANG Ying, L�� Si-dan, LI Xin, WU Ying-jie. Research advances and prospects in arsenic removal from water[J]. Environmental Science & Technology, 2010, 33(9): 102-107.
[5] NAZARI A M, RADZINSKI R, GHAHREMAN A. Review of arsenic metallurgy: Treatment of arsenical minerals and the immobilization of arsenic[J]. Hydrometallurgy, 2016, 174: 258-281.
[6] ֣�Ž�, ��ʤ��, �� ��. ����������Դ������ͭ������¹���[J]. �й���ɫ����ѧ��, 2013, 23(10): 2985-2992.
ZHENG Ya-jie, ZHANG Sheng-hua, GONG Chang. Novel technique for recovery of copper and arsenic from arsenic-containing waste acid[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(10): 2985-2992.
[7] BEDNAR A J, GARBARINO J R, RANVILLE J F, WILDEMANA T R. Effects of iron on arsenic speciation and redox chemistry in acid mine water[J]. Journal of Geochemical Exploration, 2005, 85(2): 0-62.
[8] �� ��, ����÷, ���, �Ŷ���. ���Ȼ�������(��)����[J]. ����ѧ��, 2012, 63(7): 2224-2228.
LI Na, SUN Zhu-mei, RUAN Fu-hui, DU Dong-yun. Mechanism of removing arsenic (��) with ferric chloride[J]. CIESC Journal, 2012, 63(7): 2224-2228.
[9] ������, ף ��, ���Ƚ�, �� ��, ʷ���, ��ԯ��, ������. ͭұ�������γɻ�����������[J]. ������չ, 2013, 32(9): 2246-2252.
LIAO Tian-peng, ZHU Xing, QI Xian-jin, WANG Hua, SHI Yi-feng, LI Yuan-cheng, HU Jian-hang. Formation mechanism and characteristics of sludge in copper metallurgy plant[J]. Chemical Industry and Engineering Progress, 2013, 32(9): 2246-2252.
[10] �� ��, ���ʷ�, ֣�Ž�. ��������Ʊ�������ͭ������ͭ���Һ�����е�Ӧ��[J]. ���ϴ�ѧѧ��(��Ȼ��ѧ��), 2007, 38(6): 1115-1120.
WANG Yong, ZHAO Pan-feng, ZHENG Ya-jie. Preparation of copper arsenite from waste acid containing arsenic and its application in copper electrolyte purification[J]. Journal of Central South University (Science and Technology), 2007, 38(6): 1115-1120.
[11] ������, �� ��, ������, ������, ��ѧ��. ����ƻ�������ܽ�ȼ����ȶ�����pHֵ�ı仯[J]. ������ѧѧ��, 2005, 25(12): 1652-1660.
ZHU Yi-nian, ZHANG Hua, LIANG Yan-peng, LIU Hui-li, ZHANG Xue-hong. Dependence of solubility and stability of calciun arsenates on pH value[J]. Acta Scientiae Circumstantiae, 2005, 25(12): 1652-1660.
[12] DAUS B, WEI B H, WENNRICH R. Arsenic speciation in iron hydroxide precipitates[J]. Talanta, 1998, 46(5): 867-873.
[13] �� ��, ��ѧ��, ������, �� ��, �κ���. Fe(��)������������As(��)��As(��)��ȥ��[J]. ���ҵ��ѧѧ��, 2017, 36(2): 31-36.
HAN Xu, AN Xue-liang, SONG Ya-qin, CHEN Cheng, REN Hai-tao. Removal of As(��) and As(��) by ferrous salt oxidation flocculation[J]. Journal of Tianjin Polytechnic University, 2017, 36(2): 31-36.
[14] �� ��, ��С��, �����, ������. ��е���Fe-MnO2�ȶ��������[J]. �й���ɫ����ѧ��, 2017, 27(10): 2170-2179.
XU Hui, MIN Xiao-bo, LIANG Yan-jie, WANG Yun-yan. Stabilization of arsenic bearing solid waste with Fe-MnO2 activated by mechanochemical process[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(10): 2170-2179.
[15] ���ڕN. ����������ϵ�������̽��[J]. �й�������ѧ, 1995, 15(1): 18-21.
ZHAO Zong-sheng. Mechanism of arsenic removal in oxidized Fe-As system[J]. China Environmental Science, 1995, 15(1): 18-21.
[16] RUAN H D, FROST R L, KLOPROGGE J T. The behavior of hydroxyl units of synthetic goethite and its dehydroxylated product hematite[J]. Spectrochimica Acta Part A Molecular & Biomolecular Spectroscopy, 2001, 57(13): 2575-2586.
[17] CHAI L Y, YUE M Q, YANG J Q, WANG Q G, LI Q Z, LIU H. Formation of tooeleite and the role of direct removal of As(��) from high-arsenic acid wastewater[J]. Journal of Hazardous Materials, 2016, 320: 620-627.
[18] ������, �����ȣ�������, �̷ҷ�, ����. ��������������������������[J]. ������ѧѧ��, 2009, 29(5): 1011-1020.
LIU Hui-li, LIANG Mei-na, ZHU Yi-nian, CAI Fen-fen, ZOU Hui-xian. The adsorption of arsenic by ferric hydroxide and its precipitation mechanism[J]. Acta Scientiae Circumstantiae, 2009, 29(5): 1011-1020.
[19] LONG H, ZHENG Y J, PENG Y L, JIN G Z, DENG W H, ZHANG S C. Comparison of arsenic(��) removal with different lead-containing substances and process optimization in aqueous chloride solution[J], Hydrometallurgy, 2019, 183: 199-206.
[20] ��С��, �ŵ���, ���ٷ�, �� ��, �� ��, ������. ���鹲�����е�����ƶ���̶�����[J]. ��̬ѧ��־, 2014, 33(10): 2803-2809.
LI Xiao-liang, ZHANG Dan-ni, WANG Shao-feng, WANG Xin, SONG Yu, JIA Yong-feng. Arsenic immobilization by gypsum during iron-arsenic coprecipitation process[J]. Chinese Journal of Ecology, 2014, 33(10): 2803-2809.
[21] ֣�Ž�, �� ��, ��ӳ��. ������ͭҺ��ԭ�ᾧ�������¹���[J]. �й���ɫ����ѧ��, 2012, 22(7): 2103-2108.
ZHENG Ya-jie, CUI Tao, PENG Ying-lin. New process of arsenic removal from second stage decopperizing electrolyte by reduction and crystallization[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(7): 2103-2108.
[22] PENG Y L, ZHENG Y J, CHEN W M. The oxidation of arsenic from As(��) to As(��) during copper electrorefining[J]. Hydrometallurgy, 2012, 129/130: 156-160.
[23] YU G L, ZHANG Y, ZHENG S L, ZOU X, WANG X H, ZHANG Y. Extraction of arsenic from arsenic-containing cobalt and nickel slag and preparation of arsenic-bearing compounds[J]. Transactions of Nonferrous Metals Society of China, 2014, 24(6): 1918-1927.
Recovery of arsenic trioxide from arsenic-containing wastewater by using compound salt precipitation and recycling of compound salt
XU Lei1, ZHENG Ya-jie1, LONG Hua1, PENG Ying-lin2, HE Han-bing1
(1. School of Metallurgy and Environment, Central South University, Changsha 410083, China;
2. School of Chemistry and Environmental Engineering, Hunan City University, Yiyang 413000, China)
Abstract: Arsenic-containing wastewater was treated by compound salt precipitation method. The effects of calcium-arsenic ratio, copper-arsenic ratio, iron-arsenic ratio and zinc-arsenic ratio on arsenic removal rate were studied. Taking sulfuric acid concentration, liquid-solid ratio, leaching time and leaching temperature as factors to investigate, the arsenic-containing precipitated slag was leached, and arsenic trioxide was recovered from the leaching solution, and the mother liquor after arsenic removal was reused. The results show that, under the optimal compound salt ratio conditions of n(Ca)/n(As)=1.05, n(Cu)/n(As)=0.45, n(Fe)/n(As)=1.20 and n(Zn)/n(As)=1.20, the arsenic residual concentration is lower than 14 mg/L when the arsenic-containing wastewater with ��(As)=0.05-9.7 g/L is treated, the concentrations of Ca, Fe, Cu, Zn and As in the filtrate are less than Integrated Wastewater Discharge Standard (GB 8978��1996) after the second arsenic removal by increasing the amount of compound salt. Under the conditions of liquid-solid ratio of 3:1, leaching time of 0.5 h, leaching temperature of 25 �� and sulfuric acid concentration of 0.87 mol/L, the arsenic recovery rate reaches 72.38% when arsenic-containing slag is leached and arsenic trioxide is recovered. The mother liquor after arsenic recovery is used to treat the arsenic-containing wastewater with ��(As)=50 mg/L, and the arsenic removal rate can reach 83.65% and the compound salt utilization rate can reach over 80%, which has both ecological and economic benefits.
Key words: compound salt; secondary arsenic removal; leaching; arsenic-containing wastewater; recycling
Foundation item: Project(2017SK2254) supported by the Key Research and Development Project of Hunan Province, China
Received date: 2019-07-26; Accepted date: 2019-11-05
Corresponding author: ZHENG Ya-jie; Tel: +86-731-88836285; E-mail: zyj@csu.edu.cn
(�༭ ��ѧ��)
������Ŀ������ʡ�ص��з��ƻ���Ŀ(2017SK2254)
�ո����ڣ�2019-07-26�������ڣ�2019-11-05
ͨ�����ߣ�֣�Žܣ����ڣ���ʿ���绰��0731-88836285��E-mail��zyj@csu.edu.cn