DOI: 10.11817/j.ysxb.1004.0609.2020-39582
辛基羟肟酸与油酸的密度泛函理论计算及其对氟碳铈矿和萤石浮选效果的对比
王 鹏1,曹 钊1, 2, 3, 4,王介良1,曹永丹1
(1. 内蒙古科技大学 矿业研究院,包头 014010;
2. 广东省资源综合利用研究所,广州 510650;
3. 稀有金属分离与综合利用国家重点实验室,广州 510650;
4. 中南大学 资源与生物工程学院,长沙 410083)
摘 要:通过密度泛函理论(DFT/B3LYP)计算,分析辛基羟肟酸(OHA)和油酸(OA)两种捕收剂的结构构型、前线分子轨道、Mulliken电荷布局以及与Ca2+/Ce3+离子之间的结合能,并通过纯矿物浮选对比研究OHA和OA对氟碳铈矿和萤石的浮选性能。量化计算结果表明:OHA阴离子具有最高的键合原子负电荷、最高占据分子轨道(HOMO)能量和最低的EHOMO-LUMO能隙,比OA具有更强的给电子能力和反应活性;OHA、OA与Ca2+/Ce3+离子之间结合能从强到弱顺序为OHA-Ce、OA-Ce、OA-Ca、OHA-Ca,即OHA与Ce3+结合能最大,且对Ca2+/Ce3+两种离子的结合能差异最大。浮选结果表明:OHA对氟碳铈矿浮选的捕收能力和选择性都大于OA的,与量化计算结果规律一致。
关键词:稀土矿物;捕收剂;密度泛函理论;浮选分离;前线分子轨道
文章编号:1004-0609(2020)-08-1974-08 中图分类号:TD91 文献标志码:A
稀土素有工业维生素之美称,是国民经济中极其重要的战略金属资源。我国稀土资源丰富,其中内蒙古白云鄂博稀土矿工业储量约为4350万t以REO 计),占全国稀土储量的83.6%,堪称世界第一大稀土矿[1]。由于稀土矿物和含钙矿物同属于半可溶盐类矿物,两者溶解性、表面性质和可浮性相近,两者浮选分离是稀土选矿生产面临的主要技术难题[2]。辛基羟肟酸(OHA)和油酸(OA)是稀土选矿生产常用的捕收剂,其化学结构如图1所示。由于羟肟酸与稀土金属的络合稳定常数大于碱土金属的,对稀土矿物浮选具有更好的选择性,目前,国内外多数稀土矿已将捕收剂由脂肪酸替换为羟肟酸[3]。
目前,辛基羟肟酸(OHA)和油酸(OA)对稀土及氧化矿浮选的相关实验及机理测试研究较多[4]。王介良等[5]通过吸附量测试计算发现,辛基羟肟酸在氟碳铈矿表面的吸附存在物理和化学双吸附,但以化学吸附为主,主要OHA与氟碳铈矿的作用形式为OHA-与氟碳铈矿表面暴露的Ce3+发生螯合反应生成OHA-Ce沉淀。LIU等[6]研究表明羟肟酸在烧绿石表面的吸附能力比油酸强,对烧绿石的捕收能力比油酸大。WANHALA等[7]研究表明羟肟酸与氟碳铈矿的配位能力比与脉石矿物方解石的更强[8]。羟肟酸在稀土矿物表面主要形成―C=O―RE―O―N―五元环螯合物,具有相对稳定的结构[9-11]。然而,OHA、OA与稀土矿物及含钙矿物的密度泛函理论计算相关研究较少。
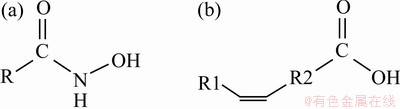
图1 OHA和OA的化学结构
Fig. 1 Chemical structures of OHA(a) and OA(b)
本文通过密度泛函理论(DFT/B3LYP)计算,分析了辛基羟肟酸(OHA)和油酸(OA)两种捕收剂的结构构型、前线分子轨道、Mulliken电荷布局以及与Ca2+/Ce3+离子之间的结合能,并通过纯矿物浮选对比研究了OHA和OA对氟碳铈矿和萤石的浮选性能,有利于建立稀土浮选捕收剂量化计算与浮选性能之间的关系,对稀土浮选捕收剂优化起到一定的理论指导意义。
1 实验
1.1 矿样和试剂
氟碳铈矿取自山东微山湖稀土矿,经手选除杂、破碎、磨矿及重选除杂和弱磁选除磁铁矿后得到氟碳铈矿纯矿物,其REO品位为71.21%,按氟碳铈矿REO理论品位74.88%计算,其纯度为95%左右。萤石取自内蒙古某矿山,经锤碎、挑选提纯后得到萤石纯矿物,其纯度大于98%,两种纯矿物采用陶瓷球磨机磨矿筛分得到38~74 μm粒级用于纯矿物浮选实验。
实验用辛基羟肟酸钠、油酸钠、NaOH和HCl均为分析纯,实验用水为去离子水(电阻率18.2 MΩ・cm)。
1.2 实验方法
1.2.1 量化计算
在本文中,所有的计算分析都是通过Gaussian 09 RevisionD.01 WIN64软件进行。为了使计算所得到的量化参数更具代表性,有关OHA、OA及其与金属离子的配合物都使用DFT/B3LYP方法进行几何优化[12-14]。在优化过程中,Ce原子使用SDD基组[15],以及H、C、O、N和Ca原子使用6-31G(d)基组[16-17],确保所有参数是在相同的基础上计算的。
相互作用能ΔE定义为ΔE=EM+col-EM-Ecol,其中EM+col是金属离子(M)与阴离子捕收剂(col)相互作用所生成配合物经过结构优化后的能量;EM和Ecol分别是具有稳定态的金属离子的能量和阴离子捕收剂的能量。通过对前线分子轨道信息以及Mulliken布局电荷分析描述分子的反应活性[18]。
1.2.2 纯矿物浮选实验
浮选实验在XFGCII型实验室用充气挂槽浮选机中进行,浮选槽容积30 mL。纯矿物浮选每次称取氟碳铈矿或萤石纯矿物2 g置于浮选槽中,加入一定用量的辛基羟肟酸钠或油酸钠捕收剂,加药后搅拌5 min,用NaOH或HCl调整pH为9,浮选刮泡5 min,浮选完成后将泡沫产品和槽内产品分别过滤、烘干、称量,计算氟碳铈矿或萤石纯矿物浮选的回收率。相同条件浮选实验重复3次,结果取3次实验回收率的平均值。
2 结果与讨论
2.1 两种阴离子捕收剂的结构几何优化
辛基羟肟酸(OHA)和油酸(OA)两种捕收剂分子及阴离子经DFT/B3LYP方法进行优化后的结构如图2所示,其中灰色原子为碳原子,白色为氢原子,红色为氧原子,蓝色为氮原子,其结构几何参数信息(键长,键角及二面角)如表1和表2所示。
由表1可以看出,OHA阴离子的O1―C3键长均大于其相应的分子结构的键长,而O2―N4、N4―C3键长比相应分子键长短,这表明OHA阴离子中的O1=C3双键和O2―N4单键发生平均化,与金属离子具有更高的配位反应活性。同时,OHA阴离子的二面角(O2―N4―C3―O1)接近于0,即OHA阴离子中的四个原子几乎在一个平面内,这种平面结构更有利于五元环内共轭键的形成,有利于向矿物表面的金属离子提供电子。
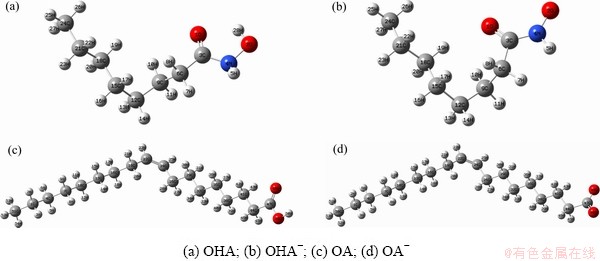
图2 OHA、OA的分子和离子优化模型
Fig. 2 Molecular and anion optimized models for OHA and OA
表1 OHA分子及其阴离子的结构参数
Table 1 Structural parameters of OHA molecule and anion
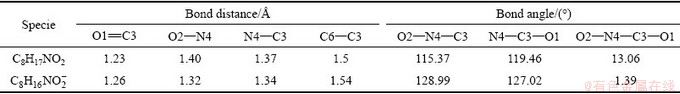
表2 OA分子及其阴离子的结构参数
Table 2 Structural parameters of OA molecule and anion
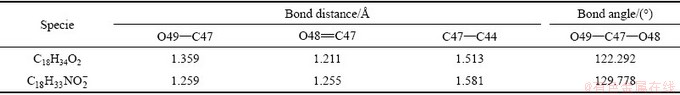
由表2可以看出,OA阴离子中O48=C47双键键长相对OA分子变长,而O49―C47键长比其分子短,表明OA阴离子中O48=C47双键与O49―C47单键发生平均化,主要由O48=C47―O49-形成的p-π共轭所致。
根据上述优化后的结构参数,两种酸的离子形式与矿物表面金属离子发生反应的活性更大,并且OHA阴离子可以与矿物表面的金属离子形成一种更加稳定的五元环螯合物,比OA阴离子具有更强的反应活性。
2.2 两种阴离子捕收剂的量化计算
2.2.1 前线分子轨道分析
根据FUKUI等[19]提出的前线分子轨道理论,分子的最高占据分子轨道(HOMO)和最低未占分子轨道(LUMO)决定了分子的反应活性,即HOMO值及LUMO值分别反映了分子的给电子能力和接受电子能力,HOMO值越大,越容易失去电子,LUMO值越大,则越容易得到电子[20]。由于捕收剂HOMO轨道对应捕收剂的中心原子,电子的活跃程度与其能量相关,HOMO值越大,捕收剂分子向矿物表面提供电子的能力越强,矿物表面与药剂之间的相互作用也会越强[21]。因此,可以通过HOMO轨道能量的大小比较OHA和OA两种捕收剂的化学反应活性。
表3所示为OHA和OA两种捕收剂不同形态的轨道能量参数,药剂分子的EHOMO排列为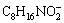 、
、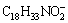 、C18H34O2、C8H17NO2,可以推测OHA和OA分子及阴离子的给电子能力由强到弱依次为OHA阴离子、OA阴离子、OA分子、OHA分子,即OHA比OA具有更强的给电子能力及化学反应活性。刘三军[22]研究发现辛基羟肟酸对一水硬铝石的捕收能力和选择性都优于油酸。高莉[23]对比美狄兰、油酸钠、辛基羟肟酸、水杨羟肟酸、氧化石蜡皂(731)、苯甲羟肟酸等六种捕收剂对白钨矿与钙质矿物的分离效果,发现美狄兰、辛基羟肟酸对白钨矿的浮选效果更佳,而油酸钠的浮选效果最差。这与HOMO值计算出来的反应活性规律相一致。
、C18H34O2、C8H17NO2,可以推测OHA和OA分子及阴离子的给电子能力由强到弱依次为OHA阴离子、OA阴离子、OA分子、OHA分子,即OHA比OA具有更强的给电子能力及化学反应活性。刘三军[22]研究发现辛基羟肟酸对一水硬铝石的捕收能力和选择性都优于油酸。高莉[23]对比美狄兰、油酸钠、辛基羟肟酸、水杨羟肟酸、氧化石蜡皂(731)、苯甲羟肟酸等六种捕收剂对白钨矿与钙质矿物的分离效果,发现美狄兰、辛基羟肟酸对白钨矿的浮选效果更佳,而油酸钠的浮选效果最差。这与HOMO值计算出来的反应活性规律相一致。
表3 OHA和OA不同形态的轨道能量参数
Table 3 Orbital energy parameters for different forms of OHA and OA
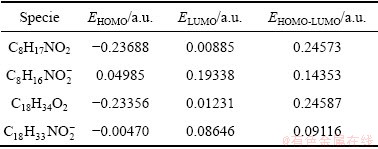
由表3可以看出,OHA阴离子的给电子能力大于OA阴离子,但OA分子的给电子能力比OHA分子的强,其主要原因为OA分子中具有C=C双键结构。图3所示为OHA和OA两种捕收剂不同形态的分子轨道图。由图3可以看出,OA分子的化学活性中心在C=C双键上,因此比OHA分子具有更强的给电子能力,而OHA和OA阴离子化学活性中心分别集中在相应的羟肟酸和羧酸官能团上。
此外,HOMO和LUMO之间的能量差也可以作为结构稳定性的依据。EHOMO-LUMO能隙越小,电子越容易发生跃迁,结构越不稳定,化学反应活性越强,反之亦然[24]。由表3可以看出,OHA阴离子能隙最小,相比OA具有更强的化学反应活性。

图3 OHA和OA不同形态的分子轨道图
Fig. 3 Molecular orbital diagrams for different forms of OHA and OA
2.2.2 偶极矩
表4所示为两种捕收剂分子及阴离子的偶极矩。由表4可以看出,OHA和OA分子及阴离子偶极矩由强到弱为OA阴离子、OHA阴离子、OHA分子、OA分子。因此,OHA和OA阴离子与其分子相比都具有更强的静电和范德华力作用[25],且OA阴离子与矿物表面的静电作用比OHA阴离子强,但由于OHA阴离子与稀土、钨等金属离子具有更高的化学反应活性,所以实际浮选中OHA对稀土矿物和白钨矿的捕收能力比OA的强[23]。
表4 OHA和OA不同形态的偶极矩
Table 4 Dipole moments for different forms of OHA and OA

2.2.3 Mulliken电荷布局分析
表5所示为OHA和OA分子及阴离子的Mulliken电荷值,对于OHA分子及其阴离子,负电荷主要集中在羟肟酸基团中的O1和O2原子上,因此,O1和O2是OHA分子及阴离子主要的给电子中心。此外,OHA阴离子的O1和O2具有更多的负电荷,表明其具有更强的给电子能力[26],由此可以推断OHA阴离子要比OHA分子具有更高的反应活性。
对于OA分子及其阴离子,负电荷则是集中在C22和C24的双键以及羧基团中的O48和O49原子上。由表5可以明显看出,羧基官能团的电荷量远大于双键的电荷量,表明OA分子及其阴离子的反应中心主要为羧基官能团的O48和O49原子。同时,OA离子形式所带电荷量更高,比其分子具有更高的反应活性。
此外,与OA阴离子相比,OHA阴离子两个O原子具有更高的负电荷,因此,OHA阴离子具有更强的给电子能力和化学反应活性。
2.3 两种阴离子捕收剂与Ca2+/Ce3+离子作用的量化计算
图4所示为OHA、OA与Ca2+/Ce3+分别发生配位作用经优化后的结构模型。可以看出,OHA中两个O原子与Ca2+/Ce3+离子产生键合,形成五元环螯合结构;OA中两个O原子与Ca2+/Ce3+离子产生键合,形成四元环的配位结构。
2.3.1 几何结构参数
表6所示为OHA与Ca2+/Ce3+反应前后的几何参数变化。由表6可以看出,与Ca2+/Ce3+反应后,OHA的O1―C3和O2―N4键长增大,原因为OHA的两个O原子与Ca2+/Ce3+发生键合,O1―C3和O2―N4电子云密度向Ca2+/Ce3+发生偏移,使得O1―C3和O2―N4电子云密度降低、键合变弱、键长增大;并且,OHA与Ca2+/Ce3+反应后,O1―Ce和O2―Ce键长都比与之相应的O1―Ca和O2―Ca短,表明OHA与Ce3+键合更加紧密;此外,OHA与Ca2+/Ce3+反应后N4―C3―O1和O2―N4―C3键角都变小,是由于OHA与Ca2+/Ce3+键合成五元环结构后使得两处键角都受到压缩。
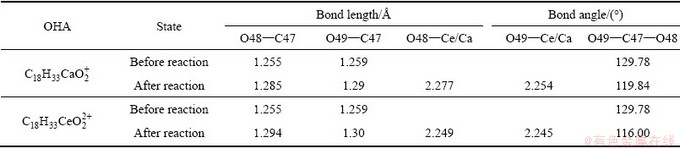
表7所示为OA与Ca2+/Ce3+反应前后的几何参数变化。OA主要通过羧基的两个O原子与Ca2+/Ce3+产生键合,键合后O48―C47和O49―C47的电子云密度向金属发生偏移,使得O48―C47和O49―C47键合变弱、键长增加。OA与Ca2+/Ce3+键合后生成的O48―Ce和O49―Ce键长都比与之相应的O48―Ca和O49―Ca短,表明OA与Ce3+键合更加紧密。
表5 OHA和OA不同形态的Mulliken电荷
Table 5 Mulliken charge values for different forms of OHA and OA
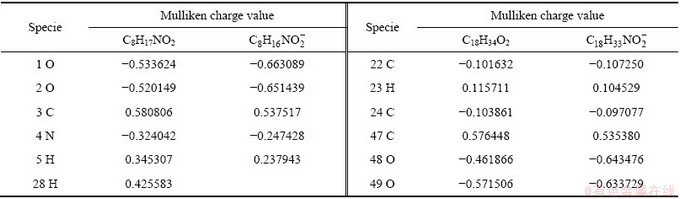
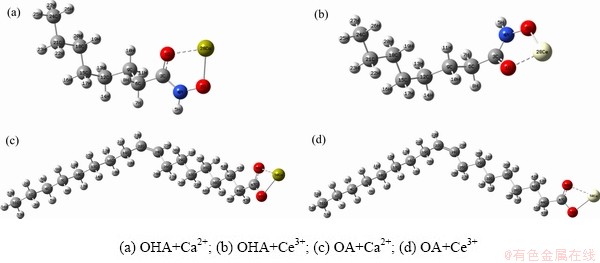
图4 OHA、OA与Ca2+/Ce3+离子配位反应后的优化结合模型
Fig. 4 Optimized model of OHA, OA combined with Ca2+/Ce3+ ions
表6 OHA与Ca2+/Ce3+反应前后的几何参数变化
Table 6 Geometric parameters changes of OHA before and after reaction with Ca2+/Ce3+
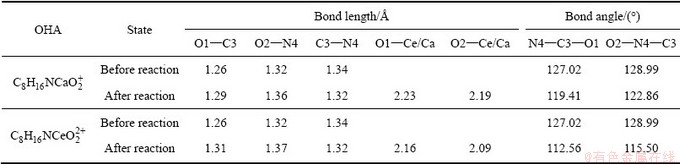
表7 OA与Ca2+/Ce3+反应前后的几何参数变化
Table 7 Geometric parameters changes of OA before and after reaction with Ca2+/Ce3+
2.3.2 结合能
捕收剂与矿物表面金属离子的结合能可用于表征捕收剂与矿物之间的作用强弱,结合能越大,捕收剂与矿物表面之间的相互作用越强,越有利于捕收剂在矿物表面发生吸附[27]。
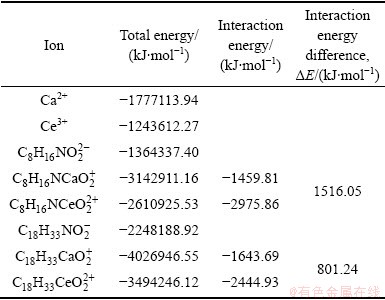
表8所示为OHA、OA与Ca2+/Ce3+离子的结合能,结合能由强到弱依次为OHA-Ce、OA-Ce、OA-Ca、OHA-Ca。可以看出,OHA与Ca2+/Ce3+离子的结合能比OA与Ca2+/Ce3+的结合能大,且OHA对Ca2+/Ce3+的结合能差异比OA的大,表明OHA不仅与含铈矿物之间的结合能比OA的强,而且在含铈矿物与含钙矿物的结合能差异也比OA的大,进而对两种矿物浮选分离的选择性比OA的强。
表8 OHA、OA与Ca2+/Ce3+离子的结合能
Table 8 Binding energy between OHA, OA and Ca2+/Ce3+ ions
2.4 纯矿物浮选实验
图5所示为pH为9时OHA、OA用量对氟碳铈矿、萤石浮选回收率的影响。由图5可以看出,随着OHA和OA两种捕收剂用量增加,氟碳铈矿和萤石浮选回收率都随之增大,在OHA和OA两种捕收剂最佳用量下,OHA对氟碳铈矿的浮选回收率大于OA的,且OHA对氟碳铈矿和萤石的最大浮选回收率差值为26.7%,远大于OA对两种矿物的最佳浮选回收率差值。结果表明OHA对氟碳铈矿浮选具有较高的捕收能力及选择性。这与量化计算结果规律一致。
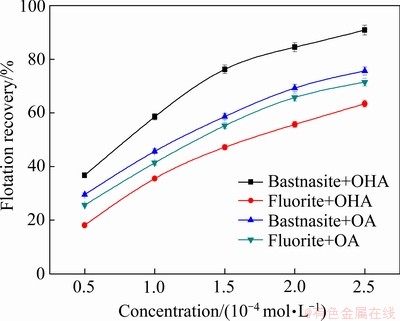
图5 OHA、OA用量对氟碳铈矿、萤石浮选回收率的影响(pH=9)
Fig. 5 Effects of OHA and OA dosage on flotation recoveries of bastnasite and fluorite (pH=9)
3 结论
1) OHA阴离子的O1=C3双键和O2―N4单键键长相对OHA分子发生平均化,且O2―N4―C3―O1二面角趋近于0,更有利于与金属离子形成稳定的五元环螯合结构;OA阴离子的O48=C47双键与O49―C47单键键长相对OA分子也平均化,由O48=C47―O49-的p-π共轭效应所致。
2) 量化计算结果表明,OHA阴离子具有最高的HOMO值和最低的EHOMO-LUMO能隙,两个O原子具有更高的负电荷,相比OA阴离子具有更强的给电子能力及反应活性。
3) 捕收剂与金属离子作用的量化计算结果表明,OHA、OA与Ca2+/Ce3+离子的结合能由强到弱依次为OHA-Ce、OA-Ce、OA-Ca、OHA-Ca,即OHA与金属离子的结合能及对Ca2+/Ce3+的结合能差异都比OA的大。
4) 浮选结果表明,OHA对氟碳铈矿浮选的捕收能力和选择性都大于OA的,与量化计算结果规律一致。
REFERENCES
[1] JORDENS A, CHENG Y P, WATERS K E. A review of the beneficiation of rare earth element bearing minerals[J]. Minerals Engineering, 2013, 41(1): 97-114.
[2] GUPTA C K, KRISHNAMURTHY N. Extractive metallurgy of rare earths[J]. International Materials Reviews, 2013, 37(1): 197-248.
[3] TAVAKOL H. Computational study of simple and water-assisted tautomerism of hydroxamic acids[J]. Journal of Molecular Structure (Theochem), 2009, 916(1/3): 172-179.
[4] 秦煦坤, 钱玉鹏, 邱 玄. EPE型双亲嵌段共聚物强化油酸钠浮选分离萤石与微细粒石英[J]. 金属矿山, 2019, 48(5): 88-92.
QIN Xu-kun, QIAN Yu-peng, QIU Xuan. Improvement of flotation separation of fluorite and fine quartz by sodium oleate with nonionic-like amphiphilic triblock copolymers[J]. Metal Mine, 2019, 48(5): 88-92.
[5] 王介良, 曹 钊, 王建英. 辛基羟肟酸在氟碳铈矿表面的吸附机理[J]. 中南大学学报(自然科学版), 2019, 50(4): 762-770.
WANG Jie-liang, CAO Zhao, WANG Jian-ying. Adsorption mechanism of octyl hydroxamic acid on bastnaesite surface[J]. Journal of Central South University (Science and Technology), 2019, 50(4): 762-770.
[6] LIU Ming-xia, LI Hao, JIANG Tao, LIU Qi. Flotation of coarse and fine pyrochlore using octyl hydroxamic acid and sodium oleate[J]. Minerals Engineering, 2019, 132: 191-201.
[7] WANHALA A K, DOUGHTY B, BRYANTSEV V S. Adsorption mechanism of alkyl hydroxamic acid onto bastnasite: Fundamental steps toward rational collector design for rare earth elements[J]. Journal of Colloid and Interface Science, 2019, 553: 210-219
[8] 饶金山, 何晓娟, 罗传胜. 辛基羟肟酸浮选氟碳铈矿机制研究[J]. 中国稀土学报, 2015, 33(3): 370-377.
RAO Jin-shan, HE Xiao-juan, LUO Chuan-sheng. Flotation mechanism of octyl hydroximic acid on bastnaesite[J]. Journal of the Chinese Society of Rare Earths, 2015, 33(3): 370-377.
[9] 卢绿荣, 陈建华, 李玉琼. 硫化矿浮选捕收剂分子结构与性能的电子态密度研究[J].中国有色金属学报, 2018, 28(7): 1482-1490.
LU Lü-rong, CHEN Jian-hua, LI Yu-qiong. Electronic states density study of molecular structures and activity of sulfide floatation collectors[J]. The Chinese Journal of Nonferrous Metals, 2018, 28(7): 1482-1490.
[10] XU Hai-feng, ZHONG Hong, TANG Qing, WANG Shuai, ZHAO Gang, LIU Guang-yi. A novel collector 2-ethyl-2-hexenoic hydroxamic acid: Flotation performance and adsorption mechanism to ilmenite[J]. Applied Surface Science, 2015, 353: 882-889.
[11] DENG Jiu-shuai, LEI Yan-hua, WEN Shu-ming, CHEN Zhao-xu. Modeling interactions between ethyl xanthate and Cu/Fe ions using DFT/B3LYP approach[J]. International Journal of Mineral Processing, 2015, 140: 43-49.
[12] HUANG Xiao-yuan, CHENG Dang-guo, CHEN Feng-qiu, ZHAN Xiao-li. A density functional theory study on the decomposition of aliphatic hydrocarbons and cycloalkanes during coal pyrolysis in hydrogen plasma[J]. Journal of Energy Chemistry, 2015, 24(1): 65-71.
[13] RAGHAVACHARI K. Perspective on “Density functional thermochemistry. III. The role of exact exchange”[J]. Theoretical Chemistry Accounts, 2000, 103(3/4): 361-363.
[14] RAGHAVACHARI B K, STEFANOV B B, CURTISS L A. Accurate density functional thermochemistry for larger molecules[J]. Molecular Physics, 1997, 91(3): 555-560.
[15] 杨宏梅, 杨作银, 王 芳. 磷桥联双金属配合物结构优化的量子化学方法研究[J]. 北京化工大学学报(自然科学版), 2006, 33(1): 82-85.
YANG Hong-mei, YANG Zuo-ying, WANG Fang. Experiment rig with multi-purpose axial displacement fault self-recovery & control[J]. Journal of Beijing University of Chemical Technology(Natural Science Edition), 2006, 33(1): 82-85.
[16] OXGAARD J, MULLER R P, GODDARD W A. Mechanism of homogeneous Ir(Ⅲ) catalyzed regioselective arylation of olefins[J]. Journal of the American Chemical Society, 2004, 126(1): 352-363.
[17] WADT W R, HAY P J. Ab initio effective core potentials for molecular calculations. Potentials for main group elements Na to Bi[J]. The Journal of Chemical Physics, 1985, 82(1): 284-298.
[18] BUENKER R J, PEYERIMHOFF S D. Molecular geometry and the Mulliken-Walsh molecular orbital model. Ab initio study[J]. Chemical Reviews, 1974, 74(2): 127-188.
[19] FUKUI K, KOGA N, FUJIMOTO H. Interaction frontier orbitals[J]. Journal of the American Chemical Society, 1981, 103(1): 196-197.
[20] 孙 伟, 杨 帆, 胡岳华, 何国勇, 刘文莉. 前线轨道在黄铜矿捕收剂开发中的应用[J]. 中国有色金属学报, 2009, 19(8): 1524-1532.
SUN Wei, YANG Fan, HU Yue-hua, HE Guo-yong, LIU Wen-li. Application of frontier orbital in developing new collectors of chalcopyrite[J]. The Chinese Journal of Nonferrous Metals, 2009, 19(8): 1524-1532.
[21] HOPE G A, WOODS R, BOYD S E. A SERS spectroelectrochemical investigation of the interaction of butylethoxycarbonylthiourea with copper surfaces[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2004, 232(2/3): 129-137.
[22] 刘三军. 羟肟酸类药剂与铝土矿铝硅矿物的相互作用及浮选研究[D]. 长沙: 中南大学, 2012.
LIU San-jun. Action of alkyl hydroxamic acid on Alumina silica minerals in flotation of bauxite[D]. Changsha: Central South University, 2012.
[23] 高 莉. 白钨矿浮选捕收剂的性能评价及浮选机理研究[D]. 赣州: 江西理工大学, 2015. GAO Li. Performance evaluation and flotation mechanism research on scheelite flotation collection[D]. Ganzhou: Jiangxi University of Science and Technology, 2015.
[24] LEWIS D F V, IOANNIDES C, PARKE D V. Interaction of a series of nitriles with the alcohol-inducible isoform of P450: computer analysis of structure-activity relationships[J]. Xenobiotica, 1994, 24(5): 401-408.
[25] 张金生. 1, 7二氧杂螺[5.5]十一烷异头效应的量子化学研究[J]. 西南大学学报(自然科学版), 2010(9): 59-63.
ZHANG Jin-sheng. Quantum chemical study on the anomeric effect of the 1,7-dioxaspiro[5.5] dundecane[J]. Journal of Southwest University (Natural Science Edition), 2010(9): 59-63.
[26] 卢 天, 陈飞武. 原子电荷计算方法的对比[J]. 物理化学学报, 2012, 28(1): 1-18.
LU Tian, CHEN Fei-wu. Comparison of computational methods for atomic charges[J]. Acta Physico-Chimica Sinica, 2012, 28(1): 1-18.
[27] ZHAO Gang, WANG Shuai, ZHONG Hong. Study on the activation of scheelite and wolframite by lead nitrate[J]. Minerals, 2015, 5(2): 247-258.
DFT calculation of octyl hydroxamic acid and oleic acid and their flotation performance comparison on bastnasite and fluorite
WANG Peng1, CAO Zhao1, 2, 3, 4, WANG Jie-liang1, CAO Yong-dan1
(1. Institute of Mining Engineering, Inner Mongolia University of Science and Technology, Baotou 014010, China;
2. Guangdong Institute of Resources Comprehensive Utilization, Guangzhou 510650, China;
3. State Key Laboratory of Rare Metals Separation and Comprehensive Utilization, Guangzhou 510650, China
4. School of Minerals Processing and Bioengineering, Central South University, Changsha 410083, China)
Abstract: The density functional theory (DFT/B3LYP) calculation was carried out to analyze the geometric structure, frontier molecular orbital and Mulliken charge values of octyl hydroxamic acid (OHA) and oleic acid (OA) as well as their respective binding energy with Ca2+ and Ce3+ ions. Besides, pure mineral flotation was used to compare the flotation performances of OHA and OA for bastnasite and fluorite. The DFT calculation results show that OHA anion has the highest binding atom charge, the strongest HOMO energy and the lowest EHOMO-LUMO energy gap, thus performing stronger electron donating ability and reactivity than OA; the binding energy strength decreases in such order as OHA-Ce, OA-Ce, OA-Ca and OHA-Ca. In other words, OHA has the biggest binding energy with Ce3+ and largest binding energy difference for Ca2+ and Ce3+ ions. The flotation results show that OHA behaves stronger collection capacity and selectivity than OA, which is consistent with the DFT calculation results.
Key words: rare earth mineral; collector; density functional theory; flotation separation; frontier molecular orbital
Foundation item: Project(51764045) supported by the National Natural Science Foundation of China; Project (GK-201804) supported by the Research Fund Program of State Key Laboratory of Rare Metals Separation and Comprehensive Utilization, China; Project(NJYT-18-B08) supported by Inner Mongolia Young Science & Technology Talent Support Plan, China; Project(2017YQL05) supported by Outstanding Youth Science Foundation of Inner Mongolia University of Science and Technology, China
Received date: 2019-09-11; Accepted date: 2019-11-20
Corresponding author: CAO Zhao; Tel: +86-18747235897; E-mail: caozhao1217@163.com
(编辑 龙怀中)
基金项目:国家自然科学基金资助项目(51764045);稀有金属分离与综合利用国家重点实验室开放基金资助项目(GK-201804);内蒙古高等学校“青年科技英才支持计划”(NJYT-18-B08);内蒙古科技大学优秀青年基金资助项目(2017YQL05)
收稿日期:2019-09-11;修订日期:2019-11-20
通信作者:曹 钊,教授,博士;电话:18747235897;E-mail:caozhao1217@163.com