文章编号:1004-0609(2008)S1-0377-04
电解法处理铬渣溶浸液的电极反应机理
许丽萍1, 2,张胜涛2,钱瑛2
(1. 中国铝业股份有限公司 郑州研究院,郑州 450041;
2. 重庆大学 化学化工学院,重庆 400044)
摘 要:运用线性电位扫描伏安法(LSV)分析电解法处理铬渣溶浸液中Cr6+初始浓度、溶液初始酸度、电位扫描速度等因素对铁电极极化曲线测定的影响,并确定了三者的最佳取值;依据峰电位,峰电流密度与扫描速度的关系,研究了体系电极过程的可逆性,发现该电极过程具有明显的不可逆性特征。
关键词:线性电位扫描伏安法;极化曲线;铬渣溶浸液
中图分类号:X 703.1 文献标识码:A
Electrode reactive mechanism of chromium residue solution treatment by electrolytic method
XU Li-ping, ZHANG Sheng-tao, QIAN Ying
(1. Zhengzhou Research Institute, Aluminum Corporation of Chins Limited, Zhengzhou 450041, China;
2. College of Chemistry and Chemical Engineering, Chongqing University, Chongqing 400044, China)
Abstract: Linear sweep voltammetry(LSV) was employed to investigate the influence of the initial concentration of Cr6+, pH of solutions and the scanning speed of potential on the polarization curves of Fe electrode. The three optimum values were given from experimental data. Based on the relationship of peak potential, peak current density and scanning speed, it is found that the electrochemical process is irreversible.
Key words: linear sweep voltammetry; polarization curve; chromium residue solution
在铬盐的生产过程中,排放出大量含铬废渣即铬渣,严重污染环境,成为铬盐企业的一大难题。目前,国内冶金和化学工业中每年排出20~30万t铬渣。铬渣主要成分是可溶性铬酸钠、酸溶性铬酸钙等六价铬离子。而Cr6+对人体具有明显的毒害作用[1]。积极探索含铬废渣、废水中的Cr6+的处理及回收利用有着重要的意义。然而,国内外学者大多数是从工艺的角度出发,对传统的电化学方法处理Cr6+废渣、废水研究得比较广泛,目前尚未看到关于电化学方法处理含Cr6+废渣、废水的机理研究, 为了进一步指导电解还原法处理铬废渣、废水的工艺,为改善工艺条件提供可靠的理论依据,有必要对其电解技术进行机理的分析研究。
本文作者对间接电解还原法处理含Cr6+废水的电极反应机理进行了研究。该方法主要原理是利用电解使铁阳极溶解产生Fe2+,Fe2+使 Cr6+还原成Cr3+同时被氧化成Fe3+,Fe3+、Cr3+与水中的OH-形成氢氧化物沉淀,起到了凝聚和吸附作用,从而除去Cr6+离子。研究中采用线性电位扫描伏安法(LSV)测定铁电极的极化曲线,分析了样品液中Cr6+初始浓度、溶液初始酸度、电位扫描速度等因素对铁电极极化曲线测定的影响;同时分析了电极过程的不可逆性。
1 实验
1.1 仪器
CHI660B型电化学工作站、pH酸度计。
1.2 样品液及工作电极的制备
样品液:称取5.252 0 g经过预处理的铬渣,溶于H2SO4(0.05 mol/L)100.00 mL,在恒温水浴槽中保持恒温60 ℃,充分搅拌,冷却浸泡1 h后,经抽滤得到黄色澄清溶液,调节溶液pH,并按需稀释,即为待处理的样品液。
工作电极的制备:将低碳钢截成长、宽均为1.00 cm的电极,电极四周用400号金刚砂纸粗磨后,再用700号水相砂纸抛光,以防止缝隙腐蚀,再用丙酮除油,蒸馏水洗净,用环氧树脂封装,暴露出1.00 cm2的工作面,工作面经400号金刚砂纸粗磨后,再用700、800、900号水相砂纸逐级抛光。每次实验后均对电极表面重新进行打磨、抛光处理,以暴露出新鲜的电极表面,然后丙酮除油、蒸馏水洗净。并更新溶液,保证了溶液的均匀性,再进行下一次的电位扫描。
1.3 电化学测试
电化学测试是在CHI660B电化学工作站上进行,采用三电极体系,参比电极为饱和甘汞电极(SCE),文中所报道的电位均相对于此参比电极,辅助电极为较大的金属铂片,工作电极为低碳钢(97.78%)。实验分别考察了样品液Cr6+浓度、扫描速度、酸度等条件对线性扫描伏安法得到的极化曲线的影响。实验均在室温下进行。
2 结果与讨论
2.1 扫描速度的影响
图1所示为LSV测定的扫描速度对极化曲线的影响,参数见表1。
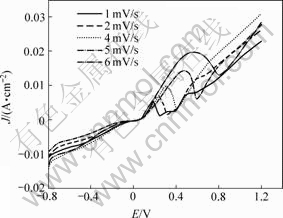
图1 扫描速度对极化曲线的影响
Fig.1 Influence of scanning speed on polarization curves (c(Cr6+)=0.10 mol/L, pH=2.2, E=-800~1 200 mV)
表1 扫描速度对极化曲线的影响
Table 1 Influence of scanning speed on polarization curves
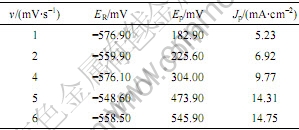
由图1和表1可以看出,随着扫描速度v的加 快,Fe的氧化峰峰电流密度Jp增大,且峰电位Ep比低扫速对应的峰电位正移。扫描速度越低,极化过程中出现的电流密度峰越明显,即Fe的氧化峰越明显。当扫描速度为1 mV/s时,得到的极化曲线铁的氧化峰效果最好。
在进行电化学研究时,可能产生两方面误差[2]:一是双电层充电电流ic=Cdv,Cd可能随电极电位变化, 所以ic也随电极电位变化,而实际测得的电流i=ir+ic,即电极反应电流与双电层充电电流之和,因此测得的电流密度会发生变化;二是欧姆极化的影响,当电流增大时,溶液的欧姆极化也在增大,所以电极电位变化速度v减小,导致峰电流密度Jp的减小。上述两种误差都随扫描速度v的增大而增大,所以,虽然提高v可以提高Jp,但是误差也随之迅速增加。因此在扫描过程中,应尽可能选择较低的扫描速度v。
考虑到当扫描速度足够小时,线性极化曲线才可以近似地认为是达到稳态的;有研究者[3]作过计算,在自然对流情况下,有效扩散层的厚度一般为(1~2)×10-2 cm,则当电位扫描速度远小于10 mV/s时,所得极化曲线近似为稳态极化曲线,因此,通常采用1~2 mV/s的扫描速度就可得到满意的结果。并且当扫描速度足够小时,极化曲线上能更加充分地体现极化过程中出现的电流密度峰。所以,实验最终选择的扫描速度为1 mV/s。
2.2 Cr6+初始浓度的影响
图2所示为LSV测定的Cr6+初始浓度对极化曲线的影响,参数如表2所示。
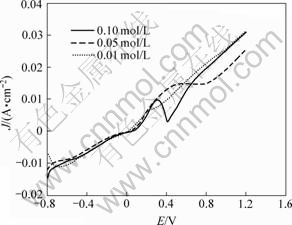
图2 Cr6+初始浓度对极化曲线的影响
Fig.2 Influence of initial concentration of Cr6+ on polarization curves (v=4 mV/s, pH=2.2, E=-800~1 200 mV)
表2 Cr6+初始浓度对极化曲线的影响
Table 2 Influence of initial concentration of Cr6+ on polarization curves
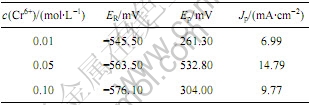
由图2看到,随着浓度增加,峰电流密度增大,Fe的氧化峰形更加明显。其主要原因可能是因为Cr6+是一种强氧化剂,具有促进Fe在酸性介质中钝化的能力。很明显,当Cr6+的浓度为0.10 mol/L时得到的极化曲线Fe的氧化峰形最好。因此,实验选择Cr6+溶液的初始浓度为0.10 mol/L。
2.3 溶液初始酸度的影响
图3 所示为LSV测定的溶液初始酸度对极化曲线的影响,参数见表3。
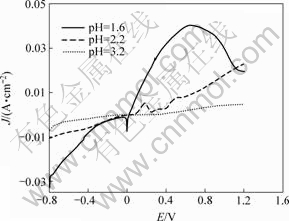
图3 溶液初始pH值对极化曲线的影响
Fig.3 Influence of initial pH of solutions on polarization curves (c(Cr6+)=0.10 mol/L, v=1 mV/s, E=-800~1 200 mV)
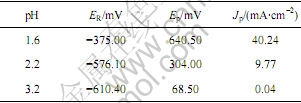
表3 溶液初始酸度对极化曲线的影响
Table 3 Influence of initial pH of solutions on polarization curves
由图3看到,溶液初始酸度越强(pH值越小),极化曲线上的电流密度峰值越高。pH=3.20的极化曲线图形平坦,整个曲线电流密度变化较小,几乎看不出存在电流密度峰,pH=1.60的极化曲线上,电流密度变化过大过快,对研究电极有较大腐蚀作用,电极反应Fe的氧化峰被遮蔽。所以,实验选择溶液的初始酸度为pH=2.2。
2.4 线性扫描伏安法研究电极过程的可逆性
扫描速度v是电极过程可逆性的一个重要判据,通过极化曲线峰电位、峰电流与扫描速度的关系曲线,容易判断出体系电极过程是否具有可逆性。
很多线性电位扫描文献中都探讨过扫描速度与反应可逆性的关系[4-7]。且由图1可以看出:随着扫描速度的加快,峰电位正移,说明该阳极氧化过程是不可逆的。随着扫描速度的加快,Fe的氧化峰峰电流密度增大,但极化曲线上的细节峰得不到体现,且峰电位比低扫速对应的峰电位正移。扫描速度越低,极化过程中出现的电流密度峰越明显,即Fe的氧化峰越明显,因此可以判定该电极过程属于不可逆过程。以lg v对Ep作图,可得图4。从图4中可以看出,当扫描速度低于5 mV/s,Ep与lg v几乎呈直线关系;以v1/2对Jp作图,可得图5,从图5中可以看出,当扫描速度小于5 mV/s,Jp与v1/2几乎呈直线关系;但当扫描速度大于5 mV/s时,Ep和Jp有增大趋势,表明当扫描速度过大时,反应不可逆程度增大。
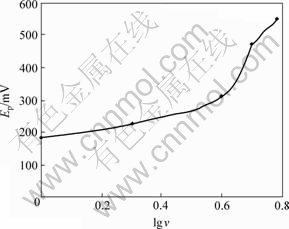
图4 峰电位与扫描速度的关系
Fig.4 Relationship between Ep and scanning speed
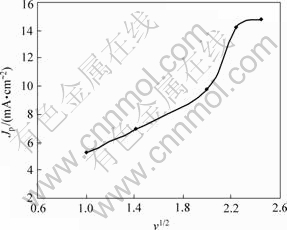
图5 峰电流密度与扫描速度的关系
Fig.5 Relationship between Jp and scanning speed
3 结论
1) LSV 法测得铁的极化曲线表明:当扫描速度为1 mV/s,Cr6+的初始浓度为0.10 mol/L,溶液pH=2.20时效果最佳。
2) LSV法研究体系电化学过程的可逆性的实验结果表明:该电极过程是不可逆过程。且当扫描速度大于5 mV/s时,随着扫描速度的增大,体系不可逆程度增加。
REFERENCES
[1] 陈雪松, 许春兰. 橡胶厂工业废水中铬的测定[J]. 内蒙古石油化工, 2002, 27(1): 40-41.
CHEN Xue-song, XU Chun-lan. Determination of chromium in industrial waste water of rubber plant[J]. Inner Mongolian Petrochemical Industry, 2002, 27(1): 40-41.
[2] 刘汝娥. 线性扫描阳极溶出伏安法测定铜、铅、锌、镉[J]. 陕西环境, 1997, 4(3): 26-29.
LIU Ru-e. Determination of Cu, Pb, Zn, Cd by linear sweep anodic stripping voltammetry[J]. Shaanxi Environment, 1997, 4(3): 26-29.
[3] 刘永辉. 电化学测试技术[M]. 北京: 北京航空学院出版社, 1987.
LIU Yong-hui. Electrochemical measurement techniques[M]. Beijing: Beijing Aviation Institute Press, 1987.
[4] BARD A J, FANLKNER L R. 电化学方法[M]. 谷林英, 译. 北京: 化学工业出版社, 1986.
BARD A J, FANLKNER L R. Electrochemical method[M]. LIN Gu-ying, transl. Beijing: Chemical Industry Press, 1986.
[5] 周仲伯, 陈永言. 电极过程动力学基础教程[M]. 武汉: 武汉大学出版社, 1989.
ZHOU Bo-zhong, CHEN Yong-yan. Basic course of electrode process dynamics[M]. Wuhan: Wuhan University Press, 1989.
[6] 田绍武. 电化学研究方法[M]. 北京: 科学出版社, 1984: 230.
TIAN Shao-wu. The electrochemical research method[M]. Beijing: Science Press, 1984: 230.
[7] 南安普敦电化学小组. 电化学中的仪器方法[M]. 柳厚用, 译. 上海: 复旦大学出版社, 1992: 179.
Southampton Electrochemistry Group. The instrumental method of electrochemistry[M]. LIU Yong-hou, transl. Shanghai: Fudan University Press, 1992: 179.
通讯作者:许丽萍,硕士研究生;电话:0371-68918462;E-mail: xuliping620@126.com
(编辑 杨幼平)