网络首发时间: 2016-07-07 16:26
稀有金属 2017,41(06),720-724 DOI:10.13373/j.cnki.cjrm.xy16040010
黄铁矿表面XPS分析与生物浸出机制研究
武彪 温建康 王淀佐
北京有色金属研究总院生物冶金国家工程实验室
摘 要:
黄铁矿的溶解过程受表面化学反应控制, 表面性质的变化是影响溶解动力学的关键因素。X射线光电子能谱技术 (XPS) 是研究矿物溶解过程先进的表面分析技术, 可分析矿物表面5 nm范围内化学组成的变化, 为解释矿物溶解机制和动力学提供可靠的数据指导。本文采用XPS分析了常温下黄铁矿生物浸出过程中矿物表面的变化, 黄铁矿表面主要由含Fe和含S的两种化合物组成。其中, 含Fe化合物主要为FeS2、针铁矿、硫酸盐、高铁络合物;含S化合物主要为FeS2、硫酸盐、半胱氨酸、多硫化合物。研究表明, 黄铁矿的溶解与表面硫的氧化密切相关 (从S22-氧化至SO42-) , 黄铁矿溶解过程首先是Fe-S键断裂, 在细菌、溶氧等氧化剂的作用下, Fe2+和S22-迅速被氧化, 化学反应界面逐步内扩至黄铁矿本体, 最后铁氧化物或氢氧化物型氧化产物稳定存在于未反应的黄铁矿表面。黄铁矿的生物浸出遵循硫代硫酸盐机制, 间接浸出和直接浸出机制同时存在, 浸出过程中形成稳定的铁氧化物或氢氧化物型氧化产物, 在一定程度上加快了表面电子传递速率, 促进了黄铁矿电化学氧化溶解。
关键词:
X射线光电子能谱技术;黄铁矿;生物浸出;矿物表面;
中图分类号: TF18
作者简介:武彪 (1979-) , 男, 甘肃白银人, 硕士, 高级工程师, 研究方向:有色金属冶金;电话:010-82241007;E-mail:angelwbiao@sina.com;
收稿日期:2016-04-13
基金:国家自然科学基金项目 (51574036) 资助;
XPS Analysis and Mechanism of Pyrite Biooxidation
Wu Biao Wen Jiankang Wang Dianzuo
National Engineering Laboratory of Biohydrometallurgy, General Research Institute for Nonferrous Metals
Abstract:
The dissolution of pyrite was controlled by the surface chemical reaction, which was the key factor affecting the dissolution process. X-ray photoelectron spectroscopy ( XPS) was an advanced surface analysis technique in study of mineral dissolution process, and a change in the chemical state of element on the surface less 5 nm could be observed by XPS, which could be good reference for understanding mechanisms and kinetics for bioleaching of pyrite. In this paper, XPS analysis was used to analyze the changes of chemical state on mineral surface during the biological leaching of pyrite at room temperature. The results showed that the surficial layer was made up of both the sulphur-bearing and the iron-bearing products, the sulphur-bearing group was comprised of pyrite, sulphate, cysteine and polysulphide, while the iron-bearing group was comprised of goethite and ferric complex. The results showed that dissolution of pyrite was related to surficial sulphur speciation. In the pyrite dissolution process, the Fe-S bond broke first, and then the surficial iron and sulphur were rapidly oxidized by bacteria and oxygen, after that the reaction interface migrated deeper into the pyrite body, and the iron hydroxides and oxides were the final remaining phase on the surface of pyrite. The pyrite was bio-degraded via thiosulfate mechanism, and multiple patterns of bioleaching coexisted, including“indirect”and“direct”leaching. To a certain extent, these stable iron hydroxides and oxides accelerated electron transfer on the surface of pyrite, and promoted the electrochemical oxidation of pyrite.
Keyword:
X-ray photoelectron spectroscopy; pyrite; bioleaching; mineral surface;
Received: 2016-04-13
黄铁矿是参与地球铁硫循环的重要矿物, 由于黄铁矿通常与金、铜、镍、钴、铀等重金属硫化物共生, 黄铁矿是重要的酸源, 可用于其他有色金属硫化物的浸出, 特别是耗酸类硫化矿物的浸出。此外, 黄铁矿在空气或冶金过程中氧化后酸化水体, 是酸性水 (AMD) 的重要成因[1]。近年来国内外学者开展了大量的基础研究工作, 试图揭示黄铁矿氧化机制并获得氧化速率控制步骤, 取得了一批重要成果。但因黄铁矿在生物浸出过程中氧化分解步骤复杂, 而且表面微环境下生成产物很难测定, 其氧化机制还没完全搞清楚[2]。黄铁矿在水溶液中存在化学、电化学和生物氧化作用, 黄铁矿表面首先在高表面能的缺陷处先氧化[3]。黄铁矿氧化过程生成的硫酸盐中的4个氧90%是来自于水而非溶氧, 黄铁矿表面与溶液界面的电化学反应是黄铁矿溶解的控制步骤[4]。黄铁矿表面的Fe (Ⅲ) O和氢氧化铁是氧化反应的中间产物而不是溶液中铁离子的沉淀物。添加高铁溶液和通氧气可促进黄铁矿的氧化, 高铁离子的氧化作用更强, 二者同时加入效果优于单一条件。黄铁矿化学氧化与电化学氧化机制不同, 化学反应是反应剂直接碰撞生成产物, 而电化学氧化不是反应剂直接碰撞, 而是反应剂与电极表面 (矿石表面) 碰撞。反应剂直接碰撞及产物的形成会放热, 而电化学反应产生电流的过程自由能发生变化, 但不放热, 在矿物/溶液界面发生的化学反应和电化学反应一般很难区分开来[5]。在浸出过程中, 黄铁矿表面很少形成元素硫, 在高压条件下易生成元素硫。p H值在特定的条件下起较大作用, 一般情况下对黄铁矿的溶解影响较小, 特别是在只有氧存在的条件下, 而有高铁离子存在时影响较大。Fe3+/Fe2+浓度比是影响黄铁矿溶解的关键因素, 即使是在有氧存在的条件下, 溶液氧化还原电位是控制溶解过程的关键因素[6,7,8]。黄铁矿的溶解是通过表面进行的, 矿物表面组成的变化也是影响溶解的关键因素[9,10]。大多数学者认为矿物表面与产物、化学及物相组成有关, 最外层的表面产物为氢氧化铁 (可能是针铁矿) 、氧化铁 (赤铁矿) 、硫酸盐、亚硫酸盐、硫代硫酸盐, 元素硫和缺金属硫化物组成。有学者通过实验和理论研究表明[11,12], 黄铁矿表面产物是随着反应时间的推移, 从OH-和O2-逐步转化为Fe OOH, 最后生成硫酸盐。通过X射线光电子能谱技术 (XPS) 分析, 可揭示矿物表面与矿物本体结合能的不同, 可用于讨论矿物表层的重构及组成。本文通过表征矿物表面组成的变化, 为黄铁矿生物浸出机制和动力学提供可靠的数据指导。
1 实验
1.1 样品
本实验采用矿样是从紫金山金铜矿挑选的黄铁矿富矿块, 经过浮选获得黄铁矿纯矿物, 然后经活性炭脱药, 用于生物浸出实验。化学分析见表1和图1。
由表1可知, 样品中铁、硫含量达到92% (质量分数) 以上, 图1中XRD结果显示其主要成分是Fe S2, 除了Fe S2的特征峰之外基本没有杂质峰, 这说明经过浮选得到的黄铁矿纯度较高, 可作为纯矿物进行实验。
1.2 实验条件
本实验采用装置为250 ml锥形瓶, 矿石磨矿细度为-74μm, 矿浆浓度为5%, 细菌为以Acidithiobacillus ferrooxidans为主的混合菌, 接种浓度为15%, 初始p H值为1.5, 将配置好矿浆的锥形瓶放入恒温振荡器中, 设置温度35℃, 转速为120 r・min-1, 浸出时间15 d。
1.3 实验方法
浸出结束后, 进行洗涤、过滤, 再在常温下晾干, 并称重, 计算渣率, 最后放入厌氧培养箱中送XPS检测分析。XPS分析采用美国Perkin-Elmer公司PHI5000CESCA型多功能电子能谱仪 (XPS) , X射线源采用Al Ka, 能谱扫描范围为0~1200 e V, 宽幅扫描间距为1 e V, 窄幅扫描间距为0.1 e V, 能谱采用以样品表面污染碳的C 1s结合能 (284.68 e V) 定标, 并校正荷电效应, 对样品进行宽程扫描, 得到总的谱图。然后通过窄程扫描得到各元素的峰, 获得结合能数据和元素组成信息, 分峰拟合采用高斯/劳伦特斯方程最小均方差Shirley消背底方法。为保持浸出渣的原始状态, XPS分析前抽真空至0.1~1.0 Pa, 用于去除表面气膜以减少污染[13]。
表1 矿石化学元素分析Table 1 Chemical compositions of ore (%, mass fraction) 下载原图

表1 矿石化学元素分析Table 1 Chemical compositions of ore (%, mass fraction)
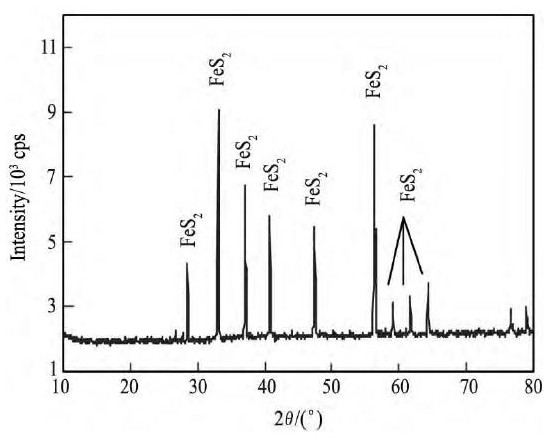
图1 黄铁矿XRD图Fig.1 XRD pattern of pyrite
2 结果与讨论
2.1 XPS全元素分析
XPS全元素扫描谱中可以得到浸出渣表层中所含C, O, Cu, Fe和S元素的峰值, 具体结果如图2所示。结合能为284.80e V的C 1s是碳校准峰值, O 1s峰值是浸渣表层空气污染或被氧化所致, 不是黄铁矿中固有的组元。由于氢元素的信息无法从光电子能谱中得到, 在表层的元素中还可能有未显示的H元素存在。
2.2 XPS窄谱分析
图3为细菌浸渣表面窄谱分析结果, 各元素占比及组成如表2, 黄铁矿中其他杂质较少, 主要元素为O, Fe和S, 其中O占比最高, 这与表面氧化状态有关。浸渣表面S 2p和Fe 2p扫描光谱如图3 (b, d) 所示, 从S 2p窄谱分析, 结合能为162.29 e V峰值的出现, 主要为未溶解的黄铁矿本体。而169.17和163.40 e V峰值的出现, 表明有半胱氨酸和硫酸盐生成, 或二者同时存在, 半胱氨酸的存在与细菌的代谢有关。由Fe2p窄谱分析可知, 铁的形态比较复杂, +2价和+3价铁离子同时存在, 707.30 e V峰值的出现, 表明浸渣表面有Fe2+离子存在。
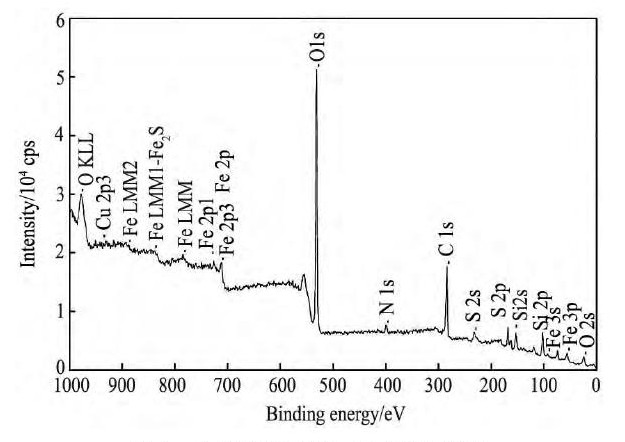
图2 生物浸渣XPS全元素分析图Fig.2Survey (full-range) XPS spectrum of bioleaching resi-due
S 2p结合能峰宽从最低值到最高值为159~173 e V, 峰值分别为162.69, 163.40和169.17 e V。结合能峰值为160.8~161.3, 161.4~162.3和162.4~162.9 e V范围内为单一的S2-单体[14,15,16]。结合能峰值在 (164.0±0.25) e V范围内主要为元素硫或半胱氨酸, 在 (166.7±0.3) e V主要为亚硫酸盐, 多硫化物比较复杂, 结合能峰值一般在 (162.5~164.0) e V之间。硫酸盐和硫代硫酸盐彼此是重叠的, 一般难以判断, 据研究报道[17], 硫代硫酸盐的峰值为 (167.7~168.4) e V, 硫酸盐的峰值为 (168.1~168.8) e V。

图3 细菌浸渣表面各元素窄谱分析Fig.3 Fitted S 2p and Fe 2p spectra for bioleaching residue
表2 细菌浸渣表面元素含量及结合能Table 2 Chemical compositions and binding energy of bi-oleaching redidues (%, mass fraction) 下载原图

表2 细菌浸渣表面元素含量及结合能Table 2 Chemical compositions and binding energy of bi-oleaching redidues (%, mass fraction)
Fe比S的形态更加复杂, 窄谱曲线比较杂乱。结合能峰值为707.30, 712.24 e V显示主要为Fe OOH, 以及高铁络合物, 络合物因为生物浸出过程中生成部分铁矾, 粘附于浸渣表面所致。
2.3 氧化动力学及机制分析
XPS分析结果表明黄铁矿在细菌存在条件下氧化过程也遵循硫代硫酸盐机制, 黄铁矿表面S-S键比S-Fe键弱, 先断裂, 释放出S-, 从相邻S-转移电子, 生成S2-, 从铁氧化物中Fe2+得电子, 形成S-OH中间产物, 然后生成硫代硫酸盐, 最终生成硫酸盐。在细菌的作用, 表面生成的元素硫先被氧化, 生成亚硫酸盐、硫代硫酸盐等化合物, 铁主要以氧化物和氢氧化物形式稳定存在。而且表面还存在细菌代谢产物半胱氨酸[18], 充分说明黄铁矿的溶解以联合浸出机制为主, 即间接浸出和直接浸出同时存在[19]。
黄铁矿浸渣主要由表层、过渡层和黄铁矿本体组成, 在酸性溶液中, 溶氧和水分子优先于黄铁矿表面的铁原子结合, 此反应过程生成二硫化物、铁氧化物、硫酸盐、元素硫等, 随着水分子氧化扩散的进行, 化学反应界面逐渐加深至黄铁矿本体。随着化学反应往深部黄体矿本体的进行, 最先消失的是元素硫, 紧接着是二硫化物、硫酸盐和硫代硫酸盐, 最后铁的氢氧化物和氧化物稳定存在于未反应的黄铁矿表面。这是由于生成的元素硫逐步向表层扩散, 然后被氧化成硫酸盐, 主要反应机制如下:
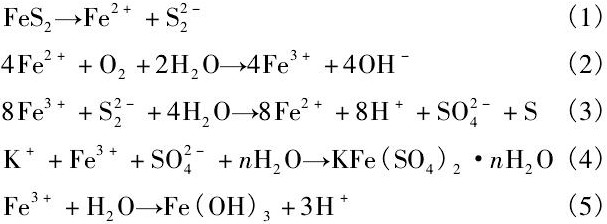
Eggleston等[20]也证实黄铁矿表面生成了稳定的氧化物或氢氧化物型氧化产物, 这些产物层促进了电子从黄铁矿的价带到氧化物/氢氧化物导带的传递, 因此有助于黄铁矿电化学氧化。
3 结论
XPS分析了常温下黄铁矿生物浸出过程中矿物表面的变化, 黄铁矿表面主要由含Fe和含S两种化合物组成。其中, 含Fe化合物主要为Fe S2、针铁矿、褐铁矿、硫酸盐、高铁络合物等;含S化合物主要为Fe S2、硫酸盐、半胱氨酸、多硫化合物等。即黄铁矿的生物浸出遵循硫代硫酸盐机制, 间接浸出和直接浸出机制同时存在。黄铁矿的溶解首先是Fe-S键断裂, 在细菌、溶氧等氧化剂的作用下, Fe2+和S22-迅速被氧化, 化学反应界面逐步内扩至黄铁矿本体, 最后铁氧化物或氢氧化物型氧化产物稳定存在于未反应的黄铁矿表面, 加快了表面电子传递速率, 促进了黄铁矿电化学氧化溶解。
参考文献
[1] Gu G H, Sun X J, Hu K T, Li J H, Qiu G Z.Electrochemical oxidation behavior of pyrite bioleaching by Acidthiobacillus ferrooxidans[J].Transactions of Nonferrous Metals Society of China, 2012, 22 (5) :1250.
[2] Rodríguez Y, Ballester A, Blázquez M L.New information on the pyrite bioleaching mechanism at low and high temperature[J].Hydrometallurgy, 2003, 71 (1-2) :37.
[3] Mc Kibben Michael A, Barnes Hubert L.Oxidation of pyrite in temperature acidic solution:rate laws and surface textures[J].Geochimica Et Cosmochimica Acta, 1986, 50 (7) :1509.
[4] Holmes P R, Crundwell F K.The kinetics of the oxidation of pyrite by ferric ions and dissolved oxygen:an electrochemical study[J].Geochimica Et CosmochimicaActa, 2000, 64 (2) :263.
[5] Bockris J O, Reddy A K N, Gamboa-Aldeco M.Modern Electrochemistry 2A:Fundamentals of Electrodics[M].New York:Kluwer Academic, 2000.85.
[6] Chandra A P, Gerson A R.The mechanisms of pyrite oxidation and leaching:a fundamental perspective[J].Surface Science Reports, 2010, 65 (9) :293.
[7] Ruan R M.A Case Study on Bio-heapleaching Practice of Zijinshan Copper Sulphide:Kinetics and Process Optimization[D].Changsha:Central South University, 2011.91. (阮仁满.紫金山铜矿生物堆浸工业案例分析―相关动力学研究与多因素匹配[D].长沙:中南大学, 2011.91.)
[8] Holmes Paul R, Crundwell Frank K.The kinetics of the oxidation of pyrite by ferric ions and dissolved oxygen:an electrochemical study[J].Geochimica Et Cosmochimica Acta, 2000, 64 (2) :263.
[9] Wu B, Liu X Y, Chen B W, Wen J K.Inhibit bioleaching of pyrite by controlling oxygen content[J].Chinese Journal of Rare Metals, 2010, 34 (6) :894. (武彪, 刘兴宇, 陈勃伟, 温建康.控制氧含量抑制黄铁矿浸出研究[J].稀有金属, 2010, 34 (6) :894.)
[10] Crundwell F K.How do bacteria interact with minerals[J].Hydrometallurgy, 2003, 71 (1-2) :75.
[11] Rosso K M, Becker U, Hochella M F.The interaction of pyrite{100}surfaces with O2and H2O:fundamental oxidation mechanisms[J].American Mineralogist, 1999, 84 (10) :1609.
[12] Rojas-Chapana J A, Tributsch H.Biochemistry of sulfur extraction in biocorrosion of pyrite by thiobacillus ferrooxidans[J].Hydrometallurgy, 2001, 59 (2-3) :291.
[13] Aude Naveau, Fanny Monteil-Rivera, Emmanuel Guillon, Jacques Dumonceau.XPS and XAS studies of copper (II) sorbed onto a synthetic pyrite surface[J].Journal of Colloid and Interface Science, 2006, 303 (4) :25.
[14] Mattila S, Leiro J A, Laajalehto K.Surface XPS corelevel shifts of Fe S2[J].Applied Surface Science, 2003, 97:212.
[15] Leiro J A, Mattila S S, Laajalehto K.XPS study of the sulphur 2p spectra of pyrite[J].Surface Science, 2003, 547 (1-2) :157.
[16] Laajalehto K, Leppinen J, Kartio I, Laiho T.XPS and FTIR study of the influence of electrode potential on activation of pyrite by copper or lead[J].A:Physicochemical and Engineering Aspects, 1999, 154:193.
[17] Cai Y F, Pan Y G, Xue J Y, Sun Q F, Su G Z, Li X.Comparative XPS study between experimentally and naturally weathered pyrites[J].Applied Surface Science, 2009, 255 (21) :8750.
[18] Rojas-Chapana J A, Tributsch H.Bio-leaching of pyrite accelerated by cysteine[J].Process Biochemistry, 2000, 35 (8) :815.
[19] Wu B, Wen J K, Chen B W, Yao G C, Wang D Z.Control of redox potential by oxygen limitation in selective bioleaching of chalcocite and pyrite[J].Rare Metals, 2014, 33 (5) :622.
[20] Eggleston C M, Ehrhardt J J, Stumm W.Surface structural controls on pyrite oxidation kinetics:an XPSUPS, STM, and modeling study[J].American Mineralogist, 1996, 81 (9) :1036.