���±�ţ�1004-0609(2009)09-1695-05
���ȵ�pHֵ��Һ��BDT����װĤ��ͭ�缫�Ļ�ʴ��Ϊ
������1��ͯҫ��2����Ⱥ2�������2���� ��1
(1. ����Ƽ�ѧԺ ��ѧ����ѧԺ������ 401331��
2. ���ϴ�ѧ ��ѧ����ѧԺ������ 400715)
ժ Ҫ�����÷�������װ��������ͭ�缫�����γ�һ��1, 3-���ϻ���(BDT)����������װĤ��ͨ�������迹���������ߺ�ѭ�������ȵ绯ѧ����̽�ָ�����װĤ��3%NaCl��Һ�ж�ͭ�缫�Ļ�ʴ���á�ʵ�������BDT�ܹ���Ч����װ��ͭ�ı����γɵ���������װĤ��BDT����װĤ����Ч������ͭ������3%NaCl��ʴ�����Լ�����NaCl��Һ�еĸ�ʴ��Ϊ����ʴЧ������װʱ����ӳ������߲������ȶ�����pHֵ�ϵ͵���Һ���Ծ��нϺõĻ�ʴЧ������BDTŨ��Ϊ1.0��10-2 mol/L����װʱ��Ϊ40 hʱ��ͭ�缫�ĸ�ʴ������С����ʴЧ����á�
�ؼ��ʣ�1, 3�����ϻ�������װĤ��ͭ�缫����ʴ
��ͼ����ţ�TG 174.42���� ���ױ�ʶ�룺A
Corrosion inhibition behavior of copper electrode by self-assembled monolayer of BDT in solution with chlorine and low pH value
HUANG Wen-zhang1, TONG Yao-bin2, LUO Hong-qun2, LI Nian-bing2, LI Dan1
(1. School of Chemistry and Chemical Engineering, Chongqing University of Science and Technology,
Chongqing 401331, China;
2. School of Chemistry and Chemical Engineering, Southwest University, Chongqing 400715, China)
Abstract: Adopting molecular self-assembly technique, a self-assembled membrane of 1, 3-benzenedithiol (BDT) was formed on the surface of the copper electrode. The effect of this membrane on the corrosion inhibition of copper electrode in 3% NaCl solution was investigated by using electrochemical impedance spectroscopy (EIS), polarization curve and cyclic voltammetry (CV). The results show that BDT can be assembled on the surface of copper electrode to form monomolecular self-assembled membrane��and the membrane can efficiently inhibit the copper base corrosion in the 3% NaCl corrosion medium and acidic solution. The inhibition efficiency increases with increasing assembling time and obtains steady state gradually. In the solution with lower pH value, BDT can also keep good inhibitor. When the copper electrode is modified with 1.0��10-2 mol/L BDT for 40 h, the corrosion current is the smallest, the inhibition efficiency is the highest.
Key words: 1, 3-benzenedithiol; self-assembled monolayer; copper electrode; corrosion
����ͭ�������õĵ��ȡ������Ժͻ�е�ӹ����ܣ���ˣ�ͭ�㷺Ӧ���ڹ�ҵ�С���ͨ������£�ͭ����ʴ�ԽϺã����ں������ӵ���Һ�лᱻ���ظ�ʴ�������ӱ�ijЩ�ۻ��������������ڽ���������ڱ��Ķۻ�Ĥ���γ�ǿ�糡��ʹ�������������ܳ���������������ȵ��������ٽ����ܽ�[1-2]��
Ŀǰ��Ӧ���ڸ�ʴ���л�����Ҫ�Ǻ���δ��Եĵ��p�����ԭ�ӵ����廷״�л�����б���������(BTA)Ӧ�ñȽϹ㷺[3-7]����BTA��ͭ��ʴ���õ����pHֵΪ6~11������pHֵ�ϵ͵�һЩ�����У�BTA�Ļ�ʴЧ�ʼ����½���ʹ��Ӧ�÷�Χ�ܵ����ơ�
1992�꣬SABATANI��RUBINSTEIN[8]�Լ�BLJIEV��HUBIN[9]�������ڿ����е���Ĥ���ǵ�Cu�ĸ�ʴ���裬�Ӵ�����װ��ʼ���ڷ���ʴ�о�������װĤ��һ��߶�����ķ�����װ��ϵ��ӵ�����õ��ȶ��Ժ��������ڽ�����ʴ���������й�����Ӧ��ǰ ��[10-12]����������װĤ�����Ʊ��������Ըߵ��ص����Ϊ����װ��ϵ�е��о��ȵ㣬����ȡ�ýϴ��չ[13-15]�����������ͨ����ǿ�Ļ�ѧ����ͭ�����ϣ��������ܵ�Ĥ���Ӷ���Ч������Ĥ����ͭ�ĸ�ʴ����������ͨ�������迹���������ߺ�ѭ���������ȵ绯ѧ�����о���BDT��Ũ�Ⱥ���װʱ��Ժ������Ӻ͵�pHֵ����������Һ��BDT����װĤ��ͭ�Ļ�ʴ���á�
1 ʵ��
1.1 ʵ�����
BDT����Sigma��˾���Ȼ���(NaCl)�������챱�ջ�ѧ�Լ���������ˮ�Ҵ��ܽ����2 mmol/L�� BDT��Һ����ȥ����ˮ����3%��NaCl��Һ�������Լ���Ϊ��������
1.2 ����װĤ���Ʊ�
�Ƚ�ͭ�缫��0.3�� 0.05 mm Al2O3��ĩ��ĥ���⣬֮�������ó���ˮ���Ҵ�������ϴ�ɾ���Ȼ����������BDT��Һ�н�����װ����װ֮�缫���� 1 h��������3%��NaCl��Һ�У�����λ�ȶ�����е绯ѧ���ܲ��ԡ�
1.3 ���Է���
���е绯ѧ���Ժ����ݷ�������AUTOLAB (PGSTAT302)�绯ѧ����վ(����)��ɡ��������缫��ϵ��ѡ��d=2 mm��ͭ�缫(����99.99%�����Ƽ���չ����˾)Ϊ�����缫���αȵ缫ΪAg/AgCl����˿�缫Ϊ�����缫���绯ѧ�迹�ײ���Ƶ�ʷ�ΧΪ20 Hz~60 kHz��ѭ����������ɨ���ٶ�Ϊ20 mV/s��ѡ��-0.5 V��Ϊ��ʼɨ���λ���Ӹ�����ɨ������ߵ�λ0.6 V��Ȼ����ɨ�����������ֵ-0.6 V��������ɨ�践�س�ʼ��λ���������ߵ�ɨ���ٶ�Ϊ1 mV/s��ɨ��ĵ�λ��ΧΪ-0.4~0.1 V��ʵ���������½��С�
2 ���������
2.1 �����迹����
ͼ1��ʾΪ��ͭ(Cu)�缫��3%NaCl��Һ�е��迹�ס���ͼ1��֪����Nyquist���ߵĸ�Ƶ������һ��Rt��С�İ�Բ�������հ缫�ϵ绯ѧ��Ӧ���ٶȺܿ죻��Ƶ������Warburg�迹��������ʴ�����д�������ɢ���ʹ��̡�

ͼ1 pH=7ʱ��ͭ�缫��3%NaCl��Һ�е��迹����
Fig.1 Impedance curve of bare Cu electrode in 3%NaCl at pH value of 7
ͼ2��ʾΪ����װBDTĤ��ͭ�缫(BDT/Cu)��3%��NaCl��Һ�е��迹���ߡ���ͼ2��֪������װ���ͭ�缫�迹��1 M?����δ����Warburg�迹����հ缫��ȣ��迹�������ӣ�����ͭ�����������װBDTĤ���ܣ���NaCl��Һ�Ľ�ʴ������Ч�������á�

ͼ2 pH=7ʱBDT/Cu�缫��3%NaCl��Һ�е��迹����
Fig.2 Impedance curve of BDT/Cu electrode in 3%NaCl at pH value of 7
���ڵ��ת�Ƶ���Rt���л�Ĥ��ͭ����ĸ��ǶȦ��йأ��Ⱥ����ۻ�ʴЧ�ʵĻ�ʴ�ʦǿ�����ʽ�õ���


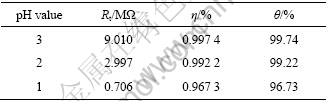
ʽ�У�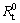 Ϊ��缫��ɴ��ݵ��裻RtΪ��������װĤ�ĵ缫��ɴ��ݵ��裻v0Ϊ������ʴ��ʱͭ�ĸ�ʴ���ʣ�vΪ���л�ʴ��ʱͭ�ĸ�ʴ���ʡ�
Ϊ��缫��ɴ��ݵ��裻RtΪ��������װĤ�ĵ缫��ɴ��ݵ��裻v0Ϊ������ʴ��ʱͭ�ĸ�ʴ���ʣ�vΪ���л�ʴ��ʱͭ�ĸ�ʴ���ʡ�
����缫����װBDTĤ��ͭ�缫���迹�����Լ���ʽ(1)��(2)����õ����迹ֵ����ʴЧ�����ڱ�1��
��1 ��ͭ�缫��BDT/Cu�缫��3%NaCl��Һ�е��迹��������������
Table 1 Fitting results of impedance curves and calculation results of bare Cu and BDT/Cu electrode

�ɱ�1��֪����װBDT���ͭ�缫����BDT�ĸ��Ƕ�Ϊ99.88%����������װBDT����Ч����ͭ�缫��3%NaCl��Һ�еĸ�ʴ���ʡ�
2.2 �绯ѧ�������߲���
ͼ3��ʾΪBDT/Cu��Cu�缫��3%NaCl��Һ�еĵ绯ѧ�������߶Աȡ�ͼ������aΪ��Cu�缫�ļ������ߣ�����bΪ��װBDT��Cu�缫�ĵ缫�����ߡ���ͼ3��֪����װBDT��Cu�缫�ĸ�ʴ���������½������������������������ƶ����ߵ�б����������

ͼ3 pH=7ʱCu�缫��BDT/Cu�缫��3%NaCl��Һ�еļ�������
Fig.3 Polarization curves of bare Cu and BDT/Cu electrode in 3% NaCl solution at pH value of 7
��ͼ3�������еĸ�ʴ����������ϣ���ʽ(3)����ɵõ�����װ�Ļ�ʴЧ�ʦ�

ͼ3�ĵ缫���������������������ڱ�2���ɱ�2�еĻ�ʴЧ�ʿ��Կ�����BDT��ͭ�����γ������ܵ�����װĤ��ʵ���һ��ӡ֤��ǰ�潻���迹�Ľ����
��2 �缫������������������
Table 2 Fitting results of polarization curves and calculation results of electrode

2.3 ѭ������������
ͼ4��ʾΪCu�缫�Լ�BDT/Cu�缫��NaCl��Һ��ѭ���������ߡ�Cu��NaCl��Һ��������ԭ�����з����ķ�Ӧ���£�

���У�������ɨ���������Ҫ����ͭ���ܽ⡢��Ϻͳ�Ĥ������Ӧ(4)~(6)����Ӧʽ��CuClaΪCu��������ϣ�CuClfΪCu�ij�Ĥ����Ӧ(7)~(9)��������ɨ������з������港ʴ������������̡�

ͼ4 pH=7ʱCu�缫��BDT/Cu�缫��3%NaCl��Һ�е�ѭ����������
Fig.4 CV curves of bare Cu and BDT/Cu electrode in 3%NaCl solution at pH value of 7
Cu�缫������ɨ�������Ϸֱ���0.03��0.267 V�õ���������������A1��B1���ڷ���ɨ����������-0.251 V�ĵ�λ���õ�һ����Ļ�ԭ������C1��������A1�뷴Ӧʽ(4)��(5)�йأ���ʾCuCl��Ĥ����γɣ�������B1�뷴Ӧʽ(6)�йأ�������Cu+�Ľ�һ��������Cu2+��������(������������)�ڵ缫����ĸ��ǣ���ԭ��C1���γ����뷴Ӧʽ(7)~(9)�йأ���Ӧ��ͭ��ʴ����Ļ�ԭ��
��ͭ�缫�ı��汻BDT����װĤ���Ǻ缫�ķ�����Ϊ�����ܴ�ı仯������װĤ���ǵ�ͭ���ĵ绯ѧ������Ӧֻ�ܷ���������װĤ�е�ȱ�ݲ�λ����Cu�缫��ȣ�����-��ԭ��������Ӧ�ĵ��������½���
2.4 ��װʱ��Խ����迹��Ӱ��
�̶�BDT��Ũ��Ϊ1.0��10-2 mol/L��������BDT��Cu�缫���治ͬ��װʱ���3%NaCl��ʴ�����н����迹��Ӱ�죬������ͼ5��ʾ��

ͼ5 pH=7ʱ��Cu�缫���治ͬ����װʱ���3%NaCl��ʴ�����н����迹ֵ��Ӱ��
Fig.5 Effect of self-assembled time on impedance in 3%NaCl solution at pH=7 on surface of Cu electrode
��ͼ5��֪�����������װʱ����Rt�����ܿ죬40 h��ﵽһ���㶨ֵ�������BDT��Cu���������װ������һ�������Ĺ��̣�����40 h����װ���γ����ȶ����ܵ�����װĤ����ˣ�ʵ��ѡȡ��װʱ��Ϊ40 h��
2.5 ���Խ��ʶԻ�ʴЧ�ʵ�Ӱ��
ʵ���BDT����װͭ�缫��pHֵ�ϵ͵�3%NaCl��Һ�еĸ�ʴ��Ϊ�������о���ͼ6��ʾΪBDT����װͭ�缫�ڲ�ͬpHֵ��NaCl��Һ�е�Nyquist���ߡ���ͼ6��֪���Ա�ͼ1������Һ��pHֵ����ʱ������a��b��c�ϵİ�Բֱ����С��˵��Rt��С����ʴЧ����������û��Warburg�迹������Rt����ͭ�缫�ߣ���˵��û����ɢ���ʹ��̷�����Ĥ���������õĿ���ʴ������
ͼ6 ��ͬpHֵʱBDT/Cu�缫��3%NaCl��Һ�е��迹����
Fig.6 Impedance curves of BDT/Cu electrode in 3%NaCl solution at different pH values
ͼ6�м������ߵķ���������ڱ�3���ɱ�3��֪��ͭ����װBDT��������NaCl��Һ�У���ʴЧ�ʺ��Ƕ��������½���������96%���ϣ���������װBDT��ͭ�缫������NaCl��Һ�п��绯ѧ��ʴ�ԽϺá�
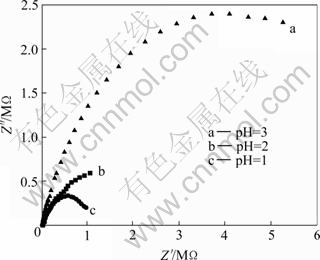
��3 ��ͬpHֵʱBDT/Cu�缫��3%NaCl��Һ���迹���ߵ�����������
Table 3 Fitting results of impedance curves and calculation results of BDT/Cu electrode in 3%NaCl solution at different pH values
3 ����
1) ���÷�������װ����������Cu��������װ 1, 3�����ϻ�������װ������Ĥ��
2) BDT����װĤ����Ч������ͭ������3%NaCl��ʴ�����еĸ�ʴ��Ϊ��
3) BDT����װĤ������NaCl��Һ�У����нϺõĿ���ʴ���ܣ���pHֵ�ϵ͵������������Զ�ͭ�����õĻ�ʴ���á�
REFERENCES
[1] BASTIDAS J M, PINILLA P. Copper corrosion inhibition by triphenylmethane derivatives in sulphuric acid media[J]. Corrosion Science, 2003, 45(2): 427-49.
[2] WANG C T, CHEN S H. Protection of copper corrosion by carbazole and N-vinylcarbazole self-assembled films in NaC1 solution[J]. Journal of Applied Electrochemistry, 2003, 33(2): 179-186.
[3] QUAN Z L, CHEN S H, ZHAO S Y, LI S L. Protection of copper corrosion by modification of self-assembled films of Schiff bases with alkanethiol[J]. Corrosion Science, 2001, 43(6): 1071-1080.
[4] ��ʤ��, Ѧ����, ����, ���. ����������ʴ����ͭ���渲����Ϊ���о�[J]. ��ʴ��ѧ���������, 2006, 18(5): 313-316.
ZHANG Sheng-tao, XUE Ming-yue, WANG Yan-bo, HOU Bao-rong. Study on covering behavior of BTA inhibitor on pure copper surface[J]. Corrosion Science and Protection Technology, 2006, 18(5): 313-316.
[5] �� ��, �� ��. �ӻ���������Ƚ���п���Ͻ�Ʋ���ϡ�����еĻ�ʴ����[J]. �й���ɫ����ѧ��, 2008, 18(1): 177-186.
JU Hong, LI Yan. Corrosion inhibition of hot dipping Zn-Al alloy coated steels by heterocyclic compounds in diluted HCl solutions[J]. The Chinese Journal of Nonferrous Metals, 2008, 18(1): 177-186.
[6] ֣�찬, �Ŵ�ȫ, �� �. HCl ��Һ�а�����������ͭ�Ļ�ʴ����[J]. ��ʴ�����, 2007, 28(12): 607-609.
ZHENG Hong-ai, ZHANG Da-quan, XING Jie. Effect of amino acid compounds in inhibitor on copper in HCl solution[J]. Corrosion & Protection, 2007, 28(12): 607-609.
[7] ������, ������, �ſ���, ������. ����װ������Ĥ�Ľṹ��������װ����[J]. �ߵ�ѧУ��ѧѧ��, 2001, 22(3): 470-476.
YANG Sheng-rong, REN Si-li, ZHANG Jun-yan, ZHANG Xu-shou. Structure and self-assembly mechanism of self-assembled monolayers[J]. Chemical Research in Chinese Universities, 2001, 22(3): 470-476.
[8] SABATANI E, RUBINSTEIN I. Electrochemical impedance analysis of polyaniline films on electrodes[J]. Journal of the Electrochemical Society, 1987, 134(12): 3078-3083.
[9] BLJIEV O, HUBIN A. Inhibition of copper corosion in chloride solutions by amino-mercapto-thiadiazol and methyl-mercapto- thiadiazol: an impedance spectroscopy and a quantum-chemical investigation[J]. Electrochimca Acta, 2004, 49(17/18): 2761-2770.
[10] �� ��, �ֲ���, �� ��, ������. ��ͭ����NaCl��Һ�и�ʴ�绯ѧ��Ϊ[J]. ������ѧѧ��, 2007, 23(9): 1342-1346.
ZHAO Yan, LIN Chang-jian, LI Yan, WANG Jing-run. Electrochemical corrosion behavior of copper clad laminate in NaCl solution[J]. Acta Physico-Chimica Sinica, 2007, 23(9): 1342-1346.
[11] OGUZIE E E, OKOLUE B N, EBENSO E E, ONUOHA G N, ONUCHUKWU A I. Valuation of the inhibitory effect of methylene blue dye on the corrosion of aluminium in hydrochloric acid[J]. Materials Chemistry and Physics, 2004, 87(2): 394-401.
[12] MA Hou-yi, ZHAO Shi-yong, CHEN Shen-hao, LIU Xiang-qian. A study of corrosion behavior of copper in the acidic solutions containing cetyltrimethylammonium bromide[J]. Journal of the Electrochimca Society, 2001, 148(5): 482-488.
[13] ������, ��ݶ��. ͭ�ĸ�ʴ�������о���չ[J]. �人����ѧԺѧ��, 2005, 27(2): 17-21.
LUO Zheng-gui, WEN Di-jiang. Research development of corrosion and protection for copper[J]. Journal of Wuhan Institute of Chemical Technology, 2005, 27(2): 17-21.
[14] ���ľ�, ���ٹ�, �ֲ���. EDA��ͭ��ϡ�����еĻ�ʴЧ���������ӵ�Ӱ��[J]. �绯ѧ, 2006, 12(1): 50-54.
QU Wen-juan, DU Rong-gui, LIN Chang-jian. Effects of sulfide ions on the inhibiting efficiency of EDA as a copper corrosion inhibitor in dilute HCI solution[J]. Electrochemistry, 2006, 12(1): 50-54.
[15] OTMACIC H, TELEGDI J. Protective properties of an inhibitor layer formed on copper in neutral chloride solution[J]. Journal of Applied Electrochemistry, 2004, 34(5): 545-550.
������Ŀ����������Ȼ��ѧ����������Ŀ(CSTC-2004BA4024)
�ո����ڣ�2009-03-10�������ڣ�2009-05-18
ͨ�����ߣ������£������ڣ���ʿ���绰��023-65023753��E-mail: hwz4889@163.com
(�༭ ����)