���-2, 6-�������������P��Tb(��)��Eu(��)������
�ϳ���ӫ������
�� ��1���� ǿ1��κ����2��������1
(1. ���ϴ�ѧ ��ѧ����ѧԺ������ ��ɳ��410083��
2. ��������ҵ��ѧ(����)����ѧԺ��ɽ�� ������264209)
ժ Ҫ�������-2, 6-������Ϊԭ�ϣ��ϳɺ��ж��������ϵ�������N2��N6-��(3-�����)-2-ȡ�����-2, 6-����������ͬʱ�Ʊ�����ϡ������Tb(��)��Eu(��)��������������������ͨ��������ס�Ԫ�ط�����X���ߵ���������ȷ������������Լ�����ṹ���о������Ĺ������Һ��ӫ�����ܡ������������Tb(��)�������ϡ��Һ�У�����ҺpHֵΪ6~7ʱӫ��ǿ�����pHֵ����7��С��6ʱӫ��ǿ�����ͣ���ˮ��Һ�У�����ҺpHֵΪ7ʱ��N2��N6-��(3-�����)-2-ȡ�����-2, 6-����������Tb(��)��ӫ��ǿ��Զǿ�����-2, 6-�������Tb(��)��ӫ��ǿ�ȣ���pHֵΪ3~11ʱ��N2��N6-��(3-�����)-2-ȡ�����-2, 6-�������������-2, 6-�������Eu(��)�γ�ϡ���������Һ��ӫ��ǿ����pHֵ���������ǿ��
�ؼ��ʣ����-2, 6-�����ϡ������ӫ��
��ͼ����ţ�O626; O614.33 ���ױ�ʶ�룺A ���±�ţ�1672-7207(2007)04-0696-05
Synthesis of Eu(��) and Tb(��) complexes with novel pyridine dicarboxylic acid derivatives and their fluorescence properties
YANG Qing1, ZHAO Qiang1, WEI Qi-feng2, TANG Rui-ren1
(1. School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China;
2. College of the Ocean, Harbin Institute of Technology (Weihai), Weihai 264209, China)
Abstract: Using pyridine-2, 6-dicarboxylic acid as starting material, a novel ligand N2,N6-bis(3-methyl- pyridine-2-yl)-pyridine-2, 6-dicarboxamide (BPDA) was synthesized��which contained multidentate and large conjugative system. Complexes of Tb (��) and Eu (��) with the ligand were prepared respectively and their single-crystals were also grown. The structures of the crystals were determined by infrared, elemental analysis and X-ray diffraction. The fluorescence properties of complexes of Tb (��) and Eu (��) with the ligand were investigated. The results show that the dilute solution of Tb(��) has the strongest fluorescence intensity when pH is 6-7 and the fluorescence intensity drops down when pH is more than 7 or less than 6. The fluorescence intensity of complex of Tb(��) with BPDA is much stronger than that of pyridine-2, 6-dicarboxylic acid(DPA) when pH is 7. The fluorescence intensities of dilute complexes solutions of Eu (��) with BPDA and DPA become stronger in the range of pH=3-11 accordingly.
Key words: pyridine-2, 6-dicarboxylic acid; lanthanide complex; fluorescence
���-2, 6-������(DPA)����������ϸ��������[1]����������Է��ӡ����-2, 6-��������Ϊ��������ϡ������(Tb(��)��Eu(��))�Ƚ���γ�������ӫ������ǿ������������ˮ���ᡢ�ڷƆ�������ͦ�-��ͪ������ӫ������[2]��������ϵ����श������������Tb(��)��Eu(��)��������ȶ��Ժ�, ���ЦҸ��������������ܵ����������㷺���ڽ�����������ϵ��װ�����ִ���λ��ѧ��Ӧ����Ϊ�㷺���������塣�й�������ѹ㷺Ӧ���ڷ��Ӵ���̫����ת������ɫ����������ʶ������װ��������ҩ�DNA̽�롢ӫ�����߷���������[3]����������һ���ṹ��ӱ�����-2, 6-�����ᱻ��ƺϳɲ��������������磺J. B. Lamture��[4]��DPA����ऻ�4λ��������ֹ����ţ�P. I. Carlos��[5]��DPA��4λ�������������Ȳ����ȡ������R. Shelkov��[6]�������ʵ�[2, 7]����ऻ�4λ�������ɻ���Ӧ�������Ǽ����ɴ�������ϵ�л�������о�����Щ��������Ϊ�����Tb(��)��Eu(��)ӫ���������ܵ�Ӱ�졣
�������Ƕ��ĺ͵����ʵĽṹ��Ԫ���о�������������Ե����ʻ��Բ�λ�ı������Ҫ���壬������������ɽ���Ԫ�ص�������о��϶࣬�����ǵ�ϡ���������о�ȴ���б���[8-10]���ڴˣ��������������-2, 6-������Ļ�����ͨ��������Ӧ����һ�ֶ������N2��N6-��(3-�����)-2-ȡ�����-2, 6-��������(N2, N6-bis(3-methyl-pyridine-2-yl)-pyridine-2, 6- dicarboxamide��BPDA)��������BPDA��ϡ������Tb(��)��Eu(��)�ĵ�������̽��BPDA��Tb(��)��Eu(��)�Ĺ�������������ϡ��Һ������ܼ��ȶ�ӫ�����ܵ�Ӱ�졣
1 ʵ ��
1.1 �������Լ�
�����У�XR-4�����۵���(�¶ȼ�δУ��)��Vario-ET-����Ԫ�ط�����(�¹�ELEMENTEAR��˾����)��Vario-ET-���ͺ˴Ź�����(400 MHz������Vanian��˾����)��PSH-3C��ȼ�(�Ϻ����������DZ�����˾����)������F-4500��ӫ����(�ձ�)��Avatar 360-FT-IR���������(����Nicolet��˾����)��SMART ATEX CCD X���ߵ���������(�¹���³�˹�˾����)��
�Լ��У����-2, 6-�����ᣬΪ�㽭���ݻ����������Ĺ�ҵƷ�������Լ�����Ϊ���ۻ�ѧ����������Լ���
1.2 BPDA�ĺϳ�·��
BPDA�ĺϳ�·����ͼ1��ʾ��
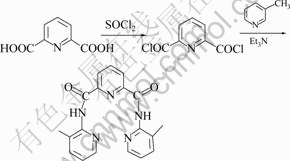
ͼ1 BPDA�ĺϳ�·��
Fig.1 Synthesis route of BPDA
1.3 ���-2, 6-�������ȵĺϳ�
�ڵ��������½�2.5 g(15 mmol)���-2, 6-��������뵽25 mL��������������У����Ȼ���6 h������Ӧ��������䣬��ѹ�����ȥ�����Ķ�����������ո���ò������-2, 6-��������3.05 g�����ﲻ��Ҫ�ᴿֱ����������ķ�Ӧ[11]��
1.4 N2��N6-��(3-�����)-2-ȡ�����-2, 6-��������(BPDA)�ĺϳ�
��6.5 g(60 mmol)��2-����-3-��-�������200 mL��ˮ�����ֱ�4.4 g(30 mmol)���-2, 6-�������ȱ���Һ��8.4 mL(Լ60 mmol)���Ұ��ڵ��������·ֱ�������2-����-3-��-��व���Һ�μӣ��μ���ɺ�Ӧ����ﱣ���ڻ�������״̬�·�Ӧ6 h������ɫ�㷨��ʾ��Ӧ��ȫ����ȴ�����ˣ�����������ϴ���˱����ռ���Һ����5%HClϴ�ӣ���ˮ�����Ƹ���������������ù��壬�����������ؽᾧ�����õ���ɫ��״����BPDA 9.21 g������Ϊ73.0%���۵�Ϊ122~124 �档1H NMR (300 MHz, CDCl3)����ѧλ�Ʀ�10.5 (s, 2H, NH), 7.2~8.5 (m, 9H, ��ऻ�), 2.4(s, 6H, CH3)��13C NMR(400 MHz, CDCl3)����161.8, 149.2, 146.1, 140.6, 139.6, 129.6, 126.0, 122.4, 18.8��IR (KBr)��3 452, 3 224, 1 740, 1 677, 1 528, 1 347, 743 cm-1��
2 Eu(��)��Tb(��)�����ĺϳ�
2.1 Tb(��)��Eu(��)�Ĺ����������Ʊ��͵������Ʊ�
�ֱ�1.4 mmol DPA��0.7 mmol BPDA�ܽ���25 mL��������ˮ�У����������Ҵ����ܣ�Ȼ��������1.00 mL 0.461 mol/L Tb3+��Һ����0.01 mol/L NaOH��Һ������2����Һ����ȵ���pHΪ6~7����50 ��ˮԡ�г�ֽ���5 h��Ȼ������Һ���·���30 d���д������峤�����ռ����壬�õ�Tb(��)������ﵥ����Eu(��)������ﵥ����������Tb(��)������ﵥ��������������ͬ��
2.2 Tb(��)��Eu(��)���������Һ���Ʊ�
����ȷ��Ũ�ȵ�Tb(��)��Eu(��)��Һϡ����1.0��10-3 mol/L����ȷ��ȡDPA��BPDA������������ˮ�ܽⲢϡ����1.0��10-3 mol��L-1����1.0��10-3 mol/L��DPA��Tb(��)��Eu(��)�������3?1��ϲ�ϡ����1.0��10-5 mol/L����1.0��10-3 mol/L��BPDA��Tb(��)��Eu (��)�������2?1��ϲ�ϡ����1.0��10-5 mol/L��
3 ���������
3.1 Tb(��)��Eu(��)������Ԫ�������������
Tb(��)��������Ԫ�ط������(����������%����������ֵΪ����ֵ)Ϊ��C��36.33 (36.69)��H��3.78 (3.72)��N��11.20 (11.26)��Tb��12.53(12.79)���������������ΪNa3Tb (BPDA)2Cl6��6H2O��
Eu(��)��������Ԫ�ط������(����������%����������ֵΪ����ֵ)Ϊ��C��36.52 (36.89)��H��3.77 (3.70)��N��11.14 (11.32)��Eu��12.11(12.37)���������������ΪNa3Eu(BPDA)2Cl6��6H2O��
����BPDA���������ĺ�����ף�BPDA�İ�����ԭ�ӵ����ճ�����3 224 cm-1�����以���칹����ǻ�������3 452 cm-1����BPDA��Tb (��)��Eu (��)�γ���������2���嶼��Ͳ����ƶ�Լ70 cm-1��˵��BPDA�İ���������λ��Na3Tb(BPDA)2Cl6��6H2O��Na3Eu(BPDA)2Cl6��6H2O��1 624 cm-1�����ֵ��ʻ����գ���BPDA��Ͳ����ƶ�Լ117 cm-1, ����ǿ�����������շ�����˵���ʻ���ԭ�Ӳ�����λ���ʻ��е���ԭ����ϡ�����ӵ���λ����ʹ�ʻ�˫���ļ��������������ʻ��������ܶȸ���ƫ����ļ������Ķ�������ԭ�ӣ�������ʻ����վ���Ͳ����ƶ�����2 010~2 060 cm-1���������շ壬˵������ﺬˮ���ӡ���������ऻ��ĹǼ���������BPDA�����Ͳ����ƶ�Լ100 cm-1������˵����ऻ��ĵ�ԭ�Ӳ�������λ����439��415 cm-1�������µ����շ壬Ϊ���γɵ���λ�������շ塣
3.2 Tb(��)��Eu(��)�����ṹ����
�������ĵ�������X���ߵ��������Dzⶨ�����ΪNa3Tb(BPDA)2Cl6��6H2O��Na3Eu(BPDA)2Cl6��6H2O��ͼ2��ʾΪNa3Tb(BPDA)2Cl6��6H2O��Na3Eu(BPDA)2- Cl6��6H2O�ľ��ͷ��������

(a) Na3Tb(BPDA)2Cl6��6H2O; (b) Na3Eu(BPDA)2Cl6��6H2O
ͼ2 Na3Tb(BPDA)2Cl6��6H2O��Na3Eu(BPDA)2Cl6��6H2O���幹��
Fig.2 Crystal structures of Na3Tb(BPDA)2Cl6��6H2O and Na3Eu(BPDA)2Cl6��6H2O
3.3 Tb(��)��Eu (��)������ӫ������
ϡ�������Ĺ��·������������塢�������ӵ��ܼ�������ء�����ļ�������̬��ϡ�����ӵ�һ����̬���ܼ�����һ��ƥ��ԭ������ʵ�����ݱ���������ļ�������̬�ܼ���Tb(��)��5D4���ܼ���С��1 500 cm-1ʱ��������Tb(��)�ķ��⣬��Eu(��)��5D0�ܼ������4 000 cm-1��Ҳ��������Eu(��)�ķ���[12]��
3.3.1 ����Tb(��)��Eu(��)������ӫ������
�ڼ�������Ϊ2.5 nm, ��������Ϊ2.5 nm����籶���ܵ�ѹ400 V�������£��ⶨTb(��)��Eu(��)������DPA��BPDA�γɵ������Ĺ���ӫ����ף��������1�ͱ�2��
��1 Tb(��)�Ĺ���������ӫ��ǿ��
Table 1 Fluorescence intensity of solid Tb(��) complexes

��2 Eu(��)�Ĺ���������ӫ��ǿ��
Table 2 Fluorescence intensity of solid Eu(��) complexes

��1�ͱ�2��ʾΪ4�ֹ�������������ӫ��ǿ�ȺͶ�Ӧ�ļ����Ⲩ�����������ռ������������ɻ�̬S0���������ؼ���̬S1��ͨ����ϵ���Ծ������̬T�����彫�������ݸ�ϡ�����ӡ�Tb(��)��DPA����������ܼ��������ǿ����ɫӫ�⣬���䲨��Ϊ491��543��582 nm���ֱ��ӦTb(��)��5D4��7F6��5D4��7F5��5D4��7F4�����ܼ�ԾǨ��Eu(��)����������ܼ��������ɫӫ�⣬���䲨��Ϊ595��618 nm���ֱ��ӦEu(��)��D0��7F1��5D0��7F2�ĵ����ܼ�ԾǨ��
�Աȱ�1�ͱ�2��֪������ͬ�ļ������������£��ڹ����������BPDA��Tb(��)��Eu (��)��ӫ��ǿ������DPA�����ǵ�ӫ��ǿ�ȡ�
3.3.2 ˮ��ҺpHֵ��Tb(��)��Eu (��)�����ӫ��ǿ�ȵ�Ӱ��
ȡ1.0��10-5 mol/L��ϡ���������Һ����ϡNaOH��ϡHCl��Һ����ϡ���������Һ��pHֵ���ֱ�ȡpHֵΪ3~11��4��ϡ�������ˮ��Һ�����������Һ��ӫ��ǿ�ȣ������ͼ3��ͼ4��ʾ��

1��Na3Tb(DPA)3; 2��Na3Tb(BPDA)2Cl6
ͼ3 ˮ��ҺpHֵ��Tb(��)�����ӫ��ǿ�ȵ�Ӱ��
Fig.3 Effect of pH on fluorescence intensity of complexes of Tb(��) solution
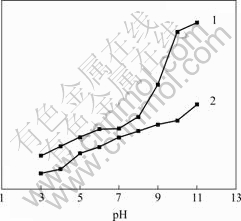
1��Na3Eu(DPA)3; 2��Na3Eu(BPDA)2Cl6
ͼ4 ˮ��ҺpHֵ��Eu(��)�����ӫ��ǿ�ȵ�Ӱ��
Fig.4 Effect of pH on fluorescence intensity of complexes of Eu(��)solution
ͼ3��ʾ��ӫ��ⶨ������ڼ�������Ϊ2.5 nm����������Ϊ2.5 nm����ex��273 nm����籶���ܵ�ѹΪ400 Vʱ��õġ���ϡ��Һ�������£�Na3Tb- (DPA)3��Na3Tb(BPDA)2Cl6��ӫ��ǿ������Һ��pHֵ�йأ���pHֵΪ6~7ʱ����2��������ӫ��ǿ�Ⱦ��ﵽ���ֵ����pHֵΪ7ʱ��Na3Tb(BPDA)2Cl6��ӫ��ǿ��Զ����Na3Tb(DPA)3��ӫ��ǿ�ȣ���������ϡ��Һ������BPDA��ϩ��ʽ�ṹ�����ϸߣ�Na3Tb(BPDA)2Cl6���Ӽ���С������BPDA��������һ��ƽ����ӣ�������ϡ������������õ���ǿ������pHֵ����(pH��7)����ȻBPDAϩ��ʽ�ṹ�����ȶ������������ߣ���BPDA��������е�λ�ñ�����������ȡ����ʹӫ��ǿ�Ƚ��͡�����pHֵ���� (pH��7)��BPDA��ϩ��ʽ�ṹ�������٣�Ҳ������������������⡣
ͼ4�е�ӫ��ⶨ������ͼ3�е���ͬ����pHֵΪ3~11ʱ��Na3Eu(DPA)3��Na3Eu(BPDA)2Cl6ϡ��Һ��ӫ��ǿ������Һ��pHֵ���������ǿ��������ҺpHֵ����(pH��3)��BPDAϩ��ʽ�ṹʽ�������ߣ�������������������pHֵ����7��Ҳ����ȡ��BPDA��������е�λ�ã���BPDA��ϡ�����ӵ�ӫ��ǿ����pHֵ�������ǿ��
3.3.3 �ܼ���ϡ�������ӫ��ǿ�ȵ�Ӱ��
�ֱ���ˮ���״����Ҵ��ܼ��ܽ���4���������1.0��10-5 mol/L��Һ���ڼ�������Ϊ5.0 nm����������Ϊ5.0 nm����籶���ܵ�ѹ400 V����Tb(��)�������ӫ��ǿ�Ȧ�em��546 nm���ⶨ�����ǿ�ȣ���Eu(��)�������ӫ��ǿ�Ȧ�em��618 nm���ⶨ�����ǿ�ȡ�����õĽ�����3��ʾ������ˮ��ż����Ϊ1.85��10-18 C?m���״���ż����Ϊ1.70��10-18 C?m���Ҵ���ż����Ϊ1.69��10-18 C?m��
��3 �ܼ�ЧӦ��ӫ��ǿ�ȵ�Ӱ��
Table 3 Solvent effect on fluorescence intensity
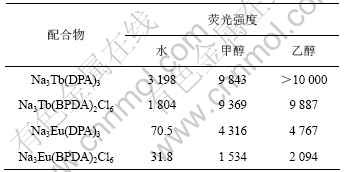
�ɱ�3�ɼ���ͬһ��ϡ��������ڲ�ͬ�ܼ���ӫ��ǿ�������ܼ�����ż�����С����������2��ż�����ˮС���ܼ��ϡ��������ӫ��ǿ�ȷ�������ˮ���ӫ��ǿ�ȴ�öࡣE. G. Mcrae��Ϊ[13]���ڷ�����ϵ����һ��Franck-Condon����̬��ż����С���ܼ����ӿ���ʹ��Franck-Condon����̬��Ӧ�Ļ�̬�ȶ�����������������̬T2(�С��Щ~)��T1(�С��Щ~)���ܼ������������S(n���Щ~)��T2(�С��Щ~)�Ľ���ԾǨ��Ϊ���ܣ����嵥��̬������̬ԾǨ�ļ������ӡ�
4 �� ��
a. �ڹ��������״̬�£�N2��N6-��(3-�����)-2-ȡ�����-2, 6-��������(BPDA)��Tb(��)��Eu(��)��ӫ��ǿ���������-2, 6-������(DPA)��Tb(��)��Eu(��)������ӫ��ǿ�ȡ�
b. ����ҺpHֵΪ7�������ϡ��Һ��N2��N6-��(3-�����)-2-ȡ�����-2, 6-���������Ķ�Tb(��)��ӫ��ǿ��Զǿ�����-2, 6-�������Tb(��)��ӫ��ǿ�ȡ�
c. ��pHֵΪ3~11ʱ��N2��N6-��(3-�����)-2-ȡ�����-2, 6-�������������-2, 6-��������Eu(��)�γ�ϡ���������Һ��ӫ��ǿ����pHֵ���������ǿ��
�ο����ף�
[1] Platas-Iglesias C, Piguet C, Andre N, et al. Lanthanide triple-stranded helical complexes with a substituted 2, 6-pyridinedicaeboxyate[J]. J Chem Soc Dalton Trans, 2001(18): 2655-2662.
[2] ������, ���Ӷ�, ���ӳ�, ��. ���-2, 6-�����������P��Tb(��)��Eu(��)�����ĺϳ�ӫ������[J]. �ߵ�ѧУ��ѧѧ��, 2006, 27(3): 472 -477.
TANG Rui-ren, YAN Zi-er, GUO Can-cheng, et al. Synthesis of Eu(��) and Tb(��) complexes with novel pyridine dicarboxylic acid derivatives and their fluorescence properties[J]. Chem J Chin Univ, 2006, 27(3): 472-477.
[3] ���Ժ�, ̷��ԣ. ���-2, 6-������������ϡ��������ӫ������[J]. �й�ϡ��ѧ��, 2001, 19(6): 555-560.
YIN Xian-hong, TAN Min-yu. Studies on luminescence properties of Tb complexes of pyridine-2, 6-dicarboxylic acid derivatives[J]. Journal of the Chinese Rare Earth Society, 2001, 19(6): 555-560.
[4] Lamture J B, ZHOU Z H, Kumar A S, et al. Luminescence properties of terbium(��) complexes with 4-substituted dipicolinic acid[J]. Inorg Chem, 1995, 34(4): 864-869.
[5] Carlos P I, Piguet C, Andr��a N, et al. Lanthanide triple stranded helical complexes with a substituted 2, 6-pyridine- dicarboxylate[J]. J Chem Soc Dalton Trans, 2001(20): 3084-3091.
[6] Shelkov R, Melman A. Free-radical approach to 4-substituted dipicolinates[J]. Eur J Org Chem, 2005, 21(7): 1397-1401.
[7] TANG Rui-ren, ZHAO Qiang, YAN Zi-er, et al. Synthesis of novel derivatives of pyridine-2, 6-dicarboxylic acid[J]. Synth Commun, 2006, 36(14): 2027-2034.
[8] Jain S L, Bhattacharyya P, Milton H L, et al. New pyridine carboxamide ligands and their complexation to copper(��). X-Ray crystal structures of mono-, di-, tri- and tetranuclear copper complexes[J]. Dalton Trans, 2004, (6): 862-871.
[9] JolantaS K, ElzbietaG K,Dobosz A, et al. Pyridine-2, 6-dihydroxamic acid, a powerful dihydroxamate ligand for Ni2+ and Cu2+ ions[J]. J Chem Soc Dalton Trans, 2002(24): 4639-4643.
[10] Alpha B, Lehn J M, Mathis G. Luminescence:quantitative photophysics energy Eu(��) and Tb(��) cryptates macrobicyclic polypyridine[J]. Angew Chem, 1987, 99(12): 1310-1318.
[11] Iwasa S, Nakamura H, Nishiyama A. Synthesis of 2, 6-bis(4R-hydroxymethyloxazolyl)-pyridine as water soluble ligand[J]. Heterocycles, 2000, 52(2): 939-944.
[12] Zucchi G, Ferrand A, Scopelliti R. Highly luminescent, visible-emitting lanthanide macrocyclic chelates stable in water and derived from the cyclen framework[J]. Inorg Chem, 2002, 41(9): 2459-2466.
[13] McRae E G. Theory of solvent effects on molecular electronic spectra: frequency shifts[J]. J Phys Chem, 1957, 61(5): 562-572.
�ո����ڣ�2006-12-30
������Ŀ������ʡ�Ƽ��ƻ���Ŀ(05JT1022)
����飺�� ��(1971-), Ů, �����۶���, ˶ʿ, ���µ绯ѧ�о�����������
ͨѶ���ߣ�������, ��, ���ڣ��绰��0731-8836961��E-mail: trr@mail.csu.edu.cn