DOI��10.19476/j.ysxb.1004.0609.2017.05.024
������ˮ��ԭ�������̿���ѧ
������1��������1�����Ȼ2��������1���� ��1
(1. �����Ƽ���ѧ ��ľ����Դ����ѧԺ������ 100083��
2. �й���ѧԺ ���̹����о��� ���������ص�ʵ���ң����� 100190)
ժҪ���Խ�����ˮΪ��ԭ�����������������������оģ���о�������ˮ��ѹֱ�ӻ�ԭ�������̿�Ķ���ѧ����������ٶȡ���Ӧ�¶ȡ����̿�����������Ũ�Ⱥͽ�����ˮCODcrŨ�ȶ��̽������ʵ�Ӱ�졣����������̽������淴Ӧ�¶ȡ�����Ũ�ȡ�������ˮCODcrŨ�ȵ����Ӻ����̿������ļ�С��������393 K~423 K�䣬������ˮ��ԭ�������̿��ܹ�Ĥ��ɢ���ƣ����ۻ��Ϊ15.2 kJ/mol������ͽ�����ˮCODcrŨ�ȵı�����Ӧ�����ֱ�Ϊ1.21��0.98�������������������̿�����������ˮ�д�����л���ֽ��С���Ӷ�����ԭ�ܳ�����С����ֱ�ӻ�ԭ�ܳ�����Ӧ�����У����̿���������Fe��Si��Al�γɿ����ڶ�Ӱ���̵��ܳ����̡�
�ؼ��ʣ�������ˮ�����̿�ԭ����������ѧ
���±�ţ�1004-0609(2017)-05-1051-10���� ��ͼ����ţ�TF111.31���� ���ױ�־�룺A
����20����60����������Զ�������Ϊ��Ҫ��ʽ���̿��������⣬�ͱ�����������[1]�������������̿�Ļ�ԭ������Ȼ�ǹ���������ȡ��һ����Ҫ��������[2]���������������Խ����У�ʪ����ԭ���̿�����Ⱦ�١����ռ���Ϊ�о��ȵ�[3]��ֱ�ӻ�ԭ���̵Ĺؼ��������ǣ�Ѱ��һ�־��á�ʵЧ�Ļ�ԭ��[4-5]������С�����л���[6]��������[7]�����۾ƾ���Һ[8]��ʪ����ԭ���̿����ر������л���ʪ����ԭ���̿�Ķ���ѧ�о�������С�������ʺ������ʣ���BEOLOCHINI��[9]�� ��[10]���ں����[11]�������ֵ�[12]�ֱ������ο�������оģ���о������ǡ����ǡ�����ɫ�ء�����ոѵȻ�ԭ�������̿�Ķ���ѧ��
��[10]���ں����[11]�������ֵ�[12]�ֱ������ο�������оģ���о������ǡ����ǡ�����ɫ�ء�����ոѵȻ�ԭ�������̿�Ķ���ѧ��
������ˮ���и�Ũ�ȵķ��ࡢ�軯��Ͱ������Լ��������オ������ࡢ��वȸ��ӻ�����������ȶ�����廯���һֱ�ǽ�����ҵ��ˮ�����Ĺ�������[13]����ͨ�����õ��ﻯ��������������[14]����������ˮ�д����Ļ�ѧ�����ã���ʵ�ַ�ˮ������ͬʱ�ֽ���ˮ��Դ�����ǽ�Լˮ��Դ�����ٻ�����Ⱦ����Ч·�����¶ȸ���100 ���ұ������Ϊһ������Ч��ǿ��������ʪ��ұ���¹��շ�չѸ��[15]��л����[16]�Ի�������Ϊ��ԭ��120 ��ӵ�Ʒλ���̿�����ȡ���̡���������ͨ��������ˮ��Ϊ��ԭ�����о����̿�ʪ�������Ĺ��������Ͷ���ѧ��Ϊʵ�ֽ�����ˮ��Ч�ܳ����̿��Լ�������ˮ��Դ�����ۺ��������ṩ�������ݣ���Ϊ����CODcr��Ⱦ��������̿��ṩ��۶���ѧ�����۲ο���
1 ʵ��
1.1 ʵ�����
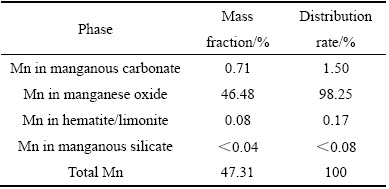
ʵ�����õ����̿�����ij��Ʒλ�����̿�����Ҫ��ѧ�ɷּ���1��XRD����ͼ1��ʾ�����̿���������2���С��ӱ�1��2��ͼ1�п��Կ��������̿���Ԫ�ػ����Ը���������ʽ���ڣ�����������ҪΪ���̿���ʯ������ʯӢΪ����
��1 ���̿����Ҫ��ѧ�ɷ�
Table 1 Chemical compositions of pyrolusite(mass fraction��%)

ͼ1 ���̿��XRD��
Fig. 1 XRD pattern of pyrolusite
��2 ���̿����̵�����
Table 2 Phase analysis of manganese in manganese ore
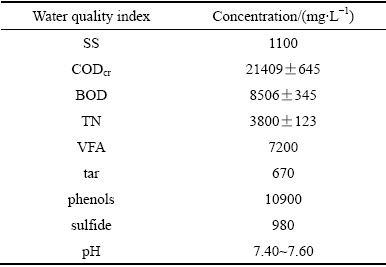
�������õĽ�����ˮȡ�Ժӱ�ij����ú������ˮ��������ˮˮ�����3���С�������ˮ��CODcr����Ϊ2.14��104 mg/L��BOD5Ũ��Ϊ8.5��103 mg/L���л����Իӷ���ͷ���Ϊ����������ʹ�õ�����ҩ����Ϊ��������
��3 ������ˮˮ��
Table 3 Quality of coking-plant wastewater (concentration, mg/L)
1.2 �����豸���������
����װ��ʾ��ͼ��ͼ2��ʾ��
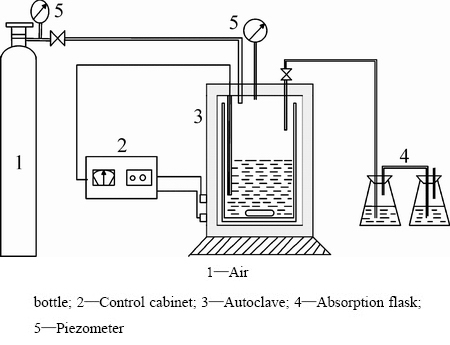
ͼ2 ����װ��ʾ��ͼ
Fig. 2 Schematic diagram of experimental apparatus
��Ҫ�������豸�������У���ĥ��(XMB-70��������Ͳ���人̽���е������)���������ͷ�Ӧ��(YZPR-500������������������˾����)�����ӷ�����ƽ(AR1140���º�˹�����Ϻ�����˾����)��X����������(D/max 2550VB+���ձ���ѧ����)�����������(ALPHA��BRUKER��˾����)��ɨ��羵(ULTRA55��CarlzeissSMTrecLMD��˾����)��
1.3 ���鷽��
��ȡ20 g���̿���뷴Ӧ���ڣ���Һ�̱�10:1�����趨Ũ�ȵĽ�����ˮ����������Һ��װ���ܷ⣬�õ����ų��������壬�ر��������������£������趨�¶�ʱ����ʼ��ʱ����Ӧ���趨ʱ�䣬��ȴ������80 �棬ͨ�����ų��������壬����ȡ����������ձó��˽��й�Һ���룬�������ϴ�Ӻ���������������������ⶨ��������Ԫ�غ�����
2 ���������
2.1 ��������ѧ����
2.1.1 �������ʶ��̽�����Ӱ��
���¶�423 K������Ũ��1.4 mol/L��������ˮCODcrŨ��20 g/L��ƽ������0.03 mm�����·�Ӧ120 min������������ʶ����̿������Ӱ�죬������ͼ3����ͼ3��֪������������100 r/min ����200 r/min���̽��������21.2%��˵������ǿ�Ȳ���ʱ��ҺĤ��ɢӰ��ϴ�[17]����ֽ�����̽������ܽ���ǿ��Ӱ���С�������ܺģ������ٶ�Ϊ200 r/min���ˡ�

ͼ3 ��ͬ�����ٶȶ��̽����ʵ�Ӱ��
Fig. 3 Effect of stirring speed on Mn leading rate
2.1.2 �¶ȶ��̽�����Ӱ��
������Ũ��Ϊ1.4 mol/L��������ˮCODcrŨ��Ϊ20 g/L��ƽ������Ϊ0.03 mm�������ٶ�Ϊ200 r/minʱ���¶ȶ��̽����ʵ�Ӱ����ͼ4��ʾ����ͼ4��֪���¶ȶ��̵Ľ���������Ӱ�졣373 Kʱ���̽�����������Ӧ240 min�����ʵ���80%��˵����ʱ���̿�ˮ��ԭ�Ļ�ѧ��Ӧ�ƶ������㣻393 Kʱ���̽���������15%���������ʱ�죬�������ڷ�ˮ�������̿�Ӧ���л������ӣ���Ӧ����ң�423 Kʱ����Ӧ180 min�����ʴ���97%��˵����ʱ���̿��������ȫ�������¶���423 K���ߵ�433 K���̽���Ч����߲����ԣ����˵��¶�����Ϊ423 K��
���ο�������оģ�͵Ĺ�Ĥ��ɢ����ģ��[18-19]��
1-2x/3-(1-x)2/3=kdt (1)
��ѧ��Ӧ����ģ�ͣ�
1-(1-x)1/3=krt (2)

ͼ4 ��ͬ�¶�ʱ�̽�������ʱ��ı仯
Fig. 4 Change of Mn leaching rate with time at different stirring temperatures
��393~423 K��Χ�ڣ���1-2x/3-(1-x)2/3��1-(1-x)1/3��ʱ��t����������ϣ�������ͼ5��ʾ����ͼ5(a)��(b)��֪�����õ�ֱ��б�ʼ�Ϊ��Ӧ���ʳ���k����lnk��1/T��ͼ���ɵý�����ˮ�������̿�İ�������˹���ߣ���ͼ6��ʾ���ɷ���(1)��(2)�ֱ����õ��������̵ı��ۻ��(Ea)Ϊ15.2 kJ/mol��12.9 kJ/mol����ѧ��Ӧ����һ���ܴ���40 kJ/mol����ɢ���Ʋ�����15 kJ/mol[20]����ˣ����¶�Ϊ393~ 423 Kʱ��������ˮ��ѹ�������̿���������ܹ�Ĥ��ɢ����[21]��
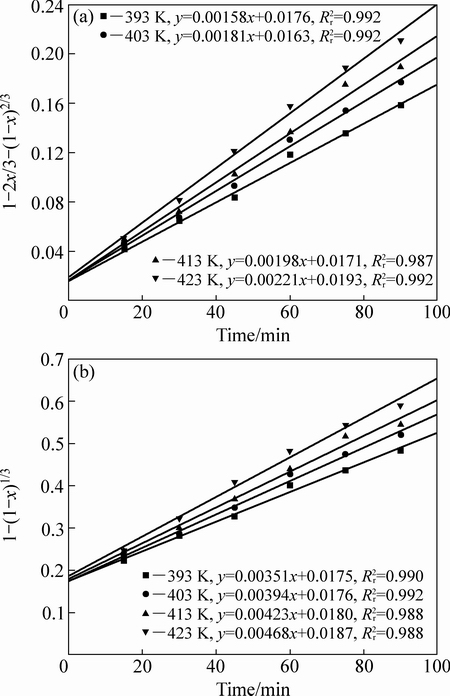
ͼ5 ��ͬ�¶���1-2x/3-(1-x)2/3��1-(1-x)1/3����
Fig. 5 1-2x/3-(1-x)2/3 (a) and 1-(1-x)1/3 (b) curves vs time at different temperatures
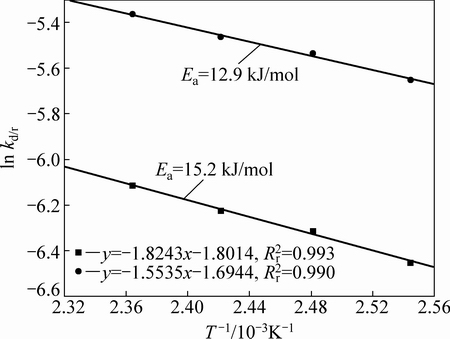
ͼ6 lnkd/r��1/T��ϵ
Fig. 6 Relationship between lnkd/r and 1/T
2.1.3 ���̿��������̽�����Ӱ��
��Ԫ���ڸ����������ȷֲ�(����4)��ƽ���������̽����ʵ�Ӱ����ͼ7��ʾ����ͼ7��֪�����̿��������ƽ�������ļ�С����������Ҫ�������л��������̿�Ӵ����������ɢ��䱡���ٽ��˷�Ӧ�Ľ���[22]��
��4 ��ͬ��������Ԫ�طֲ�
Table 4 Manganese mass content of different particle size range of pyrolusite


ͼ7 ��ͬ����ʱ�̽�������ʱ��ı仯
Fig. 7 Change of Mn leaching rate with time at different particle sizes
��ͬƽ�����������̿��������1-2x/3-(1-x)2/3��ʱ���ϵ����ͼ8����ͼ8�����������Իع飬�ó�ÿ�����߷�Ӧ���ʳ���kd����kd��r0-2��ͼ�������ͼ9����ͼ9���Կ�����kd��r0-2�����Թ�ϵ��
2.1.4 ����Ũ�ȶ��̽�����Ӱ��
�����ʼŨ��(0.8~1.6 mol/L)���̽�����Ӱ����ͼ10��ʾ����ͼ10���Կ��������̿�Ľ������������ʼŨ��Ӱ��ϴ������ʼŨ����0.8 mol/L����1.4 mol/Lʱ����Ӧ180 min���̽��������15.7%������������1.6 mol/L���̽����ٽ���С�����ǻ�����Һ����ȶ��̽����нϴ�Ӱ�죬���������һ���̶Ⱥ�����̽���Ӱ���С[23]������Ũ��1.4 mol/L���ˡ�

ͼ8 ��ͬ������1-2x/3-(1-x)2/3��ʱ��Ĺ�ϵ
Fig. 8 Relationship between 1-2x/3-(1-x)2/3 and time at different particle sizes

ͼ9 kd��r0-2��ϵ
Fig. 9 Relationship between kd and r0-2
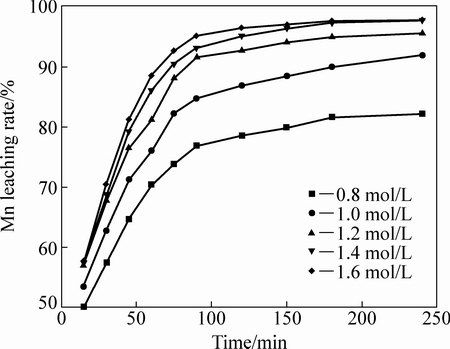
ͼ10 �����ʼŨ�ȶ��̽����ʵ�Ӱ��
Fig. 10 Effect initial H2SO4 concentrations on Mn leaching rate
��ͬ�����ʼŨ�����̽�����1-2x/3-(1-x)2/3��ʱ��t��ϵ���ߣ���ͼ11��ʾ��1-2x/3-(1-x)2/3��ʱ��t����������ء���ͼ11�����������Իع���ø����߷�Ӧ���ʳ���kd����lnkd��lncH��ͼ(��ͼ12)�������ʼŨ�ȵı�����Ӧ����Ϊ1.21��

ͼ11 ��ͬ��ʼ����Ũ����1-2x/3-(1-x)2/3��ʱ��Ĺ�ϵ����
Fig. 11 Relationship between 1-2x/3-(1-x)2/3 and time at different initial H2SO4 concentrations

ͼ12 lnkd��lncH�Ĺ�ϵ
Fig. 12 Relationship between lnkd and lncH
2.1.5 ������ˮCODcrŨ�ȶ��̽�����Ӱ��
������ˮCODcrŨ��(12~20g/L)�����̿������Ӱ���ͼ13����ͼ13��֪��������ˮCODcrŨ�ȶ��̽���Ч��Ӱ��ϴ�CODcrŨ������ѧ��Ӧ�ƶ��������̽���Ч��Խ�á�CODcrŨ��Ϊ20 g/L����Ӧ120 min���̽����ʴﵽ95.1%����Ӧʱ��ͽ�����ˮCODcr�������Ӷ��̽������ñ�С��CODcrŨ��Ϊ20 g/L������Ҫ��
��ͬ������ˮCODcrŨ�����̽�����1-2x/3-(1-x)2/3��ʱ��t�Ĺ�ϵ������ͼ14����ͼ14���Կ�����1-2x/3-(1-x)2/3��ʱ��t������������ع�ϵ����lnkd��lncw��ͼ��ͼ15��������ˮCODcrŨ�ȵı�����Ӧ����Ϊ0.98��

ͼ13 ������ˮCODcrŨ�ȶ��̽����ʵ�Ӱ��
Fig. 13 Effect of CODcr concentrations on Mn leaching rate

ͼ14 ��ͬ������ˮCODcrŨ����1-2x/3-(1-x)2/3��ʱ��Ĺ�ϵ
Fig. 14 Relationship between 1-2x/3-(1-x)2/3 and time at different concentrations of CODcr
2.1.6 ��������ѧ����
�ɷ�Ӧ���ʳ���
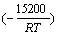 ���������Ϸ����ɵã�k0��ƽ��ֵΪ5.30��10-6����ˣ�������ˮ��ԭ�������̿�ĺ�۶���ѧģ�Ϳɱ���Ϊ
���������Ϸ����ɵã�k0��ƽ��ֵΪ5.30��10-6����ˣ�������ˮ��ԭ�������̿�ĺ�۶���ѧģ�Ϳɱ���Ϊ

 (3)
(3)
�̽����������������С�����ἰ������ˮCODcrŨ�������������ͼ16��ʾΪ��ͬ��������֤���飬ʵ��ֵ�����ֵ�Ĺ�ϵ���ߡ�
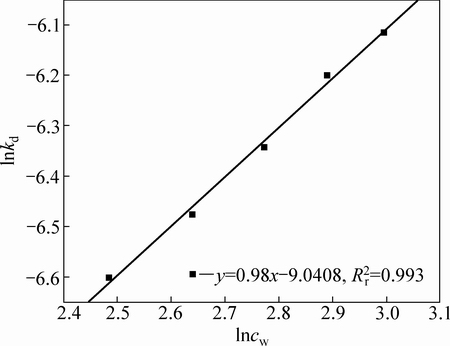
ͼ15 lnkd��lncw�Ĺ�ϵ
Fig. 15 Relationship between lnkd and lncw

ͼ16 �̽�������ֵ(xcal)������ֵ(xexp)�ıȽ�
Fig. 16 Comparison between calculated data (xcal) and experimental data (xexp)
2.2 ������������
2.2.1 ����Һ����
������ˮ��ͬ�¶Ƚ������̿�4 h������Һ��FIRT������ͼ17��ʾ����ͼ17��֪���¶���90 �����ߵ�120 ��ʱ��3196 cm-1�����ǻ����շ������vOH���Ƶ��������3405 cm-1�����ǻ��ڽ�����ˮ�У����ǻ��ĸ߾������ӷֽ��С���ӣ��������ǻ��������շ�Ķ����ƶ���֮ǰ�������У��¶���90 �����ߵ�120 �棬�̽��������36%��˵������ӵķֽ�������̵Ľ����ʡ�

ͼ17 ��ͬ�¶Ƚ���Һ�ĺ���ͼ��
Fig. 17 FIRT patterns of lixivium after leaching at different temperatures

ͼ18 ��ͬ�����·�ˮ�ͽ���Һ�ĺ���ͼ��
Fig. 18 FIRT patterns of coking wastewater and lixivium under different conditions

ͼ19 ��ͬ�����·�ˮ�ͽ���Һ��CODcrŨ��
Fig. 19 Concentrations of coking wastewater and lixivium CODcr at different conditions
������ˮ��ͬ����������FIRT������CODcrŨ�ȷֱ���ͼ18��19��ʾ����ͼ18��19��֪��δ�����̿�90 �����4 hʱ����Ҫ�ɻӷ��Է��༰�л���ֽ�������ˮ��CODcrŨ�ȵĽ��ͣ�����ӻ������ֽ⣻�����̿�Ӧ��CODcrŨ�Ƚ��ͽӽ�һ����˵����ˮ���л��ﱻ���̿����������⣻150 ��ʱ��δ�����̿��ˮ���ǻ����շ�Ϊ3114 cm-1������(90 ��)ʱ�������̿�Ӧ�ķ�ˮ��150 ��δ�����̿�Ӧ�ķ�ˮCODcrŨ�ȵ�0.7 g/L��vOH���Ƶ�����ƶ���75 cm-1�������ɷ�ˮ�д���������̿�Ӧ�ֽ����𣬶����鷶Χ�ڷ�ˮ�д�������¶����߷ֽⲻ���ԣ�150 ��ʱ�������̿�Ӧ��vOHҲ���Ƶ�����ƶ���1 h ��4 h����Һ vOH���Ƶ����ֱ�����3227 cm-1��3356 cm-1��CODcrȥ���ʷֱ����14.0%��20.0%��˵����ʱ���ӳ���ˮ�д���ӱ����̿������ֽ������࣬�̽�����Ҳ�������150 ���£���ˮ�� 2500~2700 cm-1������ϡ�OH���շ��������̿�Ӧ����ʧ��˵���Ȼ��������̿�Ӧ�⣬���DZ����ȷֽ⡣
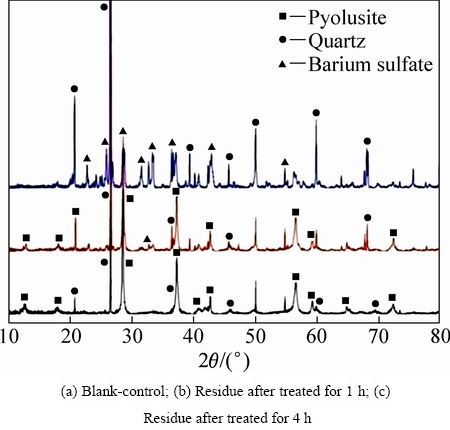
ͼ20 ��ͬ����ʱ�����XRD��
Fig. 20 XRD patterns of pyrolusite and its residue after leaching
2.2.3 ��������
��ͬʱ��Ľ�����XRD���������ͼ20����ͼ20�ɿ��������̿�����ˮ��ԭ������ʯӢ�����ᱵΪ�����ҷ�Ӧ�����У������̿���ij�����������ˣ�������ˮ��ԭ�������̿����Ϊ�ǣ����̿�����������л���ֽ��С���ӣ�������ԭ�ܳ�����С�����л���ֱ�ӻ�ԭ�ܳ�����Ӧ���̿ɸ���Ϊ[24-25]��
 (4)
(4)
 (5)
(5)
MnO+H2SO4��MnSO4+H2O (6)
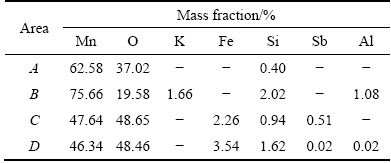
������SEM������ͼ21��ʾ��������EDS����ѧ��������5��ʾ��150 ��δ���뽹����ˮ��ѹ����1 h�Ľ����У����̿�ʿ�״������⻬ƽ������Ƿ�������ͼ21(a)�����뽹����ˮ��Ӧ1 h����ͼ21(b)�����汻��ʴ���������ܸ��ǡ��ɱ�5��֪��������ˮ�����̿�Ӧ1 h�����̿���汻Fe��Sb��Si�Ȳ����︲��[25]���ɴ˿�����Ϊ��������ˮ��ԭ�������̿�����У���ʯ�����뻹ԭ��������Ӧ������Mn��Fe��Al��Si�Ȳ����︲���ڿ������棬�γɿ����ڣ���ԭ����������Mn��Ӧ��ͬʱ����ͨ�����Dz���ɢ���ں˱��棬��Mn�ȼ�����Ӧ��

ͼ21 ������ˮ��ԭ���̿�SEM��
Fig. 21 SEM images of pyrolusite after coking wastewater reducing leaching
��5 ����������ѧ���
Table 5 Chemical composition of leaching residue tested by EDS
3 ����
1) �Խ�����ˮΪ���̿������ԭ����ʵ���˷�ˮ�ľ�������Դ����Ϊ��ˮ�����ṩ�·������ǽ��ˮ��Դ��ȱ�뻷����Ⱦ�������Ч·����
2) ���̿����¶�Ϊ423 K����ʼ����Ũ��Ϊ1.4 mol/L��ƽ������Ϊ0.03 mm��������ˮCODcrŨ��Ϊ20 g/L�������ٶ�Ϊ200 r/min����Ӧ180 min���̽����ʿɴ�97%���ϡ�
3) ��393~423 K�䣬������ˮ��ԭ�������̿�ĺ�۶���ѧ����Ϊ


�����Ϲ�ʽ�ɼ����̽��������¶ȡ�����Ũ�ȡ�������ˮCODcrŨ�ȵ���������ļ��ٶ�����
4) ���̿�����������ˮ�д���ӷֽ��С���Ӷ�����ԭ�ܳ�����С����ֱ�ӻ�ԭ�ܳ�����ʯ���������Fe��Si��Al���γɿ����ڣ�Ӱ���̽������̡�
REFERENCES
[1]  ������. ���������ͻ�����������ת��Ϊ�����η�[J]. ��ѧ����, 1955(1): 25-31.
������. ���������ͻ�����������ת��Ϊ�����η�[J]. ��ѧ����, 1955(1): 25-31.
 ZHOU Liu-gen. The extraction of Mn from pyrolusite by using ferric sulfate and pyrite[J]. Chemistry World, 1955(1): 25-31.
ZHOU Liu-gen. The extraction of Mn from pyrolusite by using ferric sulfate and pyrite[J]. Chemistry World, 1955(1): 25-31.
[2] ��ͬ��. ��Ʒλ���̿�ԭ���ռ������о���չ[J]. �й���ҵ, 2008, 26(2): 4-13.
LI Tong-qing. Technology of low grade pyrolusite ore reduction process and recent advances[J]. China��s Manganese Industry, 2008, 26(2): 4-13.
[3] MOHAMMAD S B, ALIREZA Z, ZAHRA G,MANDANA A. Reductive dissolution of manganese ore in sulfuric acid in presence of iron metal[J]. Hydrometallurgy, 2008, 90: 207-212.
[4] ţɯɯ, ��־��, ������, ���º�, ���Ľ�, ������, ���ƺ�. �������������ԭ������[J]. �й���ɫ����ѧ��, 2012, 22(9): 2662-2666.
NIU Sha-sha, WANG Zhi-xing, GUO Hua-jun, LI Xin-hai, PENG Wen-jie, HU Qi-yang, ZHANG Yun-he. Reductive leaching of manganese from manganese anode slag[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(9): 2662-2666.
[5] �� ΰ. ��Ʒλ���̿�ԭ�������̼��䶯��ѧ�о�[D]. ��ɳ: ���ϴ�ѧ, 2014: 4-8.
CHNAG Wei. Study on reductive leaching of low-grade pyrolusite ores and leaching kinetics[D]. Changsha: Central South University, 2014: 4-8.
[6] FURLANI G, PAGNANELLI F, TORO L. Reductive acid leaching of manganese dioxide with glucose: Identification of oxidation derivatives of glucose[J]. Hydrometallurgy, 2006, 81: 234-240.
[7] ������, �װ���, ���Ȼ, ��ά��. ���ոѻ�ԭ����������Ʒλ�̿��о�[J]. ������ѧѧ������Ȼ��ѧ�棩, 2015, 36(8): 1184-1187.
FENG Ya-li, YI Ai-fei, LI Hao-ran, WANG Wei-da. Reductive leaching of high iron low-grade manganese ore with pre-processed cornstalk[J]. Journal of Northeastern University (Natural Sciences), 2015, 26(8): 1184-1187.
[8] SU Hai-feng, LIU Huai-kun, WANG Fan,  Xiao-yan, WEN Yan-xuan. Kinetics of reductive leaching of low-grade pyrolusite with molasses alcohol wastewater in H2SO4[J]. Chinese Journal of Chemical Engineering, 2010, 18(5): 730-735.
Xiao-yan, WEN Yan-xuan. Kinetics of reductive leaching of low-grade pyrolusite with molasses alcohol wastewater in H2SO4[J]. Chinese Journal of Chemical Engineering, 2010, 18(5): 730-735.
[9] BEOLCHINI F, PETRANGELIPAPINI M, TORO L, TRIRONO M, VEGLIO F. Acid leaching of manganiferous ores by sucrose: Kinetic modelling and related statistical analysis[J]. Minerals Engineering, 2001, 14(2): 175-184.
[10]  F, TRIFONI M, PAGNANELLI F, TORO L. Shrinking core model with variable activation energy: A kinetic model of manganiferous ore leaching with sulphuric acid and lactose[J]. Hydrometallurgy, 2001, 60(2): 167-179.
F, TRIFONI M, PAGNANELLI F, TORO L. Shrinking core model with variable activation energy: A kinetic model of manganiferous ore leaching with sulphuric acid and lactose[J]. Hydrometallurgy, 2001, 60(2): 167-179.
[11] �ں���, ���Ⱦ�, �ބ���, �� ��, ��С��, ������. ���۾ƾ���Һ�д���ӽ���ɫ��ģ����������̿�Ķ���ѧ[J]. ��У��ѧ����ѧ��, 2011, 25(1): 43-48.
SU Hai-feng,  Yi-ju, CUI Qing-yan, WANG Fan,
Yi-ju, CUI Qing-yan, WANG Fan,  Xiao-yan, WEN Yan-xuan. Leaching kinetics of pyrolusite by macromolecular caramel of molasses alcohol wastewater[J]. Journal of Chemical Engineering Colleges and Universities, 2011, 25(1): 43-48.
Xiao-yan, WEN Yan-xuan. Leaching kinetics of pyrolusite by macromolecular caramel of molasses alcohol wastewater[J]. Journal of Chemical Engineering Colleges and Universities, 2011, 25(1): 43-48.
[12] ������, �� ΰ, �� ��, Ѧ����. ����ոѻ�ԭ������Ʒλ���̿��䶯��ѧ[J]. �й���ɫ����ѧ��, 2014, 24(8): 2158-2163.
MAN Rui-lin, CHANG Wei, WU Qi, XUE Jian-rong. Reductive leaching and leaching kinetics of low-grade pyrolusite ores using oat straw as reductant[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(8): 2158-2163.
[13] �Ŵ���, ������, ����Ƽ, ������. �绯ѧ������ˮ�����е��о���Ӧ��[M]. ����: �й�����������, 2013: 11-25.
ZHANG Chun-hui, HE Xu-wen, ZHANG Li-ping, WANG Chun-rong. Research and application of electrochemical technology in water treatment[M]. Beijing: China Environmental Science Press, 2013: 11-25.
[14] ���г�, Ѧ�ķ�, �� ��, �ΰ���, �� �. ������ˮ���������о���չ[J]. ��ҵˮ����, 2012, 32(1): 15-17.
LIU Shang-chao, HUE Gai-feng, ZHANG Lei, DUAN Ai-min, ZHANG Nan. Research progress in the treatment technology of wastewater for coke plants[J]. Industrial Water Treatment, 2012, 32(1): 15-17.
[15] л ��, ���, ������, �� ��. ��ѹʪ��ұ����Ӧ����״����չ����[C]//��ʮ�����й���Э���-��10ȫ������ɫ����ұ�������������ļ�. ����: �й���ѧ����Э��, 2014: 1-4.
XIE Gang, LI Huai-ren, HE Xiao-cai, TIAN Lin. Application status and development trend on pressure hydrometallurgy technology[C]//The 16th Session of Annual Meeting of the Association of China-10 Proceedings of the National Symposium on heavy non-ferrous metal metallurgy. Beijing: China Association for ScienceandTechnology, 2014: 1-4.
[16] л����, ������, · ��, ������, ������. ��ѹ������Ʒλ�̿�Ĺ���[J]. �й���ɫ����ѧ��, 2013, 23(6): 1701-1711.
XIE Hong-yan, WANG Ji-kun, LU Hui, JI Xiao-cang, YANG Shi-cheng. Technique of pressure leaching low grade manganese ore[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(6): 1701-1711.
[17] ����Ӣ, ����ϼ, Ԭϲ��, ������, �ﴺ��. ��⻯�������̶���ѧ[J]. �й���ɫ����ѧ��, 2014, 24(3): 814-819.
LI Shao-ying, WANG Hai-xia, YUAN Xi-zhen, ZHAO Liu-cheng, SUN Chun-bao. Leaching dynamics of gold concentrates by iodine-iodide solution[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(3): 814-819.
[18] �� ��, ��С��, �Ž�ǿ, �� ��, ��ԯ��. пұ���н���п��ԭ���������붯��ѧ[J]. �й���ɫ����ѧ��, 2016, 26(1): 197-203.
ZHANG Chun, MIN Xiao-bo, ZHANG Jian-qiang, WANG Mi, LI Yuan-cheng. Mechanisms and kinetics on reductive leaching of zinc from neutral leaching residue[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(1): 197-203.
[19] ������, ��ѧ��, �� �D. ������·��������ĩ��������������ν�������ѧ[J]. �й���ɫ����ѧ��, 2015, 25(2): 545-552.
LIU Jing-xin, GUO Xue-yi, LIU Yang. Fractal leaching kinetics of alkaline smelting product with metal enrichment from waste printed circuit boards[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(2): 545-552.
[20] ����, ֣��Զ, ������, ֣�ٻ�. ʪ��ұ��ѧ[M]. ��ɳ: ���ϴ�ѧ������, 2002: 69-87.
LI Hong-gui, ZHENG Qing-yuan, ZHANG Qi-xiu, ZHENG Di-ji. Science of hydro-metallurgy[M]. Changsha: Central South University Press, 2002: 69-87.
[21] ��ʵ��, ���Ȫ, ������, ���»�, �� ǿ. ú��¯������ú�Ҽ����ѹ跴Ӧ����ѧ[J]. �й���ɫ����ѧ��, 2014, 24(7): 1888-1894.
HE Shi-yue, LI Hui-quan, LI Shao-peng, LI Yong-hui, XIE Qiang. Kinetics of desilication process of fly ash with high aluminum from pulverized coal fired boiler in alkali solution[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(7): 1888-1894.
[22] �� ��, �� ��, �� ��, ���, ����ΰ. ���ȶԳ���ֱ�ӻ�ԭ����ѧ��Ӱ��[J]. ������չ, 2014, 33(12): 3215-3220.
GE Qi, WANG Heng, MAN Yi, LI Fu-jie, PANG Li-wei. Effect of particle size on kinetics of direct reduction of red mud[J]. Chemical Industry and Engineering Progress, 2014, 33(12): 3215-3220.
[23] �� ��, ���Ľ�, ��־��, ���º�, ������, ������. ��Ӧ���淨�Ż��������������ԭ��������[J]. �й���ɫ����ѧ��, 2013, 23(2): 528-534.
YAN Hao, PENG Wen-jie, WANG Zhi-xing, LI Xin-hai, GUO Hua-jun, HU Qi-yang. Reductive leaching technology of manganese anode slag optimized by response surface methodology[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(2): 528-534.
[24] TRIFONI M��TORO L��VEDLIO F. Reductive leaching of manganiferous ores by glucose and H2SO4: Effect of alcohols[J]. Hydrometallurgy, 2001, 59(1): 1-14.
[25] ������, ¬��־, �¶���, ����Ȩ, ��ά��, Ԭ��Ⱥ, Τ��Ƽ, Τʫ��. ���ỹԭ������Ʒλ���̿�[J]. ���̹���ѧ��, 2015, 15(6): 976-981.
MA Hua-ju, LU You-zhi, CHEN Dong-lian, MING Xian-quan, LI Wei-jian, YUAN Ai-qun, WEI Dong-ping, WEI Shi-qing. Reductive leaching of low grade pyrolusite ore with lactic acid[J]. The Chinese Journal of Process Engineering, 2015, 15(6): 976-981.
[26] Ԭ����, ÷��, ׯ����, �� ݣ, �����. ���̿��������������Ϊ[J]. ���Ϲ�ҵ��ѧѧ��, 1996, 27(1): 40-43.
YUAN Ming-liang, MEI Xian-gong, ZHUANG Jian-ming, CHEN Jin, JIANG Han-ying. The behavior of impurities in the leaching process of manganese carbonate ore[J]. Journal of Central South University of Technology, 1996, 27(1): 40-43.
Leaching kinetics of pyrolusite ores using coking wastewater as reductant
FENG Ya-li1, KANG Jin-xing1, LI Hao-ran2, DENG Xiang-yi1, SUN Ming1
(1. School of Civil and Resource Engineering, University of Science and Technology, Beijing 100083, China;
2. National Key State Laboratory of Biochemical Engineering, Institute of Process Engineering, Chinese Academy of Sciences, Beijing 100190, China)
Abstract: Using the coking wastewater as reducing agent to pressure leaching the pyolusite, the shrinking core model was used to investigate the kinetics of the manganese reductive leaching process in the sulfuric acid solution. The effects of stirring speed, reaction temperature, the particle size of the pyrolusite and the concentrations of H2SO4 and coking wastewater on the leaching rate were investigated. The results show that the leaching of manganese increases with the increase of the temperature, the concentrations of H2SO4 and coking wastewater, whereas decreases with the increase of particle size. The kinetic equation for the manganese pressure reduction is presented at the temperature ranging from 393 K to 423 K, with the apparent activation energy of the leaching process is obtained to be 15.2 kJ/mol and the reaction orders for the concentration of H2SO4 and coking wastewater are 1.21 and 0.98, respectively. It suggests that the reduction of manganese from pyrolusite is controlled by the diffusion through the ash-inert layer. The mechanism analysis shows that pyrolusite is reduced by the multikey macromolecules of coking wastewater through providing the oxygen atom for the macromolecular organic compounds decomposition, or is reduced directly by small organic molecules. The thin-walled with holes superficial layer constituted by residual of Fe, Si, Al affects the Mn leaching.
Key words: coking wastewater; pyrolusite ore; reductive leaching; kinetics
Foundation item: Project(2015ZX07205-003) supported by the Major Science and Technology Program for Water Pollution Control and Treatment, China; Project(DY 125-15-T-08) supported by the China Ocean Mineral Resources Research & Development Program; Projects(21176026, 21176242) supported by the National Natural Science Foundation of China
Received date: 2016-05-26; Accepted date: 2016-10-21
Corresponding author: LI Hao-ran; Tel: +86-10-82627063; E-mail: hrli@home.ipe.ac.cn
(�༭ ����)
������Ŀ��ˮ����Ⱦ�������Ƽ��ش�ר��������Ŀ(2015ZX07205-003)���й���������Դ�о��ƻ�������Ŀ(DY 125-15-T-08)��������Ȼ��ѧ����������Ŀ(21176026,21176242)
�ո����ڣ�2016-05-26�������ڣ�2016-10-21
ͨ�����ߣ����Ȼ�����о�Ա����ʿ���绰��010-82627063��E-mail��hrli@home.ipe.ac.cn