���±�ţ�1004-0609(2009)07-1345-05
��N503/TBP�Ӽ����軯Һ����ȡ��Ũ�Ƚ�
�� ���ѧ�ᣬ��˸�h�������
(���ϴ�ѧ ��ѧ��ѧ�빤��ѧԺ������ 650091)
ժ Ҫ���о�����N503��TBP�Ӽ����軯Һ����ȡ��Ũ��Au(��)������N503���Ũ�ȡ�ˮ��pHֵ��TBPŨ�ȡ�NaClŨ�ȡ����Լ��������ȵ����ض���ȡ�ʵ�Ӱ�졣�������������Һ��pH��7~11��Χ�ڣ�Au(��)����ȡ�ʾ�����98%����pH��11��Au(��)����ȡ��������С������TBP��Ũ�ȶ�Au(��)��ȡ�ʵ�Ӱ���С�������TBPŨ�ȿ��������ȡpH50ֵ���Կ�ɽ����Һ����ȡ���������N503/TBP��ȡ��ϵ�Խ�������õ�ѡ����, ����ȡ�������������ӵ��������Ĵ���ΪFe(CN)64?��Ni(CN)42?��Zn(CN)42?��Cu(CN)32?��Au(CN)2?��
�ؼ��ʣ��ܼ���ȡ��KAu(CN)2��N, N��-��(1-������)������������������
��ͼ����ţ�O 658.2��TF 804.2���� ���ױ�ʶ�룺A
Solvent extraction of trace Au(��) from alkaline cyanide solution by N503/TBP system
ZHOU Yang, LI Xue-ling, GU Shuo-yue, YANG Xiang-jun
(School of Chemical Science and Technology, Yunnan University, Kunming 650091, China)
Abstract: The extraction of trace Au(��) from alkaline cyanide solution by N, N��-di(1-methylheptyl) acetamide (N503) and tri-butylphosphate (TBP) was studied. The influence of several variables on the gold extraction, including the N503 volume fraction, pH value of the solution, TBP concentration, NaCl concentration and phase ratio(A/O) in aqueous phase were investigated. The results show that almost all of Au(��) in the aqueous phase can be extracted into the organic phase when the volume fraction of N503 is more than 10% and pH value of the solution is in the range of 7?11, and the extraction rate is more than 98%. When pH��11, although TBP concentration has little effect on the extraction rate of Au(��), the increase of TBP concentration can increase pH50 value of N503/TBP extraction system. The experiments with a real cyanide leaching solution show that the extractive selectivity for different metal ions from difficult to easy is Fe(CN)64?��Ni(CN)42?��Zn(CN)42?��Cu(CN)32?��Au(CN)2?.
Key words: solvent extraction; KAu(CN)2; N, N��-di(1-methylheptyl) acetamide; tri-butylphosphate
�ӿ�ʯ�в����軯�����������Ч�ʸߡ��Կ�ʯ��Ӧ��ǿ�����������ŵ㣬������ռ������λ��Ŀǰ���Ӽ����軯Һ�л��ս�Ĺ�����Ҫ�л���̼������п���û����֡������ֹ��յ�ȱ����ȱ��ѡ���ԡ������߳�������ʧ�������ܼ���ȡ���Ӽ����軯��Һ�л��ս���н��ܡ���Ч���������ڶ̡�ѡ���Ըߡ��ɱ����Լ������Ѻõ��ص�[1]�����ڴ�ͳ������ա���1983�꣬MILLER��[2]��MOOIMAN��[3]�����˼��������������Լ�����߰�����ȡ����ƽ��pHֵ�������Ӽ����軯Һ���ܼ���ȡ��һֱ�ǹ������ѧ���������о����ȵ㡣�����������о����а��༰�����ࡢ��ࡢ������ͽ���ϵ[4?6]����������δ���й�ҵӦ�õı���������Ҫԭ����Au(CN)2?ֻ����pH��9.4�ļ��������²����ȶ����ڣ������ų��綾��HCN���壬���Ѱ�Һ��ʵ���ȡ���������Ѷȡ�Ѱ�����Ӧ�����Խ��ʣ����ܶ�Au(CN)2?���и�ѡ���Ե���ȡ�����о����ص㡣���������о�����[7?9]�������͵ı�����Լ�ʮ����������廯�(CTAB)����Au(��)��Ħ���ȼ��뵽ˮ���������������(TBP)�ȴ����Ի��ŵ���ȡ����ȡ��������pHֵ��Χ�ھ��ܹ���������ȡAu(CN)2?�������ڼ���������Ӷ�Au(CN)2?���к�ǿ���������ͺ����ȶ������ܴӼ�����ؽ��л����з��ͱȽ����ѣ��Ӷ��谭�����ڹ�ҵ�ϵ�Ӧ��[10?11]����������ȡ�����������ԣ��㷺���ں��ӷ�ˮ����[12]�Ͷ��ֽ������ӵ���ȡ����[13?14]����δ�� ����������ȡ���Ӽ����軯Һ����ȡAu(��)�ı�����N, N��-��(1-������)������(N503)��һ����ȡ����ǿ���ȶ��Ըߡ�ˮ����С���ӷ��Ե͡��۸��������������ȡ�������Ա��о�ѡ������N503/TBP��ΪAu(��)����ȡ����ͬʱ�����ڿ�ɽ�軯�ѽ�Һ��۽�Һ��Au(��)��Ũ�ȷdz��ͣ�һ��Ϊ1~20 mg/L�������������ؿ�����N503/TBP�Ե�Ũ�Ƚ�(��(Au)=10 mg/L)����ȡ���ܡ�
1 ʵ��
1.1 ʵ���Լ�������
��Ҫ�Լ����£�N, N��-��(1-������)������(N503) SIDMEX���������ȴ���97%������������(TBP)�����ѧ�Լ�һ�������������ǻ�ú�ͣ�����ú�;�Ũ���ᴦ����ȥ�������ʣ�KAu(CN)2Ϊ���ƣ����ȴ���99%��
��Ҫ�������£�PHS?3C(601B��) ������ȼƣ�ZD?2�͵��ٶ�������(���ջ���������)��ԭ�����շֹ��ȼƣ����� Z8000�͡�
1.2 ʵ�鷽��
ʵ���ô���ˮ����KAu(CN)2���ƣ���(Au(��))=10 mg/L (pH 10.2, NaCl 0.2 mol/L)����ȡ�л����ǽ�һ�����Ũ�ȵ�N503��TBP ���ڻǻ�ú�����Ƶ�(һ��Ϊ20%TBP +20%N503���������)�������£���10 mL����ˮ��͵�������л����ڷ�Һ©���л�ϣ���е��10 min��(��ȡ����ѧʵ��֤�������5 min����ϵ�Ѵﵽƽ��)�����÷��࣬��ԭ�����չ������Ͳ�Һ��Au(��)��Ũ�ȣ��ɲ����������ȡ�ʡ�
2 ���������
2.1 N503���Ũ�ȶ�Au(��)��ȡ��Ӱ��
�̶�ˮ���н�Ũ��Ϊ10 mg/L��TBP���Ũ��Ϊ20%(�������)��������N503���������0~20%��Χ�ڶ�Au(��)��ȡ�ʵ�Ӱ�죬ʵ������ͼ1��ʾ����ͼ1���Կ���������N503���Ũ�ȵ�����Au(��)����ȡ�ʲ������ߣ���N503Ũ��Ϊ10%ʱ��Au(��)����ȡ���Ѵﵽ99.18%������������N503Ũ�ȣ�Au(��)����ȡ�ʱ仯����
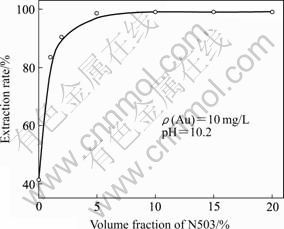
ͼ1 N503���������Au(��)��ȡ�ʵ�Ӱ��
Fig.1 Effect of volume fraction of N503 on extraction rate of Au(��)
2.2 ˮ��pHֵ��Au(��)��ȡ�ʵ�Ӱ��
�̶�ˮ����Au(��)Ũ��Ϊ10 mg/L�������л�����ɲ���(20%TBP+20%N503)������ˮ��pH��7~14��Χ�ڶ�Au(��)��ȡ�ʵ�Ӱ����ͼ2��ʾ����ͼ2 ���Կ���������ˮ��pHֵ��7~11��Χ�ڣ�N503/TBP��Au(��)����ȡ�ʼ������ֺ㶨��������98%���� pH��11ʱ��Au(��)����ȡ��Ѹ�ٽ��ͣ���pH=13.85ʱ��Au(��)����ȡ���Ѿ��½�����70%�������������ԭ�������N503��ȡ�����йأ��Ʋ��֪�������Ի������Է�Χ�ڣ�N503 �������ӻ��������ȡAu(CN)2?�������ӣ������Ժܴ�ʱ��N503����ȥ���ӻ���Ӧ������Au(CN)2?��ȡ��Ѹ���½����ɴ˿ɼ���N503��ȡ����Ԥʾͨ���ı�pHֵ�ķ�������Au(��)�ķ����ǿ��еġ�
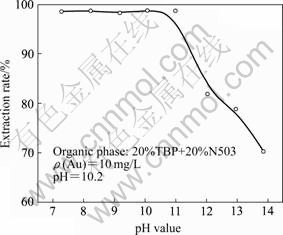
ͼ2 ����ˮ��pHֵ��Au(��)��ȡ�ʵ�Ӱ��
Fig.2 Effect of pH value of aqueous solution on extraction rate of Au(��)
2.3 ���Լ������Au(��)��ȡ�ʵ�Ӱ��
����ˮ���Ũ��Ϊ10 mg/L����1����Ϊ��ͬ��ࡢ������Լ���Au(��)��ȡ��Ӱ�졣�ɱ�1��֪��
��1 ��ͬ���Լ���Au(��)��ȡ�ʵ�Ӱ��
Table 1 Effect of different modifiers on extraction rate of Au(��)

Organic phase: 20%N503+20%modifier; ��(Au)=10 mg/L; pH= 10.2
����ȡ������ͬ������£���ѡ���Լ������Au(��)��ȡ��û������Ӱ�죬����ȡ�ʾ�����98%��ͬʱҲ��������������һ����Ҳ�����������ĸ��Լ���
2.4 ���Լ�TBPŨ�ȶ�Au(��)��ȡ�ʵ�Ӱ��
����ˮ����ɲ��䣬���л�����N503���Ũ ��Ϊ20%ʱ�������˸��Լ�TBP���Ũ�ȶ� Au(��)��ȡ�ʵ�Ӱ������ͼ3��ʾ����ͼ3��֪����ˮ��pHΪ10.2ʱ��TBPŨ�ȶ�Au(��)����ȡ��Ӱ���С��TBPŨ����0~40%��Χ�ڣ�Au(��)����ȡ�ʾ�����98%��˵��TBP��N503������Э�����á�MOOIMAN��MILLER[3]�Լ�ALGUACIL[15]�о����֣��ڰ�����ȡ��ϵ�м����������Լ��������������ȡ��ϵ��pH50ֵ(��ȡ��Ϊ50%ʱ��pHֵ)��Ϊ��һ��Ū��TBP�ڱ���ȡ��ϵ�е����ã������˲�ͬŨ�ȵ�TBP(0~20%)��pHֵΪ7~14���Au(��)Ũ��100 mg/L��Һ����ȡ��ʵ������ͼ4��ʾ����ͼ4���Կ�����TBP�ļ�������������N503��ȡAu(��)��pH50ֵ��N503��ȡAu(��)��pH50ֵԼΪ10.7������20%TBP��N503��ȡAu(CN)2?��pH50ֵ����12.04��?pH50 =1.34��
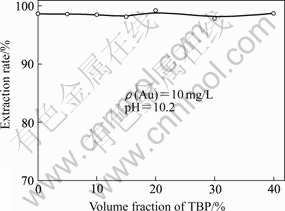
ͼ3 TBP�����������Au(��)��ȡ�ʵ�Ӱ��
Fig.3 Effect of volume fraction of TBP on extraction rate of Au(��)
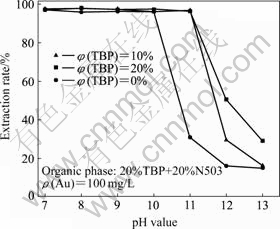
ͼ4 ��ͬ���������TBP��Au(��)����ȡ�ʵ�Ӱ��
Fig.4 Effect of volume fraction of TBP on extraction rate of Au(��)
2.5 NaClŨ�ȶ�Au(��)��ȡ�ʵ�Ӱ��
�����л������(20%TBP+20%N503)���䣬ˮ�ຬAu(��)Ũ��Ϊ10 mg/L���������ˮ����������NaClŨ�ȶ�Au(��)��ȡ�ʵ�Ӱ�죬�����ͼ5��ʾ����ͼ5���Կ�����NaClŨ�ȶ�Au(��)��ȡ�ʵ�Ӱ�첻��ˮ����NaClŨ����0~2.0 mol/L��Χ�ڣ�Au(��)����ȡ�ʾ�����99%��ʵ�鷢�֣�NaCl�ļ����������������ķֲ��ٶȣ� NaClŨ��Խ�����ٶ�Խ�졣ͬʱ������NaCl�ļ������Ӧ������ȡ�����еIJ����ɱ�����ˣ���ѡ�����ˮ���к���0.2 mol/L NaCl��
2.6 ��ȶ���ȡ�ʵ�Ӱ��
ʵ�ʹ�ҵ�����У���ɽ�ĵ��軯�۽�Һ��ѽ�Һ��Au(��)��Ũ���൱�ͣ�һ��Ϊ1~20 mg/L[16]�����Ҫ���þ����ٵ��л�����ȡ�������ˮ�ࡣ����ˮ�༰�л�����ɲ��䡣ͼ6��ʾΪ���A/O��Au(��)��ȡ�ʵ�Ӱ�졣��ͼ6��֪�������A/OΪ1~3ʱ����ȶ���ȡ��Ӱ���С��99%���ϵ�Au(��)�ܹ��������л����У���A/OΪ4~10ʱ��Au(��)����ȡ�������½�����A/OΪ10ʱ����Au(��)����ȡ��Ϊ83%����ˣ�Ϊ���ֽϸ���ȡ�ʣ����A/O���˳���3��

ͼ5 NaClŨ�ȶ�Au(��)��ȡ�ʵ�Ӱ��
Fig.5 Effect of NaCl concentration on extraction rate of Au(��)
2.7 N503/TBP��ȡ��ϵ��ʵ����Һ����ȡ
ʵ�ʵ�Au(��)��ɽ�ѽ�Һ�г����ж��ֽ������ӣ���ˣ���������ȡ��ϵ������Au(��)���иߵ���ȡЧ�ʣ����Ҷ�������������Ҫ�������õ�ѡ���ԡ������л�����ɲ��� (20%TBP +20%N503)��ѡ������ij���ѽ�ҺΪ����ˮ�࣬������N503/TBP��ϵ��ʵ����Һ����ȡЧ����������2���С�

ͼ6 ���A/O��Au(��)��ȡ�ʵ�Ӱ��
Fig.6 Effect of A/O on extraction rate of Au(��)
�ɱ�2��֪��N503/TBP��ȡ�������������ӵ����״���ΪFe(CN)64?��Ni(CN)42?��Zn(CN)42?��Cu(CN)32?��Au(CN)2?������ȡ˳����ѭ��С����ԭ��������ȡ��ϵ������ȡAu(CN)2? (��ȡ��ԼΪ95%)��Cu(CN)32?���Žϴ���ȡ��ԼΪ75%������������������ȡ�ʽϵͣ������Ǽ�������ȡFe(CN)64?��Ni(CN)42?����Fe��Ni�ķ���ϵ���·ֱ�Ϊ1 575.31��850.67����������ȡ��ϵ���кܸߵ��ͽ�ѡ���ԡ�
��2 N503/TBP��ȡ��ϵ��ѡ����
Table 2 Selectivity of N503/TBP extraction system
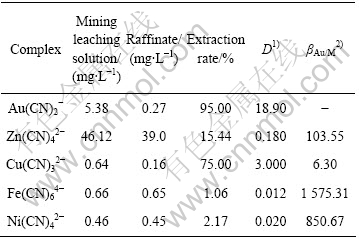
Organic phase: 20%TBP+20%N503, pH=10.05; 1) Distribution coefficient; 2) Separation coefficient, ��Au/M=DAu/DM.
3 ����
1) ��N503���Ũ�ȴ���10%��pH��11ʱ��N503/TBP��ϵ�ܹ���Ч����ȡAu(��)(��ȡ�ʴ���98%)����pH��11ʱ��Au(��)����ȡ�������½���TBP�����Ũ�ȶ�Au(��)��ȡ�ʵ�Ӱ���С�������TBPŨ�ȿ����Au(��)��ȡ��pH50ֵ����TBP���Ũ��Ϊ20%��pH50=12.04��
2) N503/TBP��ȡ��ϵ�Խ�������õ�ѡ���ԣ�����ȡ�������������ӵ��������Ĵ���ΪFe(CN)64?��Ni(CN)42?��Zn(CN)42?��Cu(CN)32?��Au(CN)2?��
REFERENCES
[1] ADAMS M D. On-site gold re?ning of cyanide liquors by solvent extraction[J]. Minerals Engineering, 2003, 16(4): 369?373
[2] MILLER J D, MOOIMAN M B. A review of new developments in amine solvent extraction systems for hydrometallurgy[J]. Separation Science and Technology, 1984/1985, 19(11/12): 895?909.
[3] MOOIMAN M B, MILLER J D. The chemistry of gold solvent extraction from cyanide solution using modified amines[J]. Hydrometallurgy, 1986, 16(3): 245?261.
[4] JIANG J Z, HE Y F, GAO H C, WU J G. Solvent extraction of gold from alkaline cyanide solution with a tri-n-octylamine/ tri-n-butyl phosphate/n-heptane synergistic system[J]. Solvent Extraction and Ion Exchange, 2005, 23(1): 113?129.
[5] ALGUACIL F J, CARAVACA C, COBO A, MARTINZ S. The extraction of gold(��) from cyanide solutions by the phosphine oxide Cyanex 921[J]. Hydrometallurgy, 1994, 35(1): 41?52.
[6] SASTRE A M, MADI ABDELHAY, CORTINA J L, FRANCISCO J A. Solvent extraction of gold by LIX79: Experimental equilibrium study[J]. Journal of Chemical Technology and Biotechnology, 1999, 74(4): 310?314.
[7] CHEN Jing, HUANG Kun, YU Jian-min, WU Jin-guang, SHI Nai, XU Guang-xian. Microscopic mechanism in solvent extraction of Au(CN)2? by cationic surfactant[J]. Trans Nonferrous Met Soc China, 2005, 15(1): 153?159.
[8] �� ��, �� ��, ��誹�, �ߺ��, �� ��, �ཨ��. CTMAB��ȡAu(CN)2?��ϵ�м��ָ��Լ��ĶԱ�[J]. �й���ɫ����ѧ��, 2001, 11(2): 307?311.
HUANG Kun, CHEN Jing, WU Jin-guang, GAO Hong-cheng, CUI Ning, YU Jian-min. Effects of modifiers on Au(CN)2? solvent extraction by CTMAB[J]. The Chinese Journal of Nonferrous Metals, 2001, 11(2): 307?311.
[9] �����, �� ��, ΤȺ��, ��誹�, ���, ����ΰ. ��CTAB/TBP��ϵ�Ӽ����軯Һ����ȡ��Ũ��Au(��)[J]. �й���ɫ����ѧ��, 2004, 14(11): 1958?1962.
YANG Xiang-jun, CHEN Jing, WEI Qun-yan, WU Jin-guang, LI Kai-zhong, LI Qi-wei. Solvent extraction of trace gold(I) in alkaline cyanide solution using CTAB/TBP system[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(11): 1958?1962.
[10] MA G, YAN W F, CHEN J, ZHOU W J, WU J G, XU G X. Stripping of gold from quaternary amine extraction system[J]. Solvent Extraction and Ion Exchange, 2000, 18(6): 1179?1187.
[11] �����, �� ��, ��誹�, ���, ��ά��, ΤȺ��, ����, ����ΰ. CTAB-TBP ��ϵ�ؽ��л����н�(��)��ת����ԭ����ȡ[J]. �й���ɫ����ѧ��, 2003, 13(6): 1565?1969.
YANG Xiang-jun, CHEN Jing, WU Jin-guang, LI Kai-zhong, ZHOU Wei-jin, WEI Qun-yan, JIANG Jian-zhun, LI Qi-wei. Au(��) stripping from gold loaded CTAB-TBP organic phase by transformation and reduction[J]. The Chinese Journal of Nonferrous Metals, 2003, 13(6): 1565?1969.
[12] WANG Yin-hua, WANG Xiang-de, ZHANG Xiu-juan. Treatment of high concentration phenolic waste water by liquid membrane with N503 as mobile carrier[J]. Journal of Membrane Science, 1997, 135(2): 263?270.
[13] TOMASZEWSKA M, BOROWIAK RESTERNA A, OLSZANOWSKI A. Cadmium extraction from chloride solutions with model N-alkyl- and N,N-dialkyl-pyridine- carboxamides[J]. Hydrometallurgy, 2007, 85(2/4): 116?126.
[14] JHA R K, GUPTA K K, KULKARNI P G, GURBA P B, JANARDAN P, CHANGARANI R D, DEY P K, PATHAK P N, MANCHANDA V K. Third phase formation studies in the extraction of Th(��) and U(��) by N,N-dialkyl aliphatic amides[J]. Desalination, 2008, 232(1/3): 225?233.
[15] ALGUACIL F J. Solvent extraction of Au(CN)2? by mixtures of the primary amine tridecylamine and the phosphine oxide cyanex 923[J]. J Chem Research, 1998(S): 792?793
[16] WAN R Y, MILLER J D. Research and development activities for the recovery of gold from alkaline cyanide[J]. Mineral Processing and Extractive Metallurgy Review, 1990, 6(1/4): 143?190.
������Ŀ�����Ҹ����о���չ�ƻ�������Ŀ(2006AA06Z127)��������Ȼ��ѧ����������Ŀ(2007CB613)
�ո����ڣ�2008-11-10�������ڣ�2009-03-12
ͨѶ���ߣ����������ʦ����ʿ���绰��0871-5032180��E-mail: gnft@ynu.edu.cn
(�༭ ����)