文章编号:1004-0609(2007)03-0402-04
Mg纳米粉的制备及其氧化特性
孙维民1,徐东年1,郑 卓1,张 毅1,刘 正2
(1. 沈阳工业大学 理学院,沈阳 110023;
2. 沈阳工业大学 材料科学与工程学院,沈阳 110023)
摘 要:分别在Ar、H2+Ar和CH4+Ar混合气氛下,用电弧放电法蒸发纯Mg制备了Mg纳米粉。用XRD、TEM、BET、化学分析、氧含量分析、DSC-TGA等测试手段研究了粉体的相组成、形貌、粒度分布、比表面积和氧化特性等。结果表明:在3种不同气氛条件下制备的纳米粉体的主相是Mg,含有少量MgO,其中在CH4+Ar混合气氛下制备的纳米粉体中还含有2%(质量分数)的C,粒子形貌均为类球形,平均粒度分别为156、195和181 nm,比表面积分别为22.12、17.70和19.07 m2/g,钝化后氧含量分别为6.9%、7.4%和5.5%;在CH4+Ar混合气氛下制备的样品抗氧化性最好,该样品在空气中加热到约550 ℃时,全部氧化为MgO。
关键词:Mg纳米粉;电弧放电法;氧化特性
中图分类号:TF 122 文献标识码:A
Preparation and oxidation resistance of Mg nanopowders
SUN Wei-min1, XU Dong-nian1, ZHENG Zhuo1, ZHANG Yi, LIU Zheng2
(1. College of Science, Shenyang University of Technology, Shenyang 110023, China;
2. College of Material Science and Engineering, Shenyang University of Technology, Shenyang 110023, China)
Abstract: Mg nanopowders were prepared by arc discharging in Ar, H2 and Ar, CH4 and Ar atmosphere. The structure and morphology as well as oxidation resistance of the powders were studied by X-ray diffractometry(XRD), transmission electron microscopy(TEM), BET, chemical analysis, gas analysis, differential thermal and thermogravimetry analysis. The results show that the nanopowders consists of Mg and a small quantity of MgO, besides there exist also 2% C (mass fraction) in as-prepared sample in CH4 and Ar mixed atmosphere. The morphologies of nanoparticles are similar spheric shape and average sizes of nanoparticles are about 156, 195 and 181 nm, the specific surface areas are 22.12, 17.70 and 19.07 m2/g, the contents of oxygen are 6.9%, 7.4% and 5.5%. The oxidation resistance of the samples prepared in CH4 and Ar mixed atmosphere is the best, which is oxidized to MgO at about 550 ℃ in air.
Key words: Mg nanopowder; arc discharge; oxidation resistance
纳米粒子表面积大,表面缺陷多,具有与大块材料不同的磁学、电学、光学、化学和热学等物性,作为潜在的新功能材料引起各界的极大关注[1-6]。Mg纳米粉在聚丙烯改性[7]、储氢材料[8-10]和制造特种电容器等方面的应用逐渐引起人们的重视,来自吉林高斯达纳米材料公司的信息,美国公司向其大量求购Mg纳米粉用于制造特种电容器。由于Mg纳米粉比普通Mg粉更易燃,所以未见有关连续制备Mg纳米粉的报道。目前实验室内Mg纳米粉的制备方法主要有两种,高能球磨法和气体冷凝法(电阻加热蒸发法)。这两种方法都有明显的缺点,高能球磨法的缺点是能耗大、生产周期长,而电阻加热法产量小,并且无法连续生产。
本文作者研究了用电弧放电法连续制备Mg纳米粉的工艺及Mg纳米粉的氧化特性。
1 实验
图1所示为用电弧放电法连续制备Mg纳米粉装置示意图,该装置由生成室、捕集室、处理室、循环系统、抽真空系统、电源系统和送料系统组成。当装置真空度抽至1 Pa后,充入Ar或H2+Ar或CH4+Ar的混合工作气体至设定压力。用高频引弧器产生等离子电弧(Mg棒作阳极,W棒或C棒做阴极),从弧根周围熔融Mg金属表面产生的纳米粒子被循环气流带到捕集室进行多级捕集[11]。根据不同的应用目的和条件,捕集后的纳米粉即可以钝化后包装,也可以在氩气保护下原位包装。
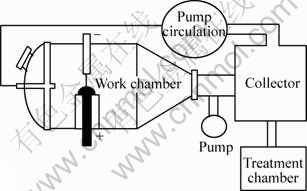
图1 实验装置示意图
Fig.1 Schematic diagram of experiment apparatus
Mg纳米粉的生产率是用捕集到的纳米粉体除以连续运行时间得到。用X射线衍射(Cu Kα , λ=0.154 05 nm)确定样品的相结构和成分,用透射电子显微镜(TEM)分析粒子的形貌和粒径分布,用BET单点法测定比表面积,用化学分析确定样品碳含量,用脉冲红外法测定其氧含量,用综合热分析仪(DSC-TGA)分析其氧化特性。
2 结果与讨论
2.1 纳米粉生产率
为方便讨论,在Ar、H2+Ar和CH4+Ar气氛下制备的样品分别记为样品a、b和c。表1给出了3种不同工作气氛条件下Mg纳米粉的生产率,由表1可知,在H2+Ar气氛下制备纳米粉的产率最高,CH4+Ar次之,纯Ar下最低,这是因为在含有H2气的非活性气体中,熔解金属所用电弧温度处于高温等离子体状态。在这样的高温下,分子状态氢气解离为原子或离子状态的气体,解离生成的氢原子比分子状氢更易溶于熔融状态的金属,于是电弧中解离后生成的原子状态氢通过熔融金属的对流作用而移动,一旦与非电弧气相(分子状态氢)接触,就成为一种氢熔融度过饱和状态,过饱和状态的氢通过金属熔解释放时,在熔融金属表面重新结合成分子,并释放生成热,熔融金属表面局部温度升高,熔融金属成为一种强迫蒸发状态而使纳米粒子产率增加。
表1 Mg纳米粉的生产率
Table 1 Production rate of Mg nanopowders

2.2 粉体的相组成
图2给出了3种样品的XRD谱。从图2中可以看到只有Mg相,所以在CH4+Ar的气氛下制备的Mg纳米粉体中无Mg-C化合物形成,化学分析表明在CH4+Ar的气氛下制备的纳米粉体中C含量为2%。XRD没有探测到壳层的物相结构,这是因为氧化物壳层较薄。样品a、b和c的晶格常数相同,表明3种粒子的芯都是Mg。

图2 3种样品的XRD谱
Fig.2 XRD patterns of three samples
2.3 粉体的形貌和粒度分布
图3给出了3种样品的TEM照片。通过TEM照片可以看到所有粒子都接近球形,没有明显的惯态[12]形成,这是因为粒子吸附活性气体分子,导致不同结晶面表面能均匀化。样品a、b和c的平均粒度分别为156、195和181 nm,比表面积(Sw)分别为22.12、17.70和19.07 m2/g。

图3 3种样品的TEM照片
Fig.3 TEM micrographs of three samples: (a) Sample a; (b) Sample b; (c) Sample c
2.4 粉体的抗氧化性
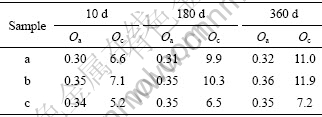
纳米粒子的氧含量可分为来自表面的吸附氧和化合态氧。为了研究粉体的耐侯性,表2给出了样品a、b和c在室温下长时间暴露于大气中时氧含量随时间的变化(Oa, Oc分别表示吸附氧和化合态氧)。从表2可看出,样品a、b和c的吸附氧随暴露于大气中时间的延长变化不大,而化合态氧均随暴露于大气中时间的延长而增加。化合态氧开始180 d左右增加较快,而后速度放慢。对样品a和b,这说明在Mg纳米粒子钝化过程中粒子表面形成的氧化物膜不致密,不能完全保护里面的芯进一步被氧化。样品c的化合态氧含量增加明显小于样品a和b,说明在室温下样品c的抗氧化性比样品a和b强。
表2 室温下Mg纳米粉暴露于大气中不同时间后的氧含量
Table 2 Contents of oxygen of Mg nanopowders after exposed in air for different time at ambient temperature (mass fraction, %)
为了进一步研究样品在高温下的氧化特性,图4给出了在升温速度10 ℃/min、流动空气30 mL/min的条件下,样品b和c的DSC-TGA曲线。样品b和c, 分别在室温至390 ℃左右和室温至500 ℃左右产生质量损失。这是由于样品表面吸附的水蒸气等杂质脱附和部分Mg的挥发造成的。样品b温度升至400 ℃左右时,氧化速度加快,并在430 ℃左右全部氧化为MgO。样品c温度升至500 ℃左右时,氧化速度加快,并在550 ℃左右全部氧化为MgO,即高温下样品c的抗氧化性也比样品b强。这是由于样品c的表面存在无定性碳,这种无定形碳存在于氧化膜的孔隙中,提高了Mg表面膜的致密度;另外,带正电荷的无定形碳,还能强烈地抑制Mg2+透过表面膜的扩散运 动[13],故也能抑制Mg的氧化。但样品c的粒子表面没有像在含CH4气体中制备的磁性金属纳米粒子表面那样形成致密的碳膜[14-16],即用电弧放电法不能制备出致密碳膜包覆的Mg纳米粒子。

图4 样品b和c的DSC-TGA曲线
Fig.4 DSC-TG curves of samples b and c
3 结论
1) 分别在Ar、H2+Ar和CH4+Ar混合气氛下,用电弧放电法蒸发纯Mg制备了Mg纳米粉。在3种不同气氛条件下制备的纳米粉的主相是Mg,含有少量的MgO,其中在CH4+Ar的混合气氛下制备的纳米粉中还含有2%的C。
2) 粒子的形貌均为类球形,平均粒度分别为156、195和181 nm,比表面积分别为22.12、17.70和19.07 m2/g,钝化后氧含量分别为6.9%、7.4%和5.5%。在CH4+Ar的混合气氛下制备的样品抗氧化性最好。样品b和c在空气中加热到大约430 ℃和550 ℃时,全部氧化为MgO。
REFERENCES
[1] Yuan F L, Hu P, Yin C L, Huang S L, Li J C. Preparation and properties of zinc oxide nanoparticles coated with zinc aluminate[J]. J Mater Chem, 2003, 13(3): 634-637.
[2] Radloff C, Halas N. Enhanced thermal stability of silica-encapsulated metal nanoshells[J]. Appl Phys Lett, 2001, 79(5) 674-676.
[3] Zhang Z D, Yu J L, Zheng J G, Skorvanek I, Korvac J, Dong X, Li Z J, Jin S R, Yang H C, et al. Structure and magnetic properties of boron-oxide-coated Fe(B) nanocapsules prepared by arc discharged in diborane[J]. J Phys Rev B, 2001, 64(2): 24404-24408.
[4] 龚荣洲,沈 翔,张 磊,张 凌. 金属基纳米复合材料的研究现状和展望[J]. 中国有色金属学报,2003,13(5):1311-1320.
GONG Rong-zhou, SHEN Xiang, ZHANG Lei, ZHANG Ling. Status and expectation of research on metal matrix nanocomposites[J]. The Chinese Journal of Nonferrous Metals, 2003, 13(5): 1311-1320.
[5] 朱兆武, 龙志奇, 崔大立, 张顺利, 张国成. 超细CeO2粉体的制备及其紫外线吸收性能[J]. 中国有色金属学报,2005,15(3):435-440.
ZHU Zhao-wu, LONG Zhi-qi, CUI Da-li, ZHANG Shun-li, ZHANG Guo-cheng. Preparation of ultra-fine particle-sized CeO2 powder and its UV absorbance[J]. The Chinese Journal of Nonferrous Metals, 2005, 15(3): 435-440.
[6] 高伟丽, 严红革, 盛绍顶, 陈振华. 气相沉积制备Ni-Al 合金纳米粉末的相生成规律[J]. 中国有色金属学报,2006,16(2):340-345.
GAO Wei-li, YAN Hong-ge, SHENG Shao-ding, CHEN Zhen-hua. Phase formation regularities of Ni-Al alloy nanopowders prepared by vapor deposition [J]. The Chinese Journal of Nonferrous Metals, 2006, 16(2): 340-345.
[7] PENG Hong-rui, ZHU Lian-chao, ZHANG Zhi-kun. Preparation, structure and property research of nano-Mg/pp composite[J]. Composite Interface, 2004, 11(3): 231-243.
[8] SHAO Huai-yu, WANG Yun-tao, XU Hai-ruo, ZHAO Jian-ping. Hydrogen storage properties of magnesium ultrafine particles prepared by hydrogen plasma-metal reaction[J]. Mater Sci Eng B, 2004, B110: 221-226.
[9] Mulas G, Schiffini L, Tanda G, Cocco G. Hydriding processes of Mg and Zr alloys by reactive milling[J]. Journal of Materials Science, 2004, 39(16/17): 5251-5254.
[10] YU Zhen-xing, LIU Zu-yan, WANG Er-de. Hydrogen storage properties of nanocomposite Mg-Ni-Cu-CrCl3 prepared by mechanical alloying[J]. J Alloys and Comp, 2002, 335: 43-48.
[11] 孙维民, 金寿日, 李志杰. 气-液两相稳定的Fe 超微粒的氧化特性和磁性[J]. 金属热处理学报, 1999, 20(4): 6-9.
SUN Wei-min, JIN Shou-ri, LI Zhi-jie. Oxidizing and magnetic behavior of ultrafine iron particles stabilized by both gas and liquid phase[J]. Transactions of Metal Heat Treatment, 1999, 20(4): 6-9.
[12] Uyeda R. Crystallography of Metal Smoke Particles[M]. Tokyo: Terra Scientific Publishing Company, 1987: 6.
[13] 刘 正,张 奎, 曾小勤. 镁基轻质合金理论基础及其应用[M]. 北京:机械工业出版社, 2002: 73.
LIU Zheng, ZHANG Kui, ZENG Xiao-qin. Theory and Application of Magnesium Matrix Light Mass Alloy[M]. Beijing: China Machine Press, 2002: 73.
[14] Dong X L, Jin S R, Sun W M, Zhang Z D, Zhao X G. Characterization of Fe-Ni(C) nanocapsules synthesized by arc discharge in methane[J]. J Mater Res, 1999, 14(5): 1782-1790.
[15] Dong X L, Jin S R, Sun W M, Zhang Z D. Surface characterizations of ultrafine Ni particles[J]. Nanostructured Materials, 1998, 10(4): 585-592.
[16] Dong X L, Zhang Z D, Jin S R, Xiao Q F. Carbon-coated Fe-Co(C) nanocapsules prepared by arc discharge in methane[J]. Journal of Applied Physics, 1999, 86(12): 6701-6706.
基金项目:国家“十五”科技攻关计划资助项目(2004BA311A09-2)
收稿日期:2006-08-31;修订日期:2007-01-15
通讯作者:孙维民,教授;电话:024-25691521;E-mail: sunwm1983@126.com
(编辑 龙怀中)