���±�ţ�1004-0609(2012)06-1785-06
������СGibbs������ԭ����CaO-SiO2¯����Si-Ca����������ϵƽ������ѧģ��
�� ��1��������1����ѧ��2
(1. �����Ƽ���ѧ ұ������̬����ѧԺ, ���� 100083��
2. �й���ѧԺ ���̹����о��� ���ิ��ϵͳ�����ص�ʵ���ң����� 100190)
ժ Ҫ�����ڷ��ƽ����ϵGibbs��������Сԭ���Ծ���SiҺ������Ca��¯��-������ϵ��������ѧģ�ͣ��ɸ�����ѧģ�͵õ�SiҺ��Ca��Ħ������xCa��CaO-SiO2��Ԫ��ϵCaO��Ħ������xCaO�Ĺ�ϵ�����ױ�����ʵ�����Ǻ����ã���0.3��xCaO��0.4��������SiҺ��Ca������ѧģ�ͼ�����������SiҺ��Si��Ca�Ļ�ȷֱ���SiO2��CaO��������Ũ�ȵı�ֵ����¯��-������Ԫ���֮��Ĺ�ϵʽ���Ҽ����������ױ��������ݾ��ȸ��ߡ���ˣ�����¯������-���ӹ������۵���������Ũ�ȿ��뾭���¯�����һ������CaO-SiO2��Ԫ��ϵ��Ԫ�ķ�Ӧ�������ɽ���������ѧģ�ͼ�����ȷ���ķ�Ӧ[Ca]+0.5(SiO2)=(CaO)+0.5[Si]�ı�Ħ����ӦGibbs�����ܱ仯����ʽΪ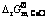 =-89 532.7-21.8T (J/mol)��
=-89 532.7-21.8T (J/mol)��
�ؼ���: CaO-SiO2��ϵ��Si-Ca���壻��С������ԭ��������ѧģ�ͣ�����-���ӹ������ۣ�SiҺ���������
��ͼ����ţ�TF61 ���� ���ױ�־�룺A
Thermodynamic model of CaO-SiO2
binary slags equilibrated with Si-Ca binary metal system based on minimized Gibbs free energy principle
WANG Fei1, GUO Han-jie1, YANG Xue-min2
(1. School of Metallurgical and Ecological Engineering, University of Science and Technology Beijing,
Beijing 100083, China;
2. State Key Laboratory of Multiphase Complex Systems, Institute of Process Engineering,
Chinese Academy of Sciences, Beijing 100190, China)
Abstract: A thermodynamic model was developed for a close system of CaO-SiO2 binary slags equilibrated with Si-Ca binary metal system based on the minimized Gibbs free energy principle of a close system, in which the reaction ability of components in slags was presented by the mass action concentration according to the ion and molecule coexistence theory. The calculated relationship between mole fraction of Ca, xCa, in silicon melt and mole fraction of CaO, xCaO, in CaO-SiO2 slags is in good agreement with the reported results, i.e., the optimal composition range for xCaO is 0.3��xCaO�� 0.4. The calculated relationship between the ratio of Si activity in melt to mass action concentration of SiO2 in slags and the ratio of Ca activity in melt to mass action concentration of CaO in slags follows the intrinsic relation, while the calculated results has higher accuracy than that from the reported results based on experiments. Therefore, the mass action concentrations of components in CaO-SiO2 slags can be successfully used to present reaction ability like component activity in slags. The determined standard molar Gibbs free energy change for reaction [Ca]+0.5(SiO2)= (CaO)+0.5[Si] from the developed thermodynamic model is 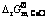 =-89 532.7-21.8T (J/mol) with reliable feasibility.
=-89 532.7-21.8T (J/mol) with reliable feasibility.
Key words: CaO-SiO2 binary slags; Si-Ca metal system; minimized free energy principle; thermodynamic model; ion- molecule coexistence theory; silicon refining; activity
����ʹ�û�ʯȼ�ϲ�������Ⱦ������������ŷ��Լ���ʯȼ�ϴ���������ʹ���������Ͷ����������Ͳ����о������Դ��̫������Ϊ���ϵ������Դ֮һ�����ܵ��㷺���ӡ��ߴ����̫���ܼ���(w(Si)��99.999 9%)�Ǹ�Ч����̫���ܵ���Ҫ�������ϡ�̫���ܼ�����w(Si)��99.7%�Ľ�����Ϊԭ�ϡ���������Ca��Al������Ԫ�صĽ�������Ҫ����CaO-SiO2-Al2O3��ϵ������ã������ѳ�Ca�Ļ���ԭ��ΪSiҺ�е�����Ԫ��Ca��CaO-SiO2��Ԫ��ϵ��SiO2����ΪCaO�������С�Ϊ�ˣ�KUME��[1]��WEISS��[2]�о�CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ��1 823~ 1 873 K�¶ȷ�Χƽ��������Ca�ڸ���ϵ��SiҺ��ķ�����ɣ�MIKI��[3-4]�о���Si-Ca��Ԫ������ϵ��Ca�Ļ��aCa��Ca���ϵ����Ca��ZHANG��[5-7]���ż�[8]�Լ�YANG��[9]����¯������-���ӹ��������о�CaO-SiO2��Ԫ¯���ṹ��Ԫ�����Ӷ�(�൱�ڴ�ͳұ��������ѧ�е���Ԫ)����������Ũ��(�൱�ڴ�ͳ������ѧ�еĻ��)���������[5-9]��CaO-SiO2��Ԫ��ϵ�нṹ��Ԫ����������Ũ��Ni������Ԫ�Ļ��ai�������ö�Ӧ��ϵ��
����ǰ�˶�CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ��ƽ�ⷴӦ�о������в��࣬��CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵƽ�ⷴӦ�ı�Ħ��Gibbs��Ӧ�����ܱ仯 Ҳ�˴˲�һ�£�ȱ�ٹ��ϵı���ʽ[10, 13-15]����ˣ����������ڷֱ����¯���� ��-���ӹ������۱���CaO-SiO2��Ԫ��ϵ��Ԫ��Ӧ�����ͻ���Henry���ɱ���Si-Ca��Ԫ������ϵ��Ca�Ļ��aCa�Ļ����ϣ����ڸ�¯��-�������ɵķ��ƽ����ϵ��������Сԭ�����о�CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ����ϵ����䷴Ӧ����ѧƽ�⡣��Ŀ�IJ����ǽ���֤��[5�C9]�����ڸ���ұ��ɷַ�Χ�ڵ�¯������-���ӹ���������չ��Si�����ɷַ�Χ��CaO-SiO2��Ԫ��ϵ����Ԫ��Ӧ����������ͬʱΪCaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ��ɵ�ƽ����ϵ�ṩ������������ȷ�ķ�Ӧ����ѧ���ݺͱ�Ħ��Gibbs��Ӧ�����ܱ仯ͨ�ñ���ʽ��
Ҳ�˴˲�һ�£�ȱ�ٹ��ϵı���ʽ[10, 13-15]����ˣ����������ڷֱ����¯���� ��-���ӹ������۱���CaO-SiO2��Ԫ��ϵ��Ԫ��Ӧ�����ͻ���Henry���ɱ���Si-Ca��Ԫ������ϵ��Ca�Ļ��aCa�Ļ����ϣ����ڸ�¯��-�������ɵķ��ƽ����ϵ��������Сԭ�����о�CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ����ϵ����䷴Ӧ����ѧƽ�⡣��Ŀ�IJ����ǽ���֤��[5�C9]�����ڸ���ұ��ɷַ�Χ�ڵ�¯������-���ӹ���������չ��Si�����ɷַ�Χ��CaO-SiO2��Ԫ��ϵ����Ԫ��Ӧ����������ͬʱΪCaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ��ɵ�ƽ����ϵ�ṩ������������ȷ�ķ�Ӧ����ѧ���ݺͱ�Ħ��Gibbs��Ӧ�����ܱ仯ͨ�ñ���ʽ��
1 ģ�͵Ľ���
1.1 ��ϵ��ƽ������
CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ��¯ ��-�������洦��Ӧ[1, 10]�ɱ���Ϊ
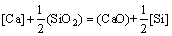 (1)
(1)
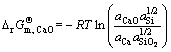 (J/mol) (2)
(J/mol) (2)
ʽ�У�a��ʾ����Ӧ������Ļ�ȡ�
����CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ���ɵ�SiҺ���ѳ�Ca�ľ��������Ƿ�յģ��������ɷ�����֪�����¶�Tһ����CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ����ϵ������������Ԫ��Ũ��(����)ȷ������÷����ϵ��ƽ��״̬��ȷ������CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ�ﵽ����ѧƽ��[12]�ij�ֱ�Ҫ����Ϊ�÷����ϵ����Gibbs��������С��
1.2 ����¯������-���ӹ������۵�CaO-SiO2��Ԫ��ϵ�нṹ��Ԫ��Ӧ��������
1.2.1 CaO-SiO2��Ԫ��ϵ��¯������-���ӹ������ۼٶ�
��������[5-9]������¯������-���ӹ������۵ļ��裬����¯������-���ӹ������۱���CaO-SiO2��Ԫ��ϵ�Ľṹ��Ԫ�����ӶԵ���������Ũ��ʱ����Ҫ����ɸ������£�
1) ��SiҺƽ���CaO-SiO2��Ԫ��ϵ�нṹ��Ԫ��Ca2+��O2-�����ӡ�SiO2���Ӽ�CaO��SiO2��Ϊ�����Ĺ����θ��Ӵ������ɡ�ÿ���ṹ��Ԫ��������ռ�������λ�ã�����ͬһ��Ԫ���������Ӻ������Ӳ����γɸ��Ӵ���ӷ�Ӧʱ����(Me2++O2-)�����������Ӷ���ʽ���뷴Ӧ��
2) �����ӶԺͼ������ɸ��Ӵ���ӵķ�Ӧ���ֻ�ѧ��̬ƽ�⣻
3) ��һ���¶Ⱥ�Ũ�ȷ�Χ�ڣ���Si-Ca��Ԫ������ϵ��Ӧ��CaO-SiO2��Ԫ��ϵ�����нṹ��Ԫ���������ԣ�
4) �γɸ��Ӵ���ӵĻ�ѧ��Ӧ�����������ö��ɡ�
1.2.2 CaO-SiO2��Ԫ��ϵ�нṹ��Ԫ�����ӶԼ�����������Ũ��
����ǰ��������CaO-SiO2��Ԫ��ϵ��¯������-���ӹ�������[5-9]�Ļ��������Լ���SiҺ�������¶ȷ�Χ��(1 823~1 873 K)��CaO-SiO2��Ԫ��ϵ����ͼ��CaO-SiO2��Ԫ��ϵ�д������ָ��Ӵ����2CaO��SiO2��CaO��SiO2������¯������-���ӹ�������[5-9]��¯���нṹ��Ԫ����������Ũ��Ni������ʽ������
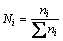 (-) (3)
(-) (3)
��¯������(Me2++O2-)���������Ӷԣ�����������Ũ��NMeO�ɱ���Ϊ
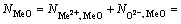
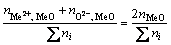 (-) (4)
(-) (4)
ʽ�У�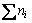 Ϊ¯��-������Ӧƽ��ʱһ��������¯�������нṹ��Ԫ��Ħ�����ܺͣ�mol��niΪ¯��-������Ӧƽ��ʱһ��������¯���нṹ��Ԫi��Ħ������mol��
Ϊ¯��-������Ӧƽ��ʱһ��������¯�������нṹ��Ԫ��Ħ�����ܺͣ�mol��niΪ¯��-������Ӧƽ��ʱһ��������¯���нṹ��Ԫi��Ħ������mol��
���о���100 g¯������Ϊ�����м��㡣��Ȼ������¯������-���ӹ�������[5-9]�����CaO-SiO2��Ԫ��ϵ�нṹ��Ԫ��Ni��������ѧ����ΪĦ����������¯�������нṹ��Ԫ��N i֮��Ϊ1.0����
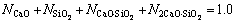 (-) (5)
(-) (5)
�Դ�����Ϊ��̬��Ħ������ΪŨ�ȵ�λ�ľ���ұ��������ѧ�������¯����Ԫ�Ļ��ai��¯����Ԫ����������Ũ��Ni����������һ�£������ڱ������������ϵ�и�¯����Ԫ�Ĵ����ʱ�Ħ��Gibbs������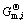 �ɲ�����������Ũ��Ni������ai����¯������Gibbs������(Gi)�ɱ���Ϊ
�ɲ�����������Ũ��Ni������ai����¯������Gibbs������(Gi)�ɱ���Ϊ
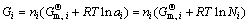 (J) (6)
(J) (6)
1.3 Si-Ca��Ԫ������ϵ����Ԫ�Ļ��
Si-Ca��Ԫ������ϵ��SiΪ�ܼ������ȷ���Raoult���ɣ�Si�Ļ�����Ӧ�Si��1.0�ƣ�SiҺ�е�Ca�Ļ��aCa����Henry���ɡ��о�����[3]��Si-Ca��Ԫ������ϵCa������Ӧ�Ca�ɱ���Ϊ
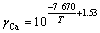 (-) (7)
(-) (7)
��ˣ�Si-Ca��Ԫ������ϵ�У�aSi��1.0��aCa=xCa��Ca��
1.4 CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ���ɵķ����ϵ��Ħ��Gibbs�����ܱ���
������Ķ�������ϵ�����¶Ⱥ�ѹ��ȷ������ϵ�����з�Ӧ�ﵽ����ѧƽ��ij�ֱ�Ҫ�����Ǹ÷����ϵ�ܵı�Ħ��Gibbs��������С���Ҹ���ϵ�еĸ�Ԫ���������غ�[12]����һ������CaO-SiO2��Ԫ��ϵ��һ������Si-Ca��Ԫ������ϵ��ɵķ����ϵ����Gibbs������Gs�ɱ���Ϊ
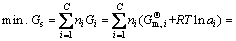
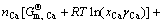
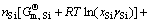
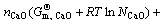


 (J) (8)
(J) (8)
ʽ�У�min. GsΪGs��Сֵ��CΪ��ϵ���ܵ���Ԫ������6��(-)��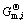 Ϊ��Ԫi��ṹ��Ԫi�ı�Ħ��Gibbs�����ܣ�J/mol��ni Ϊ100 g¯����100 g SiҺ����Ԫi�ﵽ��-��Ӧƽ��ʱ��Ħ������mol��ai Ϊ¯������Ԫi��SiҺ����Ԫi�Դ�����Ϊ��̬�Ļ�ȣ�(-)��xi ΪSiҺ����
Ϊ��Ԫi��ṹ��Ԫi�ı�Ħ��Gibbs�����ܣ�J/mol��ni Ϊ100 g¯����100 g SiҺ����Ԫi�ﵽ��-��Ӧƽ��ʱ��Ħ������mol��ai Ϊ¯������Ԫi��SiҺ����Ԫi�Դ�����Ϊ��̬�Ļ�ȣ�(-)��xi ΪSiҺ����
Ԫi��Ħ����������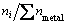 ��(-)��Ni Ϊ¯���и��ṹ��Ԫ����������Ũ�ȣ���Ħ������
��(-)��Ni Ϊ¯���и��ṹ��Ԫ����������Ũ�ȣ���Ħ������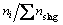 ��(-)��
��(-)��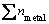 Ϊ100 g SiҺ����Ԫ����Ħ������mol��
Ϊ100 g SiҺ����Ԫ����Ħ������mol��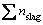 Ϊ100 g¯���нṹ��Ԫ����Ħ������mol����
Ϊ100 g¯���нṹ��Ԫ����Ħ������mol����
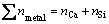 (mol) (9)
(mol) (9)
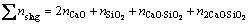 (mol) (10)
(mol) (10)
ʽ(10)�е�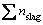 ��ʽ(4)�е�
��ʽ(4)�е�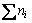 ����ֵ������������ȫһ������100 g ��CaO-SiO2��Ԫ��ϵ��100 g ��SiҺ���ɵķ����ϵ�ж���Ԫ��ΪCa��Si��O���������غ㡣Ca��Si��O���������غ����ʽΪ
����ֵ������������ȫһ������100 g ��CaO-SiO2��Ԫ��ϵ��100 g ��SiҺ���ɵķ����ϵ�ж���Ԫ��ΪCa��Si��O���������غ㡣Ca��Si��O���������غ����ʽΪ
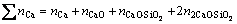 (mol) (11)
(mol) (11)
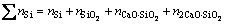 (mol) (12)
(mol) (12)
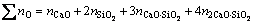 (mol)(13)
(mol)(13)
��Ȼ��ʽ(8)ΪĿ�꺯����ʽ(9)~(13)ΪԼ����������ʽ(8)��Gs�ﵽ��Сֵʱ���÷����ϵ��Ӧ�ﵽƽ�⡣���о�����Lingo 6.0���������1 823 K��1 873 Kʱ����ͬCa����Si-Ca��Ԫ������ϵ��Ӧ��ƽ��CaO-SiO2��Ԫ��ϵ�����нṹ��Ԫ����������Ũ��Ni�����õ�CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ���ɵķ����ϵ���������ി���ʱ�Ħ��Gibbs������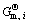 ���1[11]���С�
���1[11]����
2 ���������
2.1 ģ�ͼ�����
����ǰ������������ѧģ�ͣ�������[1-2]������1 823 K��1 873 K�¶�ʱCaO-SiO2��Ԫ��ϵ��ӦSi-Ca��Ԫ������ϵƽ����ֽ��м��㣬������2���С�Ϊ�˱Ƚϣ�������[1-2]������Si-Ca��Ԫ������ϵƽ��ʵ������Ҳ�ܽ��ڱ�2��
��1 CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ�и���Ԫ��ṹ��Ԫ�ı�Ħ��Gibbs����������[11]
Table 1 Standard molar Gibbs free energies of all possible species or structural units in both CaO-SiO2 binary slags and Si-Ca binary metal system[11]
����[1-2]�����ͱ��о�������¶�Ϊ1 823 K��1 873 KʱSiҺ��Ca��Ħ������xCaO��CaO-SiO2��Ԫ��ϵ��CaO��Ħ������xCaO(xCaO��0.5)�ı仯��ϵ��ͼ1��ʾ����ͼ1��֪�����о�����Ľ��������[1-2]������ʵ�����ǺϽϺá����¶����ߣ�CaO- SiO2��Ԫ��ϵ����ͬCaOĦ������xCaO��Ӧ��ƽ��SiҺ��CaĦ������xCa��С����������¶���1 823 K��ߵ�1 873 K�������ڸö�Ԫ��ϵ��Si������Ԫ��Ca���ѳ���������ϵ��xCaO��0.4ʱ������¯����xCaO��SiҺ��xCaӰ���С��¯����xCaO��0.4ʱ������¯����xCaO��SiҺ��xCa�������ӡ���������ڸ�CaO������¯���ɷַ�Χ�ڣ�����CaO�������������ѳ�SiҺ��Ca��������������������Ca��SiҺ�еĺ�������ȻCaO�����ϵ͵ĸö�Ԫ��ϵ�������ѳ�SiҺ������Ca�������͵�CaOʹ�ø���ϵ��Ԫ���(w(CaO)/w(SiO2))���٣�¯����������ʹ�ø���ϵ¯�������Ա�����¯��-�����䷴Ӧ���ʣ��������¯����SiҺ���Է��롣��Ȼ��0.3��xCaO��0.4�������ڸö�Ԫ��ϵ�ѳ�SiҺ������Ԫ��Ca��
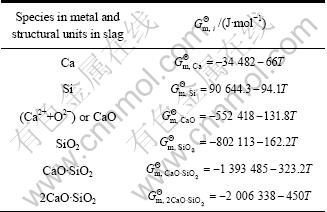
��2 CaO-SiO2 ��Ԫ��ϵ��Si-Ca��Ԫ������ϵƽ��ʵ��ʵ�����ݺ�ģ�ͼ������ıȽ�[1-2]
Table 2 Comparison of measured compositions of CaO-SiO2 binary slags equilibrated with Si-Ca binary metal system and calculated results[1-2]
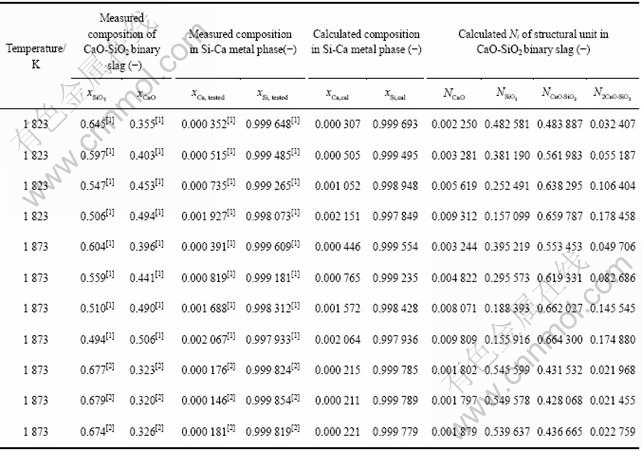
ͼ1 �¶�Ϊ1 823 K��1 873 KʱCaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵƽ����ϵ��CaO��Ħ������xCaO��SiҺ��Ca��Ħ������xCa֮���ϵ
Fig. 1 Relationship between mole fraction of CaO in CaO-SiO2 binary slags and mole fraction of Ca in Si-Ca binary metal system at 1 823 K and 1 873 K
2.2 CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ����Ԫ��Ӧ�������ȼ�Ĺ�ϵ��¯��-������Ӧ��
2.2.1 CaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵ����Ԫ��Ӧ�������ȼ�Ĺ�ϵ
ǰ������������¯�����ӨC���ӹ�������[5�C9]�������¯���ṹ��Ԫ����������Ũ��Ni�뾭��ұ��������ѧ�������¯����Ԫ���aiһ������¯����Ԫ��Ӧ��������ˣ�ʽ(1)��ʾ��CaO-SiO2��Ԫ��ϵ�ѳ�Si-Ca��Ԫ������ϵ��Ca�ķ�Ӧƽ�ⳣ��K�ɱ���Ϊ
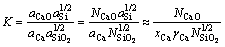 (�C) (14)
(�C) (14)
ʽ(14)�ɱ���Ϊ
 (�C) (15)
(�C) (15)
��Ȼ��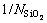 ��aCa/NCaOӦ�������õĶ��η���ϵ�����ñ��о��õ���
��aCa/NCaOӦ�������õĶ��η���ϵ�����ñ��о��õ���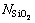 ��NCaO�ֱ���
��NCaO�ֱ��� ��
��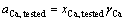 �õ���
�õ���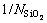 ��aCa/NCaO�ֱ�ʾ��ͼ2����Ȼ�������
��aCa/NCaO�ֱ�ʾ��ͼ2����Ȼ�������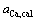 �����ʵ�����ݱ���
�����ʵ�����ݱ��� ʮ���Ǻϡ����������¯�����ӨC���ӹ�������[5�C9]����õ���SiҺ�����ɷ����÷�Χ�ڵ�CaO-SiO2��Ԫ��ϵ��CaO��SiO2����������Ũ��Ni��ȷ��������ϵ�ķ�Ӧ���������ݼ����
ʮ���Ǻϡ����������¯�����ӨC���ӹ�������[5�C9]����õ���SiҺ�����ɷ����÷�Χ�ڵ�CaO-SiO2��Ԫ��ϵ��CaO��SiO2����������Ũ��Ni��ȷ��������ϵ�ķ�Ӧ���������ݼ����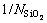 ��aCa/NCaO��ϳ���K1 823��K1 873�ֱ�Ϊ5 061��4 322.7��
��aCa/NCaO��ϳ���K1 823��K1 873�ֱ�Ϊ5 061��4 322.7��
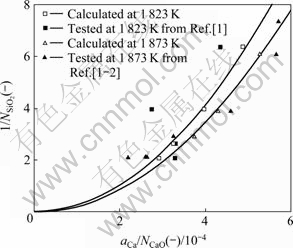
ͼ2 �¶�Ϊ1 823 K��1 873 KʱCaO-SiO2��Ԫ��ϵ��Si-Ca��Ԫ������ϵƽ����ϵ��aCa/NCaO��aSi/NSiO2�Ĺ�ϵ
Fig. 2 Relationship between aCa/NCaO and aSi/NSiO2 with aCa, cal and aCa, tested presenting aCa in close system composed of CaO-SiO2 binary slags and Si-Ca binary metal system at 1 823 and 1 873 K
2.2.2 ¯��-�����䷴Ӧ�ı�Ħ����ӦGibbs�����ܱ仯
����2.2.1��ȷ����K1 823��K1 873������CaO-SiO2��Ԫ��ϵ�ѳ�SiҺ��Ca��Ӧ�ı�Ħ��Gibbs��Ӧ�ܱ仯 ��ƽ�ⳣ��K�Ĺ�ϵ
��ƽ�ⳣ��K�Ĺ�ϵ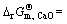
 ����ȷ����1823 K��1873 Kʱ��
����ȷ����1823 K��1873 Kʱ�� ���ݴ˻ع����
���ݴ˻ع���� ����ʽΪ
����ʽΪ
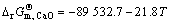 (J/mol) (16)
(J/mol) (16)
���о��õ����¶���1 823~1 873 K��Χ ������[13�C15]��������¶ȷ�Χ�ڵ�
������[13�C15]��������¶ȷ�Χ�ڵ� �ֱ�ʾ��ͼ3����ͼ3��֪����1 823~1 873 K�¶ȷ�Χ�ڣ�WAKASUGI��SANO[13]ȷ����
�ֱ�ʾ��ͼ3����ͼ3��֪����1 823~1 873 K�¶ȷ�Χ�ڣ�WAKASUGI��SANO[13]ȷ���� ����о��õ�
����о��õ� �Ĵ�֮��MIN��SANO[15]ȷ����
�Ĵ�֮��MIN��SANO[15]ȷ���� ��С��SATA��[14]ȷ����
��С��SATA��[14]ȷ���� ��С����MIN��SANO[15]��WAKASUGI��SANO[13]ȷ����
��С����MIN��SANO[15]��WAKASUGI��SANO[13]ȷ���� �뱾�о��õ���
�뱾�о��õ��� ����о��õ���
����о��õ��� ��WAKASUGI��SANO[13]ȷ����
��WAKASUGI��SANO[13]ȷ���� ����ֵΪ9 303.32 J/mol��SATA��[14]��WAKASUGI��SANO[13]ȷ����
����ֵΪ9 303.32 J/mol��SATA��[14]��WAKASUGI��SANO[13]ȷ���� ����ֵ30 111 J/mol��MIN��SANO[15]��WAKASUGI��SANO[13]ȷ����
����ֵ30 111 J/mol��MIN��SANO[15]��WAKASUGI��SANO[13]ȷ���� ����ֵ14 392.7 J/mol��WAKASUGI��SANO[13]ͨ��ʵ��ָ�����ϴ��
����ֵ14 392.7 J/mol��WAKASUGI��SANO[13]ͨ��ʵ��ָ�����ϴ�� ֵ��Ϊ���������о�ȷ����
ֵ��Ϊ���������о�ȷ���� ��WAKASUGI��SANO[13]ͨ��ʵ��ȷ����
��WAKASUGI��SANO[13]ͨ��ʵ��ȷ���� ��Ϊ�ӽ����ұ��о�������ģ�ͶԸ���Ԫ���������Ϊȷ������������ӿɿ���
��Ϊ�ӽ����ұ��о�������ģ�ͶԸ���Ԫ���������Ϊȷ������������ӿɿ���

ͼ3 [Ca]+0.5(SiO2)=(CaO)+0.5[Si]��Ӧ�ı�Ħ����ӦGibbs�����ܱ仯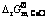 �ıȽ�
�ıȽ�
Fig. 3 Comparison of obtained standard molar reaction Gibbs free energy change 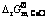 for [Ca]+0.5(SiO2)=(CaO)+ 0.5[Si] by present study and other researchers
for [Ca]+0.5(SiO2)=(CaO)+ 0.5[Si] by present study and other researchers
3 ����
1) ����ƽ����ϵGibbs��������Сԭ���Ծ���SiҺ������Ca��¯��-������ϵ����������ѧģ�ͣ�������ѧģ�͵õ���SiҺ��Ca��Ħ������xCa��CaO-SiO2��Ԫ��ϵCaO��Ħ������xCaO�Ľ�������ױ�����ʵ���������Ǻϣ���0.3��xCaO��0.4��������SiҺ��Ca��
2) ����������ѧģ�ͼ�����������SiҺ��Si��Ca�Ļ�ȷֱ���SiO2��CaO��������Ũ�ȵı�ֵ����¯��-��������Ԫ���֮��Ĺ�ϵʽ���Ҽ����������ױ��������ݾ��ȸ��ߡ���ˣ�����¯�����ӨC���ӹ������۵���������Ũ�ȿ��뾭���¯�����û��һ������CaO-SiO2��Ԫ��ϵ��Ԫ�ķ�Ӧ������
3) ������ѧģ�ͼ�����ȷ����¯��-�����䷴Ӧ[Ca]+0.5(SiO2)=(CaO)+0.5[Si]�ı�Ħ����Ӧ�����ܱ仯����ʽΪ =-89 532.7-21.8T J/mol��
=-89 532.7-21.8T J/mol��
REFERENCES
[1] KUME K, MORITA K, MIKI T, SANO N. Activity measurement of CaO-SiO2-AlO1.5-MgO slags equilibrated with silicon alloys[J]. ISIJ International, 2000, 40(6): 561-566.
[2] WEISS T, SCHWERDTFEGER K. Chemical equilibria between silicon and slag melts[J]. Metallurgical and Materials Transactions B, 1994, 25(4): 497-504.
[3] MIKI T, MORITA K, SANO N. Thermodynamic properties of aluminum, magnesium, and calcium in molten silicon[J]. Metallurgical and Materials Transactions B, 1999, 29(5): 1043-1049.
[4] MIKI T, MORITA K, SANO N. Thermodynamic properties of Si-Al, -Ca, -Mg binary and Si-Ca-Al, -Ti, -Fe ternary alloys[J]. Materials Transactions (JIM), 1999, 40(10): 1108-1116.
[5] ZHANG Jian. The application of the law of mass action in combination with the coexistence theory of slag structure to the multicomponent slag systems[J]. Acta Metallurgica Sinica, 2001, 14 (3): 177-190.
[6] ZHANG Jian. Applicability of mass action law to sulphur distribution between slag melts and liquid iron[J]. Journal of University of Science and Technology Beijing, 2002, 9 (2): 90-98.
[7] ZHANG Jian. Application of annexation principle to the study of thermodynamic properties of ternary molten salts CaCl2-MgCl2-NaCl[J]. Rare Metals, 2004, 23 (3): 209-213.
[8] �� ��. ұ������ļ�������ѧ[M]. ����: ұ��ҵ������, 2007.
ZHANG Jian. Computational thermodynamics of metallurgical melts and solutions[M]. Beijing: Metallurgical Industry Press, 2007.
[9] YANG Xue-min, JIAO Jin-sha, DING Ru-cai, SHI Cheng-bin, GUO Han-jie. A thermodynamic model for calculating sulphur distribution ratio between CaO-SiO2-MgO-Al2O3 iron making slags and carbon saturated hot metal based on the ion and molecule coexistence theory[J]. ISIJ International, 2009, 49 (12): 1828-1837.
[10] WANG Xin-guo, DING Wei-zhong, TANG Kai, JIANG Guo-chang, XU Kuang-di. Experimental thermodynamic research on equilibrium between silicon alloy and SiO2-CaO- Al2O3 melt[J]. Transactions of Nonferrous Metals Society of China, 2001, 11(4): 535-539.
[11] BARIN I. Thermochemical data of pure substances[M]. 3rd ed (part��,��). Weinheim: Federal Republic of Germany, 1995.
[12] WHITE W B, JOUNSON S M, DANTZIC G B. Chemical equilibrium in complex mixtures[J]. The Journal of Chemical Physics, 1958, 28(5): 751-755.
[13] WAKASUGI T, SANO N. Re-evaluation of standard free energy of formation of CaO[J]. Metallurgical and Materials Transactions B, 1989, 20(3): 431-433.
[14] SATA T, SASAMOTO T, MATSUMOTO K. High-temperature vaporization of calcium oxide[J]. High Temperatures-High Pressures, 1982, 14(4): 399-408.
[15] MIN D J, SANO N. Determination of standard free energies of formation of Ca3P2 and Ca2Sn at high temperatures[J]. Metallurgical and Materials Transactions B, 1988, 19(3): 433-439.
(�༭ ����)
�ո����ڣ�2011-01-05�������ڣ�2011-05-19
ͨ�����ߣ���ѧ��ʿ���绰��010-82622893��E-mail: yangxm71@hom.ipe.ac.cn