DOI��10.19476/j.ysxb.1004.0609.2018.11.25
��β������ϸ����ž�Ⱥ��ṹ���������˾��������
�����Σ������ɣ��� �棬�� �裬̷�ķ��������࣬������
(�ϻ���ѧ ��Ⱦ��������Դ����������ʡ��У�ص�ʵ���ң����� 421001)
ժ Ҫ��Ϊ�˿�����β����������������Ⱥ��ṹ��ͨ����ͨ������������ϸ����ž�Ⱥ��ṹ�������з��봿�����˾��������з�������ѧ������ͨ����ͨ�����ֱ���42706��ϸ����34346���ž�����Ч���С�����Alpha�����Է������֣�ϸ�����ࡢȺ��ḻ��������Ծ����ڹž��ġ�ͨ��ϸ��Ⱥ��ṹ����������Carnobacterium��Enterococcus��Comamondadaceae��Cronobacter��4�������β�������д��ڣ�������ȷֱ�Ϊ3.14%��2.58%��0.83%��0.53%�������������˾�ΪBacillus (49.6%)��Lactococcus (31.9%)��Streptococcus (2.87%)��Caulobacter (0.89%)��Pseudomonas (0.72%)��Enterobacter (0.62%)��ͨ���ž�Ⱥ��ṹ��������ʾ��Candidatus Nitrosotalea(74.03%)��Methanosaeta(6.37%)��Methanobacterium(3.25%)��Crenarchaeotic(3.23%)��Terrestrial Miscellaneous(1.25%)��5��ž�����β�������д��ڼ����ȡ�����β�������з����5�����˾�������������ѧ��������A1��B2�ֱ�ΪKlebsiella sp.��Acinetobacter johnsonii��������C2��D2��E2������Pseudomonas cedrina���֡�
�ؼ��ʣ���β������Ⱥ�䣻��ͨ�����ž�
���±�ţ�1004-0609(2018)-11-2383-10���� ��ͼ����ţ�X172���� ���ױ�־�룺A
�����й��˹�ҵ�ķ��ٷ�չ���Է������˵����������˿Ͽ����������������β��Ĵ������档��β���Ǵ����˿�ʯ���ɿ������������ͷ����Է����ij��������з����Ժ��غ��ؽ��������ߡ���Ⱦ��Χ���Σ�������Ե�����[1]����ΰ�ȫ����Ч�ͺĽ�����β����Ⱦ������������Ϊ�˹�ҵ�뻷�������������Ҫ���⡣
ͨ����������������Ⱦ���ƣ������ܺĵ͡���ɫ�����ص㣬�ܵ��о��߹㷺����[2]��Ŀǰ���н϶��ͷ��������[3]�������λ�ԭ��[4]��ϣ���Ͼ�[5]��������˽�����������ԭ�ı�����Ȼ��������β�����������������[6]�����������˾��ķ���[7]���ǽ���ԭλ�������Ļ�������������[8]�ó�������������۷���Biolog�����о�����β��������������Լ�Ⱥ�书�ܶ���������������ͨ������ȣ�β��������������Է����������仯�������������Ϳ�����ϸ�������������͡���������[9]���ó���ϡ��ƽ�巨�� Biolog-Eco ƽ�巽�����о��˸ߡ��С�����Ⱦ���������������������ַ�������Ⱦ�Ӹߵ���ȡ�����У�����������СΪϸ��>���>���߾�����Ψ���[10]���û���оƬ����������������������������Ⱦ����ˮ�Ĺ���������м�⣬������U(��)��ԭ�йص��������������Desulfosporosinus spp.��Anaeromyxobacter spp.�����˾���
�����о���������β���д����ܹ����˵������(Ⱥ)��������Ŀǰ��ȱ�ٶ���β��������ϸ���ž�Ⱥ��ṹ��������ı�������������ͨ����ͨ���������������Ϸ�ij��β��������ϸ�����ž���������Ⱥ��ṹ�����������˾������룬����Ϊ��β�����������ṩ����ѧ������
1 ʵ��
1.1 ��Ʒ�ɼ�
������λ���ҹ��ϲ�ijʡ��β���ÿ�ӣ���ȥ���������ѡȡ��������20 cmλ�ã��ɼ�500 g������Ʒ����������Ʒ�ܷ����ڱ��У���������ʵ���ң���-20 �������±��汸�á�����⣬�����ܶ�Ϊ1.03~1.05 g/cm3����ˮ��8.2%~9.0%����������Ũ��Ϊ47~60 mg/kg��Զ���й�������������ֵ2.8 mg/kg(�˿�ұ��������ͻ��������涨GB 23727��2009)�����⣬����Ʒ�м����ӡ�ͭ��п��Ǧ����Щ�ؽ��������������˹�����������������������
1.2 ������DNA��ȡ��PCR����
ȡ1 g��β���������������λ���Һ(PBS��pH=7.0)��ϴ3�Σ�ʹ��OMEGA ��˾ E.Z.N.A Soil DNA�Լ�����ȡ���������DNA[11]������ϸ��16S rDNA ͨ������338F/806R����PCR����V3+V4��Ƭ��[12]��ʹ��TransStart Fastpfu DNA�ۺ�ø(TransGen AP221-02)��20 ��L��Ӧ��ϵ����ABI GeneAmp 9700��PCR���Ͻ���PCR��������������Ϊ��95 �����3 min��27������ѭ��������95 �����30 s��55 ���˻�30 s��72������45 s�����Σ���72 ��������10 min�������10 ���������á�����524F/Arch958R�����ž�16S rDNA����Ƭ��[13]������ѭ��35�Σ�������������ͬϸ��PCR������ÿ������3���ظ�����PCR�����Ϻ���2%��֬��������Ӿ��⣬ʹ��AxyPrepDNA���������Լ���(AXYGEN��˾)�н�����PCR���
9700��PCR���Ͻ���PCR��������������Ϊ��95 �����3 min��27������ѭ��������95 �����30 s��55 ���˻�30 s��72������45 s�����Σ���72 ��������10 min�������10 ���������á�����524F/Arch958R�����ž�16S rDNA����Ƭ��[13]������ѭ��35�Σ�������������ͬϸ��PCR������ÿ������3���ظ�����PCR�����Ϻ���2%��֬��������Ӿ��⣬ʹ��AxyPrepDNA���������Լ���(AXYGEN��˾)�н�����PCR���
1.3 ��ͨ�����������ݷ���
ͨ������Miseq PEƽ̨(Illumina������)���и�ͨ��������õ���PE reads���ȸ���overlap��ϵ����ƴ�ӣ�ͬʱ���������������ʿغ��ˣ���������֮���������0.97��Ϊ��ֵ���ֲ������Ԫ(OTU)����Usearch����ƽ̨(Version 7.1)����OUT����������Rank-Abundance���ߡ���������Alpha������ָ������Ҫ����Chao��Ace��Sobs��Shannon��Simpson��Coverage�ȡ����⣬�����н�������������Գ鵽�������������������� OTU ����Ŀ����ϡ������[14]��ѡ��Silva���ݿ����16S rRNA�������бȶԣ����ƾ������ͼ������FastTree����(Version 2.1.3)��ѡ����ˮƽ�Ϸ�����Ϣ��Ӧ�����У����������Ȼ������ϵͳ��������
1.4 ���˾����뼰��16S rDNA����
����ϵ��ϡ�ͷ�����1 g����ϡ�ܽ���9 mLˮ�У�Ȼ��ֱ��ͳ�1��10-2��1��10-3��1��10-4��1��10-5��1��10-6 g/mL��5��Ũ�ȣ��ֱ���ֵ�LB�����������Ͻ���ƽ�廮�ߡ�����5��ƽ�廮�ߣ�������ĵ���������ֵ�Һ���������У�30 ���»18~24 h������ҺOD600ֵ��1~2֮��ʱ����10% (v/v)���ֵ�װ��10 mg/L�˵�Һ������������ƿ�У���ת��Ϊ150 r/min���¶�Ϊ30 ������������������ⶨ24 h����˵�ȥ�������ѡȡ����Ч����õ�5�־����ֱ�����ΪUSC A1��USC B2��USC C2��USC D2��USC E2��
���ջ�����DNA��ȡ�Լ���(�������)����˵������ϸ��DNA��ȡ����������27F/ 1492R����16S rDNA����PCR��������Ϊ��98 �����2 min��35������ѭ��������98 �����10 s��55 ���˻�10 s��72 ������20 s�����Σ���72 ������10 min�������4 ���������á���PCR�������������֬��������Ӿ��������DNA���и���ռ�������⣬��ABI 3730XL�����Dz���ƴ�ӡ���5��ϸ���������ύ��Genbank����õ�¼�ŷֱ�ΪMF083942��MF083941��MF476206��MF476207��MF476208����NCBI���ݿ���ͨ��BLAST���������������У������ý��ͨ��Mega 7����[15]������Neighbor-Joining �������ȶ�����1000�Σ�������������룬����ϵͳ����������ɶ����˾��ķ�������ѧ������
2 ���������
2.1 ����������OTU����
��ϸ�����о���ͨ�������������ʿأ�ȥ��������Ҫ������У��ֱ���42706��34346����Ч���У�������1���С�ϸ��ƽ����Ϊ449bp���������г�����441~460bp֮����40171����ռ�����е�94%��������2528�����г�����421~440bp֮�䣬����ԼΪ6%���ž�ƽ�����г���Ϊ448bp���������г�����441~460bp֮����33020����ռ�����е�96%�� ������461~480bp��481~500bp֮������������ֱ�Ϊ240��775��
��1 ϸ����ž���ͨ��������
Table 1 High-throughput sequencing results of bacteria and archaea

�����������ƶ�97%����OTU��ϸ����OTU����(145)���Զ��ڹž�����(20)����ӳϸ��������ࡣͳ��ÿ��OTU���������������Դ�Ϊ�����꣬��OTU�ȼ�Ϊ��������ͼ���õ�Rank-Abundance���ߣ���ͼ1��ʾ����ˮƽ���������ں����ϵķ�ΧԽ��ӳ���ֵķ��Խ�ߣ���������Խƽ����˵�����ֲַ�Խ���ȡ���ͼ1��֪��ϸ�������ַ�Ⱥ;��ȶȶ��ȹž�Ҫ�ߣ�˵������β����ϸ�����������Ҫ��ɲ��֡�

ͼ1 ϸ����ž�Rank-Abundance����
Fig. 1 Rank-Abundance curve of bacteria (a) and archaea (b)
2.2 ����Alpha�����Է���
���㲻ͬ��������µ�Alpha������ָ����������2���С�Coverage����ȡ����ȣ�ϸ��CoverageΪ0.99955���ž�Ϊ1����ӳ����������û�б�����ĸ��ʼ��ͣ��dz��õش�����������ʵ�����Ace��Chao��Sobsָ������ӳȺ��ḻ�ȣ�������ֵ��С����ء��ӱ�2��֪��ϸ����Ace��Chao��Sobs���Ը��ڹž��ģ���ӳϸ��Ⱥ��ḻ��Ҫ�ߺܶࡣShannonָ����Simpsonָ�������Է�ӳ����Ⱥ������ԣ������Դ�С��Shannonָ����ֵ����أ�����Simpsonָ������ء��ӱ�2��֪��ϸ����Shannon�ϴ�Simpsonָ����С����ӳ��β����ϸ�������Ը��ڹž���
�����������ȡ������Ϊ�����꣬�ֱ�����Ӧ��Ace��Chao��Sobsָ��Ϊ�����꣬���Ƴ��ḻ��ϡ�����ͼ���ֱ�����Ӧ��OTU��Shannon��Simpsonָ��Ϊ�����꣬���ƶ�����ϡ�����ͼ�������ͼ2��ʾ��������ϸ�����ǹž����ḻ��ϡ�����ߺܿ�����ƽ̹��˵��ȡ���������������ܺܺõط�ӳȡ����ȡ�

ͼ2 ϸ����ž�Alpha�����Է���ͼ
Fig. 2 Alpha diversity charts of bacteria (a) and archaea (b)
��2 ����Alpha������ͳ�Ʊ�
Table 2 Alpha index of microbial diversity

������ϡ�����ͼ�����������ﵽ��ӽ����ͣ�������ʵ�����õ�ϸ����ž�������Ϣ��ȫ��ط�ӳ��������ԡ�
2.3 ϸ����ž�Ⱥ��ṹ����
ϸ���ž�����(genus)ˮƽ�����ַ�ȼ���Ӧ������������ͼ3��ʾ��������ռ����С��0.5%������ͳ���ܱ������á�Other����ʾ����ͼ3(a)��֪��ϸ�����������ɴ�С�ֱ�ΪBacillus (49.6%)��Lactococcus (31.9%)��Carnobacterium (3.14%)��Streptococcus (2.87%)��Enterococcus (2.58%)��Caulobacter (0.89%)��Comamondadaceae (0.83%)��Pseudomonas (0.72%)��Enterobacter (0.62%)��Cronobacter (0.53%)��Others����Ϊ5.62%��δ֪����(unclassified)����Ϊ0.69%��
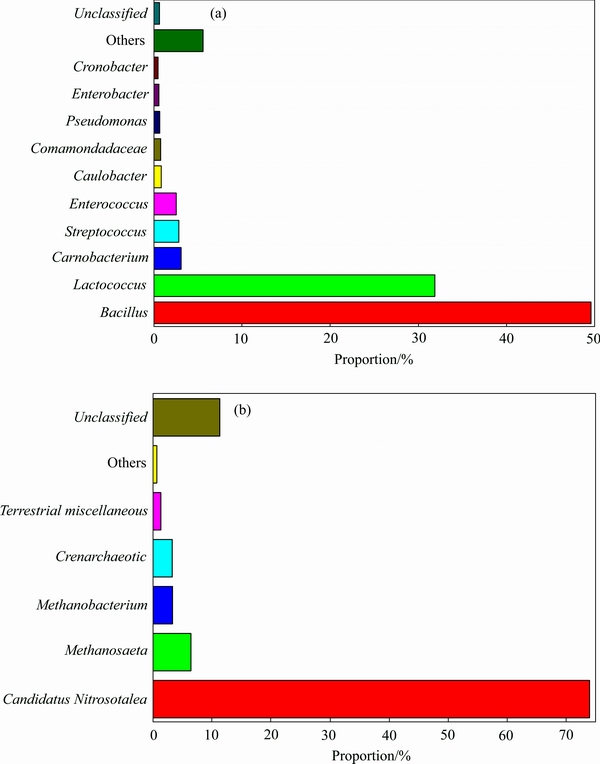
ͼ3 Genusˮƽ��ϸ����ž����ַ��ͼ
Fig. 3 Abundance of microbial species of bacteria (a) and archaea (b) in genus level
Bacillus(�ݲ�ѿ�߸˾�)����β����������ռ��������ϸ�����ӽ�ϸ��������һ�룬���б����������������õ������������˸���Ч�����������ֵ�[16]�о���������˵��������ɴ�512.5 mg/g(����)���������̷����ʺ�Freundlichģ�ͣ�˾�۵�[17]�о����֣���ʼ��Ũ��Ϊ 25~100 mg/Lʱ���ݲ�ѿ�߸˾����������������Ҷ��˾��и�����������Ҫ������λΪϸ���ڣ�Լռ��������������89%��Lactococcus(�����)����β����������ռ�����ڶ���ϸ�����ӽ�ϸ������������֮һ��OBEID��[18]�о����֣�����Ũ��Ϊ10~150 ��mol/Lʱ�������ϸ���ڵĹ������ܹ����������˶��ԣ��ⶾ�����ǹ������е��Ȼ���U(��)�����γɲ����Եĸ����
Streptococcus(�����)����������һ�����ƾ�����ռ����Ϊ2.87%��MISHRA��[19]��Streptococcus lactis��ϵ��������ϣ�����U(��)�������о���������֣��˵�����������������״�й��������������Բ��״��̬�ṹ�ɻ�������������10 min������ȡ������85%��2%����pH5.0���¶�25 ��ʱ��U(VI)�������������(qmax)Ϊ169.5 mg/g��Caulobacter ������ռ����Ϊ0.89%����ǰBRZOSKA��[20]������Ⱦ���Գ������з���õ�Caulobacter sp. OR37��������3�����ﰴ�ȱ�����ϣ���200 ��mol/L�����������У�����30������������������ȻΪ���ƾ��֣���ʾ�����õ�����������
Pseudomonas(�ٵ�����)��ռ����Ϊ0.72%�������о�����Pseudomonas���˾��кܸߵ�����Ч������������[21]�����ε�[22]��ʮ��̲�˿��мٵ����������Խ����о����������������������ʵ�鼰16S rDNA�������м��������п������ļٵ�������ҪΪPseudomonas stutzeri��Pseudomonas putida����PCR-DGGE��ʾPseudomonas stutzeri�Ǹÿ��е����Ƽٵ�������Enterobacter(���˾���)��ռ����Ϊ0.62%���þ���������β����г���[23]�����ܹ����������������Ч�����˶���[24]���������ؽ���Ҳ�������õ���������[25]��
�����4�־���Carnobacterium��Enterococcus��Comamondadaceae��Cronobacter�����Ǵ�ǰû���ں��˻����еı�����Carnobacterium������ʳ�˾�����������������ѿ�ߡ� EnterococcusΪ������������������ԣ�ϸ�����λ���Բ�Σ������������Comamondadaceae��Cronobacter���ױ������١�����ͨ����ͨ���������������˴�ǰ��δ����β���б����ľ�������֤�˸�ͨ��������һ���ܹ���Ч�����������Եķ�������ѧ��������������ھ������������Ϣ��
��ͼ3(b)��֪���ž�������ɽϼ��������ɴ�С�ֱ�ΪCandidatus Nitrosotalea (74.03%)��Methanosaeta (6.37%)��Methanobacterium (3.25%)��Crenarchaeotic (3.23%)��Terrestrial Miscellaneous (1.25%)������δ֪���б���֮��Ϊ11.29% (unclassified)��others(������������С��0.5%������ͳ��)����Ϊ0.58%��Candidatus NitrosotaleaΪ��ѡ�����ž�����־�ɵ�[26]�о���ͬʩ�ʷ�ʽ�Ժ����߲��ﰱ����ϸ���Ͱ������ž�Ⱥ���Ӱ��ʱ�������ִ�������ڣ�������������������������Ҫ�����á�MethanosaetaΪ��������SOMENAHALLY��[27]���о�Cr(��)������Ⱥ��ṹӰ���з��ִ�����Ĵ��ڣ����ڸ�Cr(��)Ũ���£�����ž��ܵ����ơ�MethanobacteriumΪ����˾���������[28]�о��˴�����ֽ��ˮ�Ŀ��������Ⱥ�ṹ���ԣ����ֿ���������Cr(32.3 mg/kg)��Mn(1850.2 mg/kg)��As(95.1 mg/kg)��Zn(761.8 mg/kg)�����ܸ�ʱ��Methanobacterium�ž���ȿɴ�4.68%����ʾ����ǿ�������ؽ�������������CrenarchaeoticΪȪ�ž�������Terrestrial Miscellaneousͨ���ں���������г���[29]��
��ǰ��δ�����Ϲž�����β�������еı���������ʵ�鷢�����������˷��价�������档�ž���ϸ���ṹ��ϸ��������ͬ�����ڶ��ص��������ԣ���������Ĺž�������ʵ�����д�����������ˣ����������˻����е���̬���������˻�����������Ҫͨ����������������оƬ��⼼�����������
2.4 ϸ����ž�ϵͳ����������
�Ծ�����ռ��������0.5%��ϸ����ž����ֱ�ϵͳ�������������ͼ4��ʾ�����и����������������������ɲο������ߡ�ͬһ��֧������Ե��ϵ�Ͻ�����ͬ��֧��ͬԴ����Խϵ͡���ͼ4(a)��֪��ϸ����ϵͳ�������ɷֳ�����֧��������β�����������ƾ������Էֳ�����ء�Caulobacter��Comamondadaceae��Pseudomonas��Enterobacter��CronobacterΪͬһ�أ�����֮����Ե��ϵ�Ͻ�������5�־���ռ���������ߣ���0.53%��0.89%֮�䡣���У�Enterobacter��Cronobacter�ڸ�ϸС�ķ�֧�ϣ���������֮����Ե��ϵ������
����һ��ذ���Bacillus��Lactococcus��Carnobacterium��Streptococcus ��Enterococcus��������ռ�����ϴ�49.6%��2.58%���ȣ�����β���������������ԡ����У�Lactococcus��Streptococcus��ͬһ��ϸС��֧�ϣ��������ǵ���Ե��ϵ������ͬ���أ�Carnobacterium��Enterococcus��Ե��ϵҲ�ܽ���
�ž���ϵͳ������Ҳ�ֳ�����֧������Candidatus Nitrosotalea��Crenarchaeotic��Terrestrial MiscellaneousΪһ�أ���Ե��ϵ�Ͻ������DZ���֮��Ϊ78.78%����Methanosaeta��MethanobacteriumΪͬһ�أ���Ϊ���Ƕ��Ǽ������������Ե��ϵ�ӽ������DZ���֮��Ϊ9.62%����ϸ����ȣ��ž���ϵͳ������Ҳ����
2.5 ���˾����롢����
�������õ�5�����˾���USC A1��USC B2��USC C2��USC D2��USC E2�����ֵ�10 mg/L����Һ���������У�����24 h���˵�ȥ����������������5�־����˵�ȥ������߷ֱ�ɴﵽ99.0%��94.7%��96.2%��99.3%��94.7%����ʾ����Ч����Ч�����������Ǿ������õ���β��ԭλ��DZ��������5��ϸ����16S rDNA��ͨ��Blast���������������У�������3���С�

ͼ4 ���ڸ�ͨ������������β��ϸ����ž�ϵͳ������
Fig. 4 Phylogenetic trees of bacteria (a) and archaea (b) in uranium tailings based on high through-put sequencing
��3 ���˾�16S rDNA���������Է���
Table 3 Similarity analysis of uranium-resistant bacterial 16S rDNA sequences

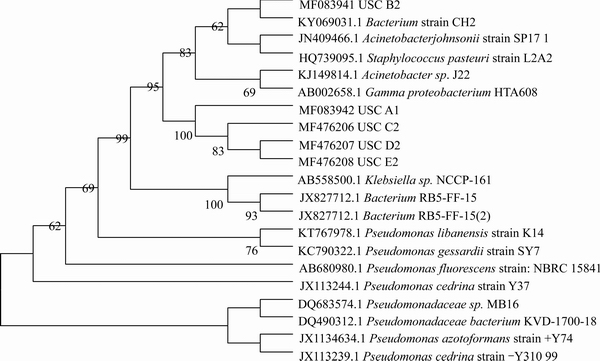
ͼ5 ���� 16S rDNA ������ϵͳ������
Fig. 5 Phylogenetic tree based on 16S rDNA
USC A1��USC B2�ֱ���Klebsiella sp. NCCP-141(AB558500.1)��Acinetobacter johnsonii strain SP171(JN409466.1)�����ƣ����ƶȾ�Ϊ99%��USC C2��USC D2����Pseudomonas cedrina strain Y37(JX113244.1)�����ƣ����ƶ�Ϊ99%��USC E2��Pseudomonas cedrina strain-Y310(JX113239.1)�����ƣ����ƶ�Ϊ99%���ɴ˿�֪��USC A1��USC B2�ֱ�ΪKlebsiella sp.��Acinetobacter johnsonii��������USC C2��USC D2��USC E2����Ϊ������Pseudomonas cedrina���֡�
��5�־��������ƾ������У�ͨ��Mega 7��������ϵͳ�������������ͼ5��ʾ����ϵͳ�����������֪��USC A1��USC C2��USC D2��USC E2��ͬһ��֧�ϣ��γ�һ�飬���ǵĽ�����ϵ�Ͻ�����USC B2������4�����˾�����ͬһ��֧���棬������ϵ��Զ��A1��B2�����ľ�������2.3����ϸ��Ⱥ��ṹ����ʱ����û�г��֣�������2�־�ԭ������β����������ռ��������0.5%��
Klebsiella sp.Ϊ���ײ��Ͼ��������ڹ̵��������ε�[30]����ʮ��̲�˿���ˮ���ʯ�з���õ�����ϸ����������Ԫ��N��ѭ��������ء�Acinetobacter johnsonii���ڲ����˾�����ISLAM��[31]�о�����ز��˿�ϸ�������ԡ��������������������������Acinetobacter��������������Ni��Zn��Cu��Hg�������õĿ��ԣ����нϸߵĹ�����������48 h�ڳ��������ﵽ50 mg/gϸ�����ء�Pseudomonas cedrina���ڼٵ�������Ŀǰ�������౨���������Ǿ������õ���ȥ������[21-22]��
3 ����
1) ϸ����ž���ͨ�����ֱ���42706��34346����Ч���С�ϸ����OTU����(145)���Զ��ڹž�(20)��ϸ����Ace��Chao��Sobsָ��Ҳ���Ը��ڹž�����ӳϸ�����༰Ⱥ��ḻ��Ҫ�ߺܶࡣ��Shannon��Simpsonָ����֪����β����ϸ��Ⱥ�������Ҳ���ڹž���
2) ����ϸ�����������ɴ�С�ֱ�ΪBacillus (49.6%)��Lactococcus (31.9%)��Carnobacterium (3.14%)��Streptococcus (2.87%)��Enterococcus (2.58%)��Caulobacter (0.89%)��Comamondadaceae (0.83%)��Pseudomonas (0.72%)��Enterobacter (0.62%)��Cronobacter (0.53%)��Carnobacterium��Enterococcus��Comamondadaceae��CronobacterΪ�״η�������β�������д��ڡ�
3) �ž���������ϼ��������ɴ�С�ֱ�ΪCandidatus Nitrosotalea (74.03%)��Methanosaeta (6.37%)��Methanobacterium (3.25%)��Crenarchaeotic (3.23%)��Terrestrial Miscellaneous (1.25%)����ǰ��δ�����Ϲž�����β�������еı���������̬���������˻����д������о���
4) ����β�������з����5�����˾�����USC A1��USC B2�ֱ�ΪKlebsiella sp.��Acinetobacter johnsonii��������USC C2��USC D2��USC E2������Pseudomonas cedrina���֡�������24 h�ڣ���10 mg/L�˵�ȥ������߷ֱ�ɴﵽ99.0%��94.7%��96.2%��99.3%��94.7%����ʾ����Ч����Ч�����������Ǿ������õ���β��ԭλ��DZ����
REFERENCES
[1] �� ��, ������, �� ��, �ƶ�ɽ, ������, ̷�ķ�. ��β����Ⱦ�������ۺ����������о���չ[J]. �й���ҵ, 2015, 24(4): 58-62.
ZHANG Biao, ZHANG Xiao-wen, LI Mi, TANG Dong-shan, L�� Jun-wen, TAN Wen-fa. The characteristics and research progress of uranium tailing comprehensives treatments techniques[J]. China Mining Magazine, 2015, 24(4): 58-62.
[2] HU N, DING D X, LI S M, TAN X, LI G Y, WANG Y D, XU F. Bioreduction of U(VI) and stability of immobilized uranium under suboxic conditions[J]. Journal of Environmental Radioactivity, 2016, 154: 60-67.
[3] Ф����, ������, ������, �� ��, ������. ���ܻ���������̶��ͷ��������������˵�������Ϊ�����[J]. �й���ɫ����ѧ��, 2016, 26(7): 1568-1575.
XIAO Fang-zhu, HE Shu-ya, PENG Guo-wen, TANG Yan, DAI Yi-min. Adsorption behavior and mechanism of uranium (��) on Deinococcus radiodurans immobilized functionalization magnetic carrier[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(7): 1568-1575.
[4] ������, лˮ��, ������, ������, �»���, �� ��. ��������δ�ϣ���Ͼ���ԭU(��)��Ӱ�켰����[J]. �й���ɫ����ѧ��, 2015, 25(8): 2309-2315.
LIU Jin-xiang, XIE Shui-bo, MA Hua-long, WANG Yong-hua, CHEN Hua-bai, LI Biao. Effect and mechanism of zero-valent iron on reducing U(��) by S. Oneidensis [J].The Chinese Journal of Nonferrous Metals, 2015, 25(8): 2309-2315.
[5] лˮ��, �� ʤ, ������, ����ƽ, ������, �� ��, ������. �����λ�ԭ����������ȥ��U(��)��Ӱ�����ؼ��ȶ���[J]. �й���ɫ����ѧ��, 2015, 25(6): 1713-1720.
XIE Shui-bo, CHEN Sheng, MA Hua-long, TANG Zhen-ping, ZENG Tao-tao, LING Hui, WU Yu-qi. Influence factors and stability of U(��) removal by sulfate reducing bacteria granular sludge[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(6): 1713-1720.
[6] YAN X, LUO X, ZHAO M. Metagenomic analysis of microbial community in uranium-contaminated soil[J]. Applied Microbiology and Biotechnology, 2016, 100(1): 299-310.
[7] SANCHEZ-CASTRO I, AMADOR-GARCIA A, MORENO- ROMERO C, LOPEZ-FERNANDEZ M, PHROMMAVANH V, NOS J, DESCOSTES M, MERROUN M L. Screening of bacterial strains isolated from uranium mill tailings porewaters for bioremediation purposes[J]. J Environ Radioact, 2017, 166(Pt 1): 130-141.
[8] ������, ��ѧ��, ������, ��³ѩ. ��β����Ⱦ����������Լ�Ⱥ�书�ܶ����Ա仯[J]. ������ѧ�뼼��, 2014, 37(3): 25-31.
WANG Li-chao, LUO Xue-gang, PENG Fang-fang, ZHAO Lu-xue. Change of microbial activity and functional diversity of contaminated soil microbes community in uranium tailings [J]. Environment Science & Technology, 2014, 37(3): 25-31.
[9] ������, ��ѧ��, ������, ��³ѩ. ��β���ܱ���Ⱦ��������Ⱥ��ṹ�빦���о�[J]. ũҵ������ѧѧ��, 2013, 32(11): 2192-2198.
PENG Fang-fang, LUO Xue-gang, WANG Li-chao, ZHAO Lu-xue. Microbial community structure and function in soils around uranium tailings[J]. Journal of Agro-Environment Science, 2013, 32(11): 2192-2198.
[10] ��Ψ��, CARLEY J, WATSON D, �˱���, BROOKS S, D.KELLY S, KEMNER K, NOSTRAND J D V, ������, ��õ Ӣ, �ܼ���, �� ��, CARDENAS E, �S����, W.FIELDS M, L.MARSH T, M.TIEDJE J, J.GREEN S, E.KOSTKA J, K.KITANIDIS P, M.JARDINE P, S.CRIDDLE C. ����ˮ����Ⱦ��ԭλ���ﻹԭ��̶�:��������Դ���������������������Ⱦ�ֳ�������[J]. ������ѧѧ��, 2011, 31(3): 449-459.
WU Wei-min, CARLEY J, WATSON D, GU Bao-hua, BROOKS S, D.KELLY S, KEMNER K, NOSTRAND J D V, WU Li-you, XU Mei-ying, ZHOU Ji-zhong, LUO JIAN, CARDENAS E, HUANG Jia-qi, W.FIELDS M, L.MARSH T, M.TIEDJE J, J.GREEN S, E.KOSTKA J, K.KITANIDIS P, M.JARDINE P, S.CRIDDLE C. Bioreduction and immobilization of uranium in situ: A case study at a USA department of energy radioactive waste site, Oak Ridge, Tennessee[J]. Acta Scientiae Circumstantiae, 2011, 31(3): 449-459.
[11] ������, ³����, ��ӭ��, ������, ����ɼ, ������, лˮ��. ���˿�����������Ⱥ��ṹ����[J]. �й���ɫ����ѧ��, 2016, 26(1): 233-241.
ZENG Tao-tao, LU Hui-zhen, LIU Ying-jiu, RONG Li-shan, MA Hua-long, XIE Shui-bo. Analysis of microbial community structure of uranium-resistant granular sludge[J]. The Chinese Journal of Nonferrous Metals, 2016, 26(1): 233-241.
[12] �Ŷ���, ����, Ф ��, �±���, ���, �� ��. ��ԭCr(��)�Ļ������ۺ����ϸ��Ⱥ��ṹ����[J]. �й�������ѧ, 2017, 37(1): 352-357.
ZHANG En-hua, DAI You-fen, XIAO Yong, CHEN Bi-lian, YANG Zhao-hui, ZHAO Feng. Analysis of extracellular polymeric substances and bacterial community in mixed cultures for Cr(��) reduction[J]. China Environment Science, 2017, 37(1): 352-357.
[13] YANG Y, LI Y, SUN Q-Y. Archaeal and bacterial communities in acid mine drainage from metal-rich abandoned tailing ponds, Tongling, China[J]. Transactions of Nonferrous Metals Society of China, 2014, 24(10): 3332-3342.
[14] ������, �� ΰ, лˮ��, ����ɼ, ������, ��С÷, ������. �������ˮ�����������������Ⱥ�ṹ����[J]. ��������ҵ��ѧѧ��, 2016, 48(8): 115-120.
ZENG Tao-tao, LIAO Wei, XIE Shui-bo, RONG Li-shan, LI Shi-you, JIANG Xiao-mei, MA Hua-long. Analysis of bacterial communtiy in anaerobic granular sludge for citric acid wastewater treatment[J]. Journal of Harbin Institute of Technology, 2016,48(8): 115-120.
[15] KUMAR S, STECHER G, TAMURA K. MEGA7: Molecular evolutionary genetics analysis version 7.0 for bigger datasets[J]. Molecular Biology and Evolution, 2016, 33(7): 1870-1874.
[16] ������, ��С��, ������, ��Ⱥ��, �� ��, �� ��, �� �, �� ��, ����Դ, ���˾�. ����������˵�������Ϊ�о�[J]. �й�������ѧ, 2015, 35(3): 825-832.
MA Jia-lin, NIE Xiao-qin, DONG Fa-qin, DAI Qun-wei, ZHANG Dong, YANG Jie, ZHOU Xian, HUANG Rong, GONG Jun-yuan, GONG Yun-jun. The adsorption behavior on uranium by three kinds of microorganisms[J]. China Environment Science, 2015, 35(3): 825-832.
[17] ˾ ��, ��ѧ��, ������, ������, �� ��. �ݲ�ѿ�߸˾����˵ĸ����������о�[J]. �й�ũѧͨ��, 2017, 33(8): 31-38.
SI Hui, LUO Xue-gang, WANG Zi-long, BAO Wen-qing, HAN Xu. Biosorption of uranium by Bacillus subtilis and its mechanism[J]. Chinese Agricultural Science Bulletin, 2017, 33(8): 31-38.
[18] OBEID M H, OERTEL J, SOLIOZ M, FAHMY K. Mechanism of Attenuation of Uranyl Toxicity by Glutathione in Lactococcus lactis[J]. Applied And Environmental Microbiology, 2016, 82(12): 3563-3571.
[19] MISHRA A, MELO J S, SEN D, D'SOUZA S F. Evaporation induced self assembled microstructures of silica nanoparticles and Streptococcus lactis cells as sorbent for uranium (��)[J]. Journal of Colloid And Interface Science, 2014, 414(2): 33-40.
[20] BRZOSKA R M, BOLLMANN A. The long-term effect of uranium and pH on the community composition of an artificial consortium[J]. FEMS Microbiology Ecology, 2016, 92(1): 1-14
[21] CHOUDHARY S, SAR P. Uranium biomineralization by a metal resistant Pseudomonas aeruginosa strain isolated from contaminated mine waste[J]. Journal of Hazardous Materials, 2011, 186(1): 336-343.
[22] ����, ����, �� ��, �� �B, �ƽ���, �Ǻ���. ʮ��̲�˿��п������ٵ�����������[J]. ������ѧ��Ӧ������ѧ, 2016, 35(7): 1743-1749.
PANG Yuan-tao, ZHU Yan-jie, ZHANG Xiao, ZHANG Jun, HUANG Jian-xin, QIAO Hai-ming. The species of cultured Pseudomonas in Shihongtan uranium ore[J]. Genomics and Applied Biology, 2016, 35(7): 1743-1749.
[23] �� ��, �� , ������, �� ÷, �� ��, �� ��, �� ��. ���Ϻ�����β���������ֲ����鼰���ƾ�����[J]. ��ȫ�뻷��ѧ��, 2013, 13(-1): 108-112.
ZHU Jie, HE Wei, CHEN Xiao-ming, LIU Mei, ZHANG E, LIU Fang, CHEN Hao. Investigation of the microbial distribution and identification of single isolates of uranuim tailings impoundment in Hunan [J]. Journal of Safety and Environment, 2013, 13(1): 108-112.
[24] NAGARAJ K, DEVASYA R P, BHAGWATH A A. Exopolysaccharide produced by Enterobacter sp YG4 reduces uranium induced nephrotoxicity[J]. International Journal of Biological Macromolecules, 2016, 82: 557-561.
[25] HACIOGLU N, TOSUNOGLU M. Determination of antimicrobial and heavy metal resistance profiles of some bacteria isolated from aquatic amphibian and reptile species[J]. Environmental monitoring and assessment, 2014, 186(1): 407-413.
[26] ��־��, �� ��, ��ǰ��, ������, �� ǿ, �ηɷ�. ��ͬʩ�ʷ�ʽ�Ժ����߲��ﰱ����ϸ���Ͱ������ž�Ⱥ���Ӱ��[J]. �й��߲�, 2015, 1(7): 33-39.
ZHOU Zhi-cheng, LUO Kui, TANG Qian-jun, RONG Xiang-min, LIU Qiang, HE Fei-fei. Effect of different fertilization on Ammonia-oxidizing bacteria and Ammonia- oxidizing archaea in red soil vegetable field[J]. China Vegetables, 2015, 1(7): 33-39.
[27] SOMENAHALLY A C, MOSHER J J, YUAN T, PODAR M, PHELPS T J, BROWN S D, YANG Z K, HAZEN T C, ARKIN A P, PALUMBO A V, VAN NOSTRAND J D, ZHOU J Z, ELIAS D A. Hexavalent chromium reduction under fermentative conditions with lactate stimulated native microbial communities[J]. PloS One, 2013, 8(12): e83909.
[28] �� ��, ������, ��˫��, ������, ������, ��־ΰ. ������ֽ��ˮ��������ѭ����Ӧ���ڿ��������Ⱥ���ṹ���ԵĶ��շ���[J]. ��ֽ��ѧ�뼼��, 2017, 36(3): 72-78.
YI Min, JIANG Ya-lei, WANG Shuang-fei, YANG Zhen-zhen, ZHANG Zhe-yun, WANG Zhi-wei. Analysis of dominant bacterial community structures in IC reactors for treating two different papermaking wastewaters from wastepaper reaycling and bagasse pulping[J]. Paper Science &Technology, 2017, 36(3): 72-78.
[29] ����, �� ��, ��Ʒ��. �Ϻ���ɳ���۱�����������������[J]. ��̬ѧ��, 2008, 28(3): 1166-1173.
LI Tao, WANG Peng, WANG Pin-xian. Microbial diversity in surface sediments of the Xi sha Trough the South of China Sea[J]. Acta Ecologica Sinica, 2008, 28(3): 1166-1173.
[30] ����. ʮ��̲�˿���ˮ���ʯ��ϸ����Ⱥ�ֲ������о�[D]. ����: ������ѧ, 2016: 23.
PANG Yuan-tao. Distribution characteristics of bacteria in Shihongtan uranium deposit Groundwater and ore[D]. Xi��an: Northest University, 2016: 23.
[31] ISLAM E, SAR P. Diversity, metal resistance and uranium sequestration abilities of bacteria from uranium ore deposit in deep earth stratum [J]. Ecotoxicology and Environmental Safety, 2016, 127(3): 12-21.
Microbial community of bacteria and archaea analysis in uranium tailing and uranium-resistant bacteria isolation
ZENG Tao-tao, LI Li-cheng, CHEN Zhen, GAO Xiang, TAN Wen-fa, LIU Hai-yan, WANG Guo-hua
(Hunan Province Key Laboratory of Pollution Control and Resources Reuse Technology, University of South China, Hengyang 421001, China)
Abstract: In order to investigate the uranium-resistant microbial communities in uranium tailings, high-throughput sequencing technique was used to analyze the community structure of bacteria and archaea. And isolation and identification of uranium-resistant bacteria were carried out. The results show that, after high-throughput sequencing, sequences of 42706 and 34346 are available for bacteria and archaea with high quality, respectively. Microbial alpha diversity analysis reveals that there are much higher microbial diversity, abundance and richness of bacteria than that of archaea. According to microbial community analysis of bacteria, it is the first report of Carnobacterium, Enterococcus, Comamondadaceae and Cronobacter in uranium tailings, which occupy 3.14%, 2.58%, 0.83% and 0.53% of the bacterial abundance, respectively. It also reveals other dominant uranium-resistant bacteria of Bacillus (49.6%), Lactococcus (31.9%), Streptococcus (2.87%), Caulobacter (0.89%), Pseudomonas (0.72%) and Enterobacter (0.62%). Besides that, according to microbial community analysis of archaea, it is the first time to show the dominant archaea genus of Candidatus Nitrosotalea (74.03%), Methanosaeta (6.37%), Methanobacterium (3.25%), Crenarchaeotic (3.23%) and Terrestrial Miscellaneous (1.25%) are available in the uranium tailings with certain abundance. In addition, five uranium-resistant bacterial genera are isolated, and molecular technique identification shows A1 and B2 are similarity with Klebsiella sp. and Acinetobacter johnsonii, respectively. And C2, D2 and E2 belong to the species of Pseudomonas cedrina.
Keywords��uranium tailings; microbial community; high-throughput sequencing; archaea
Foundation item: Project(51408293) supported by the National Natural Science Foundation of China; Project (2013XQD10) supported by the Scientific Research Staring Foundation for Doctoral Program in University of South China; Project (CX2017B535) supported by the Graduate Scientific Innovation Research Project of Hunan Province, China
Received date: 2017-08-24; Accepted date: 2017-11-05
Corresponding author: ZENG Tao-tao; Tel: +86-734-8282312; E-mail: biowater@126.com
(�༭ ��ѧ��)
������Ŀ��������Ȼ��ѧ����������Ŀ(51408293)���ϻ���ѧ��ʿ������������������Ŀ(2013XQD10)������ʡ�о������д�����Ŀ(CX2017B535)
�ո����ڣ�2017-03-24�������ڣ�2017-11-05
ͨ�����ߣ������Σ������ڣ���ʿ���绰��0734-8282312��E-mail: biowater@126.com