ОДХВұаәЕЈә1004-0609(2015)08-2176-07
»щУЪөз»ҜС§ДЈРНөДИ«№ММ¬п®АлЧУөзіШөД·ЕөзРРОӘ
әй Кч1Ј¬МАТАО°1Ј¬јЦ Гч1Ј¬°¬Бў»Ә2Ј¬ТуұҰ»Ә2Ј¬Ао „В1
(1. ЦРДПҙуС§ ТұҪрУл»·ҫіС§ФәЈ¬іӨЙі 410083Ј»
2. әюДП°¬»ӘјҜНЕ№Й·ЭУРПЮ№«ЛҫЈ¬ТжСф 413002)
ХӘ ТӘЈә»щУЪCOMSOL Multiphysics·ВХжЖҪМЁЈ¬ҪЁБўТ»О¬өз»ҜС§ДЈРНЈ¬СРҫҝ·Еөзұ¶ВКЎўөзҪвЦКЦРөДА©ЙўПөКэЎўөзј«әс¶ИөИ¶ФИ«№ММ¬п®АлЧУөзіШ·ЕөзРФДЬөДУ°ПмЎЈҪб№ыұнГчЈәЛжЧЕ·Еөзұ¶ВКөДФцјУЈ¬өзіШДЪІҝөДј«»ҜФцҙуЈ»ФЪ·ЕөзөДёчёцКұјд¶ОЈ¬өзіШДЪІҝөДј«»ҜЗйҝцТІФЪ·ўЙъұд»ҜЎЈөұА©ЙўПөКэФцјУЦБіхКјЦөөД5ұ¶КұЈ¬ёәј«/өзҪвЦКҪзГжУлХэ ј«/өзҪвЦКҪзГжөДЕЁ¶ИМЭ¶ИјхРЎ80%ЎЈөзј«әс¶ИөДұд»ҜУ°ПмА©ЙўВ·ҫ¶өДіӨ¶МЈ¬өұөзј«әс¶ИФцјУЦБФӯАҙөД2ұ¶КұЈ¬1C·ЕөзКұјдЛх¶М1.72%Ј»өзј«әс¶ИјхРЎЦБФӯАҙөД1/2КұЈ¬1C·ЕөзКұјдФцјУ0.46%ЎЈ
№ШјьҙКЈәИ«№ММ¬п®АлЧУөзіШЈ»КэЦө·ВХжЈ»өз»ҜС§ДЈРНЈ»·ЕөзРРОӘ
ЦРНј·ЦАаәЕЈәTM911 ЎЎ ЎЎ ОДПЧұкЦҫВлЈәA
Discharge behavior of all-solid-state Li-ion batteries based on electrochemical model
HONG Shu1, TANG Yi-wei1, JIA Ming1, AI Li-hua2, YIN Bao-hua2, LI Jie1
(1. School of Metallurgy and Environment, Central South University, Changsha 410083, China;
2. Hunan Aihua Group Co., Ltd., Yiyang 413002, China)
Abstract: Based on COMSOL multiphysics simulation platform, one-dimensional electrochemical model was established to study the effect of discharge rate, electrolyte diffusion coefficient, and electrode thickness on the discharge performance of the all-solid-state Li-ion batteries. The results show that the polarization within the cells increases with the increase of the discharge rate, and in each period of discharge, the polarization inside the battery also changes. When the diffusion coefficient increases to 5 times of the initial value, the concentration gradient of negative electrode/ electrolyte interface and the positive electrode/electrolyte interface decreases by 80%. The electrode thickness changes affect the length of the diffusion path, when the electrode thickness increases to 2 times of the initial value, 1C discharge time decreases by 1.72%. When the electrode thickness decreases to 0.5 times of the initial value, 1C discharge time increases by 0.46%.
Key words: all solid state lithium ion battery; simulation; electrochemical model; discharge behavior
п®АлЧУөзіШТт№ӨЧчөзС№ЎўДЬБҝГЬ¶ИҙуЎўОЮјЗТдР§УҰөИУЕөг[1-4]Ј¬ТСҫӯ№г·әөШУҰУГУЪёчАаұгРҜКҪөзЧУІъЖ·ЦРЎЈҪьДкАҙЈ¬ЖдУҰУГХэФЪПтөз¶ҜЧФРРіөЎўҙҝөз¶ҜЖыіөЎў»мәП¶ҜБҰЖыіөөИБмУтНШХ№[5-6]ЎЈИ»¶шЈ¬п®АлЧУөзіШФЪУҰУГ№эіМЦРіцПЦИјЙХЎўұ¬ХЁөДПЦПуІгіцІ»ЗоЈ¬Тэ·ўөД°ІИ«ОКМвТэЖрБЛЖХұй№ШЧўЎЈ
ёЯ»оРФУР»ъөзҪвТәөДК№УГКЗТэЖрп®АлЧУөзіШ°ІИ«ОКМвөДЦчТӘТтЛШЈ¬ФЪ№э¶Иід·ЕөзЎўДЪІҝ¶МВ·өИТміЈЗйҝц·ўЙъКұЈ¬өзіШДЪІҝ·ўИИЈ¬ҝЙДЬФміЙөзҪвТә»У·ўЎўИјЙХЙхЦБұ¬ХЁ[7]ЎЈІЙУГ№ММ¬өзҪвЦКҝЙТФәЬәГөШұЬГвУЙУЪУР»ъИЬјБөДІ»ЧгТэЖрөД°ІИ«ОКМвЈ¬ј«ҙуөШМбёЯп®АлЧУөзіШөД°ІИ«РФЎЈ ДҝЗ°Ј¬№ШУЪ№ММеөзҪвЦКөДҝӘ·ўј°РФДЬёДЙЖ·ҪГжТСУРәЬ¶аұЁөАЈ¬ЖдРФДЬТСҫӯҪУҪьІъТө»ҜТӘЗуЈ¬ЗТІ»¶ПУРИ«№ММ¬өзіШСщЖ·ГжКАЈ¬СРҫҝЦШөгТСҫӯҙУ№ММеөзҪвЦКІДБПРФДЬөДМбЙэЧӘТЖөҪФЪИ«өзіШЦРөДУҰУГЎЈ
ҙ«НіөДКөСй·Ҫ·Ё¶Ф№ММеөзҪвЦКҪшРРУҰУГСРҫҝКұЈ¬РиТӘЦЖұёіцөзіШСщЖ·ІўҪшРРІвКФЈ¬ФӯІДБПЎўИЛБҰәНКұјдіЙұҫёЯЈ¬ІўЗТОЮ·Ё¶ФөзіШДЪІҝөДұд»ҜҪшРРКөКұОў№ЫБҝ»ҜҙҰАнЎЈКэЦө·ВХжјјКхҝЙТФУРР§ГЦІ№ҙ«НіКөСй·Ҫ·ЁөДІ»ЧгЈ¬МбёЯСРҫҝР§ВКЎЈТтҙЛЈ¬ҪЁБўәПККөДөзіШДЈРН¶ФСРҫҝИ«№ММ¬п®АлЧУөзіШөДРФДЬәННЖ¶ҜЖдІъТө»ҜҪшіМУРЧЕҫЩЧгЗбЦШөДЧчУГ[8-11]ЎЈөұЗ°Ј¬ёщҫЭөз»ҜС§»ъАнҪЁБўөДөз»ҜС§ДЈРН¶ФТәМ¬өзҪвЦКп®АлЧУөзіШТСұИҪПНкЙЖЎЈ»щУЪ¶аҝЧөзј«АнВЫМбіцөДөз»ҜС§ДЈРН[12-20]ТФј°BENARDIөИ[21]ҪЁБўөДИИДЈРНөГөҪБЛ№г·әөДУҰУГЈ¬ІўЗТҫӯ№э¶юК®¶аДкөД·ўХ№Ј¬ҝЖСР№ӨЧчХЯГЗТСҫӯФЪТәМ¬п®АлЧУөзіШДЈРН·ҪГжЧцБЛҙуБҝЙоИлөДСРҫҝЈ¬°ьә¬БЛөз»ҜС§РФДЬФӨІвЎўөзіШДЪІҝөДЕЁ¶И·ЦІјЎўИЭБҝЛрК§ФӨІвј°ИИ·ЦІјөИёчёц·ҪГжЎЈө«КЗЈ¬№ШУЪИ«№ММ¬п®АлЧУөзіШөД·ВХжСРҫҝИҙПКјыұЁөАЎЈDANILOVөИ[22]ДЈДвБЛТФLiCoO2ОӘХэј«ЎўLi3PO4ОӘөзҪвЦКЎўLiҪрКфОӘёәј«өДИ«№ММ¬п®АлЧУөзіШФЪІ»Н¬ұ¶ВК·ЕөзКұөДөз»ҜС§РРОӘЈ¬ФЛУГButler-VolmerГиКцөзј«ҫЦІҝ·ҙУҰөзБчГЬ¶ИЈ¬ід·ЦҝјВЗп®АлЧУА©ЙўЎўЗЁТЖөИОпАн№эіМЈ¬ЖдДЈДвҪб№ыУлКөјКЙъ»оЦРөзіШәгБч·ЕөзЗйҝцЖҘЕдәЬәГЎЈө«ІўОҙЙоИлМҪМЦөзј«ЙијЖУлөз»ҜС§РРОӘөД№ШПөЈ¬KUBANSKAөИ[23]ІЙУГАлЧУөзөјВКҪПёЯөДLi1.5Al0.5Ge1.5(PO4)3МХҙЙЧчОӘ№ММ¬өзҪвЦКЈ¬LiFePO4ЧчОӘ»оРФІДБПЈ¬НЁ№эКөСйСРҫҝөзј«әс¶И¶Ф°лөзіШөз»ҜС§РФДЬөДУ°ПмЎЈ
ұҫОДЧчХЯК№УГCOMSOLИнјю¶ФLiCoO2/LiИ«№ММ¬п®АлЧУөзіШөДөз»ҜС§№эіМҪшРР·ВХжЈ¬¶ФөзіШөДј«»ҜәНп®АлЧУөДЕЁ¶И·ЦІјҪшРРБЛ·ЦОцЈ¬СРҫҝБЛА©ЙўПөКэЎўөзј«әс¶ИөИТтЛШ¶ФөзіШРФДЬөДУ°ПмЈ¬ТФЖЪОӘөзіШөДУЕ»ҜЙијЖМṩАнВЫЦ§іЕЎЈ
1 ДЈРНГиКц
Т»О¬И«№ММ¬п®АлЧУөзіШДЈРНУЙ3ёцІҝ·ЦЧйіЙЈәёәј«(Li)Ўў№ММ¬өзҪвЦКЎўХэј«(LiCoO2)Ј¬ДЈРНКҫТвНјИзНј1ЛщКҫЎЈ·ЕөзКұЈ¬п®ҪрКфФЪөзј«/№ММ¬өзҪвЦКҪзГж·ўЙъөз»ҜС§·ҙУҰЈ¬К§ИҘөзЧУұдіЙп®АлЧУЈ¬НЁ№эФЪ№ММ¬өзҪвЦКЦРА©ЙўәНЗЁТЖҙ«өЭөҪХэј«/№ММ¬өзҪвЦКҪзГжЈ¬·ўЙъөз»ҜС§·ҙУҰҪш¶шЗ¶ИлөҪХэј«LiCoO2ЦРЎЈ

Нј1 И«№ММ¬п®АлЧУөзіШөз»ҜС§ДЈРНКҫТвНј
Fig. 1 Schematic diagram of electrochemical model of all-solid-state Li-ion batteries
1.1 ҝШЦЖ·ҪіМәНұЯҪзМхјю
ұҫСРҫҝЦР»щУЪ¶аҝЧөзј«АнВЫЈ¬ҝјВЗ№МПаҙ«ЦКРРОӘТФј°ПаҪзГжөз»ҜС§·ҙУҰЈ¬ҪЁБўөз»ҜС§ДЈРН¶ФИ«№ММ¬п®АлЧУөзіШөД·Еөз№эіМҪшРРГиКцЎЈҫЯМеҝШЦЖ·ҪіМәНұЯҪзМхјюИзПВЎЈ
1.1.1 өз»ҜС§·ҙУҰЛЩВК
өзј«·ҙУҰ№эіМЦРЈ¬Хэёәј«УлөзҪвТәЦ®јдөДҫЦІҝ·ҙУҰөзБчГЬ¶ИІЙУГButler-Volmer·ҪіМГиКцЈ¬өзј«/ИЬТәҪзГжөҘО»Гж»эөДөз»ҜС§·ҙУҰЛЩВКvИзКҪ(1)ЛщКҫЈә
 (1)
(1)
 (2)
(2)
КҪЦРЈәJ0ОӘҪ»»»өзБчГЬ¶ИЈ»aaәНac·ЦұрОӘСфј«ЎўТхј«өзј«·ҙУҰЧӘ»ҜПөКэЈ»FОӘ·ЁАӯөЪіЈКэЈ»ҰЗОӘ№эөзО»Ј» әН
әН ·ЦұрОӘөзј«УлөзҪвЦКөзКЖЈ»
·ЦұрОӘөзј«УлөзҪвЦКөзКЖЈ» ОӘөзј«·ҙУҰЖҪәвөзКЖЈ»RОӘДҰ¶ыЖшМеіЈКэЈ»TОӘҫш¶ФОВ¶ИЎЈ
ОӘөзј«·ҙУҰЖҪәвөзКЖЈ»RОӘДҰ¶ыЖшМеіЈКэЈ»TОӘҫш¶ФОВ¶ИЎЈ
1.1.2 №МПаҙ«ЦК
1) өзҪвЦКЎЈК№УГNernst-Planck ·ҪіМ¶Фп®АлЧУҙ«өЭНЁБҝҪшРР¶ЁТеЈә
 (3)
(3)
КҪЦРЈәJОӘп®АлЧУҙ«өЭНЁБҝЈ»DeОӘөзҪвЦКЦРп®АлЧУА©ЙўПөКэЈ»ceОӘөзҪвЦКЦРп®АлЧУЕЁ¶ИЈ» ОӘөзј«өзКЖЎЈ
ОӘөзј«өзКЖЎЈ
2) Хэј«ЎЈА©Йў¶ҜБҰС§·ҪіМОӘ
 (4)
(4)
КҪЦРЈәcsОӘ№МПап®АлЧУЕЁ¶ИЈ»DsОӘ№МПаА©ЙўПөКэЈ»tОӘКұјдЎЈ
·ЕөзҝӘКјКұЈ¬өзј«ЦР»оРФОпЦКп®АлЧУЕЁ¶ИОӘ Ј¬№КіхКјМхјюОӘ
Ј¬№КіхКјМхјюОӘ
 (5)
(5)
өзј«УлөзҪвЦКҪзГжп®АлЧУПыәДәНІ№ідТФј°өзј«УлјҜБчМеҪзГжөДОпЦКҙ«өЭ·ЦұрУГКҪ(6)әНКҪ(7)ұнКҫЈә
 (6)
(6)
 (7)
(7)
КҪЦРЈәIОӘ№ӨЧчөзБчЈ»AОӘөзј«Гж»эЈ»L1әНL2·ЦұрОӘөзј«әс¶ИУлөзҪвЦКәс¶ИЎЈ
1.2 ДЈРНІОКэ
ұҫСРҫҝЦРЈ¬ФЪDANILOVАнВЫСРҫҝ»щҙЎЙП[22]Ј¬ҪЁБўИ«№ММ¬п®АлЧУөзіШТ»О¬өз»ҜС§ДЈРНЈ¬ОпРФІОКэИзұн1ЛщКҫ[21]ЎЈ
2 Ҫб№ыУлМЦВЫ
2.1 ДЈРНөДУРР§РФ
п®АлЧУөзіШөДөзј«№эіМКЗТ»ёц¶аПа¶аІҪЦиБ¬РшөДРРОӘ, Йжј°өҪ№МПаҙ«ЦКәНҪзГж»ҜС§·ҙУҰөИ№эіМЈ¬ІўЗТУЙУЪөзіШКЗТ»ёц·вұХМеПөЈ¬ДЪІҝәЬ¶аІОКэДСТФНЁ№эКөСйКөКұ¶ЁБҝөШұнКҫЎЈ
ұҫОДЧчХЯНЁ№э¶Ф·ЕөзЗъПЯөДКөСйКэҫЭәН·ВХжКэҫЭҪшРР¶ФұИЈ¬СйЦӨДЈРНөДҝЙҝҝРФЎЈНј2ЛщКҫОӘФЪ1CМхјюПВДЈДвөГөҪөД·ЕөзЗъПЯәНКөСйКэҫЭөД¶ФұИЎЈҙУНј2ЦРҝЙТФҝҙіцЈ¬ІвБҝКэҫЭУл·ВХжКэҫЭОЗәП¶ИҪПёЯЈ¬ұнГчДЈРНҫЯУРҪПёЯөДЧјИ·¶ИЎЈ

Нј2 ФЪ1CәгБч·Еөз№ӨҝцПВДЈДвөГөҪөДИ«№ММ¬п®АлЧУөзіШ·ЕөзЗъПЯУлКөСйҪб№ыөД¶ФұИ
Fig. 2 Comparison of simulated results with experimental results of discharge curves of all-solid-state Li-ion batteries at 1C rate
2.2 ·Еөзұ¶ВКөДУ°Пм
Нј3ЛщКҫОӘөзіШТФ1CЎў3CЎў5CЎў7CЎў9Cұ¶ВКәгБч·Еөз№ӨҝцПВөГөҪөД·ЕөзЗъПЯЎЈҝЙТФҝҙіцЈ¬ЛжЧЕөзіШ·Еөзұ¶ВКөДФцҙуЈ¬·ЕөзЦБПаН¬өДҪШЦ№өзС№КұЈ¬өзіШөД·ЕөзЙо¶Иҙу·щПВҪөЈ¬ТвО¶ЧЕ»оРФОпЦКАыУГВКҪөөНЎЈНј4ЛщКҫОӘФЪІ»Н¬·Еөзұ¶ВКҪбКшКұХэј«ЦРп®АлЧУөД·ЦІјНјЎЈҝЙТФҝҙіцЈ¬ёЯұ¶ВК·ЕөзМхјюПВЈ¬Хэј«әс¶И·ҪПтРОіЙБЛәЬҙуөДЕЁ¶ИМЭ¶ИЈ¬ЛөГчҙ«ЦКЧиБҰҪПҙуЎЈҙУёәј«НСЗ¶Ј¬ҫӯ№эөзҪвЦКҙ«өЭөҪХэј«өДп®АлЧУЈ¬ФЪХэј«ёчҙҰ·ҙУҰөДЛЩВКІ»Т»СщЈ¬өұҝҝҪьөзҪвЦК¶ЛөД»оРФОпЦКҙпөҪЧоҙуЗ¶п®БҝКұЈ¬јҜБчМе¶ЛөД»оРФОпЦКГ»УРөГөҪід·ЦАыУГЎЈХвұнГчЛжЧЕ·Еөзұ¶ВКөДФцјУЈ¬өзіШДЪІҝөДј«»ҜФЪФцҙуЎЈ
И«№ММ¬өзіШДЪІҝөДј«»ҜҝЙ·ЦОӘЕЁІој«»ҜәНөз»ҜС§·ҙУҰј«»ҜЎЈНј5ЛщКҫОӘ9C·Еөзұ¶ВКПВХэёәј«өз»ҜС§·ҙУҰј«»ҜТФј°Хэј«әНөзҪвЦКЦРЕЁІој«»Ҝ№эөзО»Лж·ЕөзКұјдөДұд»ҜЎЈУЙУЪп®ҪрКфёәј«өДҪ»»»өзБчГЬ¶ИҪПҙуЈ¬ФЪХыёц·Еөз№эіМЦРЈ¬Жд№эөзО»КјЦХҪПРЎЈ»¶шХэј«ФтЛжЧЕ·Еөз№эіМөДЙоИлЈ¬ФЪ·ЕөзәуЖЪ№эөзО»УРЛщФцјУЈ»Хэј«ЦРөДЕЁІој«»Ҝ№эөзО»ФЪ·ЕөзіхЖЪҪПҙуЈ¬ЛжЧЕ·Еөз№эіМөДҪшРРЈ¬Хэј«ЦРөДЕЁІој«»Ҝ№эөзО»ЦрҪҘјхРЎЈ¬И»¶шЈ¬ФЪ·Еөз342 sЦБҪбКшКұХэј«ЦРөДЕЁІој«»Ҝ№эөзО»јұҫзФцјУЈ¬іЙОӘөзіШј«»ҜөДЦчТӘІҝ·ЦЈ»өзҪвЦКЦРөДЕЁІој«»Ҝ№эөзО»ЛжЧЕ·ЕөзКұјдөДСУіӨЦрҪҘФцјУЈ¬ІўФЪ·Еөз161 sәуХјЦчөјЈ¬ТвО¶ЧЕ161 sЦБ342 sөзҪвЦКЕЁ¶И№эөзО»ЧоҙуЈ¬ЛөГчөзҪвЦКЦРп®АлЧУөДА©ЙўКЗЛЩ¶ИҝШЦЖІҪЦиЎЈ
ұн1 И«№ММ¬п®АлЧУөзіШТ»О¬өз»ҜС§ДЈРНІОКэ[21]
Table 1 One-dimensional electrochemical model parameters of all-solid-state Li-ion batteries[21]


Нј3 И«№ММ¬өзіШІ»Н¬ұ¶ВККұөД·ЕөзЗъПЯ
Fig. 3 Discharge curves of al-solid-state batteries at different rates

Нј4 І»Н¬ұ¶ВКәгБч·ЕөзҪбКшКұХэј«ЦРп®АлЧУөД·ЦІјНј
Fig. 4 Concentration of Li-ion in positive electrode at end of 1C, 5C and 9C discharge

Нј5 9CәгБч·ЕөзМхјюПВ№эөзО»Лж·ЕөзКұјдөДұд»Ҝ
Fig. 5 Change of overpotential with discharge time at 9C rate discharge
2.3 РФДЬУЕ»Ҝ
УЙНј5ҝЙЦӘЈ¬·Еөз№эіМЦРЈ¬өзіШөДј«»ҜЦчТӘКЗУЙХэј«әНөзҪвЦКЦРөДЕЁІој«»ҜФміЙЈ¬¶шУ°ПмЕЁІој«»ҜөДЦчТӘТтЛШОӘА©ЙўЛЩВКј°А©ЙўВ·ҫ¶өДіӨ¶МЎЈА©ЙўЛЩВКНЁ№эА©ЙўПөКэөДҙуРЎАҙМеПЦЎЈНј6ЛщКҫОӘ1C·ЕөзМхјюПВЈ¬ФцҙуөзҪвЦКЦРп®АлЧУөДА©ЙўПөКэ(DLi+)Ј¬јЖЛгөГөҪөД·ЕөзҪбКшКұөзҪвЦКЦРп®АлЧУөДЕЁ¶И·ЦІјЎЈУЙУЪХыёц·Еөз№эіМЦРЈ¬өзҪвЦКЦРөДЕЁІој«»ҜКЗЛжЧЕ·ЕөзКұјдөДФцјУ¶шЦрҪҘФцјУөДЈ¬ЛщТФ·ЕөзҪбКшКұЈ¬өзҪвЦКЦРөДЕЁ¶ИІоҙъұн·Еөз№эіМЕЁ¶ИІоөДЧоҙуЦөЎЈҙУНј6ҝЙТФҝҙіцЈ¬А©ЙўПөКэФҪҙуЈ¬өзҪвЦКЦРп®АлЧУЕЁ¶ИМЭ¶ИФҪРЎЈ¬ұнГчЕЁІој«»ҜФҪРЎЎЈөұА©ЙўПөКэФцјУЦБФӯАҙөД5ұ¶КұЈ¬ёәј«/өзҪвЦКҪзГжУлХэј«/өзҪвЦКҪзГжөДп®АлЧУЕЁ¶ИІоОӘ171 mol/m3Ј¬ЕЁ¶ИМЭ¶ИјхРЎБЛ80%Ј»өұА©ЙўПөКэФцјУЦБФӯАҙөД10ұ¶КұЈ¬өзҪвЦКЦРөДЧоҙуЕЁ¶ИІоОӘ85 mol/m3Ј¬УлФцјУ5ұ¶ПаұИЈ¬ЕЁ¶ИМЭ¶ИҪцјхРЎБЛ10%Ј¬ЛөГчФЪҙЛ»щҙЎЙПФЩМбёЯА©ЙўПөКэЈ¬¶ФөзіШРФДЬөДМбЙэУРПЮЈ¬ҙЛКұЈ¬өзіШДЪІҝ·ҙУҰөДЛЩ¶ИҝШЦЖІҪЦиҝЙДЬТСҫӯ·ўЙъБЛЧӘТЖЈ¬І»ФЩКЗөзҪвЦКЦРп®АлЧУөДА©ЙўЛЩ¶ИЎЈ

Нј6 І»Н¬А©ЙўПөКэМхјюПВ·ЕөзҪбКшКұөзҪвЦКЦРп®АлЧУЕЁ¶И·ЦІј
Fig. 6 Calculated concentration distribution of Li-ion in electrolyte at various diffusion coefficients
өзј«әс¶И¶ФУЪөзіШЕЁІој«»ҜөДУ°ПмЦчТӘМеПЦФЪА©ЙўВ·ҫ¶өДіӨ¶МЎЈНј7ЦРСЎ¶ЁБЛ3ЦЦІ»Н¬өДХэј«әс¶ИЈ¬·ЦұрОӘ160(іхКјәс¶И0.5L)Ўў320(іхКјәс¶ИL)әН480(іхКјәс¶И1.5L) nmЈ¬ФЪ5CәгБч№ӨҝцПВөГөҪөД·ЕөзЗъПЯЎЈФЪёДұдөзј«әс¶ИөДН¬КұЈ¬Н¬ұИөШёДұд·ЕөзөзБчЈ¬ұЈЦӨКөСйЦРДЬ№»ТФПаН¬өДұ¶ВК·ЕөзЎЈҪб№ыұнГчЈ¬ФЪ5CәгБч·ЕөзПВјхРЎөзј«әс¶ИЈ¬·ЕөзКұјдЛжЦ®СУіӨЈ»УЙНј7ҝЙјыЈ¬1.5LЈ¬1.0LЈ¬0.5L 3ЦЦІ»Н¬Хэј«әс¶И¶ФУҰөД·ЕөзКұјд·ЦұрКЗ640Ўў660әН680 sЎЈХвЛөГчФЪТ»¶Ё·¶О§ДЪјхРЎөзј«әс¶ИДЬ№»МбЙэөзіШөД·ЕөзРФДЬЈ¬МбёЯөзј«»оРФОпЦКАыУГВКЎЈ
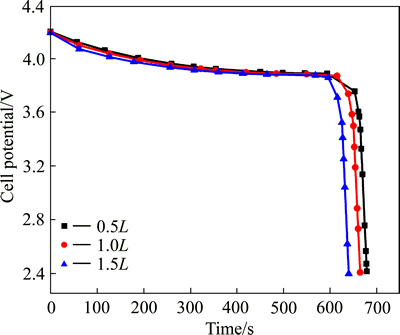
Нј7 5CәгБчМхјюПВІ»Н¬өзј«әс¶ИКұөД·ЕөзЗъПЯ
Fig. 7 Discharge curves at 5C rate with various thickness of electrode

Нј8 І»Н¬өзј«әс¶ИөДөзіШ1C·ЕөзІ»Н¬КұјдәуХэј«ёчО»ЦГөДп®АлЧУЕЁ¶И·ЦІјНј
Fig. 8 Li-ion concentration distribution of different positions in cathode electrode of batteries with different electrode thicknesses at different time during 1C discharge
ОӘБЛёьјУЦұ№ЫөШ·ҙУіІ»Н¬әс¶ИКұөзј«ДЪІҝп®АлЧУЕЁ¶ИМЭ¶ИөДҙуРЎЈ¬ұИҪПБЛ·Еөз0Ўў100әН200 sКұХэј«ЦРп®АлЧУЕЁ¶И·ЦІјЗйҝцЈ¬ЖдҪб№ыИзНј8ЛщКҫЎЈФЪ·ЕөзҝӘКјКұЈ¬өзј«ДЪп®АлЧУЕЁ¶И·ЦІјҫщФИЈ»·Еөз100әН 200 sәуЈ¬ҝЙТФҝҙіцЈ¬өзј«әс¶ИФҪРЎЈ¬өзіШХэј«әс¶И·ҪПтп®АлЧУөДЕЁ¶ИМЭ¶ИФҪРЎЈ¬»оРФОпЦКҝЙТФөГөҪёьід·ЦАыУГЎЈНј9ЛщКҫОӘ1C·ЕөзЦХЦ№КұХэј«ЦРп®АлЧУөДЕЁ¶И·ЦІјЎЈөзј«әс¶ИҪПҙуКұЈ¬ҝҝҪьјҜБчМе¶ЛөДөзј«ІДБПІ»ДЬід·ЦЗ¶п®Ј¬»оРФОпЦКАыУГВКҪөөНЈ»ЛжЧЕөзј«әс¶ИөДјхРЎЈ¬Хэј«әс¶И·ҪПтЙПөДЕЁ¶ИМЭ¶ИЦрҪҘјхРЎЈ¬өзј«ҝХјдАыУГВКЦрҪҘФцјУЎЈұн2ЛщБРОӘХэј«әс¶И·ҪПтЙП»оРФҝЕБЈДЪІҝЧЬөДп®АлЧУЕЁ¶ИәН·ЕөзКұјдЎЈөұөзј«әс¶ИҙУ2.0LҪөөНөҪ1.0LКұЈ¬Хэј«әс¶ИҪөөН1ұ¶Ј¬п®АлЧУЕЁ¶ИЦ»ҪөөН26%Ј»¶шөзј«әс¶ИҙУ1.0LҪөөНөҪ0.5LЈ¬п®АлЧУЕЁ¶ИЦ»ҪөөН28%Ј¬ХвЛөГчәс¶ИҪөөНөД·щ¶ИҙуУЪп®АлЧУЧЬЕЁ¶ИҪөөНөД·щ¶ИЈ¬п®АлЧУҝХјдАыУГВКҙуҙуФцјУЎЈө«өзј«әс¶ИТІІ»ДЬОЮПЮөДјхРЎЈ¬Т»·ҪГжКЬПЮУЪөұЗ°ұЎДӨІДБПЦЖұёөДЛ®ЖҪЈ¬¶шЗТөзј«әс¶ИөДҪөөН»бөјЦВөзіШДЬБҝГЬ¶ИөДҪөөНЈ»БнТ»·ҪГжЈ¬өзј«әс¶ИјхРЎөҪТ»¶ЁіМ¶ИЈ¬өзіШРФДЬөДМбЙэҝХјдҪ«ұдөГәЬРЎЈ¬ХвТ»өгТІҝЙТФҙУұн2 ЦРөД·ЕөзКұјдЦРөГөҪЈ¬ЛжЧЕХэј«әс¶ИҙУ2.0LҪөөНөҪ0.5LЈ¬·ЕөзКұјдТ»ЦұФЪФцјУЈ¬·ЕөзИЭБҝПа¶ФМбёЯЈ¬өзіШРФДЬІОКэПа¶ФМбёЯЈ¬ө«өұХэј«әс¶ИҙУ0.5LҪөөНөҪ0.25LКұЈ¬·ЕөзКұјдЦ»ФцјУБЛ1.9 sЈ¬ФцјУөД·щ¶ИәЬРЎЈ¬ХвЛөГчФЪХэј«әс¶ИҪөөНөҪ0.5LКұЈ¬өзіШРФДЬТСҫӯөГөҪБЛҪПҙуөДМбЙэЈ¬ФЩјхРЎХэј«әс¶И¶ФМбёЯөзіШРФДЬөДТвТеІ»ҙуЎЈ

Нј9 1C·ЕөзЦХЦ№КұХэј«ЦРп®АлЧУөДЕЁ¶И·ЦІј
Fig. 9 Concentration distribution of Li-ion in cathode electrode at end of 1C discharge curves
ұн2 І»Н¬өзј«әс¶ИөзіШ1C·ЕөзЦХЦ№КұХэј«п®АлЧУЕЁ¶ИәН·ЕөзКұјд
Table 2 Concentration of Li-ion in cathode electrode and discharge time at 1C discharge when batteries with different electrode thickness

3 ҪбВЫ
1) И«№ММ¬п®АлЧУөзіШ·Еөз№эіМЦРЈ¬өз»ҜС§·ҙУҰ№эөзО»ҪПРЎЈ»өзіШј«»ҜЦчТӘКЗЕЁІој«»ҜЎЈ9C·ЕөзҙУ0өҪ161 sТФј°342 sЦБ·ЕөзҪбКшЈ¬Хэј«өДЕЁІој«»ҜХјЦчөјЈ»·Еөз161~342 sКұЈ¬өзҪвЦКЦРөДЕЁІој«»ҜКЗөзіШј«»ҜөДЦчТӘІҝ·ЦЎЈ
2) №ММ¬өзҪвЦКЦРп®АлЧУөДА©ЙўПөКэ¶ФЕЁІој«»ҜҫЯУРәЬҙуУ°ПмЎЈөұА©ЙўПөКэФцјУЦБФӯАҙөД5ұ¶КұЈ¬ёәј«/өзҪвЦКҪзГжУлХэј«/өзҪвЦКҪзГжөДп®АлЧУЕЁ¶ИІоОӘ171 mol/m3Ј¬ЕЁ¶ИМЭ¶ИјхРЎБЛ80%Ј»өұА©ЙўПөКэФцјУЦБФӯАҙөД10ұ¶КұЈ¬өзҪвЦКЦРөДЧоҙуЕЁ¶ИІоОӘ85 mol/m3Ј¬УлФцјУ5ұ¶ПаұИЈ¬ЕЁ¶ИМЭ¶ИҪцјхРЎБЛ10%Ј¬Т»¶Ё·¶О§ДЪФцҙуА©ЙўПөКэДЬ№»МбЙэөзіШРФДЬЈ¬А©ЙўПөКэФцҙуөҪТ»¶ЁіМ¶ИәуЈ¬өзіШРФДЬөДёДұдІ»ФЩГчПФЎЈ
3) өзј«әс¶ИөДұд»ҜУ°ПмА©ЙўВ·ҫ¶өДіӨ¶МЈ¬өұөзј«әс¶ИУЙіхКјЦө·ЦұрФцјУЦБФӯАҙөД2ұ¶КұЈ¬1C·ЕөзКұјдјхЙЩ1.72%Ј»Па·ҙөШЈ¬өзј«әс¶ИјхРЎЦБ1/2КұЈ¬1C·ЕөзКұјдФцјУ0.46%ЎЈ
REFERENCES
[1] МАРЎ»Ф, Ао№ъПЈ, ёЯ№рәм, әъҪр·б, Бә№ъұк. п®АлЧУөзіШХэј«ІДБП LiCoO2-LiFePO4өДРФДЬ[J]. ЦР№ъУРЙ«ҪрКфС§ұЁ, 2012, 22(1): 139-144.
TANG Xiao-hui, LI Guo-xi, GAO Gui-hong, HU Jin-feng, LIANG Guo-biao. Performance of LiCoO2-LiFePO4 cathode materials for lithium ion batteries[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(1): 139-144.
[2] ХЕ ҝӯ, МАТАО°, ЧЮ ЦТ, іМ кА, ЛООД·ж, јЦ Гч, В¬ әЈ, ХЕЦО°І. п®АлЧУөзіШLiMn2O4/КҜД«өзј«·Еөз№эіМЦРА©Йўј«»ҜөД·ВХж[J]. ЦР№ъУРЙ«ҪрКфС§ұЁ, 2013, 23(8): 2235-2243.
ZHANG Kai, TANG Yi-wei, ZOU Zhong, CHENG Yun, SONG Wen-feng, JIA Ming, LU Hai, ZHANG Zhi-an. Simulation of diffusion polarization in LiMn2O4/graphite Li-ion battery during discharge process[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(8): 2235-2243.
[3] МАТАО°, јЦ Гч, іМ кА, ХЕ ҝӯ, ХЕәмББ, Ао „В. »щУЪөз»ҜС§УлИИДЬөДсоәП№ШПөСЭЛгҫЫәПОпп®АлЧУ¶ҜБҰөзіШөДОВ¶ИЧҙМ¬ј°·ЦІј[J]. ОпАнС§ұЁ, 2013, 62(15): 1582011-1582019.
TANG Yi-wei, JIA Ming, CHENG Yun, ZHANG Kai, ZHANG Hong-liang, LI Jie. Estimation of temperature distribution of the polymer lithium ion power battery based on the coupling relationship between electrochemistry and heat[J]. Acta Phys Sin, 2013, 62(15): 1582011-1582019.
[4] ¶ЕЛ«Бъ, АөСУЗе, јЦ Гч, іМ кА, ХЕәмББ, ХЕ ҝӯ, БхТөПи. ФІЦщп®АлЧУ¶ҜБҰөзіШөзИИМШРФ·ВХж[J]. ЦР№ъУРЙ«ҪрКфС§ұЁ, 2014, 24(7): 1823-1830.
DU Shuang-long, LAI Yan-qing, JIA Ming, CHENG Yun, ZHANG Hong-liang, ZHANG Kai, LIU Ye-xiang. Electrothermal characteristics simulation of cylindrical automotive lithium ion battery[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(7): 1823-1830.
[5] SCOSATI B, GARCHE J. Lithium batteries: Status, prospects and future[J]. Journal of Power Sources, 2010, 195: 2419-2430.
[6] ЛХГчИз, НхЦҫРЛ, №щ»Әҫь, АоРВәЈ, »ЖЛјБЦ, ёК АЧ. ХіҪбјБ¶Фп®АлЧУөзіШSi/CёҙәПІДБПРФДЬөДУ°Пм[J]. ЦР№ъУРЙ«ҪрКфС§ұЁ, 2013, 23(4): 1059-1064.
SU Ming-ru, WANG Zhi-xing, GUO Hua-jun, LI Xin-hai, HUANG Si-lin, GAN Lei. Effect of binders on performances of Si/C composites for Li-ion batteries[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(4): 1059-1064.
[7] Бх Ҫъ, РмҝЎТг, БЦ ФВ, Ао „В, АөСУЗе, Ф¬іӨёЈ, ХЕ Ҫх, Цм ҝӯ. И«№ММ¬п®АлЧУөзіШөДСРҫҝј°ІъТө»ҜЗ°ҫ°[J]. »ҜѧѧұЁ, 2013, 71(4): 869-878.
LIU Jin, XUN Jun-yi, LIN Yue, LI Jie, LAI Yan-qing, YUAN Chang-fu, ZHANG Jin, ZHU Kai. All-solid-state lithium ion battery: Research and industrial prospects[J]. Acta Chim Sinica, 2013, 71(4): 869-878.
[8] DOYLE M, NEWMAN J. The use of mathematical modeling in the design of lithium/polymer battery systems[J]. Electrochima Acta, 1995, 40(13): 2191-2196.
[9] DOYLE M, NEWMAN J,GOZDZ A S, SCHMUTZ C N,TARASCON J M. Comparison of modeling predictions with experimental from plastic lithium ion cells[J]. Journal of the Electrochemical Society, 1996, 143(6): 1890-1903.
[10] DOYLE M, FULLER T F, NEWMAN J. Modeling of galvanostatic charge and discharge of the lithium/polymer/ insertion cell[J]. Journal of the Electrochemical Society, 1993, 140(6): 1526-1533.
[11] НхҙуОӘ, АҪӯ, Ао ҫь, Со УВ. п®АлЧУөзіШөз»ҜС§·ҙУҰДЈРНСРҫҝҪшХ№ЗіОц[J]. өз»ҜС§, 2011, 17(4): 355-362.
WANG Da-wei, LI Dong-jiang, LI Jun, YANG Yong. A brief review of research progress in the development of engineering models for lithium ion batteries[J]. Electrochemistry, 2011, 17(4): 355-362.
[12] ALBERTUS P, CHRISTENSEN J, NEWMAN J. Experiments on and modeling of positive electrodes with multiple active materials for lithium-ion batteries[J]. Journal of the Electrochemical Society, 2009, 156(7): 606-608.
[13] STEWART S, ALBERTUS P, SRINIVASAN V, PLITZ I, PEREIRA N, AMATUCCI G, NEWMAN J. Optimizing the performance of lithium titanate spinel paired with activated carbon or iron phosphate[J]. Journal of the Electrochemical Society, 2008, 155(3): 253-261.
[14] KUMARESAN K, SIKHA G, WHITE R E. Thermal model for a Li-ion cell[J]. Journal of the Electrochemical Society, 2008, 155(2): 164-171.
[15] STAMPS A, HOLLAND E, WHITE R E, GATZKE E P. Analysis of capacity fade in a lithium ion battery[J]. Journal of Power Sources, 2005, 150(4): 229-239.
[16] BOTTE G, WHITE R E. Modeling lithium intercalation in a porous carbon electrode[J]. Journal of the Electrochemical Society, 2001, 148(1): 54-66.
[17] YUE T, WHITE R E. Mathematical model of a lithium/ polypyrrole cell[J]. Journal of the Electrochemical Society, 1990, 137(5): 1327-1336.
[18] GUO Meng, SIKHA G, WHITE R E. Sing-particle model for a lithium-ion cell: Thermal behavior[J]. Journal of the Electrochemical Society, 2011, 158(5): 122-132.
[19] GUO Meng, WHITE R E. Thermal model for lithium ion battery pack with mixed parallel and series configuration[J]. Journal of the Electrochemical Society, 2011, 158(10): 1166-1176.
[20] NAGARAJAN G S, VAN ZEE J W, SPOTNITZ R M. A mathematical model for intercalation electrode behavior[J]. Journal of the Electrochemical Society, 1998, 145(3): 771-779.
[21] BERNARDI D, PAWLIKOWSKI E, NEWMAN J. A general energy balance for battery systems[J]. Journal of the Electrochemical Society, 1985, 132(1): 5-12.
[22] DANILOV D, NIESSEN R A H, NOTTEN P H L. Modeling all-solid-state Li-ion batteries[J]. Journal of the Electrochemical Society, 2011, 158(3): A215-A222.
[23] KUBANSKA A, CASTRO L, TORTET L,  M, BOUCHET R. Elaboration of controlled size Li1.5Al0.5Ge1.5(PO4)3 crystallites from glass-ceramics[J]. Solid State Ionics, 2014, 266(15): 44-50.
M, BOUCHET R. Elaboration of controlled size Li1.5Al0.5Ge1.5(PO4)3 crystallites from glass-ceramics[J]. Solid State Ionics, 2014, 266(15): 44-50.
(ұајӯ Бъ»іЦР)
»щҪрПоДҝЈә№ъјТЧФИ»ҝЖС§»щҪрЧКЦъПоДҝ(51204211, 51222403)Ј»ЦР№ъІ©КҝәуҝЖС§»щҪрЧКЦъПоДҝ(2012M521543)
КХёеИХЖЪЈә2014-09-22Ј»РЮ¶©ИХЖЪЈә2015-05-29
НЁРЕЧчХЯЈәјЦ ГчЈ¬ҪІКҰЈ¬І©КҝЈ»өз»°Јә13975127722Ј»ҙ«ХжЈә0731-88710171Ј»E-mail: jiamingsunmoon@aliyun.com