ЙъОпІЈБ§МоідСАҝЖёҙәПКчЦ¬ІДБПөДЦЖұёј°ЖдРФДЬ
ЦЈ ЦО1, 2Ј¬»ЖІ®ФЖ1Ј¬ПтЖдҫь1Ј¬М·СеДЭ1Ј¬Бх УҪ1
( ЦРДПҙуС§ ·ЫД©ТұҪр№ъјТЦШөгКөСйКТЈ¬әюДП іӨЙіЈ¬410083Ј»
2. ЦРДПҙуС§ ПжСЕИэТҪФәЈ¬әюДП іӨЙіЈ¬410013)
ХӘ ТӘЈәНЁ№э№в№М»ҜөД·Ҫ·ЁЦЖұёТФБЧ»ТКҜІЈБ§МХҙЙәНЖшПа¶юСх»Ҝ№иОӘОЮ»ъМоБПөДСАҝЖёҙәПКчЦ¬ЎЈІЙУГЙЁГиөзҫө/ДЬЖЧТЗ(SEM/EDS)¶ФёҙәПІДБПөДОў№ЫРОГІҪшРР·ЦОцЈ¬ІвБҝёҙәПІДБПөДИэөгҝ№НдЗҝ¶ИЎЈІЙУГМеНвДЈДвМеТә(Simulated body fluid, SBF)ҪюЕЭ·ЁІвКФІДБПөДЙъОп»оРФЎЈСРҫҝҪб№ыұнГчЈәІДБПөДҝ№НдЗҝ¶ИҙпөҪ(137ЎА10) MPaЈ¬ДЬ№»ВъЧгСАіЭРЮёҙөДБҰС§РФДЬТӘЗуЈ»ІДБПФЪSBFЦРҪюЕЭ3 dәуЈ¬ФЪұнГжРОіЙҝу»ҜөДМјЛбБЧ»ТКҜҫ§МеІгЈ¬ұнГчІДБПҫЯУРҪПЗҝөДЙъОп»оРФЈ¬ҝЙјУҝмёГІДБПЦІИлИЛМеәуУл№ЗөДҪбәПЈ¬ІўУРАыУЪИЈіЭөДРЮёҙУъәПЎЈ
№ШјьҙКЈәБЧ»ТКҜЈ»ОЮ»ъМоБПЈ»КчЦ¬Ј»САіЭЈ»ЙъОп»оРФ
ЦРНј·ЦАаәЕЈәR783.1Ј»TQ325 ОДПЧұкК¶ВлЈәA ОДХВұаәЕЈә1672-7207(2009)01-0094-05
Preparation and property of bioglass ceramics filled dental resins
ZHENG Zhi1, 2, HUANG Bai-yun1, XIANG Qi-jun1, TAN Yan-ni1, LIU Yong1
( State Key Laboratory of Powder Metallurgy, Central South University, Changsha 410083, China;
2.The 3rd Xiangya Hospital, Central South University, Changsha 410013, China)
Abstract: Apaptite glass-ceramics and gaseous silica were used to fill light-cured dental resins. By using SEM/EDS, bending test and in vitro experiment, the microstructure, mechanical behavior and bioactivity of the composite were studied. The results show that the bending strength of the dental resin is (137ЎА10) MPa, which meets the requirements for dental restoration. After immersion in SBF for 3 d, there is a mineralized carbonyl apatite layer formed on the material surface, indicating that the dental resin has a high bioactivity and has a good bonding to human bones. The dental resins filled with bioglass-ceramics and gaseous silica is promising in restoration of dental hard tissues.
Key words: apatite; inorganic filler; resin; tooth; bioactivity
САҝЖМоідІДБПҝЙУГУЪёчАаИұЛрЎўИЈіЭідМој°»о¶Ҝ№М¶ЁРЮёҙөИЎЈЛжЧЕОТ№ъИЛҝЪФціӨЈ¬САҝЖҫНТҪИЛКэІ»¶ПФцјУЈ¬САҝЖМоідІДБПөДРиЗуБҝТІИХТжА©ҙуЎЈТш№ҜәПҪрКЗФзЖЪөДСАҝЖідМоІДБПЈ¬Т»Цұұ»УГУЪЦОБЖіРөЈҫЧҪА№ҰДЬөДәуСАіцПЦөДҙуГж»эИұЛр(ўсАаәНўтАаИұЛр)ЎЈИ»¶шЈ¬УЙУЪТш№ҜәПҪрҙжФЪТ»¶ЁөД¶ҫРФЈ¬»·ҫіОЫИҫЈ¬ГА№ЫРФІоЈ¬УлСАМеөДСХЙ«І»Т»ЦВЈ¬ФЪСАМеФӨұёКұЗЦИлРФҙуЈ¬УлСАМеУІЧйЦҜёҪЧЕБҰРЎөИОКМвЈ¬Рн¶а»јХЯІ»ФёҪУКЬТш№ҜәПҪрМоБПЈ¬¶шёь¶аөШСЎУГёҙәПКчЦ¬ІДБПЎЈСАҝЖУГ№в№М»ҜёҙәПКчЦ¬ІДБПЦчТӘУЙОЮ»ъМоБПәНУР»ъКчЦ¬ЧйіЙЈ¬ФЪКЬЛрЗшУтідМоәуНЁ№эҝЙјы№в№М»ҜЎЈСАҝЖ№в№М»ҜёҙәПКчЦ¬ІДБПҫЯУРІЩЧч·ҪұгЈ¬НёГч¶ИёЯЈ¬ХіЧЕБҰЗҝЈ¬ГА№ЫЈ¬Й«ФуәГөИУЕөгЈ¬МШұрККәПУГУЪРЮёҙРЎГж»эөДФӯ·ўИЈЎЈИ»¶шЈ¬ЛьҙжФЪТ»Р©І»ЧгЦ®ҙҰЈ¬ИзФЪКЬБҰҪПҙуЦ®ҙҰЈ¬ЦұҪУөДәуСАРЮёҙәНјдҪУөДСА№ЪРЮёҙ·ҪГжөДЗҝ¶ИІ»№»[1-2]ЎЈҙЛНвЈ¬ёГІДБПөДЙъОп»оРФөНЈ¬ЦІИлИЛМеәуУл№ЗҪбәПЛЩ ¶ИҪПВэЈ¬ИЭТЧЛЙ¶ҜЈ¬Н¬КұЈ¬І»АыУЪјУҝмИЈіЭөДРЮёҙУъәП[3-6]ЎЈ
УЙУЪёҙәПКчЦ¬ІДБПЦРөДОЮ»ъМоБПЦКБҝХјЧЬЦКБҝөД70%~80%Ј¬ЖдМе»эХјЧЬМе»эөД50%~60%Ј¬ТтҙЛЈ¬НЁ№эёДұдОЮ»ъМоБПөДЦЦАаЎўЧй·ЦЎўРОМ¬ДЬ№»ПФЦшёДұдКчЦ¬өДёчПоРФДЬЦёұкЎЈЦөөГЧўТвөДКЗЈ¬ІЙУГ°ұёДРФГЙНСНБ»т¶аҝЧСх»Ҝ№иМоБПДЬ№»ПФЦшҪөөНёҙәПКчЦ¬өДКХЛхУҰБҰЈ¬јхЙЩОўЙшВ©Ј¬ҝЙјыЈ¬ОЮ»ъМоБП¶ФёДЙЖҫЫәПКХЛхҫЯУР№гА«өДУҰУГЗ°ҫ°ЎЈҪьДкАҙЈ¬Рн¶аСРҫҝХЯ¶ФУР»ъКчЦ¬УлОЮ»ъМоБПёҙәП¶шіЙөДёҙәПКчЦ¬ІДБПҪшРРБЛСР ҫҝ[7-10]ЎЈRavehөИ[11]·ўПЦТФЙъОпІЈБ§(Bioglass?)»тБЧЛбИэёЖОӘМоБПөДЛ«·УA¶юјЧ»щұыП©ЛбЛхЛ®ёКУНЦ¬КчЦ¬(Bis-GMA)ёҙәПІДБПҝЙТФЦұҪУУл№ЗҪбәПЎЈKawanabe өИ[12]ТФCaO-SiO2-P2O5-CaF2ІЈБ§·ЫД©ОӘМоБПөДөИЦКБҝ»мәПөДЛ«·УA¶юјЧ»щұыП©ЛбЛхЛ®ёКУНЦ¬(Bis-GMA)әН¶юјЧ»щұыП©ЛбИэёКҙјхҘ(TEGDMA)ёҙәПКчЦ¬ІДБПЈ¬ҝ№С№Зҝ¶ИҝЙҙп170 MPaЈ¬ІўҝЙУл№ЗҪбәПЎЈёҙәПКчЦ¬ЦРОЮ»ъМоБПөДЖҪҫщБЈ¶ИТСУЙЧоіхөД30~50 mm ҪөөҪ1~5 mmЈ¬ЦКБҝ·ЦКэТІёЯҙп70%~80%ЎЈЛжЧЕДЙГЧ·ЫД©ЦЖұёјјКхөД·ўХ№Ј¬ФЪСАҝЖёҙәПКчЦ¬ЦРТІЦрҪҘіцПЦБЛДЙГЧОЮ»ъМоБП(ИзЖш»ҜСх»Ҝ№и)ЎЈДЙГЧОЮ»ъМоБПДЬ№»ёДЙЖёҙәПКчЦ¬өДЕЧ№вРФДЬәНБҰС§РФДЬЎЈИ»¶шЈ¬УЙУЪМоБПөДұнГжДЬёЯЈ¬УлКчЦ¬ЧчУГјУЗҝЈ¬өјЦВМоБПрӨ¶ИіКЦёКэФцјУЈ¬У°ПмБЩҙІІЩЧчЈ¬¶шЗТөұМоБПЦКБҝ·ЦКэОӘ30%ЧуУТКұЈ¬әЬИЭТЧҫЫјҜіЙНЕЎЈТтҙЛЈ¬ІЙУГөҘТ»өДДЙГЧј¶ОЮ»ъМоБП·ҙ¶шҙпІ»өҪМбёЯКчЦ¬БҰС§РФДЬөДДҝөДЈ¬НЁіЈРиТӘҪПҝнөДБЈҫ¶·ЦІјЈ¬УРАыУЪМбёЯідМоБҝ[1-2]ЎЈГА№ъ3M№«ЛҫЧоҪьҝӘ·ўіцТ»ЦЦДЙГЧёҙәПКчЦ¬Ј¬ЖдОЮ»ъМоБПУЙТ»ЦЦөҘ·ЦЙўөДДЙГЧБЈЧУ(ИзСх»Ҝ№и)әНТ»ЦЦҫӯ№эФӨҙҰАнөДДЙГЧНЕҙШ(ИзСх»ҜпҜ/Сх»Ҝ№иёҙәПМе)ЧйіЙЈ¬БЈ¶И·ЦІј·¶О§ОӘ5~75 nmЎЈІЙУГҙЛјјКхЈ¬ҝЙТФК№ОўМоБПЦКБҝ·ЦКэФцјУЦБ50%ТФЙПЈ¬¶шІ»ҪөөНКчЦ¬өДрӨ¶ИЈ¬ҙуҙуМбёЯБЛІДБПөДДНДҘРФДЬЎўЕЧ№вРФәНБҰС§РФДЬЎЈБЧ»ТКҜКЗСАіЭЦРОЮ»ъОпөДЦШТӘЧйіЙІҝ·ЦЎЈУЙУЪБЧ»ТКҜҫЯУРБјәГөДЙъОпС§РФДЬәНБҰС§РФДЬЈ¬іЈЧчОӘУР»ъҫЫәПОпөДФцЗҝПаұ»УГЧч№ЗЛ®Да»тХЯСАҝЖЦІИлІДБП[7, 12-14]ЎЈИ»¶шЈ¬өҘТ»БЧ»ТКҜіЙ·ЦөДМоБПәЬДСВъЧгёҙәПКчЦ¬БҰС§РФДЬәНБЩҙІУҰУГТӘЗуЈ¬Ҫ«БЧ»ТКҜәНЖшПа¶юСх»Ҝ№иЛ«ёҙәПЈ¬УРҝЙДЬёьҙуөШМбёЯЖдРФДЬЎЈФЪҙЛЈ¬ұҫОДЧчХЯІЙУГ№в№М»ҜөД·Ҫ·ЁЦЖұёТФБЧ»ТКҜІЈБ§МХҙЙәНЖшПа¶юСх»Ҝ№иОӘОЮ»ъМоБПөДBis-GMA/ TEGDMAСАҝЖёҙәПКчЦ¬Ј¬Іў¶ФІДБПөДҝ№НдЗҝ¶ИәНМеНвЙъОп»оРФҪшРРСРҫҝЈ¬ТФЖЪЦЖұёјИҫЯУРёЯЙъОп»оРФУЦҫЯУРБјәГБҰС§РФДЬөДОЮ»ъМоБП-КчЦ¬ёҙәПІДБПЎЈ
1 ІДБПУл·Ҫ·Ё
ОЮ»ъМоБПУЙЦКБҝ·ЦКэОӘ60%өДБЧ»ТКҜІЈБ§МХҙЙ(ЖҪҫщБЈҫ¶ОӘ0.5 ҰМm)әН40%өДЖшПа¶юСх»Ҝ№и(ЖҪҫщБЈҫ¶ОӘ14 nm)ЧйіЙЎЈОӘБЛМбёЯМоБПУлКчЦ¬Ц®јдөДҪбәПБҰЈ¬¶ФОЮ»ъМоБПҪшРР№иНй»ҜҙҰАнЎЈ№иНйЕјБӘјБОӘҰГ-јЧ»щұыП©хЈСх»щұы»щИэјЧСх»щ№иНй(silane A-174)ЎЈ№иНй»ҜҙҰАн№эіМОӘ[15]ЈәПИ°ҙХХМе»эұИV(ТТҙј)?V(Л®)ЈҪ90?10ЕдЦГИЬТәЈ¬ІўЛб»ҜЈ¬К№pHЈҪ4Ј¬јУИлЦКБҝ·ЦКэОӘ0.3%~1.0%өД№иНйЕјБӘјБsilane A-174ЎЈҪУЧЕЈ¬Ҫ«ОЮ»ъМоБПјУИлИЬТәІўҪБ°и1~2 hЈ¬ФЪОВ¶ИОӘ110~120 ЎжөД»·ҫіЦРёЙФпЎЈКчЦ¬УЙХјЦКБҝ·ЦКэ·ЦұрОӘ49.25% Bis-GMAЈ¬49.25% TEGDMAЈ¬0.5%~1.0%ХБДФх«(Camphorguinone, CQ)әН0.5%~1.0%јЧ»щұыП©Лб¶юјЧ°ұ»щТТхҘ(DMAEMA)ЧйіЙЎЈБЧ»ТКҜІЈБ§МХҙЙУЙұҫҝОМвЧйЧФЦЖ¶шіЙ[16]Ј¬ЖдЛыІДБП№әЧФГА№ъSigma-Aldrich№«ЛҫЎЈ
КчЦ¬Ул№иНй»ҜәуөДМоБП°ҙХХЦКБҝұИ(40~45)?(55~60) ЕдЦГЈ¬УГРЎ№Оө¶»мәПҫщФИЈ¬И»әуЈ¬МоИлДЈҫЯЎЈІЙУГСАҝЖ№в№М»ҜөЖҪ«СщЖ·№М»Ҝ120 sЈ¬НСДЈәуФЪҝХЖшЦР·ЕЦГ2 hЈ¬ЦГУЪ37 ЎжөДХфБуЛ®ЦРҪюЕЭ22 hЈ¬И»әуЈ¬ҪшРРёчПоРФДЬІвКФЎЈ
ІДБПИэөгҝ№НдЗҝ¶ИөДІвКФІЙУГөДҝзҫаОӘ15 mmЈ¬ФШәЙЛЩВКОӘ0.5 mm/minЈ¬ЖдІвКФҪб№ыИЎ6ёцСщЖ·өДЖҪҫщЦөЎЈІЙУГИХұҫJSM-5600LVРНЙЁГиөзҫө(SEM/EDS)¶ФСщЖ·¶ПБСГжөДОў№ЫҪб№№ҪшРРЕзҪр№ЫІмЎЈ
ІЙУГМеНвДЈДвМеТә(SBF)ҪюЕЭ·ЁІвКФІДБПөДЙъОп»оРФЎЈSBFөД»ҜС§іЙ·ЦЧйіЙУлИЛМеСӘҪ¬өДЧйіЙҪУҪь[17]Ј¬SBFөДАлЧУИЬ¶Иј°К№УГөД»ҜС§КФјБИзұн1әНұн2ЛщКҫЎЈSBFИЬТәөДpHЦөОӘ7.4ЎЈПИҪ«ЕЧ№вөДСщЖ·ФЪХфБуЛ®ЦРУГі¬ЙщІЁЗеПҙ»ъЗеПҙ15 minЎЈИ»әуЈ¬Ҫ«СщЖ··ЕИлSBF ИЬТәЦРЈ¬ІўұЈіЦФЪ37 ЎжөД»·ҫіЦРЎЈГҝ№э24 h¶ФSBFёь»»1ҙОЎЈСЎФсҪюЕЭКұјд·ЦұрОӘ3Ј¬7Ј¬14Ј¬28әН56 dЈ¬Ҫ«СщЖ·ИЎіцәуУГХфБуЛ®ЗбЗбЗеПҙЎЈёЙФпә󣬶ФСщЖ·өДұнГжЕзҪрЈ¬ІўФЪЙЁГиөзҫө(SEM/EDS)ПВ№ЫІмЖдұнГж РОГІЎЈ
ұн1 ДЈДвМеТә(SBF)УлИЛМеСӘҪ¬өДАлЧУИЬ¶И¶ФұИ
Table 1 Comparison of ion density between SBF and human blood plasma of artificial body fluid
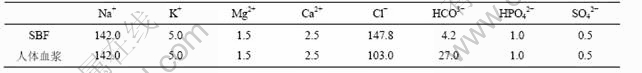
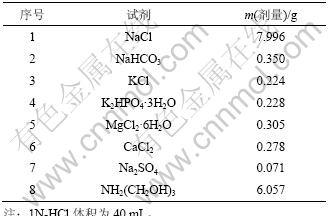
ұн2 ДЈДвМеТәЛщУГөД»ҜС§КФјБј°ЦКБҝ
Table 2 Chemical agents and mass in SBF composition of artificial body fluid
2 Ҫб№ыУлМЦВЫ
БҰС§РФДЬІвКФҪб№ыұнГчЈ¬ЦЖұёөДСАҝЖёҙәПКчЦ¬өДҝ№НдЗҝ¶Иҙп(137ЎА10) MPaЈ¬ДЬ№»ВъЧгСАіЭРЮёҙ¶ФБҰС§РФДЬөДТӘЗу[18]Ј¬ІўЗТёЯУЪЖдЛыСАҝЖёҙәПКчЦ¬өДЗҝ ¶И[7, 19-20]ЎЈХвҝЙДЬКЗМнјУБЛБЧ»ТКҜІЈБ§МХҙЙУлЖшПа¶юСх»Ҝ№иМоБПЛщЦВЎЈ¶юСх»Ҝ№иЎўІЈБ§ЎўМХҙЙөИОЮ»ъМоБПіЈіЈЧчОӘФцЗҝПаУГУЪЦЖұёСАҝЖёҙәПКчЦ¬[1, 8-10]ЎЈНј1ЛщКҫОӘёҙәПКчЦ¬ІДБПөД¶ПҝЪРОГІЎЈҙУНј1ҝЙТФҝҙіцЈ¬МоБПУл»щМеКчЦ¬ҪПәГөШИЪәПФЪТ»ЖрЈ¬ұнГчМоБПУлКчЦ¬Ц®јдҪбәПБјәГЎЈХвКЗУЙУЪҫӯ№э№иНй»ҜҙҰАнЈ¬МбёЯБЛОЮ»ъМоБПУлУР»ъКчЦ¬Ц®јдөДҪбәПЗҝ¶И[7]Ј¬ҙУ¶шМбёЯБЛёҙәПКчЦ¬ІДБПөДҝ№НдЗҝ¶ИЎЈ

Нј1 ёҙәПКчЦ¬ІДБПөД¶ПБСГжSEMНјПс
Fig.1 SEM of fracture face of composite resin
Нј2ЛщКҫОӘёҙәПКчЦ¬ІДБПФЪДЈДвМеТә(SBF)ЦРҪюЕЭІ»Н¬КұјдәуұнГжРОГІЎЈҝЙјыЈ¬ФЪҪюЕЭ3 dәуЈ¬ІДБПұнГжТСУРТ»Р©ҝу»ҜөДБЧ»ТКҜҫ§МеЙъіЙ(Нј2(a))Ј»ҫӯ№э 7 dҪюЕЭЈ¬ҝу»ҜөДБЧ»ТКҜҫ§МејёәхёІёЗБЛХыёцІДБПұнГж(Нј2(b))Ј»ҪюЕЭ14 dәуЈ¬ІДБПұнГжҝу»ҜөДБЧ»ТКҜҫ§МеІгФҪАҙФҪәсЎЈҙУНј2ҝЙТФҝҙіцЈ¬ҝу»ҜөДБЧ»ТКҜҫ§МеІгУЙТ»Р©ІгЖ¬ЧҙөДПёРЎҫ§МеЧйіЙЎЈХвЦЦІгЖ¬ЧҙөДБЧ»ТКҜРОГІУлЖдЛыЙъОпІДБПФЪДЈДвМеТәЦРҪюЕЭәуҝу»ҜөДБЧ»ТКҜҫ§МеРОГІК®·ЦПаЛЖ[21-23]ЎЈНј3ЛщКҫОӘёҙәПКчЦ¬ІДБПҪюЕЭ3 dәуұнГжЙъіЙөДҝу»ҜБЧ»ТКҜҫ§МеөДДЬЖЧ(EDS)ЎЈҝЙТФҝҙіцЈ¬ХвЦЦҝу»ҜБЧ»ТКҜҫ§Меә¬УРCЈ¬OЈ¬CaәНPФӘЛШЈ¬ұнГчЛьКЗТ»ЦЦМјЛбБЧ»ТКҜЈ¬ХвЦЦМјЛбБЧ»ТКҜУлИЛМе№ЗЦРә¬УРөДБЧ»ТКҜөДіЙ·ЦәНҪб№№ПаЛЖ[21]ЎЈ

(a) 3 dЈ»(b) 7 dЈ»(c) 14 dЈ»(d) 14 d
Нј2 ёҙәПКчЦ¬ІДБПФЪДЈДвМеТә(SBF)ЦРҪюЕЭІ»Н¬КұјдәуұнГжРОГІ
Fig.2 Appearance of composite resin soaked in SBF for different time
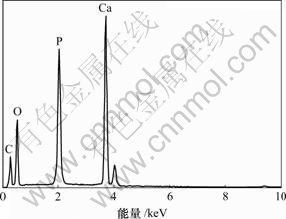
Нј3 ёҙәПКчЦ¬ІДБПҪюЕЭ3 dәуұнГжЙъіЙөДҝу»ҜБЧ»ТКҜҫ§МеДЬЖЧНј
Fig.3 Energy spectrum of mineralized apatite crystal on the surface of composite resin soaked in SBF for 3 d
ұҫСРҫҝІДБПФЪДЈДвМеТәЦРөДҝу»ҜЛЩВКУлЙъОпІЈБ§әНЙъОп»оРФІЈБ§МХҙЙөДҝу»ҜЛЩВКҪУҪь[24]Ј¬ұнГчІДБПФЪМеНвҫЯУРёЯЙъОп»оРФЎЈХвЦчТӘКЗУЙУЪФЪІДБПЦРМнјУБЛБЧ»ТКҜІЈБ§МХҙЙ·ЫД©ҝЕБЈЈ¬ЖдУХөјІДБПұнГжЙъОпРФБЧ»ТКҜЙъіЙөД№эіМЦчТӘ°ьАЁ[25-26]Јә
a. БЧ»ТКҜІЈБ§МХҙЙФЪҪюЕЭәуИЬҪвөДNa+»т K+УлSBFЦРөДH+»т H3O+ҪшРРАлЧУҪ»»»Ј¬јҙ
SiЎӘOЎӘNa+ + H+ + OH- Ўъ SiЎӘOH+ + Na++OH-ЎЈ (1)
b. SiЎӘOЎӘSiјьұ»ИЬҪвҙт¶ПЈ¬ФЪІЈБ§МХҙЙУлИЬТәҪзГжҙҰРОіЙSiЎӘOHЈ¬јҙ
SiЎӘOЎӘSi + H2O Ўъ SiЎӘOH +OHЎӘSiЎЈ (2)
c. SiЎӘOHНЁ№эҫЫәП·ҙУҰФЪІЈБ§МХҙЙұнГжРОіЙё»SiO2 ІгЈ¬јҙ
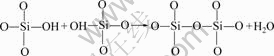 ЎЈ(3)
ЎЈ(3)
d. АҙФҙУЪІЈБ§МХҙЙМеДЪКН·ЕТФј°SBFИЬТәЦРөДCa2+әНPO43-ұ»ё»SiO2 ІгОьёҪЈ¬ФЪё»SiO2ІгөДНвІгУЦРОіЙТ»ІгОЮ¶ЁРОМ¬ё»CaO-P2O5ұЎІгЈ¬ІўЗТІ»¶ПОьКХCa2+әНPO43-¶шЙъіӨЎЈ
e. НЁ№эОьКХИЬТәЦРөДOH-әНCO32-Ј¬ОЮ¶ЁРОМ¬ё»CaO-P2O5ұЎІг·ўЙъҫ§»ҜЈ¬РОіЙә¬фЗ»щЎўМјЛбёщөДБЧ»ТКҜІг(HCA)ЎЈ
ЛжЧЕҪюЕЭКұјдөДСУіӨЈ¬ІДБПұнГжҝу»ҜөДБЧ»ТКҜҫ§МеІгФҪАҙФҪәсЈ¬ТІУРАыУЪІДБПБҰС§РФДЬөДМбёЯ[21]ЎЈТтОӘЛжЧЕІДБПұнГжөДҝу»ҜБЧ»ТКҜІгәс¶ИФцјУЈ¬ҪюЕЭИЬТәТӘҙ©НёБЧ»ТКҜІгІўА©ЙўҪшИлёҙәПКчЦ¬ІДБПК№КчЦ¬ҪөҪвХвёц№эіМ»бұдөГёьјУА§ДСЈ¬ІДБПұнГжөДҝу»ҜБЧ»ТКҜІгөДРОіЙ¶Ф»щМеКчЦ¬ЖрөҪТ»ЦЦұЈ»ӨЧчУГЎЈИЛМеСАіЭҙҰУЪІ»¶ПНСҝуУлФЩҝу»ҜөД¶ҜМ¬ЖҪәвЧҙМ¬Ј¬өұНСҝуБҝҙуҙуёЯУЪФЩҝу»ҜБҝКұЈ¬ұг»бІъЙъИЈіЭЎЈИЈіЭНЁіЈУЙЛбРФОпЦК(ИйЛбЎўҙЧЛбЎўұыЛбөИ)ТэЖрЈ¬ХвР©ЛбРФОпЦККЗУЙПёҫъ¶ФМјЛ®»ҜәПОпҙъР»әуөДІъОпІъЙъөДЎЈөұpHЈј5.5КұЈ¬САУФЦКЦРөДБЧ»ТКҜҝӘКјИЬҪвЈ¬Хвёц№эіМіЖОӘНСҝу[5]ЎЈёГСАҝЖёҙәПКчЦ¬ФЪДЈДвМеТәЦРҪюЕЭ3 dәуЈ¬ұнГжҫНУРҝу»ҜБЧ»ТКҜҫ§МеІгЙъіЙЈ¬ұнГчІДБПҫЯУРҪПЗҝөДФЩҝу»ҜДЬБҰЈ¬ҝЙјУҝмИЈіЭөДРЮёҙУъәПЎЈ
3 Ҫб ВЫ
a. НЁ№э№в№М»ҜөД·Ҫ·ЁЦЖұёБЛТФБЧ»ТКҜІЈБ§МХҙЙәНЖшПа¶юСх»Ҝ№иОӘОЮ»ъМоБПөДСАҝЖёҙәПКчЦ¬ЎЈІДБПөДҝ№НдЗҝ¶ИҙпөҪ(137ЎА10) MPaЈ¬ДЬ№»ВъЧгСАіЭРЮёҙөДБҰС§РФДЬТӘЗуЎЈ
b. ЙъОп»оРФКөСйПФКҫІДБПФЪSBFЦРҪюЕЭ3 dәуЈ¬ФЪұнГжТСРОіЙҝу»ҜөДМјЛбБЧ»ТКҜҫ§МеІгЈ¬ұнГчІДБПҫЯУРёЯөДЙъОп»оРФЈ¬ҝЙјУҝмёГІДБПЦІИлИЛМеәуУл№ЗөДҪбәПЈ¬ІўУРАыУЪИЈіЭөДРЮёҙУъәПЎЈ
c. ТтҫЯУРёЯҝ№НдЗҝ¶ИәНЙъОп»оРФЈ¬ТФБЧ»ТКҜІЈБ§МХҙЙәНЖшПа¶юСх»Ҝ№иОӘОЮ»ъМоБПөДСАҝЖёҙәПКчЦ¬ІДБПФЪСАіЭУІЧйЦҜРЮёҙ·ҪГжҫЯУР№гА«өДУҰУГЗ°ҫ°ЎЈ
ІОҝјОДПЧЈә
[1] Xu H H K, Eichmiller F C, Antonucci J M, et al. Dental resin composites containing ceramics whiskers and precured glass ionomer particles[J]. Dental materials, 2000, 16(5): 356-363.
[2] Xu H H K, Quinn J B, Smith D T, et al. Dental resin composites containing silica-fused whiskers-effects of whisker-to-silica ratio on fracture toughness and indentation properties[J]. Biomaterials, 2002, 23(3): 735-742.
[3] Miyaji F, Morita Y, Kokubo T, et al. Surface structural change of bioactivity inorganic filler-resin composite cement in simulated body fluid: Effect of resin[J]. J Biomed Mater Res, Part A, 1998, 42(4): 604-610.
[4] Deb S, Aiyathurai L, Roether J A, et al. Development of high-viscosity, two-paste bioactive bone cements[J].Biomaterials, 2005, 26(17): 3713-3718.
[5] Jones F H. Teeth and bones: applications of surface science to dental materials and related biomaterials[J].Surface Science Reports, 2001, 42(3/5): 75-205.
[6] Skrtic D, Antonucci J M, Eanes E D. Improved properties of amorphous calcium phosphate fillers in remineralizing resin composites[J].Dent Mater,1996, 12(5): 295-301.
[7] Santos C, Luklinska Z B, Clarke R L, et al. Hydroxyapatite as a filler for dental composite materials: mechanical properties and in vitro bioactivity of composites[J]. J Mater Sci: Mater in Med, 2001, 12(7): 565-573.
[8] Venhoven B A M, de Gee A J, Werner A, et al. Influence of filler parameters on the mechanical coherence of dental restorative resin composites[J].Biomaterials, 1996, 17(7): 735-740.
[9] Mccabe J F, Wassell R W. Hardness of model dental composites-the effect of filler volume fraction and silanation[J]. J Mater Sci: Mater in Med, 1999, 10(5): 291-294.
[10] Turssi C P, Ferracane J L, Vogel K. Filler features and their effects on wear and degree of conversion of particulate dental resin compostes[J]. Biomaterials, 2005, 26(24): 4932-4937.
[11] Raveh J, Stich H, Schawalder P, et al. Biocement: a new material[J]. Acta Otolaryngology, 1982, 94: 371-384.
[12] Kawanabe K, Tamura J, Yamamuro T, et al. A new bioactive bone cement consisting of BIS-GMA resin and bioactive glass powder[J]. J Appl Biomater, 1993, 4(2): 135-141.
[13] Kobayashi M, Nakamura T, Tamura J, et al. Bioactive bone cement: Comparison of AW-GC filler with hydroxyapatite and ҰВ-TCP fillers on mechanical and biological properties[J]. J Biomed Mater Res, 1997, 37(3): 301-313.
[14] Vallo C L, Montemartini P E, Fanovich M A, et al. Polymethylmethacrylate-based bone cement modified with hydroxyapatite[J]. J Biomed Mater Res, 1999, 48(2): 150-158.
[15] Furtos G, Cosma V, Prejmerean C, et al. Fluoride release from dental resin composites[J]. Mater Sci & Eng C, 2005, 25(2): 231-236.
[16] Liu Y, Sheng X X, Dan X H, et al. Preparation of mica/apatite glass-ceramics biomaterials[J]. Mater Sci & Eng C, 2006, 26(8): 1390-1394.
[17] Oliveira J M, Correia R N, Fernandes M H. Surface modifications of a glass and a glass-ceramic of the MgO-3CaO?P2O5-SiO2 system in a simulated body fluid[J]. Biomaterials, 1995, 16(11): 849-854.
[18] іВЦОЗе. ҝЪЗ»ІДБПС§[M]. ұұҫ©: ИЛГсОАКҝіц°жЙз, 2003: 210.
CHEN Zhi-qing. Dental materials[M]. Beijing: PeopleЎҜs Hygieism Press, 2003: 210.
[19] Oshida Y, Hashem A, Elsalawy R. Some mechanistic observation on water-deteriorated dental composite resins[J]. Bio-Medical Materials and Engineering, 1995, 5(2): 93-115.
[20] Fong H. Electrospun nylon 6 nanofiber reinforced BIS-GMA/TEGDMA dental restorative composite resins[J]. Polymer, 2004, 45(7): 2427-2432.
[21] Ni J, Wang M. In vitro evaluation of hydroxyapatite reinforced polyhydroxyapatite composite[J]. Mater Sci & Eng C, 2002, 20(1/2): 101-109.
[22] Zhang E L, Yang K. Biomimetic coating of calcium phosphate on biometallic materials[J]. Trans Nonferrous Met Soc China, 2005, 15(6): 1199-1205.
[23] Kasuga T. Bioactive calcium pyrophosphate glasses and glass-ceramics[J]. Acta Biomaterialia, 2005, 1(1): 55-64.
[24] Huang J, Di Silvio L, Wang M, et al. Evaluation of in vitro bioactivity and biocompatibility of Bioglass?-reinforced polyethylene composite[J]. J Mater Sci: Mater in Med, 1997, 8(12): 809-813.
[25] Hench L L, Wilson J. An introduction to bioceramics[M]. Singapore: World Scientific Publishing Co Pte Ltd, 1993: 47.
[26] Peitl O, Zanotto E D, Hench L L. Highly bioactive P2O5-Na2O-CaO-SiO2 glass-ceramics[J]. Journal of Non- Crystalline Solids, 2001, 292(1/3): 115-126.
КХёеИХЖЪЈә2008-07-02Ј»РЮ»ШИХЖЪЈә2008-10-12
»щҪрПоДҝЈә№ъјТЎ°К®ОеЎұҝЖјј№Ҙ№ШПоДҝ(2003BA310A31)
НЁРЕЧчХЯЈәЦЈ ЦО(1966-)Ј¬ДРЈ¬әюДПіЈөВИЛЈ¬І©КҝСРҫҝЙъЈ¬СРҫҝФұЈ¬ҙУКВТҪУГЙъОпІДБПөДЦЖұёУлУҰУГСРҫҝЈ»өз»°Јә0731-8618663Ј»E-mail: zheng0813@163.com