���±�ţ�1004-0609(2007)10-1705-06
���¹��෴Ӧ-���շֽⷨ�Ʊ�����������
�� ������־�ˣ������������º�������Ԫ
(���ϴ�ѧ ұ���ѧ�빤��ѧԺ����ɳ 410083)
ժ Ҫ����NiCl2?6H2O��MnCl2?4H2OΪ���Σ��ֱ���(NH4)2C2O4?H2O��NaOH��Na2CO3?10H2O�����¹���ϳ���Ӧ�����̻����Ȼ��ֱ���400��300��500 ���¶������շֽ�3 h�õ���������������֪������ѧ���ݣ������¹��෴Ӧ�ļ���˹�����ܱ���ʱ���м��㣬������ѧ�ĽǶȳ������о���ͬ�ķ�Ӧ���ͶԲ���ṹ��Ӱ�졣����DSC-TGA��XRD�ȷ��������շֽ���̡�����������������ò�����˷����������������������̲����ηֽ�õ�NiMn2O4��MnNi2O4��������������ֽ�ֻ�õ�MnNiO3������̼���ηֽ�õ�NiMn2O4��MnNi2O4��MnNiO3�������������������������˳��Ϊ����������������̲����Ρ�����̼���εIJ��
�ؼ��ʣ�������������෴Ӧ������ѧ����
��ͼ����ţ�TM 912.9���� ���ױ�ʶ�룺A
Preparation of nickel-manganese composite oxide by room temperature solid state reaction-calcining decomposition
YANG Bo, WANG Zhi-xing, GUO Hua-jun, LI Xin-hai, ZHOU You-yuan
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Using NiCl2?6H2O and MnCl2?4H2O as major reactants, nickel-manganese composites were synthesized by the solid state reaction at room temperatures with three difference reactants ((NH4)2C2O4?H2O, NaOH, NaCO3?10H2O). The nickel-manganese oxides were synthesized by calcining three precursors at 400, 300, 500 �� for 3 h.  and
and  for three solid state reactions at room-temperature were estimated by the thermodynamic data. The effects of difference reaction on the oxides were studied. The processes, particle size and crystallography characters were studied by means of DSC-TGA, XRD and TEM. The results show that spinel NiMn2O4 and MnNi2O4 are obtained by decomposing nickel-manganese oxalic acid; Ilmenite-type MnNiO3 is obtained by decomposing nickel-manganese hydroxide; Ilmenite-type MnNiO3, spinel NiMn2O4 and MnNi2O4 are obtained by decomposing nickel-manganese carbonate. The particle size of nickel-manganese oxide products increases by turn of nickel-manganese hydroxide, oxalic acid, carbonate.
for three solid state reactions at room-temperature were estimated by the thermodynamic data. The effects of difference reaction on the oxides were studied. The processes, particle size and crystallography characters were studied by means of DSC-TGA, XRD and TEM. The results show that spinel NiMn2O4 and MnNi2O4 are obtained by decomposing nickel-manganese oxalic acid; Ilmenite-type MnNiO3 is obtained by decomposing nickel-manganese hydroxide; Ilmenite-type MnNiO3, spinel NiMn2O4 and MnNi2O4 are obtained by decomposing nickel-manganese carbonate. The particle size of nickel-manganese oxide products increases by turn of nickel-manganese hydroxide, oxalic acid, carbonate.
Key words: nickel-manganese oxide; solid state reaction; thermodynamic analysis
�Դ�2001���ձ�������ҵ��ѧOhzuku[1]�״κϳ�����Ӷ��ε���������ϲ�״LiNi0.5Mn0.5O2������LiNi0.5Mn0.5O2�Կ��������ߡ�ѭ���Ժá���ȫ�Ըߡ��ɱ��������ŵ��ܵ����ڶ��о��ߵĹ�ע[2-6]��Yasuhiro��[7]������������������Ϊ����̸���������ϳ��е���Ҫԭ�ϣ������˹㷺�Ĺ�ע����ϳɷ������ṹ�����ܺ�Ӧ�õ��о���Ϊ�������о����ȵ�֮һ[8-10]�����¹�̬��ѧ��Ӧ��20����80���ĩ��չ������һ���µĺϳɷ������������ص����ڷ�Ӧ�¶Ƚ������»�����£�������б��ڲ����Ϳ��Ƶ��ŵ㡣����в�ʹ���ܼ�����ѡ���ԡ��߲��ʡ���Ⱦ�١���ʡ��Դ���ϳɹ��ռ��ص㣬��Щ�ص���ϵ��������ɫ��ѧ��չ��Ҫ��[11]����˱����������LiNi0.5Mn0.5O2��ԭ�����⣬ͨ�����¹��෨����NiCl2?6H2O��MnCl2?4H2OΪ���Σ��벻ͬ�ķ�Ӧ�ﷴӦ�ϳɲ�ͬ�����̻����Ȼ�����շֽ�õ���Ӧ����������������õ����¹��෨�������������о���ͬ����ķ�Ӧ�������������ϳɵ�Ӱ�죬�Ӷ�ɸѡ�����ʵķ�Ӧ�����ϳ��������Ӿ��Ȼ�ϵĸ����������Ϊ��״LiNi0.5Mn0.5O2���Ʊ�ԭ�ϡ��ڹ��ѧ��Ӧ�У���Ӧ�ܷ���У�ȡ���ڹ��巴Ӧ��Ľṹ������ѧ���ʡ�����������ѧ�����£����巴Ӧ��Ľṹ�����˹��෴Ӧ���е�����[11]�����о�������ѧ�ĽǶȳ������о���ͬ�ķ�Ӧ���ͶԲ����Ӱ�졣����DSC-TGA��XRD��SEM�ȷ����Ժϳɵ���������������������ò�����˷����������
1 ʵ��
1.1 ������������Ʊ�
���õ��Լ�NiCl2?6H2O��MnCl2?4H2O��(NH4)2C2O4?H2O��NaOH��Na2CO3?10H2O��Ϊ�����������У�����NiCl2?6H2O��MnCl2?4H2O�ֱ���N��M��ǣ���Ӧ��(NH4)2C2O4?H2O��NaOH��NaCO3?10H2O�ֱ���1��2��3��ǡ�
�����������£���N��M����Ӧ���1?1(Ħ����)������в�����ĥ��Ͼ��Ⱥ��ٰ�N:M:X�ķ�ӦĦ����1?1?2.4����X(XΪ��Ӧ��1��2��3�е�һ�֣���XΪNaOHʱ����ӦĦ����Ϊ1?1?4.8)�����Ⱥ���������ĥ�������ĥ30 min����Ӧ���ͷų��ᾧˮ��ʹ��Ӧ����ɳ�״ʪ��Ĺ��塣���У��ϳ����̲�����ʱ��Cl-��NH4Cl����ʽ���ڣ����ں������շֽ�ʱ�����������ȥ���ʲ��辭��ˮϴ���裬����ĥ���ò���ֱ�Ӹ�������̲�����ǰ���壻�ϳ��������������������̼����ʱ��Ϊȥ������������Cl-����ĥ��Ӧ��ȫ���ڳ�������������ȥ����ˮϴ�ӡ����ˣ�ϴ�Ӷ�κ���AgNO3��⣬ֱ����Cl-Ϊֹ��Ȼ������ˮ�Ҵ�ϴ�ӣ�60 ���¸���õ���Ӧ��ǰ���塣�������ĸ�ǰ�����ڸ��Եķֽ��¶�������3 h���õ����������
1.2 ���ܱ���
����SDT-Q600�ȷ�����(Ӣ��)���ڿ��������ж�ǰ�������DSC-TGA�����������ٶ�10 ��/min����Rigaku D/max2550VB+18KWת��X����������(�ձ�)������Ʒ���࣬Cu K�����䣬40 kV������50 mA������0.02 (?)��ɨ���ٶ�2 (?)/min��ɨ�跶Χ2��Ϊ10?~90?�����ձ�JEOL��˾��JSM-5600 LVɨ�������������Ʒ�ı�����ò���й۲졣
2 ���������
2.1 ���¹��෴Ӧ������ѧ����
���ѧ��Ӧ����Һ�еĻ�ѧ��Ӧһ����������ѭ����ѧ�Ĺ��ɣ���������Ӧ�ļ���˹�����ܱ�С���㡣��Ӧϵͳ�и����ʵı����ɼ���˹������ �ͱ���
�ͱ��� �����Բ����ã��ٸ������¹�ʽ���Լ����ָ����Ӧ�ļ���˹�����ܱ���ʱ䡣
�����Բ����ã��ٸ������¹�ʽ���Լ����ָ����Ӧ�ļ���˹�����ܱ���ʱ䡣

�ڻ����¶�Ϊ25~30 �������£��������¹��෴Ӧϵͳ���ʵļ���˹�����ܺ��ʽ���Ϊ�����ɼ���˹�����ܺͱ��ʣ��ɼ��������Ӧ�ļ���˹�����ܱ���ʱ䡣
�ɱ�1���ݣ��������Ӧʽ������˹�����ܱ���ʱ������£�
NiCl2?6H2O+(NH4)2C2O4��NiC2O4+2NH4Cl+6 H2O
 = -13.82 kJ/mol��0
= -13.82 kJ/mol��0
 = -29.37 kJ/mol��0
= -29.37 kJ/mol��0
MnCl2?4H2O+(NH4)2C2O4��MnC2O4+2NH4Cl+4 H2O
 = -34.59 kJ/mol��0
= -34.59 kJ/mol��0
 = -34.14 kJ/mol��0
= -34.14 kJ/mol��0
NiCl2?6H2O+2NaOH��Ni(OH)2+2NaCl+6H2O
 =-165.44 kJ/mol��0
=-165.44 kJ/mol��0
 = -112.55 kJ/mol��0
= -112.55 kJ/mol��0
MnCl2?4H2O+2NaOH��Mn(OH)2+2NaCl+4H2O
 = -148.98 kJ/mol��0
= -148.98 kJ/mol��0
 = -206.02 kJ/mol��0
= -206.02 kJ/mol��0
NiCl2?6H2O+Na2CO3?10H2O��NiCO3+2NaCl+16 H2O
 = -33.35 kJ/mol��0
= -33.35 kJ/mol��0
 =150.92 kJ/mol��0
=150.92 kJ/mol��0
MnCl2?4H2O+Na2CO3?10H2O��MnCO3+2NaCl+14H2O
��1 ��Ӧ������������298.15 K�µ�����ѧ����[13]
Table 1 Thermodynamic data of reactants and products at 298.15 K

 = -48.27 kJ/mol��0
= -48.27 kJ/mol��0
 = 62.05 kJ/mol��0
= 62.05 kJ/mol��0
�ɼ�������֪���������£���������Ӧ�� ��С���㣬�ʷ�Ӧ������С����У�NiCl2?6H2O��MnCl2?4H2O��(NH4)2C2O4?H2O��NaOH�ķ�ӦΪ���ȷ�Ӧ(
��С���㣬�ʷ�Ӧ������С����У�NiCl2?6H2O��MnCl2?4H2O��(NH4)2C2O4?H2O��NaOH�ķ�ӦΪ���ȷ�Ӧ(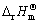 ��0)��NiCl2?6H2O��MnCl2?4H2O��Na2CO3?10H2O�ķ�ӦΪ���ȷ�Ӧ(
��0)��NiCl2?6H2O��MnCl2?4H2O��Na2CO3?10H2O�ķ�ӦΪ���ȷ�Ӧ(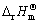 ��0)�������¹��෴Ӧ�У���Ӧ��ͨ����ĥ���л�е�����Ӧ����нϸߵı��ۻ�ܣ���Ӧ�ﻥ��Ӵ���������Ӧ�����ڲ��ᄃ��ṹ��ͬ�ڷ�Ӧ����ɵIJ���ܿ�ӷ�Ӧ���ž����������������ڲ�ķ�Ӧ������õ���е����Ӷ���Ӧ���ϵؽ��У�ֱ����Ӧ��ȫ��
��0)�������¹��෴Ӧ�У���Ӧ��ͨ����ĥ���л�е�����Ӧ����нϸߵı��ۻ�ܣ���Ӧ�ﻥ��Ӵ���������Ӧ�����ڲ��ᄃ��ṹ��ͬ�ڷ�Ӧ����ɵIJ���ܿ�ӷ�Ӧ���ž����������������ڲ�ķ�Ӧ������õ���е����Ӷ���Ӧ���ϵؽ��У�ֱ����Ӧ��ȫ��
2.2 ����ǰ�����DSC-TGA����
ͼ1(a)��ʾΪ���̲�����ǰ�����DSC-TGA���ߡ����̲�����ǰ�����������ʧ���߷�3�Ρ���1�ζ�Ӧ�¶Ƚϵ�(����160 ��)���ɲ����((NH4)2C2O4?H2O)������95 ��ʱ��ˮ���Ӹ��ȼ��ֽ������[13]��֪���˶�ӦΪ����ˮ��ʧȥ�ͷ�Ӧʣ��Ĺ�������淋ķֽ⣬������ʧ��Ϊ7.59%��������������ʧ��7.84%�ӽ�����Ӧһ�����ȷ壻��2�ζ�Ӧ�¶�Ϊ160~300 �棬�ɹ��Ϊ���̲����ηֽ�Ϊ���������������ʧ��Ϊ43.15%��������������ʧ��40.46%�ӽ�����Ӧһ�����ȷ壻��3�ζ�Ӧ�¶�Ϊ300~400 �棬�����Ȼ�淋������¶�Ϊ340 �棬��ʱ������ʧ����Ϊ��Ҫ���Ȼ����������ɣ�������ʧ��Ϊ21.19%������ֵΪ17.23%��ͼ1(b)��ʾΪ������������ǰ�����DSC-TGA���ߡ���ͼ�ɼ���300 ����ǰ����Ʒ�����ֽ⣬����һ����С�����ȷ壬������ʧ��ԼΪ4.88%���˹��̹�����������������ǰ����ʧȥ�ᾧˮ���ֽ�Ϊ���������ͼ1(c)��ʾΪ����̼����ǰ�����DSC-TGA���ߣ�������ʧ���߷ֶβ����ԣ���155 ����ǰ��15.34%��������ʧ���˶�ӦΪ����ˮ��ʧȥ��155~500 ��֮�������������Ե����ȷ壬�ֱ��Ӧ������ʧ��18.66%��5.8%���˶�ӦΪ����̼���εķֽ⣻500 ���������ʧ��������ˮƽ��������������ʧ��

ͼ1 ��ͬ���̻������DSC-TGAͼ
Fig.1 DSC-TGA curves of nickel-manganese composites: (a) Oxalic acid; (b) Hydroxide; (c) Carbonate
��ͼ1���Կ��������̲�������400 �桢��������������300 �桢����̼������500 ������ֽ���ȫ����˽����̲����Ρ������������������̼���ηֱ��������ֽ��¶�������3 h���õ���Ӧ�����������
2.3 ���շֽ���������
ͼ2��ʾΪ���̲�������400 �桢��������������300 �桢����̼������500 ��ֱ����շֽ�3 h�����õ������������SEM��ͼ�пɿ���,���̲��������շֽ�������۳���״��������СΪ50 nm���ң�������������ֽ����������ϸ��������СΪ20 nm���ң�����̼���ηֽ�����������Σ�������СΪ200 nm���ҡ�

ͼ2 ���շֽ��������������SEM��
Fig.2 SEM images of Ni-Mn composite oxides obtained by decomposition of nickel-manganese oxalic acid (a), hydroxide (b) and carbonate (c)
�����¹��෴Ӧ�ϳɵĸ�ǰ�������շֽ�����ɵIJ����н���Ni��Mn���ֽ���Ԫ�ء����������������ͪ������������NiԪ�صĺ������پ�EDTA��ѧ�ζ�������Ʒ��Ni��Mn���ܺ��������ǵõ�MnԪ�صĺ������������������������������Ħ�������ڱ�2��
��2 ��ͬ�������������������������Ħ����
Table 2 Nickel and manganese percentage of different Ni-Mn composite oxides and molar ratio
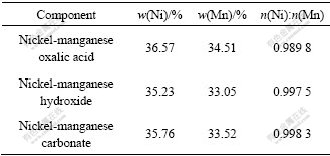
ͼ3��ʾ�ֱ�Ϊ���̲����Ρ������������������̼�������շֽ�����õ������������XRD�ס����̲����ηֽ����(ͼ3(a))��⾧ʯ��NiMn2O4(��JCPDS��01-1110)�ͷ��⾧ʯ��MnNi2O4(��JCPDS��36-0083)��λ����ǿ�Ȼ���һ�¡����ڼ⾧ʯ��NiMn2O4�ͷ��⾧ʯ��MnNi2O4�ķ��λ�û����غϣ�ǿ���������̲����ηֽ������ܺ���NiMn2O4��MnNi2O4�������࣬�ɱ�2�в�ͬǰ�������շֽ��������������������̰ٷֺ�����Ħ���ȿ�֪�����̲�����ǰ�������շֽ����õIJ���������Ħ�����뷴Ӧǰԭ�ϵ�Ͷ�ϱ�1?1����һ�£��ʲ�����NiMn2O4��MnNi2O4��������棻������������ֽ��õ��IJ���(ͼ4(b))�ķ�λ����ǿ�Ⱦ�����������MnNiO3(��JCPDS��65-3695)�����ݻ���һ�£�������������������Ƚϴ���ǿ�Ƚ���������X���߶ྦྷ�������ۣ�˵�������������Ƚ�С�����ͽϲ����̼���ηֽ��õ�NiMn2O4��MnNi2O4��MnNiO3��������(ͼ3(c))������XRD�ķ�������ͼ3(a)��ͼ3(b)������������������ľ����ߴ�ֱ�Ϊ56 nm��13.8 nm����SEM��Ľ�����Ӧ��

ͼ3 ��ͬ�������������XRD��
Fig.3 XRD patterns of Ni-Mn composite oxides obtained by decomposition of nickel-manganese oxalic acid (a), hydroxide (b) and carbonate (c)
XRD�����ݱ��������Ρ�������NaOH��Ӧ�õ���ǰ���徭���շֽ���γ�MnNiO3��һ���ʣ�����ԭ�ӻ�Ͼ��ȡ�������ͬ�ķ�Ӧ�������ɵ����������ʣ���ԭ�������������NiCl2?6H2O��MnCl2?4H2O��NaOH�����¹��෴Ӧʱ������ˮ�����̸����������������������Ϊһ�ֻ������еijɷֹ�����ˮ�����̸����������У��ﵽ���������������ӻ�Ͼ��ȵ�Ŀ�ģ������շֽ⣬�����˵�һ��MnNiO3��ͨ���Ա�������������ǰ�����XRD��(��ͼ4)��̽���[15]�ù��������ϳɵ�ˮ�����̸���������NiMnO3?H2O��XRD���Է������ߵ�����λ�á�ǿ�Ȼ���һ�£�֤���˸ù۵㡣����NiCl2?6H2O��MnCl2?4H2O����Na2CO3?10H2O��Ӧʱ�����ڷ�Ӧ�������ڴ���������ˮ��������Ӧ��ϵ���Խ�����Һ�෴Ӧ��ϵ��Ni2+��Mn2+�������ӿ�����Ϊ����Һ����˹���������������NiCO3��MnCO3���ܶȻ����ϴ�NiCO3���ܶȻ�Ϊ6.6��10-9��MnCO3���ܶȻ�Ϊ1.8��10-11[16]��������Ni2+��Mn2+���������ڹ�����ʱ���ɵIJ��ﲢ���ǰ���1?1�ı������ȳ����ģ������շֽ������������3�֣�NiMn2O4��MnNi2O4��MnNiO3������XRD��֪��MnNiO3���ǿ�Ƚ�ǿ������̼�������շֽ��IJ�����ҪΪMnNiO3��������NiCl2?6H2O��MnCl2?4H2O��(NH4)2C2O4?H2O��Ӧ�����ɵ�ˮ���ޣ�Ni2+��Mn2+����������Ҫ���ڹ�������Ϸ����Ӵ���������������û�дﵽԭ��ˮƽ�ľ��Ȼ�ϣ���ϳ̶��������շֽ������NiMn2O4��MnNi2O4�������ࡣ

ͼ4 ������������ǰ�����XRD��
Fig.4 XRD pattern of nickel-manganese hydroxide precursor
3 ����
1) ͨ������NiCl2?6H2O��MnCl2?4H2OΪ���Σ���(NH4)2C2O4?H2O��NaOH��Na2CO3?10H2O�����¹��෴Ӧ��������ѧ�����֪����Ӧ����������У�������(NH4)2C2O4?H2O��NaOH�ķ�ӦΪ���ȷ�Ӧ����Na2CO3?10H2O�ķ�ӦΪ���ȷ�Ӧ��
2) ������3�����¹��෴Ӧ�У���NaOH��Ӧ���ɵ�ǰ�������շֽ�����õ����������������ϸ����(NH4)2C2O4?H2O��Ӧ���ɵ�ǰ�������շֽ�����õIJ��������֮����Na2CO3?10H2O��Ӧ���ɵ�ǰ�������շֽ�����ò��������֡�
3) XRD�о����������̲����ηֽ�õ�NiMn2O4��MnNi2O4��������������ֽ�õ�MnNiO3������̼���ηֽ�õ�NiMn2O4��MnNi2O4��MnNiO3�Ļ�����ࡣ
4) �Ӳ���ijɷ֡���ò�ṹ���ǣ�����NiCl2?6H2O��MnCl2?4H2O��NaOH�����¹��෴Ӧ-���շֽⷨ�ϳɵ�MnNiO3������ã�����Ϊ����Ӷ��ε����������LiNi0.5Mn0.5O2��ԭ�ϡ�
REFERENCES
[1] Ohzuku T, Makimura Y. Layered lithium insertion material of LiNi0.5Mn0.5O2: A possible alternative to LiCoO2 for advanced lithium-ion batteries[J]. Chem Lett, 2001, 8: 744-745.
[2] Lu Z H, Macneil D D, Dahn J R. Layered cathode materials Li[Ni, Li(1/3-2x/3)Mn(2/3-x/3)]O2 for lithium-ion batteries[J]. Electrochemical and Solid-States Letters, 2001, 4(11): A191-A194.
[3] Saifu I M, Andrew D R. Structural and electronic properties of the layered LiNi0.5Mn0.5O2 lithium battery material[J]. Journal of Chemistry Materials, 2003, 12: 4280-4286.
[4] Yoon W S, Grey C P. In situ X-ray absorption spectroscopic study on LiNi0.5Mn0.5O2 cathode material during electrochemical cycling[J]. Journal of Chemistry Materials, 2003, 15(16): 3161-3169.
[5] Reed J, Ceder G. Charge, Potential, and phase stability of layered Li(Ni0.5Mn0.5)O2[J]. Electrochemical and Solid State Letters, 2002, 5(7): A145-A148.
[6] Ф ��, ����Ӣ, ���Ҷ�, �� ��, ������. ����ӵ����������LiNi0.5Mn0.5O2��ѭ������[J]. �й���ɫ����ѧ��, 2006, 16(8): 1439-1445.
XIAO Jin, ZENG Lei-ying, PENG Zhong-dong, ZHAO Hao, HU Guo-rong. Cycle performance of LiNi0.5Mn0.5O2 as cathode material for lithium secondary batteries[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(8): 1439-1445.
[7] Yasuhiro F, Hiroshi M. Lithium nickel manganese mixed oxides, their manufacture, and lithium ion secondary battery using them[P]. JP 2004 002141, 2004.
[8] Kovanda F, Grygar T, Dornicak V. Thermal behaviour of Ni-Mn layered double hydroxide and characterization of formed oxides[J]. Solid State Sciences, 2003, 5(7): 1019-1026.
[9] Gyrdasova O I, Bazuev G V, Krasilpnikov V N, et al. Synthesis of NiMnO3 ilmenite by thermal decomposition of double oxalates and their hydrazine compounds[J]. Journal Neorganicheskoi Khimii, 2003, 48(9): 1446-1451.
[10] Mehandjiev D, Zhecheva E, Ivanov G. Preparation and catalytic activity of nickel-manganese oxide catalysts with an ilmenite-type structure in the reactions of complete oxidation of hydrocarbons[J]. Applied Catalysis, A: General, 1998, 167(2): 277-282.
[11] �� ��, �ֵ���, ����, ��, ����Ȫ. ���ȹ��෴Ӧ�Ʊ������ײ��ϵķ���[J]. ����ѧѧ��, 2004, 8(8): 881-888.
YANG Yu, JIA Dian-zeng, GE Wei-wei, JIN Chun-fei, XIN Xin-quan. Synthetic of inorganic nano-materials by solid state reaction at low-heating temperature[J]. Wuji Huaxue Xuebao(Chinese J Inorg Chem), 2004, 8(8): 881-888.
[12] ̷ ��, �����. ���ѧ��Ӧ������ѧ������������̽��[J]. ����ʦ���ߵ�ר��ѧУѧ��, 2003, 24(5): 68-70.
TAN Ni, WANG Feng-jie. Analyzing the thermodynamics of solid chemical reaction and making an inquiry into its superiority[J]. Journal of Chenzhou Teachers College (Chinese J Inorg Chem), 2003, 24(5): 68-70.
[13] �ϰ� J A. ���ϻ�ѧ�ֲ�[M]. �о÷�, ��. ����: ��ѧ������, 1985: 1470-1520.
Dean J A. Lange��s handbook of chemistry[M]. SHANG Jiu-fang, transl. Bejing: Science Press, 1985: 1470-1520.
[14] ������, �ΰ�ƽ. ����ˮ��Һ����ѧ���ݼ����ֲ�[M]. ����: ұ��ҵ������ 1985: 429.
YANG Xian-wang, HE Ai-ping. Calculating handbook of thermodynamic data in high temperature solution[M]. Beijing: Metallurgical Industry Press, 1985: 429.
[15] �̽���, ������, ����ΰ. ���������ϳ�һ�����͵�ˮ�����̸���������NiMnO3?H2O[J]. ��ѧ�����﹤��, 2005, 22(8): 16-18.
CHENG Jin-guo, LIANG Yong-guang, Wang Chi-wei. Synthesis of a novel nickel manganese oxide hydrate-NiMnO3?H2O by coprecipitation method[J]. Chemistry and Bioengineering, 2005, 22(8): 16-18.
[16] ��Ӣ��, �����. ��������ѧ�����ֲ�[M]. ����: ������ѧ������, 1993: 618.
LIANG Ying-jiao, CHE Yin-chang. Handbook of inorganic substance thermodynamics parameter[M]. Shenyang: Northeastern University Press, 1993: 618.
�ո����ڣ�2007-02-27�������ڣ�2007-06-06
ͨѶ���ߣ���־�ˣ����ڣ��绰��0731-8836633��E-mail: zxwang@mail.csu.edu.cn
(�༭ ��ѧ��)