文章编号:1004-0609(2015)08-2236-07
钨钼分离吸附剂的选择性判据
王文强1,何利华1,赵中伟1, 2
(1. 中南大学 冶金与环境学院,长沙 410083;
2. 中南大学 稀有金属冶金与材料制备湖南省重点实验室,长沙 410083)
摘 要:借鉴浮选药剂与矿物作用的亲固能计算方法,得到钨钼分离体系吸附剂与被吸附基团的吸附能计算公式。基于逐级均分法计算出钨钼分离过程中主要原子团的基团电负性,发现钼原子团( )的基团电负性随着x的增加而减小,其与钨氧原子团(
)的基团电负性随着x的增加而减小,其与钨氧原子团( )的电负性差异也逐渐增大。通过吸附能计算公式得到钨钼原子团在不同吸附剂上的吸附能,表明吸附剂极性越低,其对四硫代钼酸根的吸附能力越强。从而预测系列化合物对钼硫原子团选择性吸附的强弱,并被选择性沉淀法及实验室实验印证。本研究中吸附剂的分子设计思路有望为新型钨钼分离试剂的开发设计提供理论指导。
)的电负性差异也逐渐增大。通过吸附能计算公式得到钨钼原子团在不同吸附剂上的吸附能,表明吸附剂极性越低,其对四硫代钼酸根的吸附能力越强。从而预测系列化合物对钼硫原子团选择性吸附的强弱,并被选择性沉淀法及实验室实验印证。本研究中吸附剂的分子设计思路有望为新型钨钼分离试剂的开发设计提供理论指导。
关键词:吸附能;钨;钼;分离;基团电负性;选择性沉淀法
中图分类号:TF841 文献标志码:A
Selectivity criterion of adsorbents for separation of tungsten and molybdenum
WANG Wen-qiang1, HE Li-hua1, ZHAO Zhong-wei1, 2
(1. School of Metallurgy and Environment, Central South University, Changsha 410083, China;
2. Hunan Key Laboratory for Metallurgy and Material Processing of Rare Metals, Central South University,
Changsha 410083, China)
Abstract: Using the calculation method of interaction energy between flotation reagent and mineral, the calculation formula of absorption energy between adsorbent and adsorbed groups was derived for the separation of tungsten and molybdenum. Group electronegativities of related atom groups were calculated based on the electronegativity equalization, the group electronegativity of  decreases with the increase of x, meanwhile, the difference between
decreases with the increase of x, meanwhile, the difference between  and
and  in group electronegativity enlarges. The adsorption energies of related atom groups on different adsorbents are obtained by the formula. The adsorption ability for
in group electronegativity enlarges. The adsorption energies of related atom groups on different adsorbents are obtained by the formula. The adsorption ability for  increases with the decrease of adsorbent polarity. The adsorption abilities of a series of compounds for
increases with the decrease of adsorbent polarity. The adsorption abilities of a series of compounds for  were predicted which were verified by selective precipitation and experiments given in this work. The method for molecular design of adsorbents may give directions for the development of new agents for separation of tungsten and molybdenum.
were predicted which were verified by selective precipitation and experiments given in this work. The method for molecular design of adsorbents may give directions for the development of new agents for separation of tungsten and molybdenum.
Key words: adsorption energy; tungsten; molybdenum; separation; group electronegativity; selective precipitation
在钨提取冶金过程中,钼是必须严格控制的元素。如国标GB/T 10116―2007规定0级APT(仲钨酸铵)产品中钼与三氧化钨的质量比不大于0.020%。钨钼属同一副族元素,其外层电子层结构相似,分别是4d55s1和5d46s1,二者离子的主要价态均为+6价,此外,由于“镧系收缩”的原因,使得二者的原子半径(钨的原子半径为0.137 nm,钼的原子半径为0.136 nm[1])、离子半径、络阴离子半径都极为接近。因此,钨钼的化学性质极为相似,很难被分离。
长期以来,国内外学者围绕钨钼分离开展了大量研究,代表性的成果主要有三硫化钼沉淀法[2]、溶剂萃取法[3-7]、离子交换法[8-11]、活性炭吸附法[12-14]等。目前工业上应用最为广泛的是选择性沉淀法。选择性沉淀法分离钨钼的原理在于利用钨亲氧、钼亲硫的地球化学性质[15],将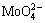 硫化为
硫化为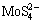 ,而钨仍然以
,而钨仍然以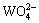 形式存在,以此扩大钨钼原子团的性质差异,再加入CuS等金属硫化物,CuS与
形式存在,以此扩大钨钼原子团的性质差异,再加入CuS等金属硫化物,CuS与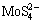 反应形成Cu-S-Mo簇合物沉淀,从而将Mo从钨酸盐中深度除去。该方法具有分离系数高、处理对象广、成本低、除钼率高(达97.41%~99.64%[16-18])等优势,目前,在我国钨冶炼企业中使用率超过90%。
反应形成Cu-S-Mo簇合物沉淀,从而将Mo从钨酸盐中深度除去。该方法具有分离系数高、处理对象广、成本低、除钼率高(达97.41%~99.64%[16-18])等优势,目前,在我国钨冶炼企业中使用率超过90%。
然而,随着钨资源的大量使用,优质钨资源已消耗殆尽,高钼钨资源的高效利用已成为制约我国钨工业可持续发展的难题之一,而解决这一难题的关键技术之一就是高钼钨酸盐溶液中钨钼的有效分离。选择性沉淀法对于钨和钼质量比大于20的钨资源能够经济有效地处理,而对于钨和钼质量比小于20的处理成本则显著增加。因此,为扩大选择性沉淀法的适应范围,本文作者课题组曾对这一钨钼分离过程的机理进行了探索研究[16, 18]。借助于分子设计理论,从亲水-疏水因素、几何因素及其他因素(容量、动力学)等方面分析了CuS、NiS、CoS等硫化物对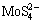 的选择性吸附作用,给出了过渡金属硫化物分离钨钼的定性判断依据。
的选择性吸附作用,给出了过渡金属硫化物分离钨钼的定性判断依据。
尽管如此,目前为止尚缺乏一个简单有效的能够定量地来解释金属硫化物对硫代钼酸根的选择性吸附作用强弱的判据。本文作者试图借鉴相关学科的理论,从分子设计的角度解释金属硫化物对硫代钼酸根的选择性吸附。
作为相关学科,矿物浮选过程也要涉及类似的液固化学反应。浮选药剂离子与矿物颗粒表面发生化学反应作用而被吸附,这与分离过程的吸附在化学本质上是一致的。分子设计方法在选矿中的应用已有大量报道[19-23]。比如带某一特定功能团的药剂的优化,或用于特定矿物浮选官能团的寻找等。但是在溶液中不但要设计溶液离子的形态,更要设计合理的吸附剂以使之易于吸附。这相当于在选矿中应要求为某种浮选药剂设计特定的矿物而使试剂呈现出特效,因而更有其难度。但种种选矿设计理论对于本研究工作仍具有极为重要的参考价值。
陈建华等[24]给出了浮选药剂与矿物作用的亲固能的计算方法,用于分析矿物表面极性、药剂分子极性和介质水的相互影响,取得了较好的结果。本文作者拟借鉴这一方法研究过渡金属硫化物对钨酸盐溶液中钼原子团的吸附机理,以期为新型钨钼分离试剂的开发提供一定的理论指导。
1 吸附模型
1.1 被吸附离子与吸附剂作用
在矿物浮选过程,药剂与矿物的作用涉及矿物表面、水分子和药剂亲固基团之间的相互作用,陈建华等[24]建立了表面键合模型,从热力学角度分析了药剂在矿物表面吸附前后体系的能量变化情况,取得了很好的效果。而选择性沉淀法中过渡金属硫化物对钼硫原子团的吸附和药剂与矿物的作用过程相类似,本研究拟类比矿物浮选中的表面键合模型建立过渡金属硫化物与钨钼原子团的吸附模型。
在此,以X-Y表示为溶液中的离子对,其中Y为被吸附离子(含钨钼原子团),在选矿过程中相应为浮选药剂的亲固基团。X为反号离子;A,B为吸附剂。据文献[24],被吸附离子与吸附剂作用形成表面配位化合物的过程可认为由4步组成:
1) 离子对与水分子分离,该过程所消耗能量为ΔE1;
X-Y・H2O→X-Y+ H2O (1)
2) 吸附剂表面与水分子分离,该过程所消耗能量为ΔE2;
AB・H2O→AB+ H2O (2)
3) 离子对与吸附剂作用,该过程释放的能量为ΔE3;
X-Y+AB→X-Y・AB (3)
4) 水分子与水分子的结合,所放出的能量为ΔE4。
H2O + H2O→H2O・H2O (4)
因此,整个过程的能量变化如式(5)所示
ΔE=ΔE1+ΔE2+ΔE3+ΔE4 (5)
式中:ΔE为吸附过程的吸附能。
1.2 吸附能的计算方法
考虑到钨、钼在工业浸出液中均以阴离子形式存在,与黄药等浮选药剂的官能团类似,因此,将钨钼的原子团类比浮选药剂,过渡金属硫化物吸附剂类比矿物,得到金属硫化物吸附钨钼原子团吸附过程的吸附能计算公式。公式的具体推导过程可参见文献[24]。将离子对中的阳离子统一为氢,从而得到

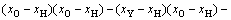
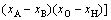 (6)
(6)
式中:x为原子或者基团的电负性;K为10;n一般情况下为1(除非特别声明)。另外,在文献[24]中,定义吸附反应放热时ΔE为正值,为与物理化学惯例相符,在本研究中改为负值。
当前钨矿分解工艺主要为碱法工艺,包括苏打压煮法、氢氧化钠分解法[25-28]等,所得含钨钼料液通常为钠盐溶液。因此,对于钨提取冶金的分离过程来说,将反号离子X统一定为氢显然有所不妥。例如,在一般情况下,钨以钨酸钠、钼以钼酸钠形式存在,而不是其相应的酸的形式。因而,对于钨钼分离体系来说,反号离子X定为钠似乎更为合理,这样可得


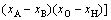 (7)
(7)
考虑到问题的一般性,在低pH下待吸附物质以HY形式存在,而在高pH下以NaY形式存在。则可近似以pH为基准,将吸附能对以上两种情况加权平均,即可得吸附能的计算公式如式(8)所示:
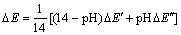 (8)
(8)
在选择性沉淀法工业实践中,钼硫化需要将pH调至弱碱性条件下,本文作者拟以pH=8.5为例进行计算可得(以下研究中的吸附能皆以pH=8.5计算得到):
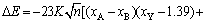

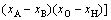 (9)
(9)
假定吸附剂表面极性连续,上式对( )求导可得
)求导可得

 (10)
(10)
由式(10)可知,当被吸附离子的基团电负性小于2.73时,有
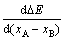 >0 (11)
>0 (11)
式中:ΔE为增函数,即吸附剂的极性( )越小,其与被吸附离子间的作用越强。
)越小,其与被吸附离子间的作用越强。
而当被吸附离子电负性大于2.73时,有
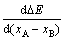 <0 (12)
<0 (12)
式中:ΔE为减函数,增大吸附剂极性有利于吸附。ΔE越负,则表示被吸附离子与吸附剂作用放出能量越大,吸附作用越强。
2 吸附模型在钨钼分离中的应用
2.1 基团电负性的计算
在计算吸附过程的吸附能之前,需要先求出吸附体系相关原子团的电负性,本体系中主要涉及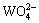 、
、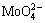 以及硫代钼酸根
以及硫代钼酸根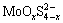 (x=0, 1, 2, 3)等基团的电负性。考虑到
(x=0, 1, 2, 3)等基团的电负性。考虑到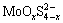 (x=1, 2, 3)与吸附剂作用时,其与吸附剂之间的键合原子可能为O也可能为S,因此,相应的基团电负性会有两个不同值。本研究采用李朝恩[29]及BRATSCH[30]推荐的逐级均分法计算相关原子团的基团电负性,
(x=1, 2, 3)与吸附剂作用时,其与吸附剂之间的键合原子可能为O也可能为S,因此,相应的基团电负性会有两个不同值。本研究采用李朝恩[29]及BRATSCH[30]推荐的逐级均分法计算相关原子团的基团电负性, (x=1, 2, 3)的电负性有两个结果,前者为以O为键合原子计算结果,后者为以S为键合原子计算结果。求得钨钼分离过程所涉及的几种主要原子团的基团电负性如表1所示。
(x=1, 2, 3)的电负性有两个结果,前者为以O为键合原子计算结果,后者为以S为键合原子计算结果。求得钨钼分离过程所涉及的几种主要原子团的基团电负性如表1所示。
由表1知,钨酸根和钼酸根原子团电负性分别为3.28和3.25,几乎相等。则按所得吸附能计算公式,凡与钼氧原子团能较好结合的吸附物质,其与钨氧原子团也应有几乎相同的结合能力。因此,难于直接分离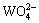 和
和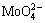 。此外,当钼氧原子团中的氧原子逐渐为硫原子所取代,其电负性逐渐趋小,与钨氧原子团电负性差异也逐渐加大,钨钼分离成为可能。因而立足于先硫化后分离的思路是比较合理的。由于钼氧与钨氧原子团的电负性均大于2.73,其与吸附剂的作用能力将随吸附剂极性的下降而减弱。而钼硫原子团则相反,因其电负性小于2.73,显然吸附剂的极性减小有利于钼的吸附。所以,从
。此外,当钼氧原子团中的氧原子逐渐为硫原子所取代,其电负性逐渐趋小,与钨氧原子团电负性差异也逐渐加大,钨钼分离成为可能。因而立足于先硫化后分离的思路是比较合理的。由于钼氧与钨氧原子团的电负性均大于2.73,其与吸附剂的作用能力将随吸附剂极性的下降而减弱。而钼硫原子团则相反,因其电负性小于2.73,显然吸附剂的极性减小有利于钼的吸附。所以,从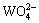 溶液中除去
溶液中除去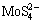 的吸附剂AB的极性(
的吸附剂AB的极性( )应尽可能小。
)应尽可能小。
表1 钨钼原子团的基团电负性
Table 1 Electronegativity of tungsten and molybdenum atom groups

2.2 吸附过程的吸附能计算与分析
上述计算时发现在计算硫代钼酸根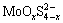 (x=1, 2, 3)基团电负性时,键合原子不同则其基团电负性值不同,所以计算吸附能前需要考虑吸附过程中的键合原子。
(x=1, 2, 3)基团电负性时,键合原子不同则其基团电负性值不同,所以计算吸附能前需要考虑吸附过程中的键合原子。
叶向荣等[31-32]对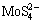 与铜形成的簇合物进行研究,通过红外光谱特征分析发现,硫主要以两种形式存在于
与铜形成的簇合物进行研究,通过红外光谱特征分析发现,硫主要以两种形式存在于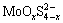 (x=1, 2, 3)配体中:一种起桥键作用,即连接Mo(W)原子与过渡金属原子形成M―S―Cu键;另一种起双键作用,这一形态的硫不会与过渡金属反应,但是能够被氧原子取代。因此,在
(x=1, 2, 3)配体中:一种起桥键作用,即连接Mo(W)原子与过渡金属原子形成M―S―Cu键;另一种起双键作用,这一形态的硫不会与过渡金属反应,但是能够被氧原子取代。因此,在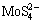 与铜形成的簇合物中
与铜形成的簇合物中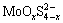 (x=1, 2, 3)中的氧原子仅为端基而非桥连,不能与铜形成M―O―Cu键。鉴于选择性沉淀法中所采用的吸附剂皆为亲硫过渡金属元素的硫化物,且较钨而言,钼亦为亲硫元素[13]。因此,在计算
(x=1, 2, 3)中的氧原子仅为端基而非桥连,不能与铜形成M―O―Cu键。鉴于选择性沉淀法中所采用的吸附剂皆为亲硫过渡金属元素的硫化物,且较钨而言,钼亦为亲硫元素[13]。因此,在计算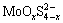 (x=1, 2, 3)与吸附剂的吸附能时,其基团电负性均以S为键合原子计算所得值为准。
(x=1, 2, 3)与吸附剂的吸附能时,其基团电负性均以S为键合原子计算所得值为准。
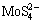 的基团电负性为2.52,从吸附能计算公式中可知,吸附剂AB的极性尽可能小以确保吸附剂对硫代钼酸根的吸附能力。考虑到硫代钼酸根与吸附剂的直接作用原子为硫,因而选择亲硫元素原子作为吸附剂的配合原子较为适宜。而与之化合的原子或原子团的选择原则应为其电负性与配合金属原子尽可能接近这一原则,筛选了大量有机和无机的亲硫金属盐类。表2所列为其中典型的计算结果。表2中
的基团电负性为2.52,从吸附能计算公式中可知,吸附剂AB的极性尽可能小以确保吸附剂对硫代钼酸根的吸附能力。考虑到硫代钼酸根与吸附剂的直接作用原子为硫,因而选择亲硫元素原子作为吸附剂的配合原子较为适宜。而与之化合的原子或原子团的选择原则应为其电负性与配合金属原子尽可能接近这一原则,筛选了大量有机和无机的亲硫金属盐类。表2所列为其中典型的计算结果。表2中 (x=1, 2, 3)的电负性取以S为键合原子为准,M为N,N-2(二硫代胺基甲酸)铜,N为磺原酸铜。作为对比,研究了极性相对较大的吸附剂对钨钼分离体系中各原子团的吸附情况,碱土金属盐BaSO4的极性计算值为2.43。图1所示为钼原子团硫代化程度对吸附能的影响。
(x=1, 2, 3)的电负性取以S为键合原子为准,M为N,N-2(二硫代胺基甲酸)铜,N为磺原酸铜。作为对比,研究了极性相对较大的吸附剂对钨钼分离体系中各原子团的吸附情况,碱土金属盐BaSO4的极性计算值为2.43。图1所示为钼原子团硫代化程度对吸附能的影响。
由理论计算结果可知,弱极性金属硫化物对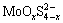 的吸附能随其硫代化程度的增大而降低,即其所形成的产物越来越稳定,对钼的选择性吸附效果越好,而对
的吸附能随其硫代化程度的增大而降低,即其所形成的产物越来越稳定,对钼的选择性吸附效果越好,而对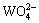 的吸附能始终远远大于0,即基本不吸附钨,具有良好的钨钼分离性能。在表2的几种金属硫化物中,以计算的吸附能判断,PbS对
的吸附能始终远远大于0,即基本不吸附钨,具有良好的钨钼分离性能。在表2的几种金属硫化物中,以计算的吸附能判断,PbS对 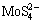 的吸附性能最好,吸附能达到-53.1 kJ/mol。而随着金属硫化物极性的增强,其对四硫代钼酸根的吸附能按NiS、CuS、CoS、FeS、ZnS的次序降低。此外,N,N-2(二硫代胺基甲酸)铜、磺原酸铜也具有较好的吸附能力,按计算结果其与
的吸附性能最好,吸附能达到-53.1 kJ/mol。而随着金属硫化物极性的增强,其对四硫代钼酸根的吸附能按NiS、CuS、CoS、FeS、ZnS的次序降低。此外,N,N-2(二硫代胺基甲酸)铜、磺原酸铜也具有较好的吸附能力,按计算结果其与 的吸附能小于-32.8 kJ/mol,因而,其对钼的吸附性能甚至优于NiS的。
的吸附能小于-32.8 kJ/mol,因而,其对钼的吸附性能甚至优于NiS的。
与之形成鲜明对比的是,强极性的离子型化合物BaSO4对硫代钼酸根的吸附能随着硫代化程度的增加而升高,即吸附过程需要吸收大量能量。BaSO4对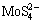 的计算吸附能为52.2 kJ/mol,已不具备吸附
的计算吸附能为52.2 kJ/mol,已不具备吸附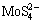 的能力。与之相反的是,BaSO4对
的能力。与之相反的是,BaSO4对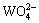 及
及 的吸附能分别达到-138.3和-130.8 kJ/mol,吸附能极大,但对钨钼没有分离效果。
的吸附能分别达到-138.3和-130.8 kJ/mol,吸附能极大,但对钨钼没有分离效果。
表2 钨钼原子团在各种吸附剂上的吸附能计算结果
Table 2 Adsorption energy of related atom groups on different adsorbents by calculating


图1 钼原子团硫代化程度对吸附能的影响
Fig. 1 Effect of sulfur substitution for  on adsorption energy
on adsorption energy
根据以上理论计算结果可知,NiS等弱极性金属硫化物对硫代钼酸根的吸附性能随着硫代化程度的增加而增强,而其对钨原子团的吸附能力极弱。因此,基于先硫化增大钨钼原子团性质差异,再选择性沉淀分离钨钼的实践中,过渡金属硫化物对钼硫原子团的选择性吸附可以用本研究的理论合理解释。
2.3 实验检验
为验证本文理论的正确性,查阅了相关研究结果并通过验证实验进行检验。
李洪桂等[18]用含150 g/L WO3、0.6 g/L Mo的Na2WO4溶液,在pH为7.6,游离S2-浓度为2 g/L的室温下硫化12 h后,加入金属硫化物,搅拌2 h,过滤,分析溶液中的残钼量。表3所列为沉淀除钼后所得滤液中钼的分析结果。由表3可知,NiS、CoS、CuS、PbS等硫化物具有很好的除钼效果,除钼率均在97%以上,FeS的除钼率已明显降低,仅为76%,而ZnS的除钼率仅为12.2%,已基本不具有作为除钼剂的价值。
表3 除钼实验结果[18]
Table 3 Experimental results of removing molybdnum[18]

霍广生等[16]对不同金属硫化物对四硫代钼酸根的吸附行为进行了研究,以含150 g/L WO3、0.6 g/L Mo的已硫化的Na2WO4溶液,分别加入不同量的金属硫化物进行选择性除钼实验。图2所示为吸附剂加入量对除钼率的影响。由图2可知,在NiS、CoS、CuS 3种金属硫化物在用量约为理论用量的3~4倍的情况下即可将约99%的钼选择性沉淀分离,从而实现钨钼的高效分离;当PbS作吸附剂时,在加入量达到理论量的5倍以上时同样具有较好的分离效果;而FeS、HgS以及ZnS即使在加入量达到理论量的6倍以上仍然不能很好的选择性吸附钼,因而不能作为高效的钨钼分离试剂。
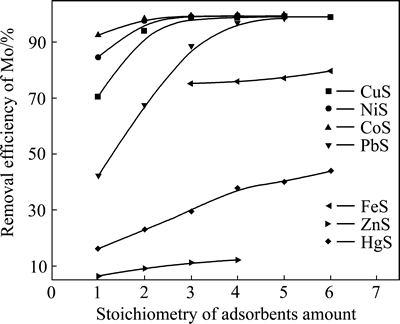
图2 吸附剂加入量对除钼率的影响[16]
Fig. 2 Effect of adsorbents amount on removal efficiency of Mo[16]
本研究理论计算的结果与文献[16, 18]的研究结果基本相符,为进一步验证本研究理论计算的正确性,选取了表2中5种比较有代表性的硫化物NiS、CuS、ZnS、N,N-2(二硫代胺基甲酸)铜以及磺原酸铜进行除钼验证试验。
以含80 g/L WO3、0.4 g/L Mo料液硫化后用各种吸附剂处理。NiS为除钼剂时的钨钼分离系数高达12000,具有极高的选择性,CuS也有类似效果,NiS、CuS都是极好的钼沉淀剂。而ZnS对钨钼的分离能力已较差,钼的沉淀率仅为13%,已不能作为钨钼的有效分离试剂。另外,本研究制备了硫代胺基甲酸树脂,与硫酸铜反应后制成N,N-2(二硫代胺基甲酸)铜吸附剂测试其效果,除钼能力极强。磺原酸棉的钨钼分离系数为4200,由于没有分析树脂吸附钨量而未能计算前者的钨钼分离系数。特别是离子交换纤维磺原酸棉具有很大的比表面积,吸附的动力学过程极快,与溶液接触数秒即因钼被完全吸附而使溶液由橙红迅速转为无色。以上吸附剂在吸附后均可方便的用Na2S解吸。但硫化胺基甲酸树脂和磺原酸棉在解吸时出现掉铜现象。这是由于硫代胺基甲酸铜和磺原酸棉铜的溶度积较硫化铜的大,在解吸时发生复分解反应而生成CuS的缘故。
3 结论
1) 借鉴分子设计理论,将浮选药剂与矿物作用的亲固能的计算方法运用到钨钼分离过程中,得出过渡金属硫化物吸附剂对钨钼原子团吸附能的计算公式。
2) 基于逐级均分法计算钨钼分离过程中相关原子团的基团电负性,发现随着钼原子团硫代化程度的增加,其基团电负性逐渐降低,与钨氧原子团的电负性差别逐渐增大,因而从基团电负性的角度证明基于先硫化再分离钨钼的思路在理论上是完全有据可依的。
3) 依据推导的吸附能公式计算出不同金属硫化物对钨钼相关原子团的吸附能,以此为理论依据筛选出具有高效钨钼分离能力的吸附剂,并进行实验检验,结果与理论预测相符,从而简单有效地阐明了选择性沉淀法中过渡金属硫化物对硫代钼酸根的选择性吸附机理,为新型钨钼分离试剂的筛选或开发提供了一定的理论指导。
REFERENCES
[1] 申泮文, 车云霞, 罗裕基. 无机化学丛书(第八卷)[M]. 北京: 科学出版社, 1998.
SHEN Pan-wen, CHE Yun-xia, LUO Yu-ji. Inorganic chemistry (Volume 8)[M]. Beijing: Science Press, 1998.
[2] BECHSTEAD L W, HOGSETT R F, HUGGINS D K, QUENEAU P B, ZIEGLER R C. Separation of trace molybdenum from tungstate solutions: USA, US4303623[P]. 1981-12-01.
[3] GUAN W, ZHANG G, GAO C. Solvent extraction separation of molybdenum and tungsten from ammonium solution by H2O2-complexation[J]. Hydrometallurgy, 2012, 127/128: 84-90.
[4] 黄蔚庄, 龚柏凡, 张启修. 溶剂萃取硫代钼酸盐分离钨钼[J]. 中国有色金属学报, 1995, 5(1): 45-47.
HUANG Wei-zhuang, GONG Bo-fan, ZHANG Qi-xiu. Separation of thiotungstate and thiomolybdate by solvent extraction[J]. The Chinese Journal of Nonferrous Metals, 1995, 5(1): 45-47.
[5] KAGERMANIAN V S, RUMYANTSEV V K, VOLDMAN G M, ZELIKMAN A N, ZIBEROV G N. Process for separation of tungsten and molybdenum by extraction: USA, US3969478[P]. 1976-07-13.
[6] KIM B M. Process for separation of molybdenum from tungsten leachates: USA, US4443414[P]. 1984-04-17.
[7] GUAN W, ZHANG G, GAO C. Precursor solution prepared by evaporation deamination complex method for solvent separation of Mo and W by H2O2-complexation[J]. Transactions of Nonferrous Metals Society of China, 2013, 23(4): 1139-1146.
[8] 陈洲溪, 陈树翘. 用离子交换法分离钨酸盐溶液中的钼[J]. 中国钨业, 1996(8): 8-14.
CHEN Zhou-xi, CHEN Shu-qiao. Separation of molybdenum from tungstate solution by ion exchange method[J]. China Tungsten Industry, 1996(8): 8-14.
[9] 陈洲溪. 离子交换法从钨酸盐溶液中除钼新工艺已通过鉴定[J]. 中国钨业, 1993(1): 35.
CHEN Zhou-xi. A new process for separation of molybdenum from tungstate solution by ion exchange passed identification[J]. China Tungsten Industry, 1993(1): 35.
[10] 刘旭恒, 胡 芳, 赵中伟. 大孔型树脂处理高浓度钨酸钠溶液[J]. 中国有色金属学报, 2014, 24(7): 1895-1900.
LIU Xu-heng, HU Fang, ZHAO Zhong-wei. Treatment of high concentration sodium tungstate with macroporous resin[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(7): 1895-1900.
[11] LU X, HUO G, LIAO C. Separation of macro amounts of tungsten and molybdenum by ion exchange with D309 resin[J]. Transactions of Nonferrous Metals Society of China, 2014, 24(9): 3008-3013.
[12] 黄蔚庄, 龚柏凡. 柱式吸附法从钨酸钠溶液中分离钼的研究[J]. 稀有金属与硬质合金, 1994(1): 1-4.
HUANG Wei-zhuang, GONG Bo-fan. Use of absorption column for separation of molybdenum from sodium tungstate solution[J]. Rare Metals and Cemented Carbides, 1994(1): 1-4.
[13] GONG Bo-fan, HUANG Wei-zhuang, ZHANG Qi-xiu. A study on separation of molybdenum from tungsten by an adsorption process using activated carbon[J]. International Journal of Refractory Metals and Hard Materials, 1996, 14(5/6): 319-323.
[14] 万林生, 代亚琦, 赵立夫, 肖学有, 章小兵, 李 飞. 高纯钨酸铵溶液中活性炭深度除钼研究[J]. 中国钨业, 2009, 24(6): 20-22.
WAN Lin-sheng, DAI Ya-qi, ZHAO Li-fu, XIAO Xue-you, ZHANG Xiao-bing, LI Fei. The study of deep molybdenum removal by activated carbon in high-purity solution of ammonium tungstate[J]. China Tungsten Industry, 2009, 24(6): 20-22.
[15] 赵中伟, 何利华. 地球化学对钨钼分离的借鉴[J]. 中国有色金属学报, 2014, 24(6): 1637-1647.
ZHAO Zhong-wei, HE Li-hua. Enlightenment of geochemistry on separation of molybdenum and tungsten[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(6): 1637-1647.
[16] 霍广生. 钨冶炼过程中钨钼分离新工艺及其理论研究[D]. 长沙: 中南大学, 2001.
HUO Guang-sheng. The new technics and basics theory of removing molybdenum from tungsten in the process of the process of tungsten metallurgy[D]. Changsha: Central South University, 2001.
[17] ZHAO Z, GAO L, CAO C, LI J, CHEN X, CHEN A, LIU X, SUN P, HUO G, LI Y, LI H. Separation of molybdenum from tungstate solution―Scavenging thiomolybdate by copper compound[J]. Metallurgical and Materials Transactions B, 2012, 43(6): 1284-1289.
[18] 李洪桂, 赵中伟, 霍广生. 相似元素的深度分离[J]. 中国有色金属学报, 2003, 13(1): 234-240.
LI Hong-gui, ZHAO Zhong-wei, HUO Guang-sheng. Deep separation of resemble elements[J]. The Chinese Journal of Nonferrous Metals, 2003, 13(1): 234-240.
[19] 王淀佐, 胡岳华. 浮选剂找药分子设计理论的应用与发展[J]. 矿冶工程, 1987(2): 18-23.
WANG Dian-zuo, HU Yue-hua. Recent development and application of theory of design of molecular structure of flotation agents[J]. Mining and Metallurgical Engineering, 1987(2): 18-23.
[20] 王淀佐. 浮选理论的新进展[M]. 北京: 科学出版社, 1992.
WANG Dian-zuo. New evolve in flotation theories[M]. Beijing: Science Press, 1992.
[21] 王淀佐, 林 强, 蒋玉仁. 选矿与冶金药剂分子设计[M]. 长沙: 中南工业大学出版社, 1996: 8-11.
WANG Dian-zuo, LIN Qiang, JIANG Yu-ren. Molecular design of regents for mineral and metallurgical processing[M]. Changsha: Central South University of Technology Press, 1996: 8-11.
[22] 见百熙. 浮选药剂的分子结构及其规律性―用高等药物化学原理探讨浮选药剂分子的设计[J]. 有色金属, 1983, 35(1): 48-57.
JIAN Bai-xi. The molecular structures and their regulations of flotation reagents―Discussing the flotation reagents molecular design by using the principals of high reagent chemistry[J]. Nonferrous Metals, 1983, 35(1): 48-57.
[23] 王淀佐. 浮选剂作用原理与应用[M]. 北京: 冶金工业出版社, 1982.
WANG Dian-zuo. Flotation reagent-fundamentals and application[M]. Beijing: Metallurgical Industry Press, 1982.
[24] 陈建华, 冯其明, 卢毅屏. 浮选药剂的亲固能计算[J]. 中国有色金属学报, 1999, 9(2): 351-357.
CHEN Jian-hua, FENG Qi-ming, LU Yi-ping. Calculation for energy of interaction of flotation reagent with mineral surface[J]. The Chinese Journal of Nonferrous Metals, 1999, 9(2): 351-357.
[25] 赵中伟, 梁 勇, 刘旭恒. 反应挤出法碱分解黑钨矿[J]. 中国有色金属学报, 2011, 21(11): 2946-2951.
ZHAO Zhong-wei, LIANG Yong, LIU Xu-heng. Sodium hydroxide digestion of wolframite by reactive extrusion[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(11): 2946-2951.
[26] 曹才放, 赵中伟, 刘旭恒, 王小波. 硅酸钠分解白钨矿的热力学研究[J]. 中国有色金属学报, 2012, 22(9): 2636-2641.
CAO Cai-fang, ZHAO Zhong-wei, LIU Xu-heng, WANG Xiao-bo. Thermodynamic study of decomposition of scheelite with sodium silicate[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(9): 2636-2641.
[27] ZHAO Z, LI J, WANG S, LI H, LIU M, SUN P, LI Y. Extracting tungsten from scheelite concentrate with caustic soda by autoclaving process[J]. Hydrometallurgy, 2011, 108(1): 152-156.
[28] ZHAO Z, LI H. Thermodynamics for leaching of scheelite―Pseudo-ternary-system phase diagram and its application[J]. Metallurgical and Materials Transactions B, 2008, 39(4): 519-523.
[29] 李朝恩, 郝晓娟. 逐级均分法计算基团电负性[J]. 化学通报, 1989(7): 58-59.
LI Chao-en, HE Xiao-juan. The calculation of group electronegativity by gradual equalization method[J]. Chemistry, 1989(7): 58-59.
[30] BRATSCH S G. Electronegativity equalization with Pauling units[J]. Journal of Chemical Education, 1984, 61(7): 588.
[31] 叶向荣. 固相配位化学反应研究: LXVII.金属铜表面M-S(M=Mo,W)簇合物的组成[J]. 应用化学, 1995, 12(2): 5-8.
YE Xiang-rong. Studies on solid state reaction of coordination compounds LXVII. Constitution of M-S(M=Mo,W) cluster compound[J]. Chinese Journal of Applied Chemistry, 1995, 12(2): 5-8.
[32] 叶向荣, 忻新泉. MoS42-在铜表面的配位化学反应[J]. 化学学报, 1995(5): 462-467.
YE Xiang-rong, XIN Xin-quan. Coordination chemical reaction of MoS42- on the surface of copper[J]. Acta Chemica Sinica, 1995(5): 462-467.
(编辑 王 超)
基金项目:国家自然科学基金重点项目(51334008);湖南省研究生科研创新项目(1105-71380100001)
收稿日期:2015-01-15;修订日期:2015-04-28
通信作者:赵中伟,教授,博士;电话:0731-88830476;E-mail: zhaozw@csu.edu.cn