��������Һ�����彻����������ȱ������ӳ��
����������������������
(���ϴ�ѧ ��ѧ����ѧԺ������ ��ɳ��410083)
ժҪ���������彻���Ļ������о���������������Һ����Ϊ�������������ȱ������ӳ��ķ�����������ѧ���̣�������������Һ�����������ͭ����Ũ�ȡ�����Һ��Ũ�ȡ�pH���¶ȵ����ض����ȱ������ӳ������Ӱ�졣�о������������1-����-3-������L-������([C4mim][Pro])Ũ��Ϊ6 mmol/L��CuSO4Ũ��Ϊ8 mmol/L���״��������Ϊ15%��pHΪ 5.1�ͷ����¶�Ϊ 25 �� �����������£����ȱ������ӳ����ԽϺõػ��߷��룬������Ϊ1.69����ֹ�����һ�����ȵ��ʿع��̡�
�ؼ��ʣ���������Һ�壻���彻����֣�����ѧ�����ȱ�����
��ͼ����ţ�O65 ���ױ�־�룺A ���±�ţ�1672-7207(2013)09-3593-06
Enantioseparation of 2-chloromandelic acid enantiomers by ligand exchange based on chiral ionic liquids
LI Jing, JIAO Feipeng, JIANG Xinyu, DENG Qiaoyue
(School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China)
Abstract: Enantioseparation of 2-chloromandelic acid enantiomers by ligand exchange and its thermodynamical process were studied with chiral ionic liquids (CILs) containing imidazolium cations and L-Proline anions as chiral selector. Some influencing separation factors such as alkyl chain length of CILs, concentrations of Cu2+ and CILs, pH and temperature were investigated. The results show that the optimal conditions are as follows: The concentration of [C4mim][Pro] is 6 mmol/L, the concentration of Cu2+ is 8 mmol/L, volume fraction of methanol and water is 15%, pH is 5.1, and the temperature is 25 ��. Under the optimal conditions, 2-chloromandelic acid enantiomers can be baseline separated with a resolution of 1.69. The chiral separation of 2-chloromandelic acid enantiomers is an enthalpy-controlled process.
Key words:chiral ionic liquids; ligand exchange enantioseparation; thermodynamics; 2-chloromandelic acid
���ȱ�����(2-chloromandelic acid)��һ�־��й㷺��;��ҩ���м���;�ϸ������Ʒ����ҽҩ���������Գƺϳɺ�ѧ��ֵȶ�����õ�Ӧ�ã�����(R)-���ȱ�������Ժϳ�����Ч�Ŀ�ѪС��ۼ�ҩ����������[1]�������������ij����Լ����ȱ�������;�Ľ�һ�����������ȱ����ᵥ���������������ˣ��о���Ч�����ȱ������ӳ���ַ���������Ҫ��Ŀǰ�����ȱ������ӳ������Բ�ַ������б���������������ЧҺ��ɫ��[2]��ëϸ�ܵ�Ӿ[3]�ȡ��������彻��ɫ�������ý������Ӻ����������ڷ����Թ̶����Ͻ��ж�ӳ���ֵķ��������ڷ�������Ч��������㷺��ע[4-5]������������������Һ��(AAILs)��һ���������������ӺͰ����������ӹ��ɵ���������Һ�壬������������Һ��Ⱦ�������Һ������ʣ�������ѹ�͡�����ȼ�ԡ��絼�ʸߵȣ��ֱ����������������Ȼ����[6-7]��������Ϊ�������������������彻��ɫ���У����Ѳ��ijЩ�����������ɳ�Ƕ�ӳ��[8-10]��֤ʵ����нϺõ�����ʶ�����á�Ϊ�ˣ����������Ը���������������Һ����Ϊ���壬�����������彻��ɫ��������ȱ������ӳ�壬�о�Ӱ���ֵ����أ�����������Һ�������������������Ӻ������Ũ�ȡ��������pH�ȣ���������ѧ�Ƕȶ����ֹ��̽��з�����
1 ʵ��
1.1 �Լ�������
�Լ�Ϊ�����ȱ������������壬(R)-���ȱ������(S)-���ȱ�����(��3���Լ����ȡ�99%���Ϻ��Ѱػ�ѧƷ��������˾����)����ˮ����ͭ(������������п���ŷ��ѧ�Լ�����˾����)��1-���-3-������L-������([Cnmim][Pro])(���ȣ�97%���Ϻ��ɽݻ�ѧ����˾����)���״�(ɫ�״����Ϻ�½�ҹ�ó����˾����)�������Լ���Ϊ�������Լ���ʵ����ˮΪ��������ˮ��
����Ϊ���ձ�����LC-2010A��ЧҺ��ɫ���ǣ���SPD-10AV����������CLASS-VPɫ�ײ���ϵͳ��LichrospherC18��(���պ���Ƽ�����˾����)��PHSJ-3F����ȼ�(�Ϻ��״�����������)��BS-210S������ƽ(�ձ�����˾����)��D1810C�Զ�˫�ش�ˮ������(�Ϻ���ʤ���\������˾����)��KQ-50DE�����س�������ϴ��(��ɽ�г�����������˾����)��
1.2 ���ȱ������ӳ������彻��ɫ����
���ȱ������ӳ������彻��ɫ������Kromail C18ɫ�����Ͻ��У�������Ϊ��6 mmol/L 1-����-3-������L-�������8 mmol/L CuSO4��ˮ��Һ��״��Ļ��Һ�����м״����������Ϊ15%��pHΪ5.1����������Ϊ0.9 mL/min���¶�Ϊ25 �棬��Ⲩ��Ϊ280 nm��ͼ1��ʾΪ���ȱ������ӳ���ֵ�ɫ��ͼ��
1.3 ��������
�������ӣ� ��
��
�������ӣ�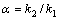 ��
��
����ȣ�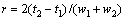 ��
��
ʽ�У�t��t0�ֱ�Ϊ��ӳ�屣��ʱ��Ͳ��������ͨ��ɫ������ʱ�䣻t1��t2�ֱ�Ϊ2����ӳ�屣��ʱ�䣻k1��k2�ֱ�Ϊ2����ӳ����������ӣ�w1��w2�ֱ�Ϊ2����ӳ��Ļ��߷����
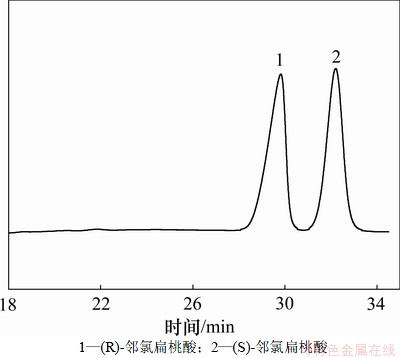
ͼ1 ���ȱ������ӳ��IJ��ɫ��ͼ
Fig.1 Chromatogram of 2-chloromandlic acid enantioseparation
2 ���������
2.1 ��������������Һ����������Բ��Ч����Ӱ��
���������彻��ɫ����,��������Ӧ���������ص㣺(1) ���������ĸ�������2����2�����ϵ���Ϲ����ţ�(2) ����1���ϴ�Ļ����Բ����ռ��ų����ã�(3) Ϊ��ѧ���������ͬ������������Բ���������ܴ��и��Խṹ���������壬�ر�����Щ������״�ṹ��������L-�ǻ��������L-������ȣ�����Щ�����������������Ⱦ��нϺõĶ�ӳ��ѡ����[11]������������������Һ��ȱ����˸�����ĸ��Խṹ���ֱ�������˫�������ʻ��Ͱ�������ˣ�������Ϊ���彻��ɫ���������塣ʵ���У����첻ͬ��������ĸ�������������Һ��([Cnmim][Pro]��n=2~8)�����ȱ�������Ч����Ӱ�죬�����ͼ2��ʾ����ͼ2�ɼ���1-����-3-������L-������([C4mim][Pro])��Ϊ����ʱ���Ի�����ķ���ȣ����������������������ѡ���������½��������Ϊ����ʱ����һ���Ŀռ�����������������Һ�壬Cu2+�����ȱ�������Ԫ�������γɣ��������������һ�����ӣ��ռ�λ������Ҳ��������Ԫ�������γɱ����Ѷ�ʹ��������½�[9]������ͬ�����£����Ը�����(Pro)Ϊ�������������ʵ�飬���������[Cnmim][Pro]������ʶ����������ǿ��û��������ĸ������ʶ�����á���ˣ�ѡ��[C4mim][Pro]Ϊ��һ���о����������塣
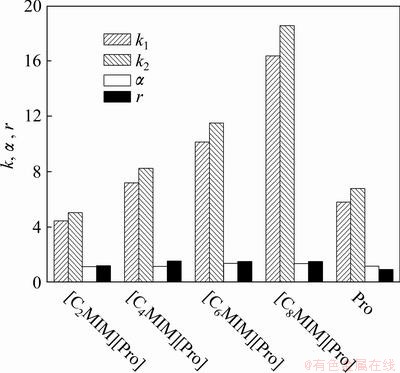
ͼ2 ����������Һ��������������ȱ������ӳ����Ч����Ӱ��
Fig.2 Effect of alkyl chain length of CILs on enantioseparation of 2-chloromandlic acid
2.2 ͭ����Ũ�ȶԲ��Ч����Ӱ��
�����彻��ɫ���У��������������塢�������ӳ���γɿ�����Ԫ�����Ľ������Ӷ�����Ϊ���彻��ɫ���������ӣ�2�ַǶ�ӳ��Ԫ�������ȶ��Բ�����ʵ�����Է�������ܶ���ɽ������Ӷ�����Ϊ�������ӣ���õ���Cu2+[12-13]����������Ũ�ȶԶ�ӳ��IJ�����Žϴ��Ӱ�죬��[C4mim][Pro]Ũ��Ϊ4 mmol/L��Cu2+Ũ��Ϊ2~12 mmol/Lʱ����������ȱ������ӳ����Ч����Ӱ�죬�����ͼ 3����ͼ3�ɼ����� Cu2+Ũ��С��8 mmol/L ʱ������Cu2+Ũ��������ϵ�п����и����[C4mim][Pro]-Cu2+����������ȱ����������λ�����γ���Ԫ�����Ӷ�������ȱ������ӳ��ķ���Ч��������Cu2+Ũ�ȼ�������ʱ�������Cu2+�ֿɾ����Եطֱ�����Ԫ������е����ȱ����ᡢ[C4mim][Pro]�γɶ�Ԫ�����ƻ���Ԫ�����Ĵ��ڣ���ʹ���ȱ������ӳ��ķ�����½�������Ч����
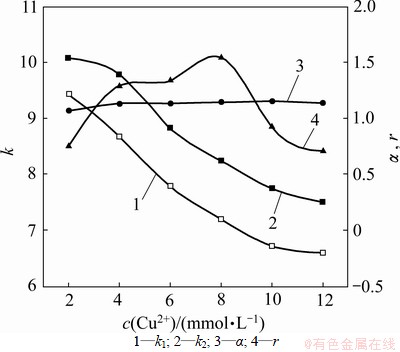
ͼ3 ͭ����Ũ�ȶ����ȱ������ӳ����Ч����Ӱ��
Fig.3 Effect of Cu2+ concentration on enantioseparation of 2-chloromandlic acid
2.3 [C4mim][Pro]Ũ�ȶԲ��Ч����Ӱ��
���ȱ������ӳ��IJ�ֹ������£�����C18�̶�������[C4mim][Pro]-Cu2+������γɶ�̬�ġ����Թ̶��ࡱ��Ȼ�������ȱ������ӳ�巢�������γɾ��в�ͬ���͵�2����Ԫ��������������ȶ��Ժ���̶����������IJ�ͬ��ʵ�ַ��룬���ԣ���������[C4mim][Pro] ��Ũ�ȶԲ�ֵ�Ӱ��Ҳ�ϴ���ͼ4��ʾ��Ũ�������ڣ����ȱ������ k������r����[C4mim][Pro]Ũ�ȵ����������������Ϊ����[C4mim][Pro]Ũ�ȵ���������Cu2+���ɵĶ�Ԫ������Ũ�����˶�Ԫ������ڹ̶����ϵ�ƽ��Ũ��Ҳ���������ȱ������ӳ����֮����������Ӧ�Ļ���ͻ�Խ�࣬���ԣ���ӳ��ı���ʱ��ͷ����Ҳ��֮�����ڻ�ýϺû��߷���Ч����ǰ���£�Ϊ�˽���[C4mim][Pro]��������ѡȡ[C4mim][Pro]��Ũ��Ϊ6 mmol/L��
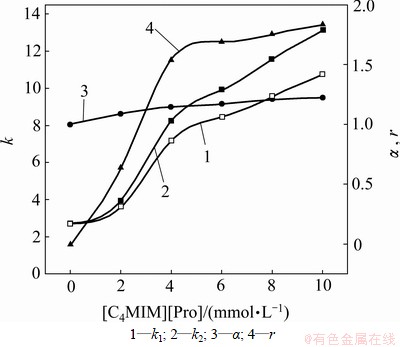
ͼ4 [C4mim][Pro]Ũ�ȶ����ȱ������ӳ����Ч����Ӱ��
Fig.4 Effect of [C4mim][Pro] concentration on enantioseparation of 2-chloromandlic acid
2.4 pH�Բ��Ч����Ӱ��
pHӰ���ӳ�������Ĵ�����ʽ���Ӷ�Ӱ��������Ԫ����ﷴӦ����ʽ��ƽ���ƶ���������pH��������Ͷ�ӳ������ӻ��̶ȼ�����������Cu2+����λ������ǿ����Ԫ�������ȶ�����ǿ����ˣ����ȱ������ӳ��ķ���Ⱥ�ѡ�����Ӿ��������ǣ���pH�����������е�Cu2+���������������������pHΪ3.5~5.1ʱ�������ȱ���������������в�֣������ͼ5��ʾ����ͼ5�ɼ�����pH=5.1ʱ�����ȱ������ӳ��ķ���ȴﵽ���ֵ��������Ϊ����pH�������ȱ������ӳ����Ҫ�Է����ӻ����ǻ����ź��Ȼ������ӵ���ʽ���ڣ����������Ե�ͭ���Ӽ�����������ϣ��Ӷ����������ȱ������ӳ��ķ��롣
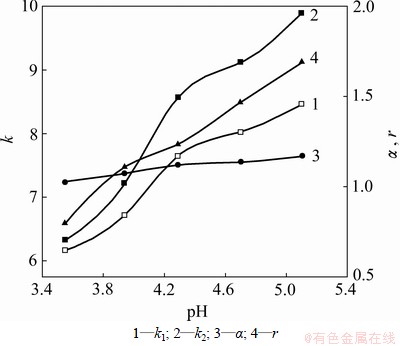
ͼ5 pH�����ȱ������ӳ����Ч����Ӱ��
Fig.5 Effect of pH on enantioseparation of 2-chloromandlic acid
2.5 �������м״���������Բ��Ч����Ӱ��
���������л����Լ������������ı�������̶���������ã��Ӷ����Ե�������ʱ��ͷ��Ρ�ʵ����ѡ��״�Ϊ�л����Լ������ż״���������������������ӡ��������Ӻͷ���Ⱦ���С��������Ϊ�����������м״������ϸ�ʱ��������ļ��Ի���Ӧ���ͣ������Ԫ������ϴ��������ǿ�������ٶȼӿ죬�����ڶ�ӳ��ķ��롣�ڱ�֤�Ϻ÷���ȵ�ͬʱ��Ϊ�˻�ý϶̵ķ���ʱ�䣬ѡ��״��������Ϊ15%��
2.6 ���¶Բ��Ч����Ӱ��
��25~45 ��ķ�Χ�ڿ������¶����ȱ������ӳ�����Ч����Ӱ�죬�����ͼ6��ʾ����ͼ6�ɼ������¶�����ʱ����ӳ��ķ���ʱ�����̣����θ�������Ȼ�������ӱ仯�����Ƿ����ȴ��1.69����1.11����������¶�����ʱ����Ԫ�������ȶ��Ա����������ٶȼӿ죬�Ӷ���ɫ�����ϵı���ʱ�����̣����ȱ������ӳ��֮��ķ���Ч���½�����ˣ�ѡ��25 ��Ϊ�ϼѷ����¶ȡ�
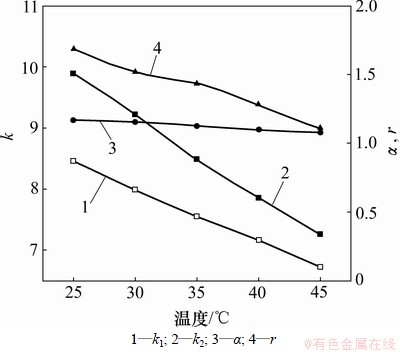
ͼ6 �¶ȶ����ȱ������ӳ����Ч����Ӱ��
Fig.6 Effect of temperature on enantioseparation of 2-chloromandlic acid
2.7 ��ֵ�����ѧ�о�
�����ȱ������ӳ��ķ�������У����������� k ���¶� T �Ĺ�ϵ����Van��t Hoff���̣�
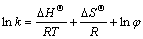
ʽ�У�kΪ�������ӣ� Ϊ��ȣ�TΪ����ѧ�¶ȣ�RΪ���峣����
Ϊ��ȣ�TΪ����ѧ�¶ȣ�RΪ���峣����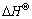 ��
�� �ֱ�Ϊ���ȱ������ڹ̶�����������������ʱ���ر䡣
�ֱ�Ϊ���ȱ������ڹ̶�����������������ʱ���ر䡣
��ln k��1/T��ͼ����һֱ�ߣ���ͼ7����ͼ7�ɼ������ϵ��R������0.999 0��˵���ڸ��¶ȷ�Χ�ڣ�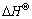 ��
�� ��
�� �����¶��صĶ�ֵ�����ȱ������ӳ��IJ�ֻ���Ҳ�����¶ȱ仯���仯[14]����ͼ8��ʾ��Van��t Hoff����б�ʺͽؾ�ɵ�25~45 ��ʱ���ȱ������ӳ���
�����¶��صĶ�ֵ�����ȱ������ӳ��IJ�ֻ���Ҳ�����¶ȱ仯���仯[14]����ͼ8��ʾ��Van��t Hoff����б�ʺͽؾ�ɵ�25~45 ��ʱ���ȱ������ӳ���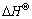 ��
��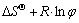 ������1������ѧ����
������1������ѧ����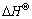 ��ʾ���ȱ������������ת�Ƶ��̶���ʱ����ЧӦ��Ϊ��ֵ����ʾ���ڹ̶����ϵ�������һ�����ȹ��̡�����ͬ��ɫ���������£����S-�������ȱ������
��ʾ���ȱ������������ת�Ƶ��̶���ʱ����ЧӦ��Ϊ��ֵ����ʾ���ڹ̶����ϵ�������һ�����ȹ��̡�����ͬ��ɫ���������£����S-�������ȱ������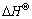 ��R-���͵�С����˵��S-���ͱ�R-������ϴ�ѣ�����ʱ�����������ͼ1��ʾ�ij���˳����һ�¡�
��R-���͵�С����˵��S-���ͱ�R-������ϴ�ѣ�����ʱ�����������ͼ1��ʾ�ij���˳����һ�¡�
�����ȱ������ӳ��ķ�������У���������� ���¶�T�Ĺ�ϵ�����Gibbs-Holmholtz���̣�
���¶�T�Ĺ�ϵ�����Gibbs-Holmholtz���̣�
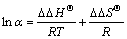
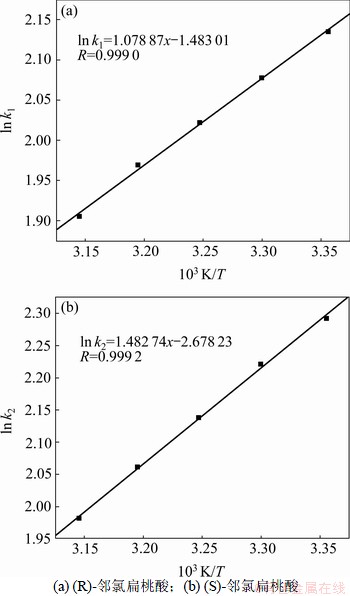
ͼ7 ���ȱ������ӳ���ln k-1/Tͼ
Fig.7 Plots of ln k-1/T for 2-chloromandlic acid enantiomers
��1 25~45 ��ʱ���ȱ������ӳ�������ѧ����ֵ
Table 1 Thermodynamic parameters of 2-chloromandlic acid enantioseparation at 25-45 ��
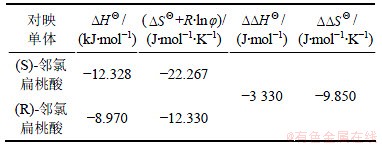
ʽ�У� Ϊ�������ӣ�����H0��
Ϊ�������ӣ�����H0��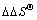 �ֱ�Ϊ���ȱ���������ӳ�������������ֹ����е��ʱ���ر�IJ�ֵ����
�ֱ�Ϊ���ȱ���������ӳ�������������ֹ����е��ʱ���ر�IJ�ֵ����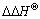 ��
��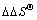 ��Ϊ��ֵʱ����ֹ������ʿع��̣���
��Ϊ��ֵʱ����ֹ������ʿع��̣���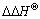 ��
��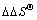 ��Ϊ��ֵʱ����ֹ������ؿع��̣���
��Ϊ��ֵʱ����ֹ������ؿع��̣���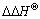 Ϊ��ֵ����
Ϊ��ֵ����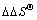 Ϊ��ֵʱ��˵���ڲ�ֹ������ʡ���2�����ضԲ�ֹ��̶�����[15-16]����
Ϊ��ֵʱ��˵���ڲ�ֹ������ʡ���2�����ضԲ�ֹ��̶�����[15-16]����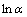 ��1/T��ͼ����һֱ�ߣ����ϵ��RΪ0.993 4��˵���ڸ��¶ȷ�Χ�ڣ�
��1/T��ͼ����һֱ�ߣ����ϵ��RΪ0.993 4��˵���ڸ��¶ȷ�Χ�ڣ�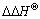 ��
��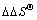 �����¶��صĶ�ֵ������Ķ�ӳѡ���Բ����¶ȵı仯���仯����ͼ8��ʾ����б�ʺͽؾ�ɵ����ȱ������ӳ���
�����¶��صĶ�ֵ������Ķ�ӳѡ���Բ����¶ȵı仯���仯����ͼ8��ʾ����б�ʺͽؾ�ɵ����ȱ������ӳ���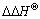 ��
��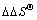 ������1���ӱ�1�ɼ����� 25~45 �淶Χ�ڣ�
������1���ӱ�1�ɼ����� 25~45 �淶Χ�ڣ�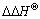 ��
��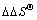 ��Ϊ��ֵ������
��Ϊ��ֵ������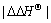 ��
�� ���������Բ�ֹ���Ϊ�ʿع��̡�����������£��������칹�������̶����и�ǿ������ã�����Ȼ������¶ȵ����߶��½�������ͼ6��ʾ���һ�¡�
���������Բ�ֹ���Ϊ�ʿع��̡�����������£��������칹�������̶����и�ǿ������ã�����Ȼ������¶ȵ����߶��½�������ͼ6��ʾ���һ�¡�
ͼ8 ���ȱ������ӳ���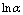 �C1/Tͼ
�C1/Tͼ
Fig.8 Plots of 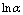 -1/T for 2-chloromandlic acid enantiomers
-1/T for 2-chloromandlic acid enantiomers
3 ����
(1) ��1-����-3-������L-������([C4mim][Pro])Ũ��Ϊ6 mmol/L��CuSO4Ũ��Ϊ8 mmol/L���״��������Ϊ15%��pHΪ5.1���¶�Ϊ25 ������Ŵ������£����ȱ������ӳ����ԽϺõ�ʵ�ֻ��߷��룬�����ȿɴ�1.69������������ЧҺ��ɫ����ëϸ�ܵ�Ӿ���������ȱ������ӳ����ȣ��������彻������������൱��������ʹ�ð���������������������������С�
(2) ��ֹ�����һ�����ȵ��ʿع��̣����ȱ������ӳ��ķ�������¶ȵ����߶��½���(S)-���ȱ���������н�С��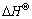 ������塣
������塣
(3) ����������������Һ��������õ�����ʶ�����ã��п����ڶ�ӳ�廯��������彻������ϵõ�Ӧ�á�
�ο����ף�
[1] ������, �ܾ�, ����ɽ, ��. �������ĺϳ�[J]. ��³ҩ��, 2012, 33(1): 3.
ZHAO Mingmei, ZHOU Ju, CAO Ruishan, et al. The synthesis of clopidogrel[J]. Qilu Pharmaceutical Affairs, 2012, 33(1): 3.
[2] ����, ����. ��ЧҺ��ɫ���������������ӷ��������������ȱ������ӳ��[J]. ������ѧ, 2005, 33(7): 1050.
WANG Jinchao, ZENG Su. The resolutionof mandelic acid and enantiomers using high performance liquid chromatography with chiral mobile phase additives[J]. Analytical Chemistry, 2005, 33(7): 1050.
[3] �⽡, ����, �����, ��. ëϸ�ܵ�Ӿ�ⶨ�������ȱ����ἰ�ڲ������ɸѡ�е�Ӧ��[J]. ��ϸ����, 2008, 25(8): 750-754.
WU Jian, LIAO Luo, DAl Guifu, et al. Enantioselective resolution of D-chloromandelic acid by capillary electrophoresis and its application in resolution strain screening[J]. Fine Chemicals, 2008, 25(8): 750-754.
[4] ����, ���, �ַ�, ��. �������彻��ɫ��������ҩ���ӳ����������Ӧ��[J]. ҩ�������־, 2010, 30(12): 2446-2451.
CHENXing,GUANJin,YANFeng, et al. Application of CLEC method in separation of chiral drug enantiomers[J]. Chinese Journal of Pharmaceutical Analysis, 2010, 30(12): 2446-2451.
[5] Ravikumar M, Varma M S, Raju T S, et al. Enantiomeric separation of moxifloxacin and its (R,R)-isomer by ligand-exchange chiral chromatography[J]. Chromatographia, 2009, 69(1): 85-89.
[6] Bica K, Gaertner P. Applications of chiral ionic liquids[J]. Eur J Org Chem, 2008, 19: 3235-3250.
[7] ��麣, ����, ������, ��. ��������Һ��ĺϳ�[J]. ��ѧ��չ, 2008, 20(5): 698-712.
SUN Honghai, GAO Yu, ZHAI Yongai, et al. Synthesis of chiral ionic liquidsprogress in chemistry[J]. Progress in Chemistry, 2008, 20(5): 698-712.
[8] LIU Qian, WU Kangkang, TANG Fei, et al. Amino acid ionic liquids as chiral ligands in ligand-exchange chiral separations[J]. Chem Eur, 2009, 15(38): 9889-9896.
[9] Bi W T, Tian M L, Row K H. Chiral separation and determination of ofloxacin enantiomers by ionic liquid-assisted ligand-exchange chromatography[J]. Analyst, 2011, 136: 379-387.
[10] TANG Fei, ZHANG Qianli, REN Dandan, et al. Functional amino acid ionic liquids as solvent and selector in chiral extraction[J]. J Chromatogr A, 2010, 1217(28): 4669-4674.
[11] ������, ����. �������彻��ëϸ�ܵ�Ӿ�о���չ[J]. ��ѧ�Լ�, 2010, 32(5): 422-426.
ZHAO Minmin, ZHAO Yanfan. Progress in study on chiral Iigand-exchange capillary electrophoresis[J]. Chemical Reagents, 2010, 32(5): 422-426.
[12] Tian M L, Row H S, Row K H. Chiral separation of ofloxacin enantiomers by ligand exchange chromatography[J]. Monatsh Chem, 2010, 141: 285-290.
[13] Nishizawa H, Tahara K, Hayashida A, et al. Continuous separation method with liquid enantioseparation of (��)-mandelic acid particle extractor[J]. Analytical Sciences, 1993, 9: 611-615.
[14] SHI Jiehhua, DING Zuojing, HU Ying. Experimental and theoretical studies on the enantioseparation and chiral recognition of mandelate and cyclohexylmandelate on permethylated ��-cyclodextrin chiral stationary phase[J]. Chromatographia, 2011, 74(3/4): 319-325.
[15] O��Brien T, Crocker L, Thompson R, et al. Mechanistic aspects of chiral discriminationon modified cellulose[J]. Anal Chem, 1997, 69(11): 1999-2007.
[16] WEN Weng, ZENG Qingle, YAO Bixia, et al. Enantioseparation of amino acid derivatives with a cellulose-based chiral stationary phase[J]. Chromatographia, 2006, 64(7/8): 463-467.
(�༭ �²ӻ�)
�ո����ڣ�2012-09-24�������ڣ�2012-11-28
������Ŀ��������Ȼ��ѧ����������Ŀ(21176262)������ʡ�Ƽ��ƻ���Ŀ(2010WK3029)����ɫ������Դ��ѧ�������ص�ʵ����(���ϴ�ѧ)������Ŀ(2012)
ͨ�����ߣ�������(1968-)���У����ϳ�ɳ�ˣ���ʿ�������ڣ��������Ի���������о����绰��0731-88830833��E-mail: jiangxinyu@csu.edu.cn