网络首发时间: 2016-05-13 08:29
稀有金属 2017,41(08),912-917 DOI:10.13373/j.cnki.cjrm.XY16011801
盐酸加盐浸出攀西钛铁矿的研究
王雷 车小奎 陈树忠 王雪飞 向俊 邓巧娟
北京有色金属研究总院稀有金属冶金材料研究所
四川省攀枝花新中钛科技有限公司
摘 要:
使用含有氯化盐的盐酸和纯盐酸浸出钛铁矿, 试验发现, 在盐酸浓度为18%、液固比4.2, 135℃的条件下, 含有氯化盐的盐酸在30 min内浸出所得人造金红石品位与盐酸直接浸出得到的人造金红石品位相近, 均在83.77%左右;且在含盐盐酸浸出1 h左右, 反应基本达到终点, 所得人造金红石品位约为93.19%以上。同时测试了盐酸中氯化盐的浓度对所得人造金红石品位和粉化率影响以及浸出前盐酸活度, 发现含盐盐酸活度与氯化盐浓度以及种类有关, 提高氯化盐阳离子价态或者氯化盐浓度对盐酸活度都有大幅度提升, 但不同种类相同价态阳离子对盐酸活度影响相同;含盐盐酸浸出所得人造金红石品位比盐酸直接浸出所得高, 但粉化率也更为严重。通过扫描电镜 (SEM) 分析可以发现, 反应过程中氯化氧钛水解生成大量针状金红石并且发生聚结, 形成球状颗粒, 即化学因素是造成金红石粉化的主要原因。
关键词:
钛铁矿;浸出;人造金红石;含盐盐酸;粉化率;活度;
中图分类号: TD95
作者简介:王雷 (1989-) , 男, 辽宁大连人, 硕士, 研究方向:盐酸法制备人造金红石;E-mail:lndlwanglei@sina.com;;车小奎, 教授;电话:010-82241301;E-mail:xkche@grinm.com;
收稿日期:2016-01-18
基金:国家科技部高技术研究发展计划项目 (2013AA065703);四川省科技支撑计划项目资助;
Leaching Ilmenite from Panxi Ilmenite by Using HCl and Chloride Slat Solutions
Wang Lei Che Xiaokui Chen Shuzhong Wang Xuefei Xiangjun Deng Qiaojuan
Division of Rare Metals Metallurgy and Materials, General Research Institute for Nonferrous Metals
Panzhihua ZTi Science & Technology Co., Ltd.
Abstract:
The experiments of leaching ilmenite were conducted by using HCl-chloride salt solution and hydrochloride acid solution respectively. The results showed that when the concentration of hydrochloride acid was 18% with a liquid-solid ratio of 4. 2 at 135 ℃, the grade of synthetic rutile achieved by leaching with HCl-chloride salt solution for 30 min was similar to those achieved by leaching with hydrochloride acid solution for 1 h. After leaching for 1 h, the reaction by using HCl-chloride salt solution was nearly reaching its endpoint, and the grade of synthetic rutile was about 89%. Experiments were performed to investigate the effects of different chloride salt concentrationson the grade of synthetic rutile and activity of hydrochloride acid solution with chloride salt. The test showed that the activity of hydrochloride acid solution increased with the rise of hydrochloride salt concentration, and the fining rate and the grade of synthetic rutile also increased dramatically. The analysis of scanning electron microscope (SEM) image showed that needle-like synthetic rutile got together, and the chemical factors caused the increase of pulverization.
Keyword:
ilmenite; leaching; synthetic rutile; HCl-chloride salt solution; pulverization rate; activity;
Received: 2016-01-18
金红石是生产海绵钛以及钛白的理想原料, 研究表明, 使用金红石为原料可以大大减少能源等的消耗, 同时具有产能高, 消耗低, 工业三废少等优点。
目前世界上制造人造金红石的方法主要有3种, 即酸浸法、还原锈蚀法, 电炉熔炼法[1,2,3,4]。这些方法的基本原理就是除去钛铁矿中的铁以及其他杂质, 从而尽量提高二氧化钛的品位, 然而电炉熔炼法和还原锈蚀法仅能除去钛铁矿中的铁, 对于我国高钙镁钛铁矿并不适用。酸浸法又分为盐酸法和硫酸法, 硫酸法由于工业三废量大, 设备繁多、副产品市场销路以及不能适应目前对环保质量的高要求等问题而逐渐被淘汰;与之相比, 盐酸法具有产品分离度较好, 工业三废少等优点, 逐渐成为新的生产人造金红石的方法[5,6,7,8,9,10,11]。
由于盐酸法浸出钛铁矿可以去除钙镁杂质, 并且具有污染小的优点, 使用金红石为原料生产钛产品将逐渐代替用钛精矿为原料的方法。盐酸法生产的人造金红石可以为氯化法生产钛产品提供合适品位的人造金红石, 但盐酸法所生产的人造金红石由于存在高粉化率的现象导致其难以达到沸腾炉标准[12,13]。因此, 研究如何增强盐酸法浸出效果并且降低产品粉化率问题对实际工业生产具有重要意义。本文在原有的盐酸法浸出工艺中引入氯化盐, 并与原工艺生产的钛渣进行比较, 从活度的角度分析氯化盐对浸出效果的影响。
1 实验
1.1 原料和设备
本实验样品采用攀枝花攀钢矿山公司密地选钛厂所生产浮选钛精矿, 经180和106μm的筛分所得-180~+106μm的部分, 其主要化学成分如表1所示, 所用设备为卧式旋转锆制加压反应釜。
1.2 试验过程
工艺流程见图1。实验的主要步骤为将盐酸和氯化盐与钛精矿同时加入高压反应釜中, 加热加压浸出, 对浸出时间和氯化盐浓度对人造金红石氧化钛品位和粉化率的影响进行研究, 试验结束后对产品的品位和粉化率进行分析。
表1 钛精矿主要化学成分Table 1 Ilmenite composition (%, mass fraction) 下载原图

表1 钛精矿主要化学成分Table 1 Ilmenite composition (%, mass fraction)

图1 试验工艺流程图Fig.1 Flow sheet of experiments
2 结果与讨论
浸出时间的长短影响着浸出的效率, 短时间内得到高品位人造金红石可以提高生产量。试验分为两组, 在盐酸浓度为18%、液固比4.2、在135℃的条件下, 分别对加入氯化盐 (浓度为1 mol・L-1) 与不加入氯化盐两组盐酸溶液进行钛铁矿浸出试验, 浸出时间分别为0.5, 1, 2, 3, 4, 5 h, 比较浸出人造金红石的品位以及粉化率情况。浸出时间对产品Ti O2品位的影响图2所示。
从图2中可以看出, 在相同时间条件下, 加入了氯化盐的盐酸具有更高的浸出效率。在浸出0.5h左右后, 所生产的人造金红石品位可达到约84%以上。与之相比, 纯盐酸浸出1 h的产品品位为82.73%, 就时间而言, 加入氯化盐的盐酸浸出效率更高。在用含盐盐酸浸出1 h后, 人造金红石品位约为93.19%左右, 随后浸出时间对人造金红石品位的影响不大。而用纯盐酸在浸出5 h后, 人造金红石品位逐渐变得与加入氯化盐所浸出的人造金红石品位相近。
试验结果表明, 使用含盐盐酸浸出的效率更高, 在短时间内就可以得到高品位的人造金红石产品。而纯盐酸浸出钛铁矿的速率随着时间的延长逐渐变慢, 并且所得到的人造金红石品位略低。
在本文中粉化率定义为浸出后人造金红石小于106μm (原料的最小粒度) 的产品占人造金红石总量的比率。将浸出的产品进行106μm筛分, 对所得的人造金红石粉化率进行分析, 筛分结果如图3所示。

图2 浸出时间对产品Ti O2品位的影响Fig.2 Effect of leaching time on Ti O2grade
从图3中可以看出, 随着浸出时间的延长, 含有氯化盐的浸出液浸出所得人造金红石粉化率呈现上升趋势, 而使用盐酸直接浸出的人造金红石粉化率在开始一段时间内呈现升高趋势, 随后开始下降, 两种不同的结果表明, 两种浸出溶液的浸出机制或者最终人造金红石相互团聚与覆盖堆积方式存在着一定的差异。
图4表示盐酸中氯化盐浓度对浸出所得人造金红石品位和粉化率的影响。如图4所示, 产品粉化率随着氯化亚铁浓度的增加而上升, 在氯化亚铁浓度达到0.5 mol・L-1之后, 粉化率增长速率开始变慢。但从产品品位来看, 氯化亚铁浓度的增高到一定程度之后, 产品品位开始下降。此时产品中因为氯化亚铁浓度已经饱和, 抽滤过程中出现大量的氯化亚铁结晶。由于氯化亚铁是盐酸浸出钛铁矿的反应产物, 溶液中过饱和的Fe Cl2阻止了反应产物Fe Cl2向溶液中扩散与反应的进行, 从而降低了产品的Ti O2品位。
3 机制分析及讨论
上述实验相比较, 两组试验的差异仅在于浸出盐酸中是否加入了氯化亚铁, 而试验结果产生了较大差异, 说明氯化亚铁的存在对溶液的性质有一定的影响。溶液浸出效率的提高说明溶液中有效成分增加, 即盐酸的活度系数提高。配制18%浓度盐酸, 并使盐酸中分别含有0.1, 0.2, 0.3, 0.5 mol・L-1氯化亚铁, 并在25℃的条件下分别测试溶液活度[14], 不同溶液活度曲线图如图5所示。

图3 浸出时间与产品粉化率的关系Fig.3 Effect of leaching time on pulverization rate

图4 氯化盐浓度对产品品位和粉化率的影响Fig.4Effect of ferrous chloride concentrations on Ti O2grade (a) and pulverization rate (b)
从图5中可以看出, 盐酸的活度随着氯化盐浓度的升高而增强, 在试验过程中, 配制的含氯化亚铁的盐酸存在大量的氯化盐, 与纯盐酸溶液相比, 这两种溶液的离子强度有了较大的提高。据资料表明, 在离子强度较高时, 普通溶液的溶液活度系数会呈现下降的趋势。但是有一些特殊溶液, 它们的活度随着离子强度的上升而上升, 盐酸就是其中的一种典型代表。盐酸浓度上升之后, 其溶液活度系数会逐渐上升, 甚至会存在大于1的情况。在加入氯化盐时, 溶液中阴阳离子浓度增加, 活度也得到了提升, 增加了盐酸中有效成分的含量, 因此加强了的浸出效率。在其他盐酸浸出湿法冶金领域, 人们对氯化盐成倍增加盐酸活度 (更正确表述为质子活度) 己非常熟悉。Demopoulos和Janssen等[15,16]的研究工作证实了在常压下含盐盐酸浸取液是一种非常高效的浸取介质。而本实验与Janssen和Demopoulos等的研究工作相符。
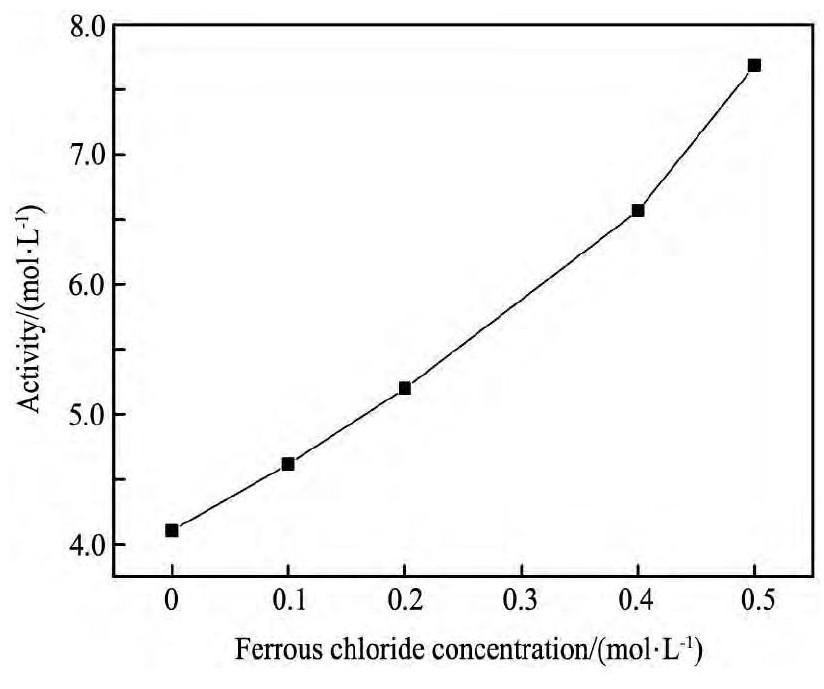
图5 氯化亚铁浓度对盐酸活度的影响Fig.5 Effect of Fe Cl2concentration on activity of HCl
图6为在HCl 18%;液固比4.2;FeCl21 mol・L-1;反应温度135℃;浸出时间4 h的条件下浸出渣的扫描电镜图片。据图6以及表2中的能谱分析可知, 在钛铁矿颗粒与盐酸浸出的过程中, 矿粒与酸之间发生接触, 而矿粒某一个表面溶解速度会大于其他表面, 导致图6 (a) 所示情况。随后, 酸与矿物颗粒之间的反应在矿物颗粒内部进行, 如图6 (b) 所示, 矿物颗粒内部为生成的二氧化钛, 而这点与文献正好相符。
钛精矿盐酸加压浸出制取人造金红石分为浓盐酸法 (华昌法) 和稀盐酸法 (贝利法等) 两种方法[17]。这两种方法都是在一定温度和压力下使钛铁矿和盐酸行化学反应, 钛精矿中的铁、钙、镁等氧化物转化成相应的可溶性氯化盐进入溶液, 并且同时存在少量的二氧化钛被盐酸溶解生成TiOCl2, Ti OCl2发生水解, 又生成带有结晶水的二氧化钛和盐酸。试验最终所生成的细化颗粒主要是Ti OCl2水解所生成的二氧化钛。水解生成的Ti O2和大部分未被溶解的Ti O2存留在固相中富集, 形成所需要的人造金红石。浸出过程的主要反应为:

图6 被腐蚀颗粒内部扫描电镜图片Fig.6 SEM images of internal partial ilmenite
表2 图6扫描区域 (点) 化学成分分析Table 2 Chemical analysis of areas (point) in Fig.6 (%, mass fraction) 下载原图

表2 图6扫描区域 (点) 化学成分分析Table 2 Chemical analysis of areas (point) in Fig.6 (%, mass fraction)

在稀盐酸浸出过程中有部分钛溶解而后又水解, 水解反应为:

导致人造金红石出现较为严重的粉化现象的主要原因是水解反应的存在, 水解所生成的的二氧化钛粒度较细, 细粒级的人造金红石由于比表面积大, 表面能比较高, 因此颗粒之间相互吸附堆积, 形成球状颗粒 (图7) 。
稀盐酸浸出钛精矿的过程系液―固相非均相反应, 这个多相反应过程至少同时进行着下面5个过程: (1) 盐酸分子扩散到钛精矿颗粒表面的界面层; (2) 盐酸分子进一步扩散通过固体膜; (3) 盐酸分子与钛精矿颗粒发生化学反应; (4) 反应产生的可溶性化合物 (如Fe Cl2等) 扩散通过固体膜; (5) 反应所产生的可溶性化合物 (如Fe Cl2等) 从颗粒表面的界面层向溶液扩散。

图7 粉化颗粒扫描电镜图Fig.7 SEM image of fine particle
表3 图7扫面点化学成分分析Table 3Chemical analysis of point in Fig.7 (%, mass fraction) 下载原图

表3 图7扫面点化学成分分析Table 3Chemical analysis of point in Fig.7 (%, mass fraction)
而整个浸出过程的反应速度却是由上述5个步骤中最慢的一个控制[17]。由反应式可以看出:在反应开始时虽然有化学反应要耗去部分盐酸, 但由于体系中酸矿比较大, 因而溶液本体中盐酸浓度变化不大。由于参与化学反应, 存在于钛精矿颗粒表面液膜中的盐酸不断消耗, 因此使溶液内盐酸和截面膜中盐酸的浓度产生比较大的浓度梯度, 所以盐酸分子以比较快的速度扩散到钛精矿颗粒表面[18]。又因反应生成的可溶性化合物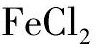 在盐酸溶液中具有较大的溶解度, 反应产物
在盐酸溶液中具有较大的溶解度, 反应产物 向溶液中扩散的速度也相当快, 反应中形成的固体Ti O2残留在钛铁矿骨架中, 因此在反应开始后的相当长的一段时间内, 化学反应属于控制反应过程, 盐酸活度主导了钛铁矿浸出效果, 并且盐酸溶液活度越高, 浸出所得人造金红石品位越高, 浸出时间也会相应的缩短。
向溶液中扩散的速度也相当快, 反应中形成的固体Ti O2残留在钛铁矿骨架中, 因此在反应开始后的相当长的一段时间内, 化学反应属于控制反应过程, 盐酸活度主导了钛铁矿浸出效果, 并且盐酸溶液活度越高, 浸出所得人造金红石品位越高, 浸出时间也会相应的缩短。
4 结论
1.由于少量氯化盐可以成倍的增加盐酸活度, 因此在用18%盐酸浓度浸出钛铁矿时, 向盐酸中加入一定量氯化盐不仅可以把人造金红石的Ti O2品位提高到93%以上, 而且可增加反应动力学和缩短浸出时间。
2.含有氯化盐盐酸浸出钛铁矿所得产品粉化率一般比较高, 且随着浸出时间的增加, 产品粉化率上升。含有氯化盐盐酸与钛铁矿反应是从局部表面开始进行, 并且生成的针状纳米氯化氧钛水解物颗粒。水解物由于比表面很大, 产生团聚物, 团聚物可在被浸出的钛铁矿骨架内部相互覆盖堆积或充填于被浸出的钛铁矿骨架之中。同时, 团聚物之间进一步团聚形成更大的团聚的聚合物。钛铁矿盐酸溶解、氯化氧钛水解与水解物团聚是化学因素方面造成产品粉化的主要原因。
参考文献
[1] Yang J, Li K, Tang A T, Pan F S.Present utilization of ilmenite[J].Materials Review, 2003, 17 (8) :44. (杨佳, 李奎, 汤爱涛, 潘复生.钛铁矿资源综合利用现状与发展[J].材料导报, 2003, 17 (8) :44.)
[2] Guo Y F, Liu X, Qiu G Z, Jiang T.Strengthening of metallic iron rust in reduced ilmenite[J].Journal of Central South University:Science and Technology, 2012, 43 (3) :797. (郭宇峰, 刘霞, 邱冠周, 姜涛.还原钛铁矿中金属铁锈蚀反应速率过程的强化[J].中南大学学报:自然科学版, 2012, 43 (3) :797.)
[3] Fan Y Q, Jiang X X, Wang S D, Jiang W, Feng L Y, Zhang D G, Liu W.Experimental study on preparation of synthetic rutile by titania slag[J].Mining&Metallurgy, 2012, 21 (4) :50. (范艳青, 蒋训雄, 汪胜东, 蒋伟, 冯林永, 张登高, 刘巍.钛渣制备人造金红石的试验研究[J].矿冶, 2012, 21 (4) :50.)
[4] Zhang W, Zhang L, Wang C, Feng N X.Study on modification of the slag[J].Journal of Materials and Metallurgy, 2011, 10 (3) :184. (张武, 张力, 王晨, 冯乃祥.一种改性钛渣钛组分的分离方法[J].材料与冶金学报, 2011, 10 (3) :184.)
[5] Cheng H B.Technology on Preparation of Synthetic Rutile by Using Hydrochloride Acid[D].Kunming:Kunming University of Science and Technology, 2004.42. (程洪斌.人造金红石盐酸加压浸出技术研究[D].昆明:昆明理工大学, 2004.42)
[6] Tang W Q, Lu L M.Present situation of titanium dioxide industry in China[J].Inorganic Chemicals Industry, 2009, 41 (10) :4. (唐文骞, 路利民.中国钛白粉工业生产现状及发展思路[J].无机盐工业, 2009, 41 (10) :4.)
[7] Chen K D.Integration of Port Resource on Low-Grade Ilmenite[D].Changsha:Central South University, 2013.57. (陈凯达.低品位钛铁矿综合利用研究[D].长沙:中南大学, 2013.57.)
[8] Fu Z B, Huang B W, Wang X F.Study on hydrochloric acid leaching for synthetic rutile preparation[J].Iron Steel Vanadium Titanium, 2006, 27 (2) :1. (付自碧, 黄北卫, 王雪飞.盐酸法制取人造金红石工艺研究[J].钢铁钒钛, 2006, 27 (2) :1.)
[9] Wang Z J, Zhang L H, Wang H B, Jiang X X, Xue JL, Hu W M, Wang J.Ilmenite hydrochloric acid leaching for synthetic rutile preparation in Panxi[J].Nonferrous Metals, 2007, 59 (4) :108. (王曾洁, 张利华, 王海北, 蒋训雄, 薛济来, 扈维明, 王舰.盐酸常压直接浸出攀西地区钛铁矿制备人造金红石[J].有色金属, 2007, 59 (4) :108.)
[10] Cui T, Peng J R, Yuan Y, Lai J, He X C, Tian L.Synthesis of rutile by pressure leaching ilmenite with hydrochloric acid[J].Chinese Journal of Rare Metals, 2016, 40 (12) :1260. (崔涛, 彭建蓉, 袁野, 赖浚, 和晓才, 田林.钛铁矿盐酸加压浸出制备人造金红石试验研究[J].稀有金属, 2016, 40 (12) :1260.)
[11] Tang Y, Deng K, Zhang D M.Hydrochloric acid leaching for synthetic rutile preparation[J].Chlor-alkli Industry, 2014, 50 (6) :22. (唐勇, 邓科, 张定明.盐酸法人造金红石生产技术[J].氯碱工业, 2014, 50 (6) :22.)
[12] Ma G Q, Zhou M.Enrichment of titanium slag by using hydrochloric acid[J].Hydrometallurgy of China, 2015, 34 (1) :46. (马光强, 邹敏.用盐酸浸出含钛高炉渣富集钛的试验研究[J].湿法冶金, 2015, 34 (1) :46.)
[13] Cheng H B, Wang D J, Huang B W, Sun G.Pulverization of synthestic rutile in ilmenite pressure-leaching process with hydrochloric acid[J].Nonferrous Metals, 2004, 56 (4) :82. (程洪斌, 王达健, 黄北卫, 孙刚.钛铁矿盐酸法加压浸出中人造金红石粉化率的研究[J].有色金属, 2004, 56 (4) :82.)
[14] Liu X M, Hou J, Li R, Li H.Application of ion selective electrode direct determination of ion concentration of iterative computation method[J].Journal Press of Southeast University, 2010, 32 (11) :124. (刘新敏, 侯捷, 李睿, 李航.应用离子选择电极直接测定离子浓度的迭代运算法[J].西南大学学报:自然科学版, 2010, 32 (11) :124.)
[15] Demopoulos G P, Li Z, Becze L, Leventen Becze, Geriana Moldoveanu, Terry C Cheng, Bryn Harris.New technologies for HCl regeneration in chloride hydrometallurgy[J].World of Metallurgy-ERZMETALL, 2008, 61 (2) :89.
[16] Janssen A, Putnis A, Geisler T, Putnis C V.The experimental replacement of ilmenite by rutile in HCl solutions[J].Mineralogical Magazine, 2010, 74 (4) :633.
[17] Deng K.Preparation of synthetic rutile[J].Chlorlakali Industry, 2013, 49 (7) :23. (邓科.盐酸法钛白粉工艺的研究[J].氯碱工业, 2013, 49 (7) :23.)
[18] Ye E D, Cheng X Z, Liao H J, Zhang J B, Wu X.Preparation of synthetic rutile by using ilmenite in Panxi[J].Iron Steel Vanadium Titanium, 2015, 36 (1) :7. (叶恩东, 程晓哲, 缪辉俊, 张溅波, 吴轩.攀西钛精矿制备人造金红石研究[J].钢铁钒钛, 2015, 36 (1) :7.)