��������ﴢ�������о���չ
��Դ�ڿ����й���ɫ����ѧ��2013���6��
�������ߣ�֣���� ¬ �� ������
����ҳ�룺1575 - 1585
�ؼ��ʣ�CeO2-ZrO2���ǹ���������������������
Key words��CeO2-ZrO2; non-noble metals; precious metals; oxygen storage capacity
ժ Ҫ����������������β��������Ч�����Ĺؼ�����֮һ�������˴��������ܼ�ʹ������������ŷV�ŷŷ����ʵʩ��������������ϵ���������˸��ϸ��Ҫ��CeO2������β������������һ����Ҫ��֣�ϡ�������ɽ�����������IJ��Ӷ�����һ���̶������CeO2�����ȶ��ԡ����������ʹ����ԡ�������������Ч�����еĴ������������������������о�״����������Zr��La��Pr��Sn��Ti�ȷǹ�����IJ��ӡ�Pd��Ru��Pt�ȹ�����IJ��Ӷ�CeO2�������ܵ�Ӱ�죬�ܽ��˽������ӵ�CeZr����Ԫ�������CeZrAl���о���״��
Abstract: Oxygen storage material is one of the key materials in automobile exhaust catalyst which determines the catalytic performance and life of three-way catalyst. With the implementation of Euro V emission regulations, more strict requirements are presented for the performance of ceria-based material. As an important component in the catalyst, its thermal stability, oxygen storage capacity and catalytic activity can be improved by doping of rare earth, transition metals and precious metals to some extent. The recent research status about ceria-based oxygen storage materials which used in three-way catalyst were reviewed, the effects of non-noble metal doping such as Zr, La, Pr, Sn, Ti, precious metals doping such as Pt, Pd, Ru on the properties of CeO2 oxygen storage capacity were expounded, and the current research situation about metal modification ternary CeZr-based composite oxides and CeZrAl were also introduced.
���±�ţ�1004-0609(2013)06-1575-11
֣����1, 2��¬ ��2��������1, 2
(1. ����������о��� ϡ������ۺ������¼��������ص�ʵ���ң����� 650106��
2. �������д����������ι�˾ ����ʡ����������Ϲ��̼����о����ģ����� 650106)
ժ Ҫ����������������β��������Ч�����Ĺؼ�����֮һ�������˴��������ܼ�ʹ������������ŷV�ŷŷ����ʵʩ��������������ϵ���������˸��ϸ��Ҫ��CeO2������β������������һ����Ҫ��֣�ϡ�������ɽ�����������IJ��Ӷ�����һ���̶������CeO2�����ȶ��ԡ����������ʹ����ԡ�������������Ч�����еĴ������������������������о�״����������Zr��La��Pr��Sn��Ti�ȷǹ�����IJ��ӡ�Pd��Ru��Pt�ȹ�����IJ��Ӷ�CeO2�������ܵ�Ӱ�죬�ܽ��˽������ӵ�CeZr����Ԫ�������CeZrAl���о���״��
�ؼ��ʣ�CeO2-ZrO2���ǹ���������������������
��ͼ����ţ�O643.36 �� �� ���ױ�־�룺A
ZHENG Ting-ting1, 2, LU Jun2, ZHAO Yun-kun1, 2
(1. State Key Laboratory of Advanced Technologies for Comprehensive Utilization of Platinum Metals, Kunming Institute of Precious Metals, Kunming 650106, China;
2. Precious Metal Catalytic Materials Engineering Technology Research Center in Yunnan Province, Kunming Sino-platinum Metals Catalysts Co., Ltd., Kunming 650106, China)
Abstract: Oxygen storage material is one of the key materials in automobile exhaust catalyst which determines the catalytic performance and life of three-way catalyst. With the implementation of Euro V emission regulations, more strict requirements are presented for the performance of ceria-based material. As an important component in the catalyst, its thermal stability, oxygen storage capacity and catalytic activity can be improved by doping of rare earth, transition metals and precious metals to some extent. The recent research status about ceria-based oxygen storage materials which used in three-way catalyst were reviewed, the effects of non-noble metal doping such as Zr, La, Pr, Sn, Ti, precious metals doping such as Pt, Pd, Ru on the properties of CeO2 oxygen storage capacity were expounded, and the current research situation about metal modification ternary CeZr-based composite oxides and CeZrAl were also introduced.
Key words: CeO2-ZrO2; non-noble metals; precious metals; oxygen storage capacity
����β����������Ⱦ�����ڵ��������������Խ��Խ������ӣ���ת��������Ӧ����ʵ�����������ŷŵ�����Ч�ֶΡ���Ч����[1](TWC)��20����70�����ʼ�����ھ���������β����������Ч�ؽ�β���е�CO��HC��NOxת��Ϊ����CO2��H2O��N2��������β����Ч����(TWC)�У���������������β�����������Ĺؼ����ϣ������˴��������ܺ�������CeO2��һ����Ҫ����֣�������Ҫ��������ͨ��2CeO2��Ce2O3+1/2O2��Ӧʵ�ִ����ͷ������ؿ���������Ч���ڡ����⣬�����ܹ��ٽ�������ķ�ɢ������Al2O3��������ȶ��ԣ���ǿˮ��ת����ˮ����������Ӧ����߽���-�������λ�Ĵ�����[2]������1 123 K���ϣ�CeO2�������սᣬʧȥ��ṹ���Ӷ�ʹ���������ͱȱ�������ͣ��������´����Ե��½�����Ч�����ڸ��¸߿����±�����нϺõ����ȶ��ԣ���ˣ���߲��ϵ����ȶ��Լ����Էdz���Ҫ�������о�������ϡ�����������ɽ������������ӵ����ӿ������CeO2�����ȶ��Ժ�������ԭ��������Zr4+[3-4]��Pr4+[5]��La3+[6]��Fe2+[5]��Y3+[5]�ȵļ�������ǿCeO2�Ŀ��ϻ����ܼ���������(OSC)��
1 �������Ե�Ce������������
��CeO2�IJ��Ӹ�����Ҫ�ǻ��������������Ӵ����ijߴ�ЧӦ�����ƽ��ЧӦ��Ԫ���������е�������ԭ�ԡ���CeO2���Ե�Ч�������ӵ�Ԫ�ء����������Ʊ��������йء�
1.1 Zr4+���Ӳ���
���ڣ���������������о��϶����CeO2-ZrO2�����壬���������CeO2-ZrO2�������ר��Ҳ�ܶࡣ����ר��U.S 7612011[7]��U.S 7314846[8]�ȹ�����CeO2-ZrO2���Ʊ��������ڴ����е�Ӧ�ã���ʾ�����������ȶ��Ժʹ����ܡ��й�ר��CN 1935359 A[9]��CN 101269963 A[10]��Ҳ������CeO2-ZrO2���Ʊ��������������о���ΪZr4+��CeO2�ĸ���Ч���ȼѣ����Ӱ뾶��С��Zr4+(0.084 nm) ȡ�������Ӱ뾶�ϴ��Ce4+(0.097 nm)������CeO2������䣬һ������γɸ���ȱ�ݺ;���Ӧ������һ������Բ�����Ce4+��Ce3+�仯�����������ͣ��Ӷ�������������ɢ�Ļ�ܣ���������������Ǩ�ƺ���ɢ�������������ԭ���ܡ�����ڴ�CeO2�������ȶ��Խϸߣ���һ���棬 CeO2-ZrO2������ĸߴ����������Լ���TWC�й�������������Ӷ����� TWC �ijɱ���KASPAR��[1, 6]��ȫ���ܽ���CeO2-ZrO2��ϵ�Ľṹ�ص㼰�Ʊ������������ܵ�Ӱ�죬��Ҫ������CeO2-ZrO2��ϵ�Ĵ���������
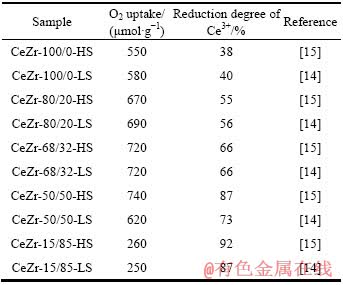
CeO2-ZrO2����������������ԭ��Ϊ�ʹ�������ȡ���ڶ������أ��������������ɡ��ṹ��֯�������һ�Ժ�Ԥ�����ȣ��������һ��������Ҫ���á��봿CeO2��ȣ�CeO2-ZrO2�ȱ�������仹ԭ����ֱ�ӵĹ�ϵ[11](����1)����˵����������������ṹ���ʱȱȱ������Ҫ��ZHAO��[12]�о��˱ȱ����������ṹ��Ce0.67Zr0.33O2������Ӱ�죬����������ȱ�����Զ�̬������Ӱ�����¶��йأ����¶����߱ȱ�����Զ�̬������Ӱ���С�����ܴ�������ȱ�����أ�����Ǩ�ƶ����������Ѩ��ɢ�Դ�����������Ҫ����������Ǩ����Ҫ�����ϵ�����ṹ�йأ�����������Ѩ��������CeO2-ZrO2�Ĵ�������������ȡ������ṹ��������ԭ�������γɸ����ȵĽṹ��Zr4+��������ǿ���γɽṹȱ�ݵ���������Щȱ�������ڻ�ԭ���ʵ���ߡ�DATURI��[13]��Ϊ��Ce����(Ħ������)��15%������80%����ԭ������·����ƶ���˵��������Ce4+Ũ����������������ƶ�������������Zr�Դ��������дٽ����ã��봿CeO2��ȣ�CeO2-ZrO2�����������и��õ�������ԭ���ʡ��͵���ʼ��ԭ�¶Ⱥ��ߵĻ�ԭ�ȡ���VIDAL��[14-15]���о������������CeO2-ZrO2��Zr���������ӣ���ԭ������(��1)������Zr�����ø������¶��壬���Ǽ��е�Zr��Ϊ�������ߵĽ�ɫ������������ԭ�Ӳ�ת�Ƹ�Ceԭ�ӣ���������䴢������[16]���ܵ���˵�����º������¸�Ce��ɵ�CeO2-ZrO2��ϵ���ܽϺã��������£���Zr��������Ʒ��������е����ȶ��Ժ���Ե͵��ս�������ά�ֲ��ϵ����ܣ�����Ce�����ϵͶ�������Ce4+�ܱ���ԭ��������Ϊƽ��Ce��Zr�����ã��д���Ѱ��Ce��Zr�����Ħ���ȡ�VIDAL[15]����ΪCeO2�м���20%~50%(Ħ������)��Zr�ɵõ�����ֵ�ߵIJ��ϡ���1�г���ͬCe��Zr�ȺͲ�ͬ�ȱ������CeO2-ZrO2��O2��������Ce4+�Ļ�ԭ�ȣ�����HS�����߱ȱ������LS��ʾ�ͱȱ������
��1 ��ͬCe��Zr�ȺͲ�ͬ�ȱ������CeO2-ZrO2��O2������(700 �����ֵ)��Ce4+�Ļ�ԭ��
Table 1 O2 uptakes measured at 700 �� over HS/LS CeO2-ZrO2 oxides and reduction degree of Ce4+
Ϊ����CeO2-ZrO2��ԭ�Ե���ǿ������������߶�CeO2-ZrO2����������������ṹ�������˴������о������ó��˲�ͬ�Ľ��ۣ�һ����Ϊ�����е�ȱ�ݡ�����Ѩ�IJ���������Ѩ��������Ce�����ϵĴ�������������Ҫ���á����������өʯ��������ܶѻ��ṹ�����������������������Ӱ뾶��r+/r-Ӧ�õ���0.723�����Ǵ�CeO2���������������Ӱ뾶��Ϊ0.693����������ֵ�����Ϊά�ֽṹ���ȶ����������ڸ����ܵ����У����Ӱ뾶С��Ԫ�صļ�������˾����������̡���Ce4+��ԭΪCe3+���뾶����r+/r-���ӽ�0.732�����Zr����������ľ��������õ��˲�����ʹ����ṹ�����ȣ�������ǿ������Ce4+�Ļ�ԭ[17]��MAMONTOV��[18]�����������������о���CeO2��CeO2-ZrO2������ԭ��ˮƽ�Ľṹ��������Ʒ���������Ǿ����д����İ���������϶���Ӻ�����������Ѩ��CeO2������Ѩ��Ũ�����϶���ӵ�Ũ����ȣ������ܻ�ѧ�������õ���ά�֡�CeO2-ZrO2�п�Ѩ�����ڼ�϶���ӣ�����ȱ���ܼ�Ϊ8%�����Ǹ��������ڼ�϶�������Ѩ������CeO2��Frenkel��ȱ����ʧ��ֻ������С����ȱ�ݣ���CeO2-ZrO2������Zr4+������ֲ�ԭ�ӱ������ڽ��ܵ�������λ�����¼�϶�����Ӻ��ѵ���������λ���Ѩ��ϣ����Լ�϶���ӺͿ�Ѩû�б仯����ˣ���CeO2���CeO2-ZrO2����ȱ���ڸ����µõ���ά�֣��䴢�������õ�����ǿ��NAGAI��[19]�о��˾��в�ͬ�����Ե�CeO2-ZrO2��ƷZr��Ce�ľֲ��ṹ�����������Ʒ�IJ�ͬ�����Ե���Zr������Χ�в�ͬ����λ������Ce���ӵ���λ����������Ʒ�ж�Ϊ8������VLAIC��[20]���о���Zr����̫С�������ڵ�һ����λ��Χ�ڲ�������8����ԭ�ӣ���������������Zr���ӷǼ�λ��һ����ԭ�ӵ�ȡ����CeO2��Zr�����뵼�µ����Ǿ����������� ����ǿ�˻��������Ļ�ԭ�ԡ���HEGDEС����о�����ΪCeO2-ZrO2������ĸ�ԭ�������Ǿ���Ť���������̲�һ��Ce��O��Zr��O���Ľ����DUTTA��[21]�õ�һ��ԭ��������EXAFS�о�������Һȼ�շ��Ʊ���CeO2-ZrO2���иߴ���������ԭ����ó��ľֲ�ԭ�ӽṹ˵������M��O���Ĵ���ʹ�����ӳ�4��λ��EXAFSҲ֤ʵ����һ�㡣�ṹ��̬�����������ó���Ʒ�д��ڲ�ͬǿ�ȵ�M��O����ͼ1��ʾΪCe0.75Zr0.25O2�����Ӿֲ���λ������ṹʾ��ͼ����ͼ1��ʾ��O1��O3��O6��O8�γɶ̵�Zr��O������O2��O4��O5��O7�γɳ�Zr��O����8���������ԭ������4������Zr��ʹ����λ��Ϊ4��O3�γ�һ���̵�Zr��O����һ����Ce��O������O7���γ�һ������Zr��O����һ���̵�Ce��O�������̼��Ĵ����γ����������͵�����ǿ������������������CeO2-ZrO2������Ѩ�Ĵ��ڵ����˳�Mn+��O�����γɣ���Mn+��O��������ǿ���������������˴���������
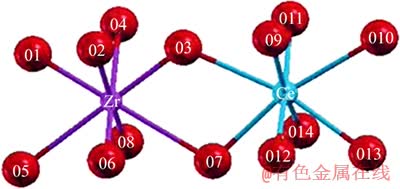
ͼ1 Ce0.75Zr0.25O2�����Ӿֲ���λ������ṹʾ��ͼ[21]
Fig. 1 Schematic diagram of local coordination of cations in optimized structure of Ce0.75Zr0.25O2[21]
�Ӹ�������˵��CeO2-ZrO2������ֻ��һ�ֺܼ��������ϣ�Ȼ����ṹ�����ʵĸ�����һֱ��Լ���Ƕ����Ľ�һ����ʶ��
1.2 �����ǹ����Ԫ�ز���
��Zr4+���⣬La3+��Pr4+��Hf4+��Tb4+��Fe3+��Ti4+��Sn4+�Ȳ��Ӹ���CeO2Ҳ�����ױ���[5, 22-27]��������Zr�������������ɽ�����ϡ���ͼ�������CeO2��ר����������١��������ȶ��Զ��ԣ������ٽ�뾶��Ԫ�ظ���Ч���Ϻá�La3+(0.116 nm) ��Ҫ������������ǿCeO2�����ȶ��ԡ���Ҳ���о�������Ce1-xLaxO2-x/2��������ÿ����La3+ȡ������Ce4+�γ�һ����״������Ѩ������ȱ������������������ʡ�DEGANELLO��[22]�������ᷨ�ϳ���Ce-La����Ч��������O2����������ȡ����Ce-La��������La�ĺ�������ȱ������CeO2�ľ�����С�أ�O2������ֵ��Ce-La��������La��CeĦ���ȵ����Ӷ����ӣ�����La��Ce��Ħ���ȴ���0.18ʱ��O2����������С��REDDY��[23]�ù��������Ʊ���Ce0.8Hf0.2O2��Ce0.5Zr0.5O2��XRD�������1 073 K���պ�Ce0.8Hf0.2O2��ֻ���ڵ�������Ce0.5Zr0.5O2�г����������(Ce0.75Zr0.25O2��Ce0.6Zr0.4O2)��Ce0.8Hf0.2O2�Ĵ��������������Ծ���Ce0.5Zr0.5O2�ĺá�
Ce1-xZrxO2��������γ���Ȼ��ǿ��CeO2�Ļ�ԭ�Ժʹ�����������ZrO2���ܱ�H2��ԭ����PrO2��TbO2��TiO2��SnO2��Fe2O3��CeO2���ƣ������ض��ı�����ԣ�����CeO2ͬʱ����ԭ������Ti4+��Sn4+�����Ӱ뾶��С������ȡ��Ce4+���������Ǿ����Ť�������˳��̲�һ��Ce��O��Ti��O��Sn��O��[27-30]�������������������ױ�CO��H2��ԭ��REDDY��[24]�ù����������ڲ�ͬ�¶��±����Ʊ���Ce-Pr�������壬����XRD��TEM-HREM��RS��XPS�ȱ��������о�����ṹ��������ԭ���ʡ�Pr����CeO2�������˱ȱ������XPS���������Ce��Pr��Ce3+��Pr4+���棬Pr�ļ�������������Ѩ��������ͨ�����ٸı�������̬������Ce4+��ԭΪCe3+��Ce-Pr�Ĵ�������ֵ�Ǵ�CeO2��5�����������ԭ�õ�����ǿ����Ce-Zr��ȣ�Ce-Pr��CO���������Ը��ߡ�SHIGAPOV��[25]���л�ģ�巨�ϳ��˸߱ȱ������Pr-Ce��������������Ϊ����β���������������塣�����������Щ�����ڵ�����(��350 ��)��Ce-Zr���ṩ����Ĵ���������Zr��Y��Ca�ļ��������˱ȱ���������ȶ��ԣ����ǵ��´��������½���SINGH��[5]���ö���ϩ����(DETA)�������谷Ϊ��ϼ�ˮ�Ⱥϳ��˾�����Ϊ5~10 nm��Ce1-xMxO2-��(M=Zr, Ti, Pr, Y �� Fe)������������������Ce1-xFexO2-���Ļ�ԭ�¶ȱ�Ce1-xMxO2-��(M=Zr, Ti)��Ҫ�ͣ�Ce0.85Fe0.15O1.85�ڵ����¶�CO���������Ա�Ce0.75Zr0.25O2�ĸߡ��绯ѧ�����Ʊ���Ce1-xTbxO2-���������CO����Ҳ�и���[26]����Ce0.8Zr0.2O2��ȣ�Sn4+ȡ��CeO2�����Ļ���������ʹ������������[27]��50%(Ħ������)��Snȡ��CeO2����ά������өʯ�ṹ��������700 �����ȶ����ڡ�������200~400 ���¶�����Ce4+/Ce3+�� Sn4+/Sn2+������ԭ��ԵĴ���ʹCe1-xSnxO2�Ĵ���������Ce1-xZrxO2��ǿ[28]����ͬ����ȡ����Ce1-xMxO2�Ĵ���ֵ����2��
1.3 ��������ӵ�Ce������������
�����������̬ȡ��CeO2��������ǿ�������������ҹ������������Ϊ��ԭ�Է��ӵ�����λ����ǿ�����¶�CO��NO��HC�Ĵ����ԡ���Pt��Pd��Rh��Ru(Ħ������������3%)����ȡ��CeO2���Լ��ٴ����й����������[33-34]���о����������������̬ȡ��CeO2�γ�Ce1-xMxO2-������������ڹ����ֱ�Ӹ�����Al2O3��CeO2�Ͼ��и��ߵĴ�����[33-35]��HEGDE��[31-36]�о��ŶӶ�Ce1-xMxO2-��(M=Pt, Pd, Rh, Ru)����������������о�����ΪPt4+/2+/0��Pd2+/0��Rh3+/0��Ru4+/3+��Ce3+/4+������ԭ���֮��ĵ����������Ce1-xMxO2-�����иߴ��������ߴ����Ե�ԭ��ͨ��������ԭ���֮���Эͬ��ԭ����ʹCe1-xMxO2-�� (M=Pt, Pd, Rh, Ru)���п���Ĵ�����������Ce1-xRuxO2-����Ʒ�оʹ�������������ԭ��Ӧ[32]��
Ce4++Ru3+��Ce3++Ru4+ (1)
3Ce4++Ru0��3Ce3++Ru3+ (2)
���Ϸ�Ӧ��Ce1-xRuxO2-���Ŀ��洢����������Ҫ���á���O2��Ce4+��O2-��Mn+��O2-(n=2, 4)[34-35]����Rh3+��O��Ce4+[33]�Ĵ�������ǿ�˹������CeO2�����á�
SINGH��[32]�������谷Ϊ��ϼ�����ˮ�ȷ��ϳ���8~10 nm��Ce1-xRuxO2-��(x=0.05, 0.10)�����塣��XRD��TEM��XPS��EDX�����˱������û����ᄃ�����өʯ�ṹ��RuΪ+4�ۣ�CeΪ(+3~+4)�Ļ�ϼۡ�����ȡ��CeO2��Ru4+���Ӽ��������Ce1-xRuxO2-x/2 ��x=0.05��0.10ʱ�ֱ�����ͷ�0.22[O]��0.42[O]�����Ce0.50Zr0.50O2���ܵ����������0.22[O]�ߡ�����Ru4+���ӣ�Ce1-xRuxO2-����ֻ��һ���ߴ������ϣ�Ҳ��ʾ����Ч������CO��HC�ĸ��������Ժ�CO���»�ԭNOΪN2�ĸ�ѡ���ԡ�ROY��[37]�Ƚ���Ce1-xMxO2-��(M=Pt, Pd, Rh)��CO+NO��Ӧ�Ĵ����ԣ�Pdȡ����Ce1-xMxO2-����NO��ȥ����Ӧ������ߣ�Ce0.98Pd0.02O2-����NO��ת�����ʼ�N2��ѡ������ã���Ruȡ������Ʒ���ܸ���[32]��
��2 ��ͬ�����Ĵ���ֵ��H2-TPR��ԭ��IJ���Ա�
Table 2 Oxygen storage capacity measured from H2/TPR experiment and composition of reduced oxides
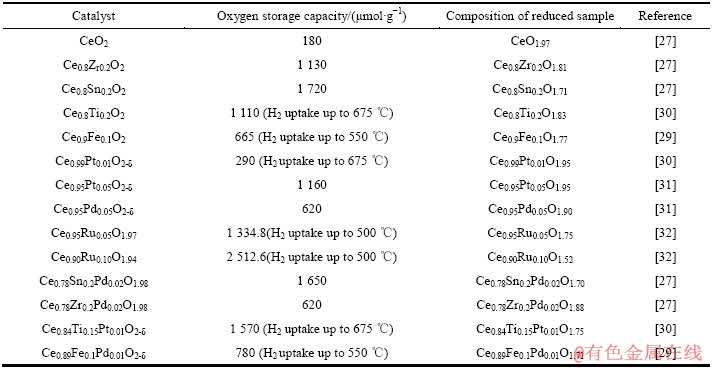
����ڵ�����ȡ����CeO2��˫������ͬȡ��CeO2�Ĵ����Ը���[27-30, 38-39]����Pd�����û�Ce0.8Sn0.2O2ʹ���Ļ��һ���õ�����ǿ�� Pd2+��ȡ�������ڵ����´�����Эͬ��ԭ��ʵ����Ҳ˵��Ce4+��Sn4+��Pd0ͬʱ��ԭ��Эͬ���õĽ������ʹ�ô����ڵ����¾��иߵĴ�������[27]��ͬ����Ce0.9Fe0.1O2-����Pd���ӵĴ���������Fe3+��ȫ��ԭΪFe2+�͵�����(105 ��)Ce4+���ֻ�ԭΪCe3+[29]��
SHARMA��[40]����-Al2O3��Ce0.98Pd0.02O2-������������������ʯ�����ϣ��ƵõĴ�����3����Ҫ��Ⱦ�����¶ȵ���220 �漴��ȫת����������������������ֱ������������������������ϵ�ճ���Ժ�ǿ������ڹ����ֱ�Ӹ�����Ce1-xZrxO2������ȫת���¶Ƚ���������[41]����Ȼ�����������̬ȡ��CeO2�γɵĹ������HC��CO�кܸߵĵ��´����ԣ������ü��Ʊ������Ʊ������������������Ч�ؽ���CeO2�����Ʊ������������乤ҵӦ�ã���������������ȶ��Բ��ã�һ����600~700 ���¶ȷ�Χ�ھ����������[31]��
2 CeZrM��Ԫ����������
��������ڴ�CeO2��CeO2-ZrO2�����������ȶ��ԡ�������ԭ���ʼ����������������˺ܴ����ߣ���CeO2-ZrO2��Ȼ���ںܶ����⣬������µ�֯�������ȶ��Խϲ�ȱ������С���ڽϸ��¶�����������룬��������������࣬ʹ��һ��������ת��ɶ���棬Zr4+��Ce4+���Ӱ뾶������������Ce��Zr��������ṹ��ͬ(ZrO2����б�࣬P21/c��CeO2������өʯ��Fm3m)����ʹ���������ɷַ�Χ�ڲ����γ�����ѧ������ѧ���ȶ��Ĺ����塣Ϊ����Խ��Խ�ϸ���ŷŷ��棬�д��ڿ���һ�ָ��õĴ������ϣ���˽�������CeZrM��Ԫ������������о���Ϊ��һ���ȵ㡣����CeZrM��Ԫ�������������һ���ķ������ǹ�˾�������˺ܶ������ﯡ�ϡ��La��Sm��Nd��Gd��Pr�Ⱥ��ɽ���Y�ȸ��Ե����ר��[42-46]���廪��ѧ��Ҳ������CeZrLa[47]��CeZrLaPr[48]����Ԫ����Ԫ����������ר����������Ͼ����ض��ıȱ�����ͻ�ԭ���ܣ��������ȶ��Ժܺá�
CeO2-ZrO2��������Ե�Ч��ȡ���ڲ������ӵ����ʺͲ��������о���������Zr��ɵ�CeO2-ZrO2����������Ӵ����Ӱ뾶��Ԫ��������Ce������������ȶ��ԣ��෴��С���Ӱ뾶Ԫ�ص�������������ս�����ʡ����磬����Y[49]��������ﯹ�����ıȱ���������ȶ��ԣ���������La[50-51]����ﯵ����ȶ�������ǿ���ã���������La��ʹ�ȱ���������������½�[41, 52]��SI��[53]�о���RE(La, Pr, Nd, Y)���Ӹ��Ե�CexZr1-xO2(x=0.4~0.6) ����������ȶ��Ժʹ�����������Ϊ����ȫ�ȶ�������Ce0.5Zr0.5-yREyO2-z�м�������t���������Ͳ�������RE3+�������Ӱ뾶�ļ�С�����ӣ����������Ӱ뾶��La��Y����С�����������ӡ�RE�IJ��������CexZr1-xO2(x=0.4~0.6) �ıȱ����������������
WANG��[41]�о���La�����Ӷ�Ce0.2Zr0.8O2�ṹ����Pd������ܵ�Ӱ�죬�������La�ļ���������CZ֯�����ܵ��ȶ��ͻ�ԭ�Ե���ǿ��La������Ϊ5%(Ħ������)ʱ��Ʒ������ߵ����ȶ��Ժ���ߵĴ���������Pd/CeZrLa(5%) �Ķ�̬����ֵ��߹�����La��������ǿ��Pd ��CeZr������á�Pr��Nd�ļ���Ҳ����ǿCeO2-ZrO2�����ȶ��Ժʹ�����������Ce��ͬ��PrҲ��ͨ�������ƶ�����Ѩ�ĵ��Ӷ��ı��̬��ά��өʯ�ṹ��Pr��������������Ѩ��Χ���ӵ�Ť��ʹ�����ƶ��Ļ����Խϵͣ��ٽ�Ce������������ (OTC) ������ɢ���� (OBC)[54]��WANG��[55]�Ʊ���Y��Ca��Ba���Ե�Pd/Ce-Zr-M/Al2O3��Y�IJ�������˴����Ա�����������ԡ�HE��[56]�Ʊ���CZ��CZY��M/CZY���������˵��CZ��Ʒ�ȱ����Ϊ52.9 m2/g������Ce��Zr��Ϊ0.34��Y3+������ʹ��CZY�ıȱ��������Ϊ69.1 m2/g������Ce��Zr��Ϊ0.78��Y�����ӽ�����TPR��ԭ����¶ȣ��ٽ���H2������Ce4+��ԭΪCe3+��O2������Ce3+����ΪCe4+������Y3+���Ӱ뾶��Ce4+���ӵĴ�������̬����Ce4+�����Y����CZ�������������Ѩ�����ٽ��˾�������������ɢ��
CeO2-ZrO2������Bi����Чά�ֵ����µĻ�ԭ����(��300 ��)��Ag������Ҳ��ά�ֹ�����ĵ��»�ԭ����[57]����CeO2-ZrO2-Y2O3��ȣ�CeO2-ZrO2-Bi2O3�ڵ���������Ч�ͷż��洢O2���һ�ԭ�¶�Զ����ǰ��[58]��Sr������������CeO2-ZrO2�����ȶ���[59]��Si�ļ��������˱ȱ�����ʹ�������[11]��WANG��[59]�Ա���Pd/CeZrSr��Pd/CeZr��CO��C3H8��NO�Ĵ����ԣ�������ƷPd/CeZrSr��Pd/CeZr��CO���������Ի�����ͬ��CO��ת�����ڿ�ȼ�Ȧˣ�1�������´ﵽ��100%�������ڦˣ�1�������ת�����½�����Sr���Ե���Ʒ�������˷�Χ�ڶ�C3H8��ת����������ߡ��ϻ����ڦˣ�1��������Pd/CeZrSr��Ʒ��CO��C3H8��NO�Ĵ����Ծ�����Pd/CeZr�ġ�
һ�����CeO2-���������ȶ��Եķ����Ǽ���Al2O3�γ�һ�����ṹ��������ַ���������1980�������ʱ������CeO2��Al2O3��������������Al2O3�����γɸ߷�ɢ�Ļ�ԭCe3+����[2]��2001��CeO2-ZrO2-Al2O3�������屻����TWC�У�CeO2-ZrO2-Al2O3���Ͻ���˴������� (OSM) ��Al2O3�Ĺ�ͬ�ŵ㣬ͬʱ���д������ϵĴ���������Al2O3������������MORIKAWA��[60]��Ϊ��Al2O3����CeO2-ZrO2���������γ���ɢ�ϰ��㣬Ԥ�Ƹ�����CeO2-ZrO2�������������Ӿۼ�����������ȶ������ӣ���ԭ��ͼ��ͼ2��ʾ��ͬʱCeO2-ZrO2Ҳ��ֹ��Al2O3(�úͦ�)������ת�䡣�ձ�ר��JP2005104799[61]��JP2005104798[62]������һ��β����������������Pt��Rh������CeO2-ZrO2-Al2O3�����������ϣ������ĵ��»��Եõ�����ǿ���Ż�Al2O3�� CeO2-ZrO2�ı�������Ч����Pt��Rh���ӵ��������������������ø��ַ����Ʊ�CeO2-ZrO2-Al2O3[63-66]��CeO2-ZrO2/Al2O3[3, 67-69]���������˴������о���
MORIKAWA��[60]�ù��������Ʊ���CeO2-ZrO2- Al2O3��CeO2-ZrO2��������ACZ��CZ��ʾ����700 �決�պ�ACZ�ıȱ������CZ��2����900 �決�պ�ȱ����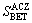 =40 m2/g��
=40 m2/g��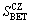 =2 m2/g������ACZ��CZ��CZ+Al2O3�����ӳߴ���6~8 nm�����������𣬵�1 000 �洦����ACZ�ľ����ߴ���CZ��CZ+Al2O3��һ�롣����ACZ��CZ����ͬ�����ͷ�������������ACZ�����ͷ�������CZ��2�����ϻ�����5����CZ+Al2O3�����ȶ��Խ���ACZ��CZ��֮�䡣
=2 m2/g������ACZ��CZ��CZ+Al2O3�����ӳߴ���6~8 nm�����������𣬵�1 000 �洦����ACZ�ľ����ߴ���CZ��CZ+Al2O3��һ�롣����ACZ��CZ����ͬ�����ͷ�������������ACZ�����ͷ�������CZ��2�����ϻ�����5����CZ+Al2O3�����ȶ��Խ���ACZ��CZ��֮�䡣
ͼ2 ACZ����ɢ��������ͼ[60]
Fig. 2 Diffusion barrier concept for ACZ compared with CZ[60]
2.1 Al2O3��CeO2-ZrO2�����庬����Ӱ��
Al2O3����Խ�ߣ���Ʒ�ıȱ����������Խ���ϻ�����Խǿ���о�������CeO2-ZrO2-Al2O3�к�10%~75%(��������)��Al2O3���ȶ���Ʒ�Ľṹ���������ȶ��ԡ����������ͻ�ԭ���ʶ��õ�����ǿ[64]��DIMONTE��[68]����������ϸ��ط��Ʊ���CeO2-ZrO2/Al2O3�����������Al2O3������Ce0.2Zr0.8O2�ĸ�����Ӱ�������֯�������ȶ���CeO2-ZrO2�ľ����ߴ磬����Ce0.2Zr0.8O2�����ӣ������ߴ������ϻ���Ce0.2Zr0.8O2������Ϊ7%(��������)����Ʒ�ž۳̶���͡����⣬��ﯺ�������Ʒ������Ceԭ�ӵ�������[63]���ȶ���-Al2O3�������溬������Ʒ�����ȶ���-Al2O3�ͦ�-Al2O3��Ce��Al2O3�����ó̶�����CeO2-ZrO2�����帺�����ļ�С������[68]��
2.2 �Ʊ�������Ӱ��
��ͬ�Ʊ������ᵼ��CeO2-ZrO2��Al2O3����õIJ�ͬ����������֯�����ṹ�ʹ����ԵIJ�ͬ[70]��DIMONTE[68]��Ϊ��Ce0.2Zr0.8O2��Al2O3���ӵĹ�����Al2O3�ȶ���ԭ�����ֹ����������������¶�����ʱCe0.2Zr0.8O2�������ȶ���ά��������������ṹ�������ڲ����и����֮�������á�CHUANG��[65]�û�ѧ���������ϳ���Ce0.5Zr0.5O2���ֱ��ù��������ͻ�е��Ϸ��ϳ���Al2O3-Ce0.5Zr0.5O2������XRD��BET��Raman�����˱�����������������¶ȵ���1 000 ��ʱ��CZ�Ե�����ڣ��¶ȸ���1 100 ��ͷ�������롣�Ի�е���Ʊ���ACZ-M��Ce0.5Zr0.5O2��1 100 �淢������룬1 200 ��ʱ�Ц�-Al2O3�γɡ���ѧ���������Ʊ���ACZ-C��500~1 200 �淶Χ��������룬���Ц�-Al2O3 �γɣ���Al2O3��1 100 ��ʱ���Ц�-Al2O3�γɡ�500~1 200 �淶Χ��CZ��ACZ-M��ACZ-C�ľ����ߴ�ֲ��ֱ�Ϊ4.8~92.3 nm��5.2~68.4 nm��2.6~23.1 nm��ACZ-M��ACZ-C�ıȱ��������CZ�ģ���ɹ�����Al2O3�����á�900 �����պ����ɴ���С��˳��ΪAl2O3��ACZ-C��ACZ-M��CZ��1 000 ���ս������ɴ���С��˳��ΪAl2O3��ACZ-C��ACZ-M��CZ����ˣ���ѧ���������Ʊ���ACZ�����ƾ����ij�������룬������ߴ���������
ZHANG��[71]�о��˲�ͬ��Ϸ�����Ce0.7Zr0.3O2- Al2O3���ܵ�Ӱ�죬�������ԭ�ӻ�ϵ���Ʒ��������ã���������ϵ���Ʒ����õ����ȶ��ԡ�ADAMOPOULOS��[72]�ù��������ֲ������Ʊ���CeO2-ZrO2-Al2O3���ֲ��������Ʊ�����Ʒ�ȹ������Ʊ��Ĵ�������С����ȼ�¶ȸߣ�����Al(OH)3�����˸���Ļ���λʹ�������½���MASUI��[73]���鷨�Ʊ���Ce0.2Zr0.8O2/Al2O3���������ӳߴ��С����CO���������Ը����ù��������Ʊ��ġ�FERNANDEZ-GACCI��[67]���鷨�Ʊ��˺�ZrCeO4 10%��33%(��������)��CeO2-ZrO2/ Al2O3��Ʒ������������鷨�ʺ��Ʊ�Ce��ZrĦ����Ϊ1.0���߶ȷ�ɢ�������������ϡ������������Ӵ�С(ƽ������Ϊ2 nm)��CeO2-ZrO2�����塣
Al2O3�ļ���������CexZr1-xO2�����ȶ��ԣ���һ���潫Ce��Zr�ع�������Al2O3�����Ʊ�����Ʒ��1 273~1 373 K����5~100 h��ȱ��������60~80 m2/g��ʹ�üĽ��շ�������������Ϊǰ���岢����һ�ֺ��ʵķ��������ڷǾ���CexZr1-xO2���γ��������м��������γ�[2]���鼰�ܽ�-��������Ϊ��һ�����γɾ�����ɵĿ��з���������Щ�������ѹ�ҵ��Ӧ�á�Ŀǰ���й�CeZrAl�Ʊ������ר�����٣�Ũ�����[74]������һ���Ʊ�CeZrAl�ķ�������Ce��Zr�Ŀ������λ����Һʹ�ü�����Һ��������Al�Ŀ�������Һʹ�ü�����Һ����������ͨ�����Ƴ»�ʱ�����Ce��Zr��Al������ó̶ȣ���þ��о�һ������ṹ��CeZrAl����������CeZrAl��Ϳ����ϵıȱ���������ȶ��Ժʹ�������������һ��CeZrAl������Ϳ����ϵġ�Ԭ���µ�[75]���üı�����Լ�(CTMACl)��һ���Ʊ����߱ȱ����(200~250 m2/g)�Ľ��Ce1-x-yZrxAlyO2(x=0.10~ 0.45��y=0.10~0.45)�����塣���۵�[76]������CeZrAl����1 000 �決��10 h�ȱ�������ٿɴ�60 m2/g����1 100 �決��5 h�ȱ�������ٿɴ�40 m2/g���������м���������������ϵĿ��ϻ����ܡ�
���ܶ�CeO2-ZrO2-Al2O3Ҳ���˴������о������д����Σ�CeO2-ZrO2-Al2O3��Ȼ���������������⣺1)���������ȶ��Բ2) �����CeO2-ZrO2- Al2O3�����ȣ����ڸ�Ce�������Zr�ķ��ࣻ3) CeO2-ZrO2������ֱ�Ӹ�����Al2O3�ϣ�������Ce��Al������Ӧ����CeAlO3���û����ﲻ�ױ���ԭ�����´�������(��������)�½���4) �Ʊ����������Zr��Al�γɹ����壬�����ȶ��Ը��5) �ɱ��ߣ��Ʊ����ո��ӵȡ���ˣ���Ȼ��Ҫ�������������о��������CeO2-ZrO2-Al2O3�����ܣ����⣬����ӹ�ҵ���Ƕ�̽��������Ʊ����ա�
3 ����
������������Ч�����е�Ϳ�����������������������10����о�״����ϡ�������ɽ�����������IJ��Ӷ�����һ���̶������CeO2�����ȶ��ԡ����������ʹ����ԡ�Zr�IJ���Ч���ȼѣ��������CeO2-ZrO2�������CeO2-ZrO2�IJ����о�Ҳ�϶࣬��CeO2-ZrO2����������Ҳ�����������⣬�д��ڽ�һ���о���Pr��Sn��Fe��������ض��ı�����ԣ������Ǹ��Ե�CeO2����Zr���Եľ��нϸߵĴ����������͵Ļ�ԭ�¶ȡ������(Pt��Pd��Ru��Rh)������̬ȡ��CeO2�γ�Ce1-xMxO2-���������CO��HC�ĵ��������кܺõĴ����ԡ�Al2O3����CeO2-ZrO2���������γ���ɢ�ϰ��㣬Ԥ�Ƹ�����CeO2-ZrO2�������������Ӿۼ������������ȶ��ԣ���ͬʱ����CeO2-ZrO2��Al2O3�Ĺ�ͬ�ŵ㡣Ŀǰ���ڹ����ϣ���CeO2-ZrO2-Al2O3�������ϵ��о��д����Σ���֯���ȶ��Ժʹ������ܻ��д������о�����������������β�����������Ĺؼ����ϣ��������������ܺ�ʹ�������������ŷŷ���������ϸ���������ȶ��Լ�������ԭ�����Ե�������Ҫ��
REFERENCES
[1] Kaspar J, Fornasiero P. Nanostructured materials for advanced automotive de-pollution catalysts[J]. Journal of Solid State Chemistry, 2003, 171: 19-29.
[2] DiMonte R, Kaspar J. Heterogeneous environmental catalysis�Ca gentle art: CeO2-ZrO2 mixed oxides as a case history[J]. Catalysis Today, 2005, 100: 27-35.
[3] Yao M H, Baird R J, Kunz F W, Hoost T E. An XRD and TEM investigation of the structure of alumina-supported ceria- zirconia[J]. Journal of Catalysis, 1997, 166: 67-74.
[4] Kaspar J, Fornasiero P, Balducci G, DiMonte R, Hickey N, Sergo V. Effect of ZrO2 content on textural and structural properties of CeO2-ZrO2 solid solutions made by citrate complexation route[J]. Inorganica Chimica Acta, 2003, 349: 217-226.
[5] Singh P, Hegde M S. Controlled synthesis of nanocrystalline CeO2 and Ce1-xMxO2-�� (M= Zr, Y, Ti, Pr and Fe) solid solutions by the hydrothermal method: Structure and oxygen storage capacity[J]. Journal of Solid State Chemistry, 2008, 181: 3248-3256.
[6] DiMonte R, Kaspar J. Nanostructured CeO2-ZrO2 mixed oxides[J]. Journal of Materials Chemistry, 2005, 15: 633-648.
[7] VANDERSPURT T H, WIJZEN F, TANG X, LEFFLER M P, WILLIGAN R R, NEWMAN C A, RADHAKRISHNAN R, FENG F, LAUBE B L, DARDAS Z, M. OPALKA S, SHE Y. Ceria-based mixed-metal oxide structure, including method of making and use: USA, US 7612011[P]. 2009-11-03.
[8] KUNO O. Method for preparing metal oxide particles and an exhaust gas purifying catalyst: USA, US 7314846[P]. 2008-01-01.
[9] ¬����, �� ��, ��־��, ������, ������, ������, ������, ������. һ��������ﯻ����������P���Ʊ�����: �й�, CN1935359 A[P]. 2007-03-28.
LU Guan-zhong, GUO Yun, ZHANG Zhi-gang, GUO Yang-long, WANG Jun-song, WANG Yan-qin, LIU Xiao-hui, WANG Xing-yi. A method of preparation spherical CeO2-ZrO2 based mixed oxides: CN1935359 A[P]. 2007-03-28.
[10] ���, ŷ����, �ư���, �Ŵ���, �ۿ���. һ�־��н�ṹ��CeO2-ZrO2��������Ʊ�����: �й�, CN 101269963 A[P]. 2008-09-24.
YANG Hua-ming, OUYANG Jing, TANG Ai-dong, DU Chun-fang, HAN Kai-jing. A method of preparation CeO2-ZrO2 solid solution with mesoporous structure: CN 101269963 A[P]. 2008-09-24.
[11] Raju V, Jaenicke S, Chuah G K. Effect of hydrothermal treatment and silica on thermal stability and oxygen storage capacity of ceria-zirconia[J]. Applied Catalysts B: Environmental, 2009, 91: 92-100.
[12] Zhao Min-wei, Shen Mei-qing, Wang Jun. Effect of surface area and bulk structure on oxygen storage capacity of Ce0.67Zr0.33O2[J]. Journal of Catalysis, 2007, 248: 258-267.
[13] Daturi M, Finocchio E, Binet C, Lavalley J C, Fally F, Perrichon V, Vidal H, Hickey N, Kaspar J. Reduction of high surface area CeO2-ZrO2 mixed oxides[J]. Journal of Physical Chemistry B, 2000, 104: 9186-9194.
[14] Vidal H, KaSpar J, Pijolat M, ColonG, Bernal S, Cord��n A, Perrichon V, Fally F. Redox behavior of CeO2-ZrO2 mixed oxides ��: Influence of redox treatments on low surface area catalysts[J]. Applied Catalysis B: Environmental, 2001, 30: 75-85.
[15] Vidal H, KaSpar J, Pijolat M, Colonb G, Bernal S, Cord��nc A, Perrichon V, Fallyd F. Redox behavior of CeO2-ZrO2 mixed oxides I: Influence of redox treatments on high surface area catalysts[J]. Applied Catalysis B: Environmental, 2000, 27: 49-63.
[16] Dong Fei, Suda A, Tanabe T, Nagai Y, Sobukawa H, Shinjoh H, Sugiura M, Descorme C, DUPREZ D. Dynamic oxygen mobility and a new insight into the role of Zr atoms in three-way catalysts of Pt/CeO2-ZrO2[J]. Catalysis Today, 2004, 93/95: 827-832.
[17] Ouyang Jing, Yang Hua-ming. Investigation of the oxygen exchange property and oxygen storage capacity of Ce1-xZrxO2nanocrystals[J]. Journal of Physical Chemistry C, 2009, 113: 6921-6928.
[18] Mamontov E, Egami T, Brezny R, Koranne M, Tyagi S. Lattice defects and oxygen storage capacity of nanocrystalline ceria and ceria-zirconia[J]. Journal of Physical Chemistry B, 2000, 104: 11110-11116.
[19] Nagai Y, Yamamoto T, Tanaka T, Yoshida S, Nonaka T, Okamoto T, Suda A, Sugiura M. X-ray absorption fine structure analysis of local structure of CeO2-ZrO2 mixed oxides with the same composition ratio (Ce/Zr=1)[J]. Catalysis Today, 2002, 74: 225-234.
[20] Vlaic G, Fornasiero P, Geremia S, KaSpar J, Granziani M. Relationship between the zirconia-promoted reduction in the Rh-loaded Ce0.5Zr0.5O2 mixed oxide and the Zr-O local structure[J]. Journal of Catalysis, 1997, 168: 386-392.
[21] Dutta G, Waghmare U V, Baidya T, Hegde M S, Priolkar K R, Sarode P R. Reducibility of Ce1-xZrxO2: origin of enhanced oxygen storage capacity[J]. Catalysis Letters, 2006, 180: 165-172.
[22] Deganello F, Martorana A. Phase analysis and oxygen storage capacity of ceria-lanthana-based TWC promoters prepared by sol-gel routes[J]. Journal of Solid State Chemistry, 2002, 163: 527-533.
[23] Benjaram M R, Bharali P, Saikia P. Structural characterization and catalytic activity of nanosized CexM1-xO2 (M=Zr and Hf) mixed oxides[J]. Journal of Physical Chemistry C, 2008, 112: 11729-11737.
[24] Benjaram M R, Thrimurthulu G, Katta L. Structural characteristics and catalytic activity of nanocrystalline ceria praseodymia solid solutions[J]. Journal of Physical Chemistry C, 2009, 113: 15882-15890.
[25] Shigapov A N, Jen H W, Graham G W, Chun W, McCabe R W. Thermally stable, high-surface-area, PrOy-CeO2-based mixed oxides for use in automotive-exhaust catalysts[J]. Studies in Surface Science and Catalysis, 2000, 130: 1373-1378.
[26] Li Gao-ren, Qu Dun-lin, Wang Zi-long, Su Cheng-yong, Tong Ye-xiang, Arurault L. Ceria-terbia solid solution nanobelts with high catalytic activities for CO oxidation[J]. Chemical Communications, 2009, 48: 7557-7559.
[27] Gupta A, Hegde M S, Priolkar K R, Waghmare U V, Sarode P R, Emura S. Structural investigation of activated lattice oxygen in Ce1-xSnxO2 and Ce1-x-ySnxPdyO2-�� by EXAFS and DFT calculation[J]. Chemistry of Materials, 2009, 21: 5836-5847.
[28] Baidya T, Gupta A,Paraag A, Deshpandey G M, Hegde M S. High oxygen storage capacity and high rates of CO oxidation and NO reduction catalytic properties of Ce1-xSnxO2 and Ce0.78Sn0.2Pd0.02O2-��[J]. Journal of Physical Chemistry C, 2009, 113: 4059-4068.
[29] Gupta A, Kumar A,Umesh V W, Hegde M S. Origin of activation of lattice oxygen and synergistic interaction in bimetal-ionic Ce0.89Fe0.1Pd0.01O2-�� catalyst[J]. Chemistry of Materials, 2009, 21: 4880-4891.
[30] Baidya T, Gayen A, Hegde M S, Ravishankar N, Dupont L. Enhanced reducibility of Ce1-xTixO2 compared to that of CeO2 and higher redox catalytic activity of Ce1-x-yTixPtyO2-�� compared to that of Ce1-xPtxO2-��[J]. Journal of Physical Chemistry B, 2006, 110: 5262-5272.
[31] Singh P, Hegde M S. Sonochemical synthesis of thermally stable hierarchical Ce1-xMxO2-��(M=Pt or Pd, 0��x��0.10) nanocrystallites: Redox properties and methanol electro- oxidation activity[J]. Crystal Growth Design, 2010, 10: 2995-3004.
[32] Singh P, Hegde M S. Ce1-xRuxO2-��(x=0.05, 0.10): A new high oxygen storage material and Pt, Pd-free three-way catalyst[J]. Chemistry of Materials, 2009, 21: 3337-3345.
[33] Gayen A, Priolkar K R, Sarode P R, Jayaram V, Hegde M S, Subbanna G N, Emura S. Ce1-xRhxO2-�� solid solution formation in combustion-synthesized Rh/CeO2 catalyst studied by XRD, TEM, XPS, and EXAFS[J]. Chemistry of Materials, 2004, 16: 2317-2328.
[34] Priolkar K R, Bera P, Sarode P R, Hegde M S, Emura S, Kumashiro R, Lalla N P. Formation of Ce1-xPdxO2-�� solid solution in combustion-synthesized Pd/CeO2 Catalyst: XRD, XPS, and EXAFS investigation[J]. Chemistry of Materials, 2002, 14: 2120-2128.
[35] Bera P, Patily K C, Jayaram V, Subbannaz G N, Hegde M S. Ionic dispersion of Pt and Pd on CeO2 by combustion method: Effect of metal-ceria interaction on catalytic activities for NO reduction and CO and hydrocarbon oxidation[J]. Journal of Catalysis, 2000, 196: 293-301.
[36] Bera P, Priolkar K R, Gayen A, Sarode P R, Hegde M S, Emura S, KumashiroV, Jayaram R, Subbanna G N. Ionic dispersion of Pt over CeO2 by the combustion method: structural investigation by XRD, TEM, XPS, and EXAFS[J]. Chemistry of Materials, 2003, 15: 2049-2060.
[37] Roy S, Hegde M S. Pd ion substituted CeO2: A superior de-NOx catalyst to Pt or Rh metal ion doped ceria[J]. Catalysis Communications, 2008, 9: 811-815.
[38] Baidya T, Marimuthu A, Hegde M S, Ravishankar N, Madras G. Higher catalytic activity of nano- Ce1-x-yTixPdyO2-�� compared to nano-Ce1-xPdxO2-�� for CO oxidation and N2O and NO reduction by CO: role of oxide ion vacancy[J]. Journal of Physical Chemistry C, 2007, 111: 830-839.
[39] Gayen A, Baidya T, Biswas K, Roy S, Hegde M S. Synthesis, structure and three way catalytic activity of Ce1-xPtx/2Rhx/2O2-�� (x=0.01 and 0.02) nano-crystallites: Synergistic effect in bimetal ionic catalysts[J]. Applied Catalysis A: General, 2006, 315: 135-146.
[40] Sharma S, Hegde M S. Single step direct coating of 3-way catalysts on cordierite monolith by solution combustion method: High catalytic activity of Ce0.98Pd0.02O2-��[J]. Catalysis Letters, 2006, 112: 69-75.
[41] Wang Qiu-yan, Li Guang-feng, Zhao Bo, Shen Mei-qing, Zhou Ren-xian. The effect of La doping on the structure of Ce0.2Zr0.8O2 and the catalytic performance of its supported Pd-only three-way catalyst[J]. Applied Catalysis B: Environmental, 2010, 101: 150-159.
[42] VERDIER S, LARCHER O, ROHART E, PACAUD B, TAKEMORI H, SUDA E. Composition based on zirconium oxide and cerium oxide, with a high reproducibility and a stable specific surface area, method of preparation and use in the treatment of exhaust gases: WIPO, WO/2007/107546[P]. 2007-09-27.
[43] LARCHER O, VERDIER S, ROHART E. Composition based on oxides of zirconium, cerium and lanthanum and of yttrium, gadolinium or samarium, with high specific surface and reducibility, preparation method and use as a catalyst: WIPO, WO/2007/131901[P]. 2007-11-22.
[44] LARCHER O, VERDIER S, ROHART E, HUANG Ai-min. Composition based on oxides of zirconium, cerium, yttrium, lanthanum and of another rare earth, method for preparing same and catalytic use: WIPO, WO/2007/093593[P]. 2007-08-23.
[45] LARCHER O, ROHART E, IFRAH S. Catalytic compositions containing zirconium, cerium and yttrium oxides and use thereof in the treatment of exhaust gases: WIPO, WO/2009/130202[P]. 2009-10-29.
[46] FAJARDIE F, VERDIER S. Composition with high reducibility made of a nanometric cerium oxide on a support, method of preparation and use as catalyst: WIPO, WO/2008/025753[P]. 2008-03-06.
[47] ������, �� ��, �γ���, ���˺�. һ������Ϊ������Ԫ����ϡ�����������P���Ʊ�����: �й�, CN 14033767 A[P]. 2003-03-19.
WEN Ming-fen, YU Bo, SONG Chong-Li, WANG Xing-hai. A method of preparation ternary nanoscale rare earth composite oxide: CN 14033767 A[P]. 2003-03-19.
[48] ������, �� ��, �γ���, ����Ƽ. һ������Ϊ������Ԫ����ϡ�����������P���Ʊ�����: �й�, CN 1403376 A[P]. 2003-03-19.
WEN Ming-fen, YU Bo, SONG Chong-Li, WANG Qiu-ping. A method of preparation quaternary nanoscale rare earth composite oxide: CN 1403376 A[P]. 2003-03-19.
[49] ëС��, ��ҫǿ, ��ï��. ������Ce0.35Zr0.55Y0.1O1.95ϡ���������ϵ��о�[J]. ����ѧѧ��, 2006, 22(8): 1521-1524.
MAO Xiao-bo, CHEN Yao-qiang, GONG Mao-chu. High performance Ce0.35Zr0.55Y0.1O1.95 rare earth oxygen storage material[J]. Chinese Journal of Inorganic Chemistry, 2006, 22(8): 1521-1524.
[50] ������, Ԭ�黪, ��ï��, �� ��, �ⶬ��, �� ��, ��ҫǿ. Ce0.35Zr0.55La0.10O1.95�Ե����Pt-Rh����Ч�������ܵ�Ӱ��[J]. ������ѧѧ��, 2007, 23(1): 73-78.
GUO Jia-xiu, YUAN Shu-hua, GONG Mao-Chu, ZHANG Lei, WU Dong-dong, ZHAO Ming, CHEN Yao-qiang. Influence of Ce0.35Zr0.55La0.10O1.95 solid solution on the performance of Pt-Rh three-way catalysts[J]. Acta Phys-Chim Sin, 2007, 23(1): 73-78.
[51] ��ƽƽ, ¬����, ������, �� ��, ������, ��˳��, ������. ��CeO2-ZrO2�м���La�Ը��Ƶ�Pd��Ч�������ܵ�����[J]. ����ѧѧ��, 2004, 20(12): 1390-1396.
JIANG Ping-ping, LU Guan-zhong, GUO Yang-long, GUO Yun, WANG Yun-song, ZHANG Shun-hai, WANG Xing-yi. Effect of La2O3 in CeO2-ZrO2 on catalytic performance of Pd-only three-way catalyst[J]. Chinese Journal of Inorganic Chemistry, 2004, 20(12): 1390-1396.
[52] LI Mei, LIU Zhao-gang, HU Yan-hong, WANG Mi-tang, LI Hang-quan. Effect of doping elements on catalytic performance of CeO2-ZrO2 solid solutions[J]. Journal of Rare Earths, 2008, 26(3): 357.
[53] SI Rui, Zhang Ya-wen, Wang Li-min, Li Shi-jie, Lin Bing-xiong, Chu Wang-sheng, Wu Zi-yu, Yan Chun-hua. Enhanced thermal stability and oxygen storage capacity for CexZr1-xO2 (x=0.4-0.6) solid solutions by hydrothermally homogenous doping of trivalent rare earths[J]. Journal of Physical Chemistry C, 2007, 111: 787-794.
[54] WU Xiao-di, WU Xiao-dong, LIANG Qing, FAN Jun, WENG Duan, XIE Zhi, WEI Shi-qiang. Structure and oxygen storage capacity of Pr/Nd doped CeO2-ZrO2 mixed oxides[J]. Solid State Sciences, 2007, 9: 636-643.
[55] WANG Gang, MENG Ming, ZHA Yu-qing, DING Tong. High-temperature close coupled catalysts Pd/Ce-Zr-M/Al2O3 (M=Y, Ca or Ba) used for the total oxidation of propane[J]. Fuel, 2010, 89: 2244-2251.
[56] He H, Dai H X, Ng L H, Wong K W. Pd-, Pt-, and Rh-loaded Ce0.6Zr0.35Y0.05O2 three-way catalysts: An investigation on performance and redox properties[J]. Journal of Catalysis, 2002, 206: 1-13.
[57] Imanaka N, Masui T, Minami K, Koyabu K. Promotion of low-temperature reduction behavior of the CeO2-ZrO2-Bi2O3 solid solution by addition of silver[J]. Chemistry of Materials, 2005, 17: 6511-6513.
[58] Minami K, Masui T, Imanaka N, Dai L, Pacaud B. Redox behavior of CeO2-ZrO2-Bi2O3 and CeO2-ZrO2-Y2O3 solid[J]. Journal of Alloys and Compounds, 2006, 408/412: 1132-1135.
[59] Wang Jian-qiang, Shen Mei-qing, An Yuan, Wang Jun. Ce-Zr-Sr mixed oxide prepared by the reversed microemulsion method for improved Pd-only three-way catalysts[J].Catalysis Communications, 2008, 10: 103-107.
[60] Morikawa A, Suzuki T, Kanazawa T, Kikuta K, Suda A, Shinjo H. A new concept in high performance ceria-zirconia oxygen storage capacity material with Al2O3 as a diffusion barrier[J]. Applied Catalysis B: Environmental, 2008, 78: 210-221.
[61] MORIKAWA A, YAMAMURA Y, SUDA A. Compound oxide and catalyst for cleaning exhaust gas: Japan, JP2005104799[P]. 2005-04-21.
[62] MORIKAWA A, YAMAMURA Y, SUDA A. Compound oxide and catalyst for cleaning exhaust gas: Japan, JP2005104798[P]. 2005-04-21.
[63] LI Hong-mei, ZHU Qing-chao, LI Yi-le, GONG Mao-chu, CHEN Yong-dong, WANG Jian-li, CHEN Yao-qiang. Effects of ceria/zirconia ratio on properties of mixed CeO2-ZrO2-Al2O3 compound[J]. Journal of Rare Earths, 2010, 28(1): 79-82.
[64] Wei Zhen-ling, Li Hong-mei, Zhang Xiao-yu, Yan Sheng-hui,  Zhen, Chen Yao-qiang, Gong Mao-chu. Preparation and property investigation of CeO2-ZrO2-Al2O3 oxygen-storage compounds[J]. Journal of Alloys and Compounds, 2008, 455: 322-326.
Zhen, Chen Yao-qiang, Gong Mao-chu. Preparation and property investigation of CeO2-ZrO2-Al2O3 oxygen-storage compounds[J]. Journal of Alloys and Compounds, 2008, 455: 322-326.
[65] Chuang Chia-che, Hsiang H I, Hwang J S, Wang Tai-shen. Synthesis and characterization of Al2O3-Ce0.5Zr0.5O2 powders prepared by chemical coprecipitation method[J]. Journal of Alloys and Compounds, 2009, 470: 387-392.
[66] �� ��, ������, ��ɽ��, Ҧ����, ��ï��, ��ҫǿ. CeO2-ZrO2-Al2O3���Ʊ����为������Ч�����Ĵ�����[J]. ��ѧ��, 2010, 31(4): 429-434.
ZHAO Ming, WANG Hai-rong, CHEN Shan-hu, YAO Yan-ling, GONG Mao-chu, CHEN Yao-qiang. Preparation of CeO2-ZrO2-Al2O3 and catalytic performance of palladium-based three-way catalyst[J]. Chinese Journal of Catalysis, 2010, 31(4): 429-434.
[67] Fernandez-Garcia M, Martinez-Arias A, Iglesias-Juez A, Belver C, Hungria A B, Conesa J C, Soria J. Structural characteristics and redox behavior of CeO2-ZrO2/Al2O3 supports[J]. Journal of Catalysis, 2000, 194: 385-394.
[68] DiMonte R, Fornasiero P, Desinan S, Kaspar J. Thermal stabilization of CexZr1-xO2 oxygen storage promoters by addition of Al2O3: Effect of thermal aging on textural, structural, and morphological properties[J]. Chemistry of Materials, 2004, 16: 4273-4285.
[69] Ozawa M, Matuda K, Suzuki S. Microstructure and oxygen release properties of catalytic alumina-supported CeO2-ZrO2 powders[J]. Journal of Alloys and Compounds, 2000, 303/304: 56-59.
[70] Wang Jun, Wen Jing, Shen Mei-qing. Effect of interaction between Ce0.7Zr0.3O2 and Al2O3 on structural characteristics: Thermal stability, and oxygen storage capacity[J]. Journal of Physical Chemistry C, 2008, 112: 5113-5122.
[71] ZHANG Qing-wei, WEN Jing, SHEN Mei-qing, WANG Jun. Effect of different mixing ways in palladium/ceria-zirconia/ alumina preparation on partial oxidation of methane[J]. Journal of Rare Earths, 2008, 26(5): 700-704.
[72] Adamopoulos O,  E, Zhang Yu, Muhamme M, Bog T, Mussmann L, Lox E. A nanophase oxygen storage material: Alumina-coated metal-based ceria[J]. Journal of the European Ceramic Society, 2009, 29: 677-689.
E, Zhang Yu, Muhamme M, Bog T, Mussmann L, Lox E. A nanophase oxygen storage material: Alumina-coated metal-based ceria[J]. Journal of the European Ceramic Society, 2009, 29: 677-689.
[73] Masui T, Fujiwara K, Peng Yu-min, Sakata T, Machida K, Mori H, Adachi G. Characterization and catalytic properties of CeO2-ZrO2 ultrafine particles prepared by the microemulsion method[J]. Journal of Alloys and Compounds, 1998, 269: 116-122.
[74] ������, �� ��, �� ��, �� ��. ���������Ʊ���һ�����������Ϳ����ϼ��乤�շ���: �й�, CN 101433831 A[P]. 2009-05-20.
SHEN Mei-qing, WENG Duan, WEN Jing, WANG Jun. Homogeneous cerium-zirconium-aluminum solid solution prepared by Co-precipitation and its technological process: CN 101433831 A[P]. 2009-05-20.
[75] Ԭ����, ������, ��Ի��. һ�ֽ�ṹ�������������������弰���Ʊ�����: �й�, CN 101112683 A[P]. 2008-01-30.
YUAN Zhong-yong, WANG Zhen-yu, MING Yue-xin. The preparation method of cerium-zirconium-aluminum solid solution with mesoporous structure: CN 101112683 A[P]. 2008-01-30.
[76] �� ��, ����ϲ. �������������������ϼ����Ʊ�����: �й�, CN 101745375 A[P]. 2010-06-23.
ZHOU Zhou, JIAN Yong-xi. The preparation method of cerium-zirconium-aluminum based mixed oxides: CN 101745375 A[P]. 2010-06-23.
(�༭ ������)
�ո����ڣ�2012-05-19�������ڣ�2012-12-20
ͨ�����ߣ������������ڣ���ʿ���绰��0871-68316562��E-mail: yunkunzhao@gmail.com

