���±�ţ�1004-0609(2016)-06-1324-08
CO��ԭ��������п��ѡ���Էֽ���Ϊ
����ΰ1���� ά1��������1���� ��2������1������ΰ1
(1. ���ϴ�ѧ ��Դ�ӹ������﹤��ѧԺ����ɳ 410083��
2. ���ϴ�ѧ ұ���뻷��ѧԺ����ɳ 410083)
ժ Ҫ��Ϊ�˽�п��ɰ������пѡ���Եطֽ�ΪZnO��Fe3O4���о���CO��ԭ���չ���������п�ķֽ���Ϊ������HSC��Factsage������������п��CO��ԭ�����·ֽ������ѧ��������ͨ����תҤ�������鿼�컹ԭ��������������п�ֽ���Ϊ��Ӱ�졣��������������˵��¶Ⱥ�������п��ɰ�е�����п��ѡ����ת��ΪZnO��Fe3O4��COŨ�ȡ�p(CO)/p(CO+CO2)ֵ�������¶Ⱥ�ʱ����Ӱ������п�ֽ����Ҫ���أ���߱����¶ȡ��ӳ�ʱ�䡢����COŨ�Ⱥͷ�ѹ����������п�ķֽ⣬Ҳ��ٽ�FeO�����ɣ�����������£�����п�ķֽ��ʽ�70%���ҹ���ԭ�����ء���XRD��SEM/EDS������������Ҫ��ZnO��Fe3O4��ZnS��Zn2SiO4Ϊ�����ҿ������Ƚ�С�����ɶ������������ء�
�ؼ��ʣ�����п��п��ɰ��п��������ԭ���գ��ֽ���Ϊ
��ͼ����ţ�TD952���� ���ױ�־�룺A
���������ҹ�п�������������������������һ��2013������ߴ�530��t������70%����ͨ������������-�������-����-���������ʪ����п���ղ���[1-3]�����������չ����У�п��������Ĵ����������ɱ���ػ�������п��Ӧ��������п(ZnFe2O4)[4-5]������п�ṹ�ȶ������������ᣬ�������º���п�����ʵͣ����Ҳ�������������пΪ���Ľ��������ݹ���ÿ����1��t���п����1~1.05��t�����������к��д������ؽ���Ԫ�أ���Zn��Fe��Pb��Ga��Ag�ȣ������˷��˱���Ľ�����Դ�����ҳ��ڶѷŻ���������Ⱦ����[6-7]����ˣ���Ч����п�����е��м۽������������ڻ�����Դ����ì�ܣ��������ڻ���������
���п�������м۽������յ����⣬������ѧ�߽����˴����о���20����60�����ǰ��п������Ҫ���û��մ���[8-9]�����תҤ�̻����͵�¯��п���ȡ���Щ�������մ����ܺĸߡ����̳�����������ʵ͵�ȱ�㡣20����60������ڣ�п�����Ĵ�����תΪ���������ʪ�����գ������Ƽ�������[10-12]��������[13-14]�ͳ�����[15]�ȡ�����������ɹ����п�����ʵͺ��м۽���Ǧ�������ѵ����⣬�������ų����������ء��������ӡ������ɱ��ߡ��м�Ԫ����������ʧ������Դ������Ч���ú������д��ڴ������ȶ��ؽ�����Ⱦ����ɶ�����Ⱦ��ȱ�㡣��������һЩѧ��������˻�ʪ�����ϴ������¹��գ���ͨ�����յķ�����п�����е�����пת��Ϊ����п���࣬��ͨ�����Ի����������ջ���п������ת�����շ�[16-17]�����ữ���շ�[18]�ͻ�ԭ���շ�[19-21]�ȡ���Ȼ��Щ�·����ڼ����ܺĺͻ��������ȷ�����ھ��DZ�������Դ�������Σ����������д������
���п������������⣬�������о���Ӧ���Ǵ������ĽǶ����֣����ٴ�Ԥ���ĽǶȿ��ǡ�������������ۺϻ��յ�˼�룬������ڳ���ʪ����п����������������������֮�����ӻ�ԭ���չ���[22]�������������յ��¶���900 �����ϣ���ԭ��������Ե����½��У������Ϳ�������������ɰ���������Ƚ��л�ԭ���գ���п��ɰ�е�����пѡ���Եķֽ�Ϊ����п�����������������ɵ�����п�ں����ĵ�������������ܽ��ڽ���Һ������������������������ڽ������У���ͨ���༶��ѡ���ջ�������ͬʱ�����Ĺ����(��Pb��Ag)�����ڴ�ѡβ���У������һ�����ա��������������ۺϻ���п��ɰ�е��м۽����ͽ��ͽ���������������ʡȥ������ʴ��ǿ����������ͷ��ӵij����������ڸù��ճɰܵĹؼ���п��ɰ�е�����п�ܷ��ڵ�����ʵ��ѡ���Էֽ⣬���Ա���������Ҫ�о�����п��CO��ԭ�����µ�ѡ���Էֽ���Ϊ��
1 ʵ��
1.1 ����ԭ��
������������ԭ��Ϊ���ɹ�ijʪ����п����п��ɰ���仯ѧ�ɷ���ɡ�п��������ɺ�XRD��������ֱ����1����2��ͼ1��ʾ���ɱ�1��֪������Ʒ��Ҫ��Zn��Fe�����м�Ԫ�أ����ΪPb��Cu��Mn��Cd�ȣ�����һ������Ag����XRD��֪��п��ɰ����Ҫ����ZnO��ZnFe2O4��Fe3O4��ZnS��Zn2SiO4�����ࡣ��������п��������������XRD�弸���ص��������������յ�Ӱ�죬п��ɰ������ľ���ṹ��������Ȼ����������IJ����ˣ�������XRD�����ֶ��ߣ���������о������Ѷȡ�ԭ���Ļ�ѧ����������(����2)������п��Ҫ��ZnO��ZnFe2O4����ʽ���ڣ�����������������96%������Ҫ��ZnFe2O4����ʽ���ڣ�ռ����������82.53%����ˣ�������Ϊ���͵ĸ���п��ɰ�����⣬�����������õĻ�ԭ����CO���壬����������N2��CO2��N2��Ҫ������������ͱ������壬CO2��Ҫ�����ǿ��Ʒ�Ӧ���յĻ�ԭǿ�ȡ�
1.2 ���鷽��
Ԥ�Ƚ�п��ɰĥϸ��0.074 mm���£�����ɹ�����ʹ�á�ÿ�������ȡ120g��Ʒ���������ܱջ�תҤ[23]���ĸ�����У��ٽ�װ����Ʒ�ĸ���ް�װ�ڻ�תҤ�н��б��ա�����N2�����¼��Ȼ�תҤ����������¶ȴﵽ�趨ֵ����ͨ�����������CO��CO2���壬���±���һ��ʱ���ֹͣͨ��CO��CO2��ͬʱֹͣ���ȣ���N2��������ȴ�����º�ȡ����Ʒ��������XRD��SEM�������ղ����������ɺ�����ò���������������ZnFe2O4��Fe2+��ȫ��(FeT)�ĺ���������������п�ķֽ��ʺ�w(Fe2+)/w(FeT)��ֵ��
�������в�������п�ķֽ��ʺͲ�����w(Fe2+)/w(FeT)�ı�ֵ����п��ɰ������пѡ���Էֽ��Ч��������ǰ��̽��ʵ�飬�ڸ�ʵ��������п��ɰ�е�����п�������ᱻ��ԭΪ�����������ɵ���������������Ϊ�������w(Fe2+)/w(FeT)ֵ��Ҫ��ӳ�˱��ղ�����������Ļ�ԭ�̶ȡ����豺�ղ�������ȫ����Fe3O4��ʽ���ڣ���w(Fe2+)/w(FeT)=1/3�����������w(Fe2+)/w(FeT)��1/3��˵������п�ֽⲻ���ף����������1/3��w(Fe2+)/w(FeT)��1�������������������ԭΪFeO��
��1 п��ɰ��ѧ�ɷ�

��2 п��ɰ��п�����������

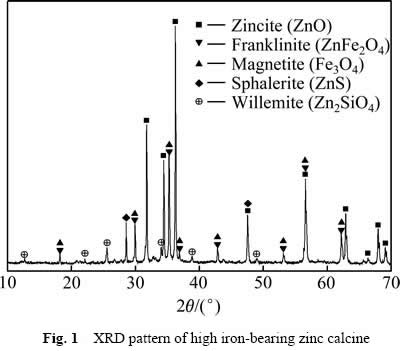
ͼ1 ����п��ɰ��XRD��
2 ���������
2.1 ����п��ԭ����ѧ����
����˹�����ܱ仯(?G)�ǻ�ѧ��Ӧ�ܷ����ĵ�һ�оݣ�ֻ�е���Ӧ��?G��0ʱ���÷�Ӧ���ܷ�������CO��ԭ����п�����п��ܷ�������Ҫ��Ӧ��ʽ(1)~(5)��ʾ������HSC Chemistry 5.0���������˸���Ӧ�ı�����˹�����ܱ仯(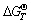 )���¶ȵı仯��ϵ�������ͼ2��ʾ��
)���¶ȵı仯��ϵ�������ͼ2��ʾ��
3ZnFe2O4+CO(g)=3ZnO+2Fe3O4+CO2(g) (1)
ZnFe2O4+CO(g)=ZnO+2FeO+CO2(g) (2)
Fe3O4+CO(g)=3FeO+CO2(g) (3)
FeO+CO(g)=Fe+CO2(g) (4)
ZnO+CO(g)=Zn+CO2(g) (5)
��ͼ2��֪����Ӧ(1)�ı�����˹�����ܱ仯��100~1000 ���¶ȷ�Χ�ں�Ϊ�����������¶ȵ����ӣ���Ӧ�ļ���˹�����ܱ仯���½����ƣ�˵��CO�ܽ�����п��ԭΪ����п��������������������¶ȿ��Դٽ���Ӧ�ķ�������Ӧ(2)�ı�����˹�����ܱ仯���¶ȵ��������ͣ����¶ȸ���250�������п�ڱ�״̬�¿��Ա���ԭΪ����п��������������Ӧ(3)�ı�����˹�����ܵı仯ֵ�����¶ȵ����������为����700 ��Ϊת��㣬��������¶���ʹ������������ԭΪ������������Ӧ(2)�ͷ�Ӧ(3)�ķ����ᵼ�����ܵķǴ��Ե����������IJ���������������пѡ���Եķֽ�Ϊ����п��������������������100~1000 ���¶ȷ�Χ�ڣ���Ӧ(1)���ܷ������������Դ��ڷ�Ӧ(2)�ͷ�Ӧ(3)�ģ���ˣ�����ͨ�����ڱ����¶�ʹ����пѡ���Եķֽ�Ϊ����п����������������������п�������������Ĺ���ԭ�����⣬�ڱ�״̬�£�����������600 �����ϲ��ܱ���ԭΪ������������п��1000 �����²��������ԭΪ����п��
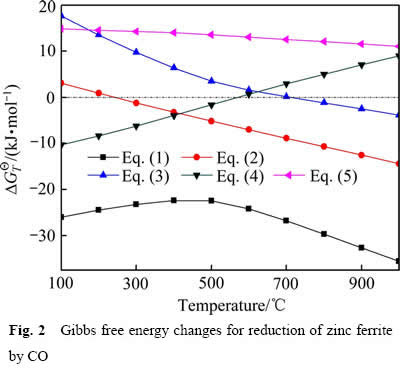
ͼ2 CO��ԭ����п�ı�����˹�����ܱ仯
Ϊ�˽�һ��������ѧ���о���ԭ���պ��¶ȶ�����п�ֽ�����Ӱ�죬����Factsage��������������п��650~900 ���¶ȷ�Χ�ڵ���������������ͼ3��ʾ���ٶ���Ӧ��ϵ��ѹΪ101 kPa����ͼ3���Կ�������CO��CO2��ѹ��10.1 Pa~101 kPa��Χ�ڣ�����CO��ѹ�����ӡ�CO2��ѹ�Ľ��ͣ�����п��ԭ�����ƽ����������ΪZnFe2O4+ZnO��Fe3O4+ZnO��FeO+ZnO��Fe+ZnO����Fe3C+ZnO�������¶ȵ����ӣ�ZnFe2O4+ZnO��Fe3C+ZnO��������С��FeO+ZnO��Fe+ZnO����������Fe3O4+ZnO����δ�������Ա仯��һֱ���ֽϹ����������������������пѡ���Եػ�ԭΪ����п��������������˵��CO2�����������ڿ���������Ĺ���ԭ���ɴ˿ɼ���CO��CO2�ķ�ѹ����ʵ������п��ѡ���Էֽ�Ĺؼ��������¶ȶ�����п�Ļ�ԭ����Ҳ��һ����Ӱ�죬�¶ȹ��Ͳ���������п�ķֽ⣬�¶ȹ������������������������ɡ���ˣ�������ѧ�Ͻ������¶������˵ķ�Χ�ڣ�ͨ������CO��CO2�ķ�ѹ�ȿ���ʵ������п��ѡ���Էֽ⡣
2.2 ��������������п�ֽ���Ϊ��Ӱ��
Ϊ�˿��컹ԭ����������п��ɰ������пѡ���Էֽ���Ϊ��Ӱ�죬��ʵ���в��ÿ��Ʊ�����ϵͳ���о��˸����ض�����п�ֽ��ʺͱ��ղ���w(Fe2+)/w(FeT)ֵ��Ӱ�죬������ͼ4��ʾ������ǰ��̽�����飬�趨��ʼ����Ϊ��COŨ��5%(�������)��p(CO)/p(CO+CO2)=0.2����������1 L/min�������¶�700 �桢��תҤת��5 r/min������ʱ��1 h���ڽ��е���������ʱ���˿������ر仯������������Ϊ�ó�ʼֵ��
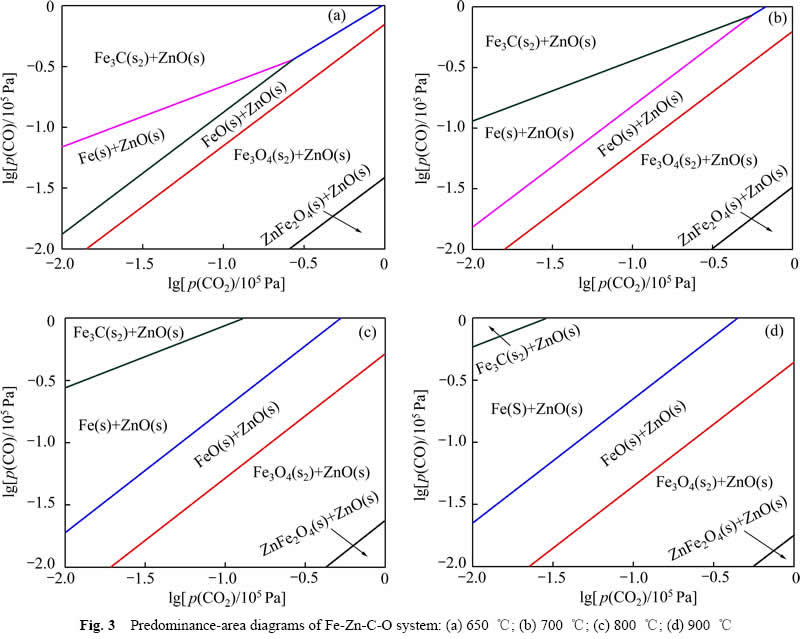
ͼ3 Fe-Zn-C-Oϵ��п���ֵ���������ͼ
��ͼ4(a)��֪�����ű���������COŨ�ȴ�1%������9%������п�ķֽ��ʴ�48.2%��������65.3%�Ͳ����w(Fe2+)/w(FeT)ֵ��0.26��������0.53����COŨ��Ϊ3%ʱ�����ղ����w(Fe2+)/w(FeT)ֵԼΪ1/3����COŨ�ȳ���3%���ղ����еIJ���������ͻᱻ����ԭΪ����������������п�ķֽ���һֱ������66%���ڣ���˵���ڻ�ԭ���չ����У���Ӧ(2)�ͷ�Ӧ(3)����淴Ӧ(1)�������ٽ��ͼ2��֪���ڸ�������������������ԭ����Ҫԭ���Ƿ�Ӧ(2)�ķ�������COŨ������5%ʱ������п�ķֽ��ʴﵽ60%����ʱw(Fe2+)/w(FeT)ֵԼΪ0.4��������������ֵ1/3����ˣ��ۺϿ��ǣ�COŨ��Ϊ5%ʱ��ԭ����Ч���ϼѡ���ͼ4(b)���Կ�������ԭ������CO��CO+CO2�ķ�ѹ�ȶ�����п�ķֽ���ΪӰ�����p(CO)/p(CO+CO2)ֵ��0.1���ڣ�����CO��ѹ�����ӣ�����п�ķֽ���Ѹ�����ӣ���p(CO)/p(CO+CO2)����0.1�Ժ�����п�ֽ��ʵ������ٶȱ仺������Fe2+�ĺ������ԣ�����CO�ķ�ѹ�������ӣ�������Fe2+�����Ȼ������ӣ���p(CO)/p(CO+CO2)����0.2�Ժ�Fe2+�����������ٶȼӿ졣�ɴ˿ɼ���p(CO)/p(CO+CO2)����0.2�Ļ�ԭ������������������п�Ĺ���ԭ����ͼ4(c)��֪����ԭ��������������п�ķֽ�Ч����һ����Ӱ�졣��������������1 L/minʱ������п�ķֽ��ʺͲ����w(Fe2+)/w(FeT)ֵ�����������������Ӷ����ӣ���������������1 L/min��������ָ�겻�������������������Ӷ���������������������Ϊ1 L/minʱ�����ṩ�㹻�Ļ�ԭ���գ������������������һ���ı仹ԭ�������յ���ɣ���˶�����п�ķֽ���Ϊ�����������Ӱ�졣
���˻�ԭ�����⣬�����¶�Ҳ��Ӱ�컹ԭ��Ӧ����Ҫ���ء���ͼ4(d)��֪���¶ȶ�����п�ķֽ���ΪӰ��ϴ����ű����¶ȴ�500 ��������900 �棬����п�ķֽ��ʴ�40.9%������68.8%�������w(Fe2+)/w(FeT)ֵ��0.31�����ӵ�0.57���������¶���700 �����ڣ����ű����¶ȵ���������п�ķֽ���Ѹ�����ӣ������ղ����w(Fe2+)/w(FeT)ֵ�������ӣ����¶ȳ���700 ���Ժ����ű����¶ȵ���������п�ķֽ��������ٶȱ仺�������ղ����w(Fe2+)/w(FeT)ֵ�����ٶȼӿ졣�ɴ˿�֪������Ե���������п�Ļ�ԭ��Ӧ��Ҫ�Է�Ӧ(1)����ʽ���У������¶ȿ��������ٽ���Ӧ(1)��������У����¶ȸ���700 ����Ʒ�Ӧ(1)���е���Ҫ�������¶�ת��Ϊ��������������Ӧ(2)�ͷ�Ӧ(3)���¶ȵ��������Լӿ죬����Fe2+������ʼѸ�����ӣ������2.1������ѧ�������һ�¡���ͼ4(e)���Կ�������תҤת�ٶ�����п�ֽ���Ϊ��Ӱ���뻹ԭ����������Ӱ�����ƣ���ת�ٴﵽ5 r/min��תҤ����Ʒ�ķ���Ч���ﵽ��ѣ���������ת�ٲ������ܽ�һ���ٽ�����п�ķֽ�������Դ�˷ѡ���ͼ4(f)���Կ���������ʱ�������п�ķֽ���ΪҲ����Ҫ��Ӱ�졣����ʱ���15 min����60 min������п�ķֽ��ʴ�39.9%Ѹ��������60.2%�������w(Fe2+)/w(FeT)ֵ��0.28������0.40�����ŷ�Ӧ�ļ������У�����п�ķֽ�����120 minʱ��������69.1%����Fe2+�ĺ����������ٶ���1 h��仺����ˣ��ӳ�����ʱ������������п�ķֽ⣬����ʱ�����������ܺĵļӴ�ͱ���Ч�ʵ��½����ʱ���ʱ�䲻�˳���2 h��

ͼ4 ��������������п�ֽ���Ϊ��Ӱ��
������ԣ�������������ض���Ӱ������п�ķֽ���Ϊ��COŨ�ȡ�p(CO)/p(CO+CO2)ֵ�������¶Ⱥ�ʱ����Ӱ������п�ķֽ���Ҫԭ�����������ͻ�תҤת��ֻ��һ����Χ�ڶ�����п�ķֽ���Ϊ�нϴ��Ӱ�졣�������Ϸ����ɵã�ʹп��ɰ������пѡ���Եķֽ�Ϊ����п���������������Ż��������£�COŨ��5%��p(CO)/p(CO+CO2)=0.2����������1 L/min�ͱ����¶�700 �桢��תҤת��5 r/min������ʱ��2 h���ڴ�����������п�ķֽ��ʽ�70%����������Ĺ���ԭ�����ء�
2.3 ��ԭ���չ��̿���ѧ�����仯�о�
Ϊ�˽�һ���о���ԭ���չ���������п�ķֽ���Ϊ������XRD�����˲�ͬ����ʱ���²���ľ�������������������ͼ5��ʾ����ͼ5��֪�����ղ�������������Ҫ����ΪZnO��Fe3O4��ZnS��Zn2SiO4����ϵ�1.1�ڵ����ۿ�֪��δ����ԭ������Ʒ�е���������Ҫ������п��ʽ���ڡ�����ԭ����ʱ��Ϊ30 minʱ��ZnFe2O4���������н��ͣ�ͬʱ�����������������������ӣ�������ʱ����С��������пת��Ϊ������������������ʱ��ﵽ60 minʱ��ZnFe2O4�����岻����һ�����Ͷ��һ�����ƫ�ƣ�ͬʱ����п�ķ��������ӡ�ZnFe2O4���������Ƶ���Ҫԭ�����ڷ�Ӧ������ZnFe2O4���ӽṹ�еIJ���Zn2+��Fe2+ȡ������Fe2+���Ӱ뾶С��Zn2+���Ӱ뾶����������п�ľ����С���Ӷ�ʹZnFe2O4���������ơ�������ʱ��Ϊ120 minʱ��п��ɰ�еĴ�����пת��Ϊ�����������������ӳ�����ʱ�������ڽ�п��ɰ�е�����пѡ���Ե�ת��Ϊ����п��������������
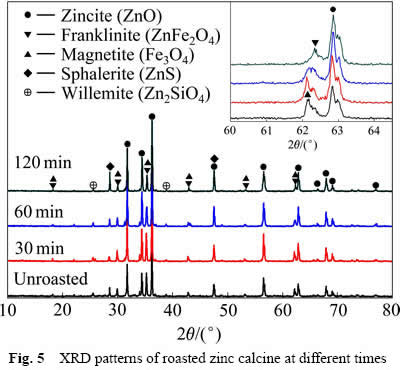
ͼ5 ��ͬʱ���±��ղ����XRD��
Ϊ�˿��컹ԭ���ղ��������ò����������ɳɷ֣��������SEM��EDS�Ա���ʱ��Ϊ2h�IJ���������о���������ͼ6��ʾ����ͼ6���Կ��������ղ�������Ƚ�С��������20 ��m���£�����������ɶ�ף�����以��������أ�δ�������Ե��ս�������ˣ��ں��������к���ͨ����ĥ��-��ѡ���ķ���ʵ��п�����룬�˲��õ�������ķ�������п�����롣��EDS������ͼ6(a)�б������ܹ⻬�Ļ�ɫ����(A)��Ҫ����Zn��O������������Fe������Mn��˵���������Ǽ�����������Fe3O4��Mn���ʵ�ZnO��ͼ�б�����Դֲڵİ�ɫ����(B)��Ҫ����Zn��O������һ������Fe��SԪ�أ������ⲿ�����������ZnO��Fe3O4��ZnS�Ļ���
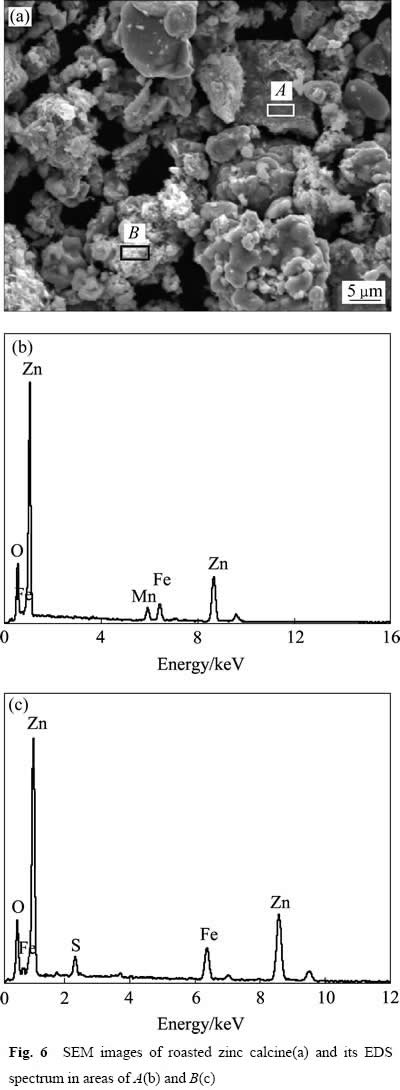
ͼ6 ��ԭ���ղ����SEM��EDS��
3 ����
1) ��������ѧ������֪��CO�ܽ�ZnFe2O4��ԭΪZnO��Fe3O4����Ҳ����ԭΪFeO����Ӧ�¶ȼ�CO��CO2�ķ�ѹ������п��ԭ��������Ӱ��ϴ�����¶ȡ�����CO��ѹ�ͽ���CO2��ѹ��ٽ�ZnFe2O4�ķֽ⣬ͬʱҲ������FeO��Fe���������������˵��¶Ⱥ������£�����ʵ������п��ѡ���Էֽ⡣
2) ͨ����ԭ���տ��Խ�п��ɰ�дֵ�ZnFe2O4ѡ���Էֽ�ΪZnO��Fe3O4��COŨ�ȡ�p(CO)/p(CO+CO2)ֵ�������¶Ⱥ�ʱ����Ӱ������п�ֽ���Ϊ����Ҫԭ��ԭ���������ͻ�תҤת��ֻ��һ����Χ�ڶ�����п�ķֽ���Ϊ�нϴ��Ӱ�졣���ű�������Ϊ��COŨ��5%��p(CO)/p(CO+CO2)=0.2����������1 L/min�ͱ����¶�700 �桢��תҤת��5 r/min������ʱ��2 h���ڴ�����������п�ķֽ��ʽ�70%����������Ĺ���ԭ�������ء�
3) ��XRD������֪�����ղ�����Ҫ��ZnO��Fe3O4��ZnS��Zn2SiO4����Ϊ����ZnFe2O4����ԭΪZnO��Fe3O4����SEM��EDS��������ԭ��Ʒ�������ɶ�ף����Ƚ�С������������أ�δ�������Ե��ս�������ˣ��ں��������к���ͨ����ѡ�ķ���ʵ��п�����룬Ӧ���õ�������ķ�������п�����롣
REFERENCES
[1] BALARINI J C, LUDMILA de O P, MIRANDA T L S, CASTRO R M Z d, SALUM, A. Importance of roasted sulphide concentrates characterization in the hydrometallurgical extraction of zinc[J]. Minerals Engineering, 2008, 21(1): 100-110.
[2] SANTOS S M C, MACHADO R M, CORREIA M J N, REIS M T A, ISMAEL M R C, CARVALHO J M R. Ferric sulphate/chloride leaching of zinc and minor elements from a sphalerite concentrate[J]. Minerals Engineering, 2010, 23(8): 606-615.
[3] ?OPUR M, ?ZMETIN C, ?ZMETIN E, KOCAKERIM M M. Optimization study of the leaching of roasted zinc sulphide concentrate with sulphuric acid solutions[J]. Chemical Engineering and Processing: Process Intensification, 2004, 43(8): 1007-1014.
[4] ������. ����ʪ����п������п����Ϊ�о�[J]. ������ɫ����, 2004, 20(5): 20-22.
PENG Hai-liang. Study on the behavior of zinc ferrite in conventional hydrometallurgical zinc production process[J]. Hunan Nonferrous Metals, 2004, 20(5): 20-22.
[5] CHEN T, DUTRIZAC J. Mineralogical changes occurring during the fluid-bed roasting of zinc sulfide concentrates[J]. JOM, 2004, 56(12): 46-51.
[6] JHA M K, KUMAR V, SINGH R J. Review of hydrometallurgical recovery of zinc from industrial wastes[J]. Resources, Conservation and Recycling, 2001, 33(1): 1-22.
[7] ERDEM M, ?ZVERDI A. Environmental risk assessment and stabilization/solidification of zinc extraction residue: ��. Stabilization/solidification [J]. Hydrometallurgy, 2011, 105(3): 270-276.
[8] TURAN M D, ALTUNDOGAN H S, TUMEN F. Recovery of zinc and lead from zinc plant residue[J]. Hydrometallurgy, 2004, 75(1/4): 169-176.
[9] ?OPUR M, PEKDEMIR T, ?OLAK S, KUNKUL A. Industrial symbiosis: High purity recovery of metals from Waelz sintering waste by aqueous SO2 solution[J]. Journal of Hazardous Materials, 2007, 149(2): 303-309.
[10] �� ��. ��ʪ����п���������-�Ƽ��������յ�̽��[J]. ����ұ��, 2010, 32(3): 56-58.
YANG Bin. Discussion on hot acid leach-jarosite process of hydrometallurgy zinc[J]. Gansu metallurgy, 2010, 32(3): 56-58.
[11] WANG Xin, SNINIVASAKANNAN C, DUAN Xin-hui, PENG Jin-hui, YANG Da-jin, JU shao-hua. Leaching kinetics of zinc residues augmented with ultrasound[J]. Separation and Purification Technology, 2013, 115: 66-72.
[12] JU Shao-hua, ZHANG Yi-fei, ZHANG Yi, XUE Pei-yi, WANG Yi-hui. Clean hydrometallurgical route to recover zinc, silver, lead, copper, cadmium and iron from hazardous jarosite residues produced during zinc hydrometallurgy[J]. Journal of Hazardous Materials, 2011, 192(2): 554-558.
[13] ������, ����Ԫ, ������, ��ƽ��. п����Һ��������[J]. ��ɫ����(ұ������), 2010, 62(3): 80-84.
DENG Yong-gui, CHEN Qi-yuan, YIN Zhou-lan, ZHANG Ping-min. Removal of ferrous/ferric iron from zinc leaching solution by goethite process[J]. Nonferrous Metals (Extractive Metallurgy), 2010, 62(3): 80-84.
[14] �� ��, ����ϲ, ����ȫ, ���ǻ�. ��������п�����̳����������Һ�г���[J]. ��ɫ����(ұ������), 2005(5): 13-15.
ZHAO Yong, JIANG Kai-xi, WANG De-quan, GUO Ya-hui. Iron removal from hot acid Leaching solution of zinc roasting dust by goethite process[J]. Nonferrous Metals (Extractive Metallurgy), 2005(5): 13-15.
[15] �� ��, ������, �� ��, �۽���, ����ɽ, �����E, ½ҵ��. п����Һ������ֱ��ˮ�����������̽��[J]. �й���ɫұ��, 2012, 41(4): 80-85.
YUE Ming, SUN Ning-lei, ZOU Xing, SHAO Jian-chun, LIU Jin-shan, WANG Kui-ting, LU Ye-da. The discussion on hydrolysis precipitation of ferric oxide directly from ferric-iron rich zinc leachate[J]. China Nonferrous Metallurgy, 2012, 41(4): 80-85.
[16] HOLLOWAY P C, ETSELL T H, MURLAND A L. Roasting of La oroya zinc ferrite with Na2CO3[J]. Metallurgical and Materials Transactions B, 2007, 38(5): 781-791.
[17] HOLLOWAY P C, ETSELL T H, MURLAND A L. Use of secondary additives to control the dissolution of iron during Na2CO3 roasting of La oroya zinc ferrite[J]. Metallurgical and Materials Transactions B, 2007, 38(5): 793-808.
[18] ZHANG Ya-li, YU Xian-jin, LI Xiao-bin. Zinc recovery from franklinite by sulphation roasting[J]. Hydrometallurgy, 2011, 109(3): 211-214.
[19] ������, �� ��, ����Ԫ, �� ��, �� ��. п������ԭ�� ��-��ѡ������[J]. �й���ɫ����ѧ��, 2012, 22(5): 1455-1461.
WANG Ji-ming, PENG Bing, CHAI Li-yuan, LI Mi, PENG Ning. Recovery iron from zinc leaching residues by reduction roasting and magnetic separation process[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(5): 1455-1461.
[20] LI Min, PENG Bing, CHAI Li-yuan, WANG Ji-ming, PENG Ninf, YAN Huan. Element distribution of high iron-bearing zinc calcine in high gradient magnetic field[J]. Transactions of Nonferrous Metals Society of China, 2012, 22(9): 2261-2267.
[21] YAN Huan, CHAI Li-yuan, PENG BING, LI Mi, PENG Ning, HOU Dong-ke. A novel method to recover zinc and iron from zinc leaching residue[J]. Minerals Engineering, 2014, 55: 103-110.
[22] LIU Wei, HAN Jun-wei, QIN Wen-qing, CHAI Li-yuan, HOU Dong-ke, KONG Yan. Reduction roasting of high iron-bearing zinc calcine for recovery of zinc and iron[J]. Canadian Metallurgical Quarterly, 2014, 53(2): 176-182.
[23] ����ΰ, �� ά, ������, ����Ԫ, ֣����, �� ��. ����п��ɰѡ���Ի�ԭ����-���ν���п[J]. �й���ɫ����ѧ��, 2014, 24(2): 511-518.
HAN Jun-wei, LIU Wei, QIN Wen-qing, CHAI Li-yuan, ZHENG Yong-xing, YANG Kang. Leaching zinc from high iron-bearing zinc calcine after selective reduction roasting[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(2): 511-518.
Selective decomposition behavior of zinc ferrite by reduction roasting with CO
HAN Jun-wei1, LIU Wei1, QIN Wen-qing1, CAI Xin2, LUO Hong-lin1, WANG Da-wei1
(1. School of Minerals Processing and Bioengineering, Central South University, Changsha 410083, China;
2. School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: In order to selectively decompose ZnFe2O4 contained in zinc calcine to ZnO and Fe3O4, the decomposition behavior of zinc ferrite during CO reduction roasting process was studied. The thermodynamic basis of ZnFe2O4 decomposition with CO was firstly calculated by HSC and Factsage software, then the effects of reduction roasting conditions on ZnFe2O4 decomposition behavior were investigated by reduction roasting test using rotary kiln. The results show that ZnFe2O4 can be selectively converted into ZnO and Fe3O4 at appropriate temperature and atmosphere. CO concentration, p(CO)/p(CO+CO2), roasting temperature and time have significant effects on the selective decomposition behavior, and increasing them are conducive to the decomposition of ZnFe2O4 and the generation of FeO. Under the optimum condition, the decomposition rate of ZnFe2O4 is nearly 70% without substantive over-reduction of iron. The roasting product mainly composes of ZnO, Fe3O4, ZnS and Zn2SiO4, and the particles are small, loose, porous and seriously mutual encapsulated according to XRD and SEM / EDS analyses.
Key words: zinc ferrite; zinc calcine; zinc residue; reduction roasting; decomposition behavior
Foundation item: Project(51204210) supported by the National Natural Science Foundation of China; Project (2012BAC12B04) supported by the National Science and Technology Pillar Program during the 12th ��Five-year�� Plan Period; Project(2011AA061001) supported by the National High Research Development Program of China
Received date: 2015-01-30; Accepted date: 2016-03-10
Corresponding author: LIU Wei; Tel: +86-731-88830884; E-mail: ase.6520@163.com
(�༭ ������)
������Ŀ��������Ȼ��ѧ����������Ŀ(51204210)�����ҡ�ʮ���塱�Ƽ�֧�żƻ�������Ŀ(2012BAC12B04)�����Ҹ����о���չ�ƻ�������Ŀ(2011AA061001)
�ո����ڣ�2015-01-30�������ڣ�2016-03-10
ͨ�����ߣ��� ά����ʦ����ʿ���绰��0731-88830884��E-mail: ase.6520@163.com