网络首发时间: 2013-12-27 16:44
稀有金属 2014,38(03),447-453 DOI:10.13373/j.cnki.cjrm.2014.03.016
D001树脂静态吸附钕离子的热力学与动力学研究
杨幼明 沈文明 黄振华 蓝桥发 余攀
江西理工大学冶金与化学工程学院
摘 要:
为达到Nd3+富集目的, 实验研究D001树脂静态吸附稀土Nd3+过程。通过单因素实验优化平衡吸附条件, 并研究树脂吸附稀土Nd3+的热力学和动力学特征。结果表明:T=293 K, pH=3.5, [Nd3+]浓度10 mmol・L-1条件下, 树脂的饱和吸附容量达到698.9×10-3mmol・g-1;吸附过程遵循Langmuir等温方程, 热力学参数为:ΔH=13.45 kJ・mol-1, ΔS=53.035 J・mol-1・K-1, ΔG=-2.09 kJ・mol-1。热力学函数ΔG<0表明D001树脂吸附Nd3+过程能够自发进行。准二级动力学模型能够很好拟合DO01树脂吸附Nd3+的过程并且其相关系数在0.99以上。吸附活化能Ea=1.04857 kJ・mol-1, 反应控制步骤为膜扩散和颗粒内扩散联合扩散控制。
关键词:
钕;D001树脂;静态吸附;热力学;动力学;
中图分类号: O647.32
作者简介:杨幼明 (1965-) , 男, 江西都昌人, 硕士, 教授, 研究方向:稀土冶金、稀土材料及钨钼冶金等;电话:13879789029;E-mail:yanguming@126.com;
收稿日期:2013-07-29
基金:国家科技部“863”计划项目 (2012AA061901) 资助;
Thermodynamics and Kinetics of Static Adsorption of Neodymium Ions with D001 Ion Exchange Resin
Yang Youming Shen Wenming Huang Zhenhua Lan Qiaofa Yu Pan
School of Metallurgy and Chemical Engineering, Jiangxi University of Science and Technology
Abstract:
The static adsorption properties of D001 resin for rare earth neodymium ions was studied in order to enrich Nd3 +. Equilibrium adsorption conditions was optimized by single factor experiments, and the thermodynamics and dynamics characteristics of the resin adsorption of Nd3 +were studied. It showed that, under the conditions of T = 293 K, pH = 3. 5, [Nd3 +]=10 mmol・L- 1, the saturation adsorption capacity of resin was 698. 9 × 10- 3mmol・g- 1. The adsorption behavior of D001 resin for neodymium ions was based on the Langmuir isotherm equation. The adsorption thermodynamic parameters were: ΔH = 13. 45 kJ・mol- 1, ΔS =53.035 J・mol- 1・K- 1, ΔG =-2.09 kJ・mol- 1. ΔG < 0 implied that the process of D001 resin adsorption neodymium ions could occur spontaneously. The correlation coefficient was greater than 0. 99. The activation energy Ea= 1. 04857 kJ・mol- 1. The controlling step was joint diffusion of liquid film diffusion and particle diffusion in the course of adsorption.
Keyword:
neodymium; D001 resin; static adsorption; thermodynamics; kinetics;
Received: 2013-07-29
由于稀土具有3d4f电子层, 在催化、光电转换、磁性材料、发光材料、新能源等方面的广泛应用而被称为工业“维生素”[1]。稀土钕因其单自旋电子, 在钕铁硼永磁体, 尖端科技如航空航天行业需求加大。随着科技发展, 对钕以及相关产品的需求量越来越大, 随着资源贫竭, 对低品位矿的开发利用以及废钕材料的回收富集成为我国稀土资源二次利用的战略方向。
目前工业上采用溶剂萃取富集稀土, 但由于萃取过程中大量使用有机物质, 容易出现“乳化”现象, 导致后续增加破乳工艺, 使工艺加长并且稀土资源流失, 产生大量氨氮超标的废水。针对这种情况, 有学者用BK110, D155树脂吸附铒、镝离子进行研究[2,3,4], 其特点D155和BK110树脂是含-COOH功能基, 与稀土离子有很强的亲合力, 具有富集能力大、操作简便、可以重复使用、成本较低等优点。这为稀土的富集提供了一种新的思路, 利用树脂吸附分离富集稀土成为稀土湿法冶金的研究热点。
根据软硬酸碱理论, 稀土离子由于具有较高的电荷, 较小的离子半径常被认为是硬度较大的阳离子, 与各种原子的络合能力的大小顺序为:O>N>S>F>Cl>Br>I, D001树脂是大孔型苯乙烯系强酸阳离子交换树脂, 结构就是乙烯双键两头挂两个苯环, 在苯环邻对位连接上一个磺酸基。本文初次尝试用D001树脂吸附Nd3+, 并对D001树脂吸附Nd3+行为及机制进行研究, 取得较好的效果, 为D001树脂在工业上吸附富集稀土钕提供基础数据并为理论研究打下基础。
1实验
1.1药品和仪器
药品:D001树脂;Nd3+溶液由Nd2O3 (99.99%) 溶于浓盐酸配制;0.002811 mol・L-1EDTA标定液;1 mol・L-1盐酸;其他药品均为分析纯。
仪器:酸滴定管、DF-1集热式磁力搅拌水浴锅、p H试纸, 广泛试纸 (0~14) 和 (0~5) 的精密试纸。
1.2实验方法
1.2.1树脂预处理
树脂实验先用1 mol・L-1的氢氧化钠体积比VNa OH/V树脂=3浸泡24 h, 用去离子水洗至中性, 再用1 mol・L-1的盐酸体积比VHCl/V树脂=3浸泡24 h, 用去离子水洗至中性, 并浸泡在蒸馏水中待用。
1.2.2分析方法
EDTA络合法滴定溶液中稀土的浓度[5,6]:用移液管吸取1~2 ml稀土料液于锥形瓶中, 并加入20 ml蒸馏水。加10 ml配好的20%六次甲基四胺缓冲溶液, 摇匀。滴加2~3滴0.5%二甲酚橙指示剂, 则溶液颜色变为紫色 (滴定槽样时, 铁对指示剂产生干扰, 可加入少量抗坏血酸作为还原剂, 将三价铁还原为二价铁从而避免了三价铁的干扰) 。用EDTA标准溶液进行滴定, 直至溶液由紫色变为亮黄色, 则认为是滴定终点, 记录此时消耗的EDTA体积。则稀土浓度的计算公式为:

式中C1为被测稀土料液浓度mol・L-1;C2为EDTA标准液的浓度mol・L-1;V1为消耗EDTA的体积L;V2为吸取的稀土料液体积L。
1.2.3吸附平衡实验
称取预先处理好的的10 g树脂于一系列烧杯中, 加入700 ml初始p H为5.5、初始浓度为10 mmol・L-1钕溶液, 在恒温水浴锅中反应, 每隔2 h取上清液用EDTA络合法滴定溶液中稀土的浓度直至平衡, 用下式计算


式中Qt为吸附平衡每克树脂的吸附容量 (mmol・g-1) ;V1为水相的体积 (L) ;C0, Ct为溶液中Nd3+的始、末浓度 (mmol・L-1) ;D为分配比;m为树脂质量 (g) 。
2结果与讨论
2.1平衡吸附容量的测定
在10 g树脂, T=303 K, 取C0=10 mmol・L-1的钕离子1000 ml的条件下进行静态吸附试验, 测定不同吸附时间t对吸附容量Qt的影响, 结果如图1所示。
由图1可知, D001树脂的吸附容量随着时间的增大而增加, 最后达到一定数值后不再变化。在12 h左右, 树脂对Nd3+的吸附几乎达到平衡, 平衡吸附容量为690.9×10-3mmol・g-1。原因是:开始时溶液中钕浓度大, 树脂吸附Nd3+的速度大于Nd3+的解吸速度, 随着时间增长, 当解吸速率和吸附速率达到相等时, 此时, 溶液中钕离子的化学位和树脂中钕的化学位相等, 此时达到动态平衡, 树脂达到最大荷载量Nd3+。
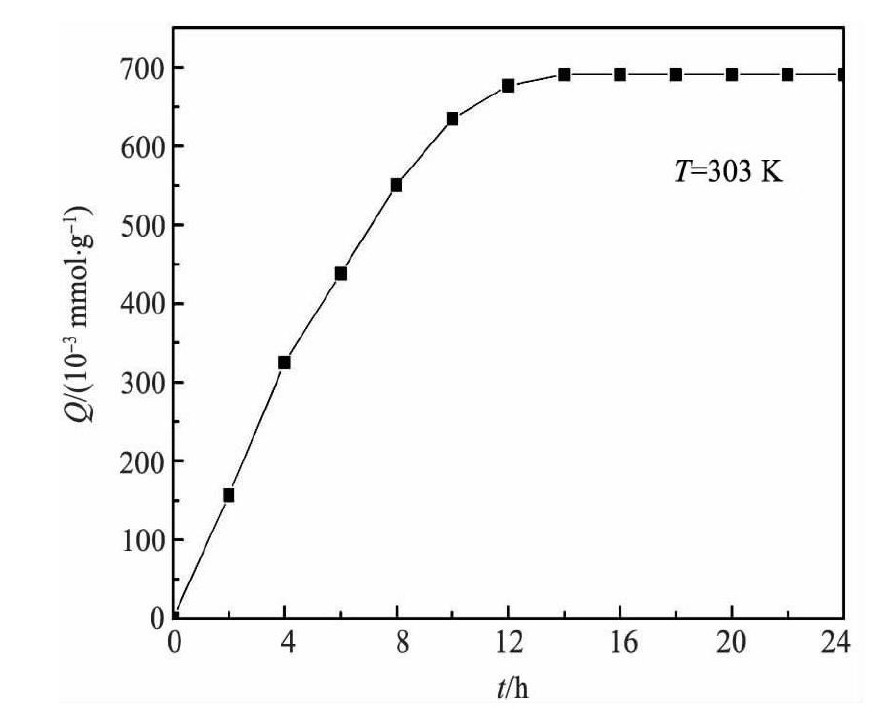
图1 吸附时间对钕吸附容量的影响Fig.1 Effect of time on adsorption capacity of neodymium
2.2不同p H值对分配比 (D) 、吸附容量 (Qt) 的影响
在10 g树脂, T=303 K, 取C0=10 mmol・L-1的钕溶液700 ml的条件下进行静态吸附试验, 测定在不同的p H值对分配比 (D) 、吸附容量 (Qt) 的影响, 结果如图2, 3所示。
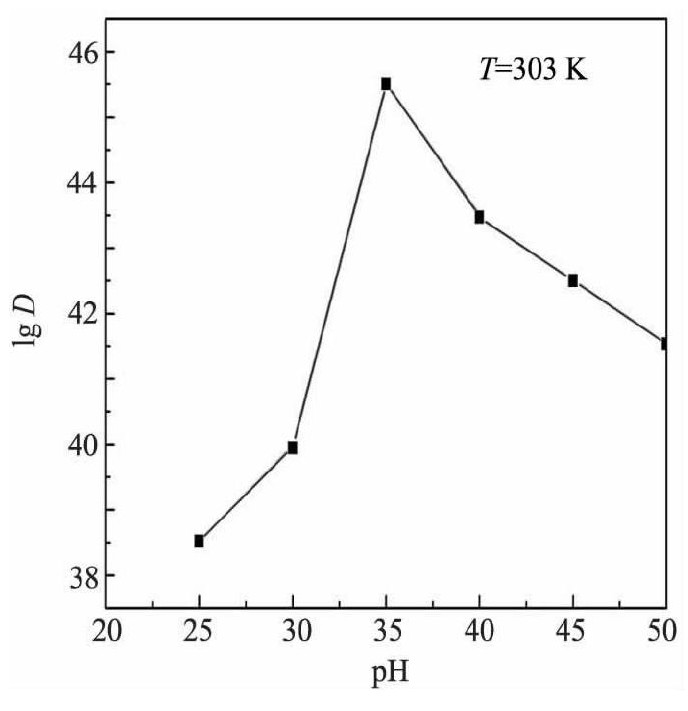
图2 p H值对分配比的影响Fig.2 Effect of p H on distribution ratio
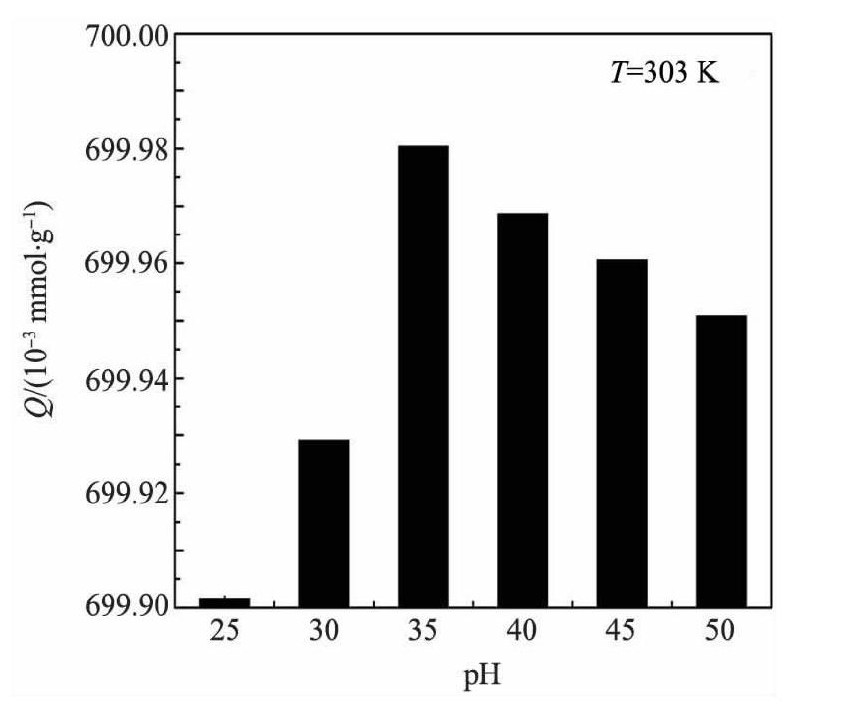
图3 p H值对吸附容量 (Q) 的影响Fig.3 Effect of p H on adsorption capacity
从图2可知, 随着p H值的升高, 分配比先升高后降低, p H在3.0~3.5之间时, 斜率最大, 并在p H=3.5时分配比达到最大。表明在p H=3.5时D001对Nd3+的吸附量最大。从图3可知, 当PH逐渐增大时, D001树脂的吸附容量随着增加, 在p H=3.5吸附量达到最大, p H>3.5时, 吸附容量随着PH的增加而减少。主要原因:在p H<2.5时, D001树脂优先吸附水中的H+, 而当p H>5.5时Nd3+易与水中的OH-结合形成沉淀, 不利于树脂对Nd3+的吸附[7]。
2.3不同浓度钕溶液对树脂吸附容量的影响
在10 g树脂, T=303 K, p H=3.5, 取钕溶液1000 ml的条件下进行静态吸附试验, 测定在不同浓度的钕溶液对吸附容量 (Qt) 的影响, 结果如图4。
由图4可知:Nd3+的浓度为5 mmol・L-1时, 树脂的吸附容量为500×10-3mmol・g-1, 达到吸附平衡的时间为16 h;Nd3+的浓度为10 mmol・L-1时, 树脂的吸附容量为690.8×10-3mmol・g-1, 达到吸附平衡的时间为12 h;Nd3+的浓度为15 mmol・L-1时, 树脂的吸附容量为698.9×10-3mmol・g-1, 达到吸附平衡的时间为11 h。说明吸附容量随着Nd3+的浓度增大而增加, 吸附平衡时间Nd3+的浓度增大而减少。当钕溶液浓度>10 mmol・L-1时, 平衡吸附量基本没有变化, 吸附平衡时间相差不大。这表明随着溶液中钕浓度的增大, 液膜的传质速率加快, 但钕初始浓度大于一定值时, 外扩散变成了内扩散[8]。实验表明, 选择Nd3+的初始浓度为10mmol・L-1比较适宜, 吸附时间为12 h, D001树脂对Nd3+的饱和吸附容量为698.9×10-3mmol・g-1。
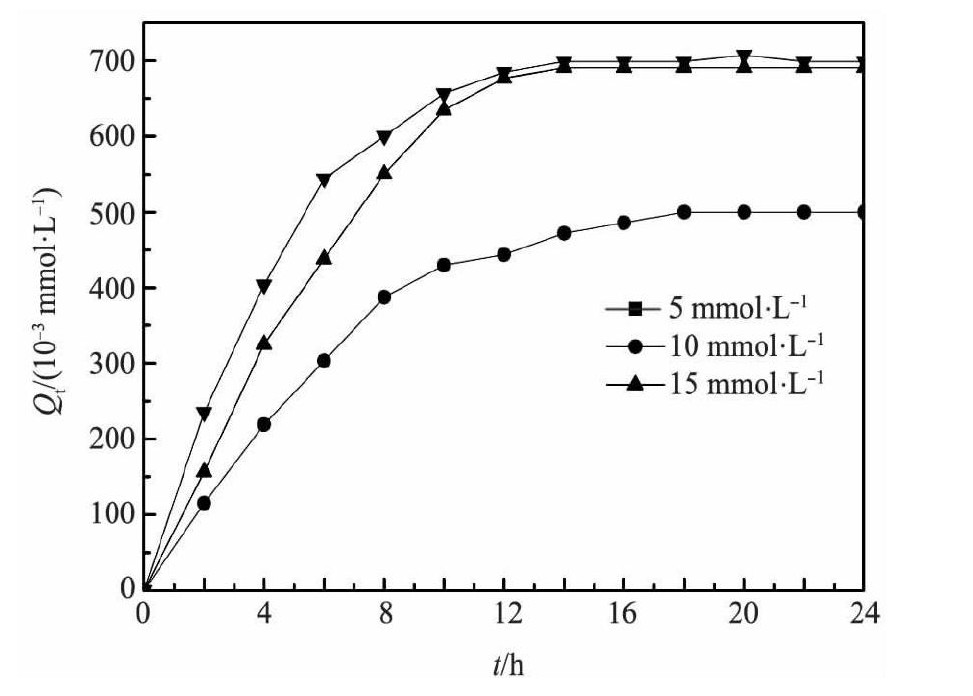
图4 钕浓度对树脂吸附容量的影响Fig.4 Effect of concentration of neodymium on adsorption capacity
2.4 Langmuir等温吸附曲线
在T=303 K, p H=3.5, C0=10 mmol・L-1的钕溶液700 ml的条件下进行静态吸附试验, 分别取10, 11, 12, 13 g D001树脂。根据测得的平衡浓度Ct和吸附容量Qt。根据兰缪尔 (Langmuir) 等温式的函数表达式[9]

式中KF为吸附系数;Qt, Qe分别表示t时刻树脂吸附容量和树脂饱和吸附容量。
以 和Ct作图, 再用Origin软件进行拟合得出如图5所示。
和Ct作图, 再用Origin软件进行拟合得出如图5所示。
根据兰缪尔 (Langmuir) 等温式的函数可求KF=2.0102, Qe=704.2×10-3mmol・g-1, 表明树脂D001吸附Nd3+属于表面单层吸附。D001树脂表面均一、具有相等量的可利用的结合位点, 吸附在表面的物质不互相影响。在树脂吸附处于平衡状态时, 树脂平衡吸附量Qt随Nd3+浓度C0增加, 会达到一个极限值[10]。
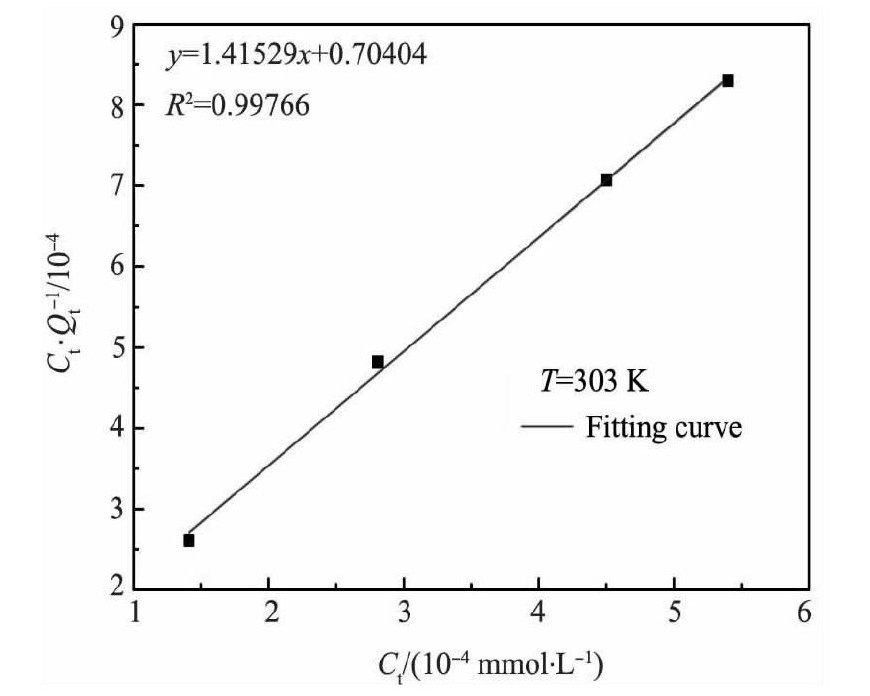
图5 等温吸附曲线Fig.5 Freundlich isotherm curve
2.5温度对分配比的影响及热力学函数的测定
在10 g树脂3份, p H=3.5, C0=10 mmol・L-1的钕溶液700 ml的条件下进行静态吸附试验, 测定温度在293, 303, 313 K时树脂吸附钕离子分配比的变化。以lg D对T-1作图6。
从图6中可知, 随着温度的升高, 吸附能力加强, 所以吸附过程是吸热过程, 吸附过程是化学吸附。根据范霍夫等温方程[9] (vant Hoff plot) 。
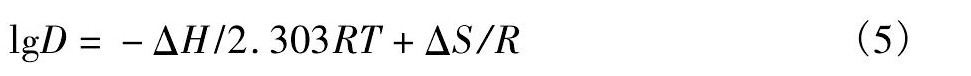
求得ΔH=13.45 k J・mol-1, ΔS=53.035 J・mol-1・K-1, ΔG=-2.09 k J・mol-1。由于ΔS>0, ΔG<0, 表明在293 K条件下, 热力学函数ΔG<0表明D001树脂吸附Nd3+过程能够自发进行;ΔH>0表明离子交换过程为吸热过程, ΔS>0表明吸附过程的熵变是增大的。
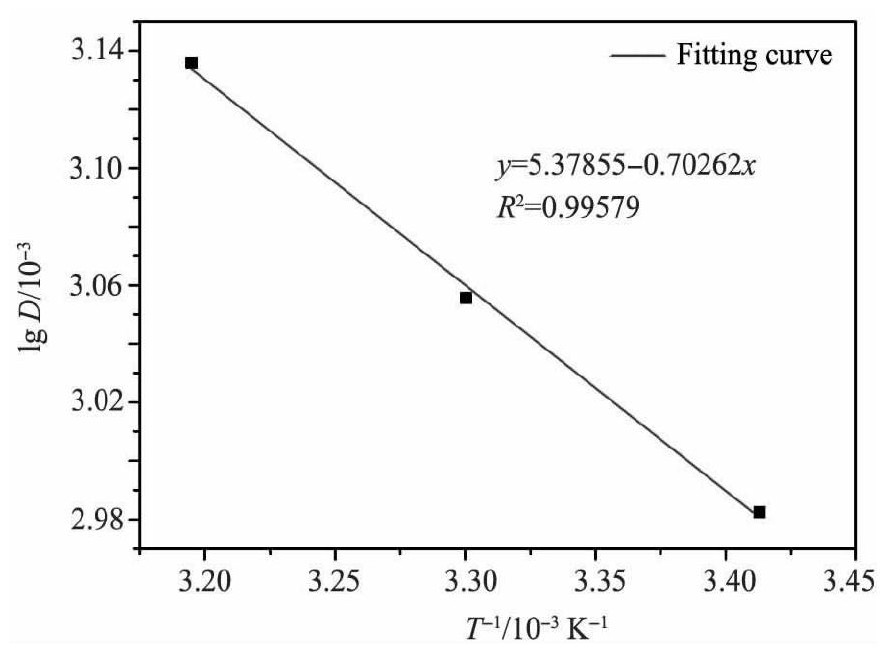
图6 温度对分配比的影响Fig.6 Influence of temperature on distribution ration
2.6吸附动力学模型选择和吸附常数的测定
吸附动力学模型重金属的吸附反应常遵循Lagergren方程 (准一级吸附动力学方程) [11]、准二级吸附动力学方程、二级动力学方程[12]。必须满足下面的等式:

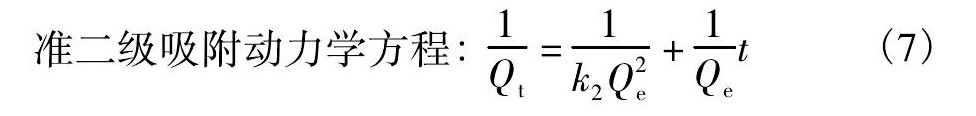
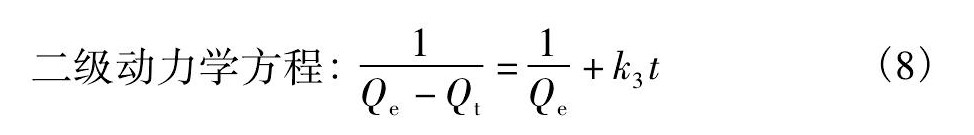
式中Qe, Qt为树脂吸附平衡时的吸附量, t时刻树脂的吸附量;k1, k2, k3为对应方程式的反应速率常数。
在10 g树脂3份, p H=3.5, C0=10 mmol・L-1的钕溶液700 ml的条件下进行静态吸附试验, 分别以D001树脂吸附钕的lg (Qe-Qt) , t/Qt, 1/ (Qe-Qt) 与t进行线性拟合, 结果如图7。
由图7可知上述方程的相关系数R2分别为0.991, 0.999, 0.924, 3个方程都能很好的解释树脂吸附钕离子的过程, 但t・Qt-1与t的性关系数最大, 由此可判定D001树脂吸附钕离子最符合准二级吸附动力学模型, 根据计算出理论吸附量为699.3×10-3mmol・g-1, 吸附速率常数为K2=2.730 mol・g-1・h-1。根据实验结果可知:D001树脂对钕离子的吸附量为698.9×10-3mmol・g-1, 与计算结果非常相似。
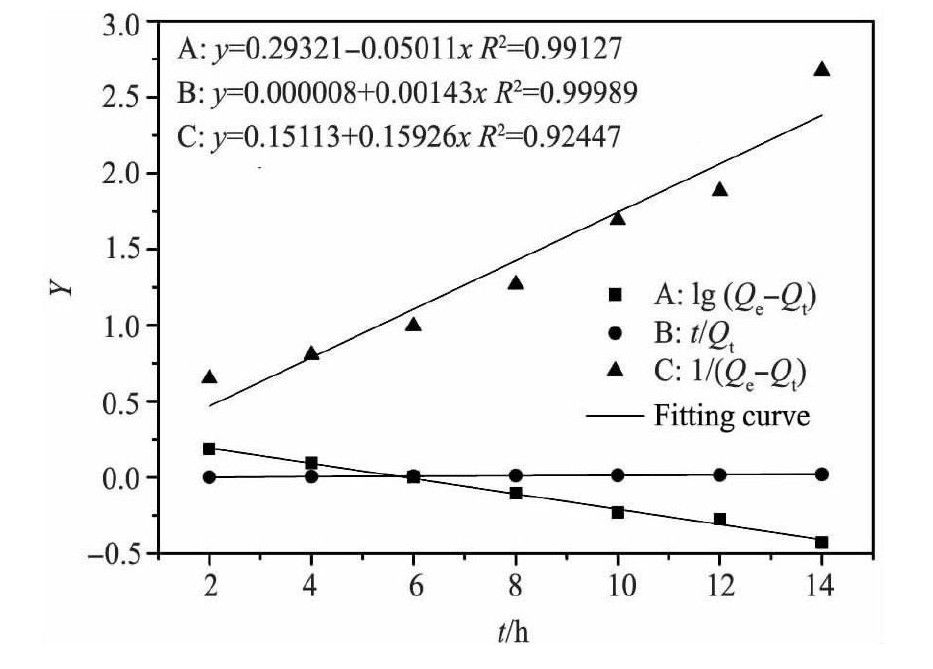
图7 不同的动力学模型对D001树脂吸附Nd3+拟合图Fig.7 Kinetic parameters of adsorption of neodymium ion with D001
A:Quasi first level of adsorption dynamics equation;B:Quasi two stage adsorption kinetics equation;C:The secondary dynamics equation
2.7温度对吸附常数的影响及吸附活化能的测定
在10 g树脂3份, p H=3.5, C0=10 mmol・L-1的钕溶液700 ml的条件下进行静态吸附试验, 温度分别为293, 303, 313 K。根据准二级吸附动力学方程, 以t/Qt对t作图。对图进行拟合求得的截距, 截距=k-1Qe-1, 分别求得K293 K=0.00024086mol・g-1・h-1, K303 K=0.00024431 mol・g-1・h-1, K313 K=0.00024757 mol・g-1・h-1。说明温度对吸附常数有影响, 随着温度的升高, 吸附常数增大。
根据阿累尼乌斯 (Arrhenius) 方程[9]:
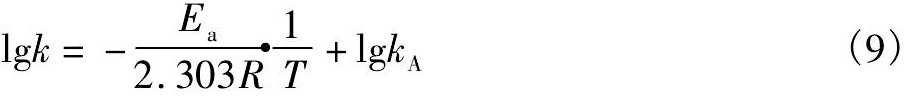
以lgk对T-1作图8。直线的斜率:

求得该吸附反应的活化能Ea=1.04857 k J・mol-1<10 k J・mol-1, 表明D001吸附钕离子的控制步骤非化学反应控制[2]。
2.8吸附控制机制判断
吸附过程包括4个连续的步骤[13,14]: (1) 在溶液中进行外扩散; (2) 在吸附剂表面的液膜中进行膜扩散; (3) 在吸附剂内部孔径中进行粒扩散; (4) 吸附质在吸附剂上进行吸附和解吸反应。4个步骤中任何一个都可以是控制吸附速率的素。通常用快速混合消除外扩散对吸附速率的影响。这样, 吸附过程就可认为是由膜扩散、粒扩散和吸附-解吸反应组成, 其中的慢者为吸附全过程的速率控制步骤。加快较慢扩散步骤的速率, 则可提高整个吸附速率。
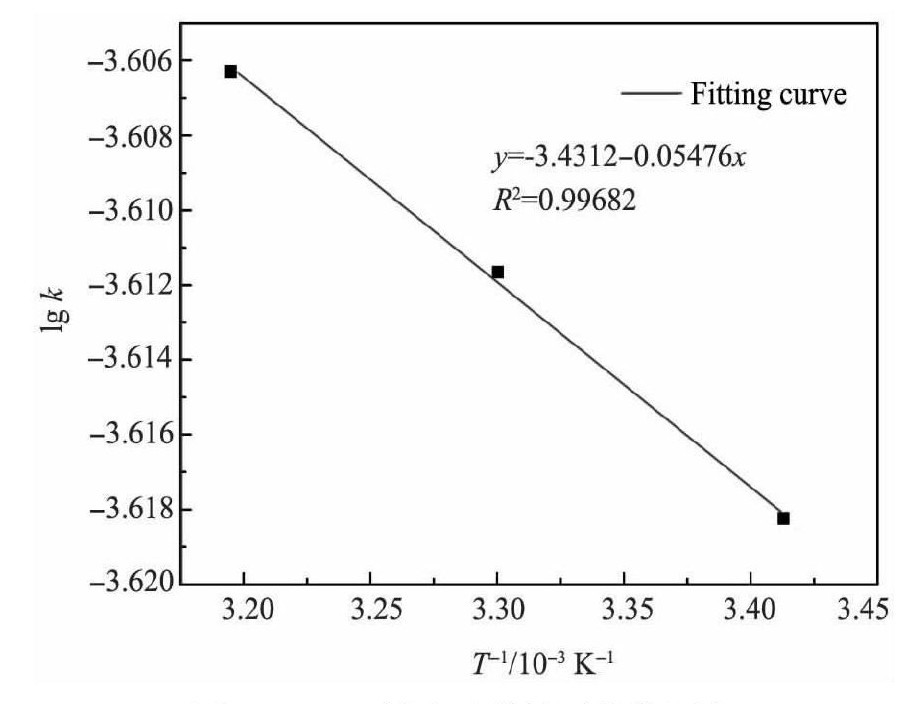
图8 D001树脂吸附钕活化能测定Fig.8 Adsorption of neodymium with D001 activation energy curve
根据动力学边界模型的膜扩散、颗粒内部扩散、吸附化学反应控制方程[15]:
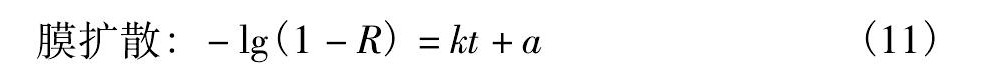
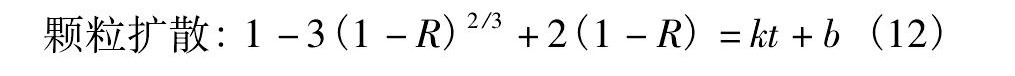
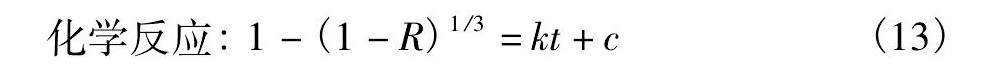
式中R=Qt/Q0为吸附百分率;a, b, c为对应方程的修正常数;k为速率常数。
Ea<10 k J・mol-1, 表明D001吸附Nd3+的控制步骤非化学反应控制。所以分别以-lg (1-R) , 1-3 (1-R) 2/3+2 (1-R) 与t作图, 结果如图9, 10所示。
由图9, 10可知:膜扩散、颗粒内扩散线性相关系数R2分别为0.99204, 0.98155。两者相关系数相差不大, 说明属于膜扩散和颗粒内扩散联合扩散控制[16]。
3结论
1.D001树脂的吸附容量随时间的增大而增加, 最后达到一定数值后不变。在12 h左右, 树脂对Nd3+的吸附几乎达到平衡, 吸附静态饱和容量为698.9×10-3mmol・g-1, 在p H=3.5时D001对Nd3+的吸附量最大。吸附容量随着p H逐渐变大先增后减。
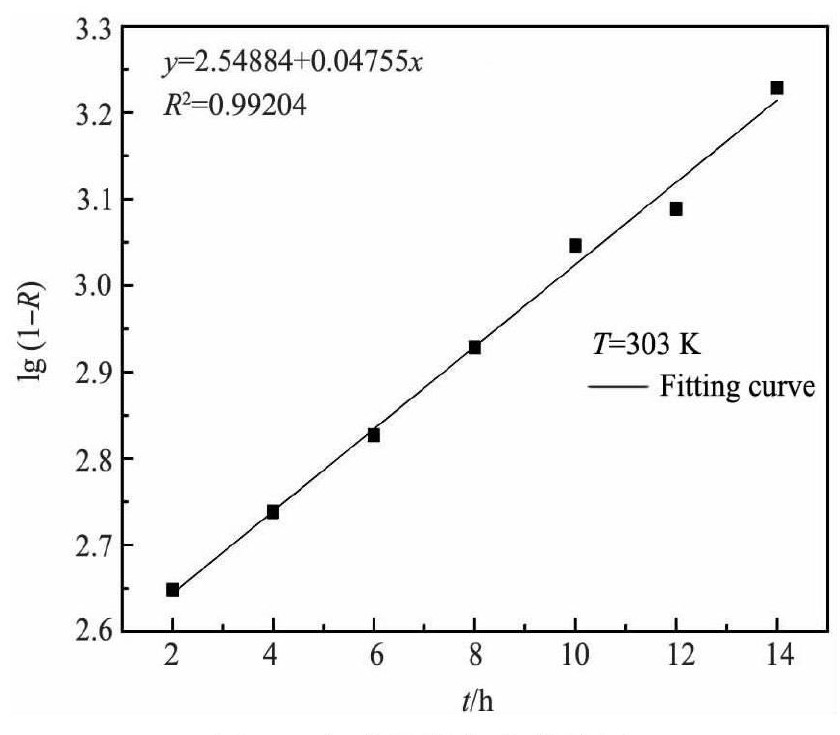
图9 液膜扩散拟合曲线图Fig.9 Fitting curve of liquid film diffusion
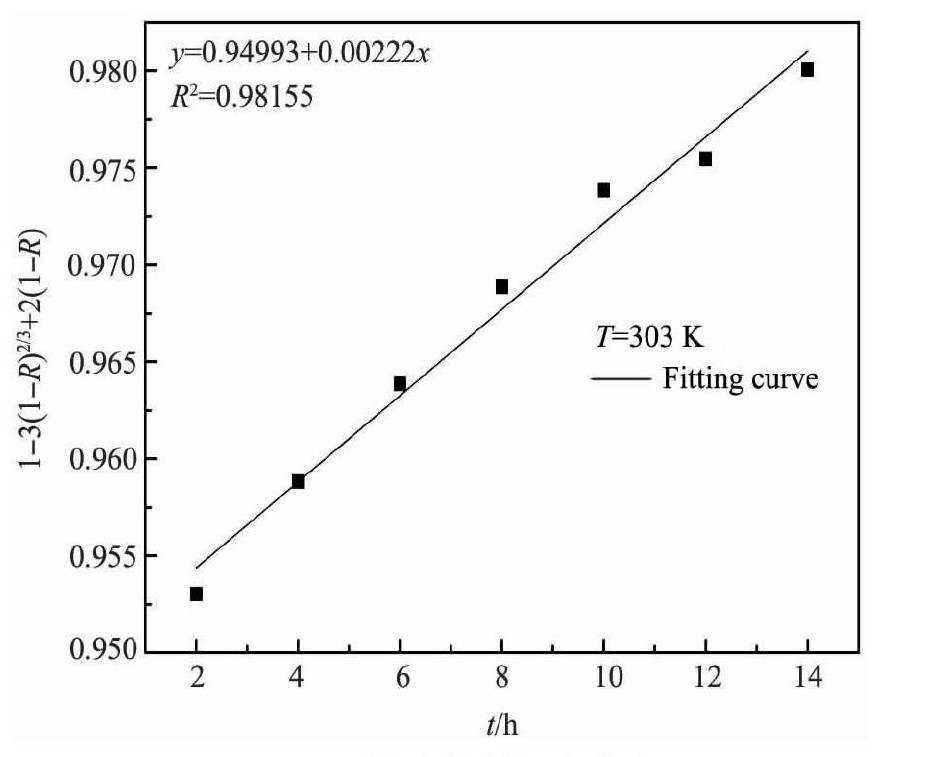
图1 0 颗粒内扩散拟合曲线Fig.10 Fitting curve of particle diffusion
2.吸附过程遵循Langmuir等温方程, 测得的热力学参数为:ΔH=13.45 k J・mol-1, ΔS=53.035 J・mol-1・K-1, ΔG=-2.09 k J・mol-1。由于ΔS>0, ΔG<0, 表明在293 K条件下, 树脂D001可以自发吸附Nd3+。
3.D001吸附Nd3+过程符合准二级吸附动力学过程, 吸附速率随温度升高而增大。吸附活化能Ea=1.04857 k J・mol-1, Ea<10 k J・mol-1表明D001吸附钕离子的控制步骤为非化学反应控制。
4.根据吸附机制判断的拟合方程结果得出:膜扩散和颗粒内扩散联合扩散控制为D001树脂吸附Nd3+的主要控制步骤。与树脂吸附活化能得出的结果吻合。
参考文献
[1] Liu G H.Rare-Earth Materials and Application Technology[M].Beijing:Chemical Industry Press, 2005.217. (刘光华.稀土材料与应用技术[M].北京:化学工业出版社, 2005.217.)
[2] Wang H J, Gao W B, Gao P.Study on adsorption of erbium with BK110 resin[J].Chinese Rare Earths, 2011, 32 (2) :19. (王惠君, 高伟彪, 高鹏.BK110树脂吸附铒的研究[J].稀土, 2011, 32 (2) :19.)
[3] Wang H J, Gao P.Study on adsorption of dysprosium with BK110 resin[J].Chinese Rare Earths, 2007, 28 (3) :64. (王慧君, 高鹏.BK110树脂对镝的吸附及机理研究[J].稀土, 2007, 28 (3) :64.)
[4] Shi L M, Wang H J.Study on adsorption of erbium with D155 resin[J].Chinese Rare Earths, 2008, 29 (4) :26. (施林妹, 王惠君.D155树脂对铒 (Ⅲ) 的吸附行为研究[J].稀土, 2008, 29 (4) :26.)
[5] Jiang Z C, Cai R X, Zhang H S.Rare Earth Element Geochemistry[M].Beijing:General Science Press, 2000.495. (江祖成, 蔡汝秀, 张华山.稀土元素分析化学[M].北京:科学出版社, 2000.495.)
[6] GB/T 14635-2008.Rare earth metals and their compounds.Determination of total rare earth contents[S].Chinese Standard, 2008. (GB/T 14635-2008.稀土金属及其化合物化学分析方法.稀土总量的测定[S].中国标准, 2008.)
[7] Liu D, He X, Xiong X D.Preparation of high purity cobalt with deep purification by ion exchange[J].Chinese Journal of Rare Metals, 2013, 37 (1) :112. (刘丹, 贺昕, 熊晓东.离子交换法深度除杂制备高纯钴的研究[J].稀有金属, 2013, 37 (1) :112.)
[8] Xu G X, Yuan C Y.Solvent Extraction of Rare Earths[M].Beijing:General Science Press, 1987.1 . (徐光宪, 袁承业.稀土的溶剂萃取[M].北京:科学出版社, 1987.1.)
[9] Chun H X, Cai P Y.Study on the adsorption ofcadmium (II) from aqueous solution by D152 resin[J].Journal of Hazardous Materials, 2009, 166:815.
[10] Wang S L, Liang Y J.Physical Chemistry[M].Beijing:Metallurgical Industry Press, 2008.169. (王淑兰, 梁英教.物理化学[M].北京:冶金工业出版社, 2008.169.)
[11] Liu J S, Yuan Y X.Adsorption property of P507levextrel resin for indium (III) iron hydrochloric acid system[J].Rare Metals and Cemented Carbidies, 2008, 26 (4) :1. (刘军深, 袁延旭.P507萃淋树脂在盐酸介质中吸附铟 (Ⅲ) 的性能[J].稀有金属与硬质合金, 2008, 26 (4) :1.)
[12] Gao F, Yan W B, Shi M L, Zhou Z X, Yin C W.Study on static adsorption properties and kinetics of vanadium for D2O1 resin[J].Applied Chemistry, 2010, 39 (6) :806. (高峰, 颜文斌, 石美莲, 周再兴, 尹朝旺.D201树脂吸附钒的静态性能及动力学研究[J].应用化学, 2010, 39 (6) :806.)
[13] Xiong C H, Zhu S, Yao C P, Chen Q.Adsorption behavior of Pd (Ⅱ) from aqueous solutions by D201resin[J].Rare Metals, 2011, 30 (5) :470.
[14] Zhao Z Y, Xu X Y, Chen X Y, Zhuo G S, Chen A L, Liu X H, Xu H.Thermodynamics and kinetics of adsorption of molybdenum blue with D301 ion exchange resin[J].Trans.Nonfrrous Mct.Soc., 2012, (22) :686.
[15] Mo J J, Shi L M, Gu Y B, Yan G B.Adsorption of platinum (Ⅳ) onto D301R resin[J].Rare Metals, 2008, 27 (3) :233.
[16] Bai G H, Li J C, Zhang G F.Adsorption behavior of D201 resin for vanadium (V) [J].Mineral Engineering, 2010, 30 (5) :62. (白国华, 李建臣, 张国范.D201树脂吸附钒 (Ⅴ) 的行为研究[J].矿冶工程, 2010, 30 (5) :62.)