DOI: 10.11817/j.ysxb.1004.0609.2021-39791
Cu-Zn-Ni-Sn仿金合金在人工海水和人工汗液中的腐蚀行为
于翔宇1,盛晓菲1,周 涛1,于 倩1,李 周1, 2,傅 悦1
(1. 中南大学 材料科学与工程学院,长沙 410083;
2. 中南大学 粉末冶金国家重点实验室,长沙 410083)
摘 要:采用色差测试、电化学测试、静态腐蚀测试、扫描电镜分析、电化学阻抗测试和X射线光电子能谱分析等方法,研究仿金Cu-Zn-Ni-Sn合金在人工海水和人工汗液中的腐蚀行为。合金在人工海水腐蚀初期的腐蚀产物层主要为较为致密的Cu2O和具有良好耐腐蚀性能的ZnO、Zn5(CO3)2(OH)6和 Zn5(OH)8Cl2・H2O等氧化产物,该氧化膜两侧界面的传质过程是腐蚀反应发生的决速步骤。在人工汗液中腐蚀初期的主要腐蚀产物主要为疏松的CuO和不稳定的SnO,使其腐蚀产物膜疏松、易剥落。在人工汗液的腐蚀过程中,早期形成的腐蚀产物层会开裂,而裂纹末端界面的固相扩散决定了腐蚀反应的速率。
关键词:黄铜合金;显微组织;电化学;腐蚀行为
文章编号:1004-0609(2021)-05-1143-13 中图分类号:TG 113;TG146.1 文献标志码:A
引文格式:于翔宇, 盛晓菲, 周 涛, 等. Cu-Zn-Ni-Sn仿金合金在人工海水和人工汗液中的腐蚀行为[J]. 中国有色金属学报, 2021, 31(5): 1143-1155. DOI: 10.11817/j.ysxb.1004.0609.2021-39791
YU Xiang-yu, XIAO Zhu, YU Qian, et al. Corrosion behaviour of Cu-Zn-Ni-Sn imitation-gold copper alloy in artificial seawater and perspiration[J]. The Chinese Journal of Nonferrous Metals, 2021, 31(5): 1143-1155. DOI: 10.11817/j.ysxb.1004.0609.2021-39791
铜合金以其优异的导电、导热、机械加工等性能被广泛应用于电子、化工、机械、建筑、医疗、装饰等不同领域[1]。目前,已有200多种铜合金的结构材料与功能材料广泛应用于各行各业。随着黄铜合金中锌元素含量的增加,合金的颜色逐渐由紫红色、橙黄色、黄色向金色转变[2]。仿金黄铜合金以其瑰丽明艳的色泽与独特的抗菌性能在造币、珠宝、建筑等行业广受青睐[3]。但是由于黄铜合金的脱锌腐蚀和应力开裂,Cu-Zn系仿金合金经常会出现表面变色等腐蚀问题[4]。近些年来,开发的仿金合金大都具有不同金色度,但鲜见兼具良好金色度与耐腐蚀、抗变色性能的仿金铜合金,因此,铜基仿金合金需要进行进一步的探索和研究。
铜合金腐蚀过程中生成的富铜腐蚀产物层在一定程度上能抑制脱锌发生,但在含铵根离子的腐蚀介质中,铜会与之反应生成络合物,破坏腐蚀产物结构[5]。铜合金中镍元素有助于在腐蚀反应中生成NiO、Ni(OH)2从而抑制腐蚀反应的发生[6-7]。在腐蚀过程中,锡元素会以岛状形式析出,因其难溶性沉淀于金属表面以减少金属表面的活性面积,达到抑制腐蚀反应发生的目的[8-9]。CHANG等[10-11]研究指出由于Cu5Zn5Al1Sn合金具有良好的微观组织,可以最大限度地减小微电流和其他局部腐蚀作用,并表示该合金所有的氧化物都有助于提高整体的耐腐蚀性。陈景林等[12]设计了一种新型仿金合金(CuZnAlNiMeRe),通过加入稀土元素显著提高了合金的抗变色性能。肖柱等[13]设计了一种新型仿金合金(CuZnAlNiSnReB),该合金具有较好的抗变色性能,通过对阻抗谱和等效电路分析证实,在盐雾环境中腐蚀一段时间后,该合金表面形成的腐蚀产物膜使合金具有良好的耐蚀性。稀土元素或硼的加入可以提高合金的耐腐蚀性能,抑制黄铜脱锌,但由于稀土元素在铸造、生产过程中的不可控性限制了这两种合金在工业上的应用[12-13]。目前,关于含Ni、Sn的黄铜合金在人工海水和人工汗液中的腐蚀行为研究鲜见报道。
本文设计了一种Cu-Zn-Ni-Sn仿金合金,通过静置腐蚀试验、电化学试验、扫描电镜和X射线光电子能谱分析,比较了该合金中在人工海水和人工汗液腐蚀的行为差异并讨论了各自的腐蚀机理,对设计和应用具有耐腐蚀、抗变色等优良性能的仿金铜合金提供指导。
1 实验
1.1 试样制备
实验原料使用99.9%的纯金属,采用用感应熔炼和铸造法制备所需的Cu-Zn-Ni-Sn合金(以下简称H-NS合金),熔炼温度为1300 ℃,使用覆盖剂保护熔体,待金属全部融化后,浇筑于铁模中。表1列出了合金的名义化学成分。将熔铸好的铸锭铣去表面缺陷后,置于电阻炉1003 K加热1 h,进行均匀化退火,制得均匀化退火样品。将铸锭从厚度35 mm热轧至3 mm,然后冷轧至2 mm。1003 K去应力退火1 h,退火后样品的初始组织金相如图1所示。所有切下的样品都先使用1000号金相砂纸研磨,经90%(体积分数)乙醇脱水后,再用热风干燥。用去离子水和试剂级化学品制备人工海水(3.5% NaCl)和人工汗液(3.5% NaCl(质量分数)和0.5 mol/L NH4Cl)。
表1 实验合金的名义化学成分
Table 1 Chemical compositions of designed alloy (mass fraction, %)

1.2 腐蚀性能表征

图1 1003 K退火后H-NS合金样品金相照片
Fig. 1 Metallograph of initial microstructure of samples annealed at 1003 K.
人工海水和人工汗液的腐蚀试验同时在308 K的HH-8恒温水浴箱中进行。抗变色性能测试使用35 mm×35 mm×2 mm的样品,分别在人工海水和人工汗液中浸泡30 d。测试使用CC-6801精密色差仪测量样品浸没于不同天数的色差变化,该值将用于合金抗变色性能的表征。
H-NS合金浸没于两种腐蚀介质不同天数的色差可以用CIEDE1976标准计算[13-14]:
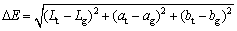 (1)
(1)
式中:L为明度;a和b为色品。a为红绿度,a>0表示色度偏红,a<0表示色度偏绿;b为黄蓝度,b>0表示色度偏黄,b<0表示色度偏蓝;Lg、ag和bg表示通过色差仪所测得的24 K金的标度(Lg=90.36, ag=4.2, bg=36)。
在静置腐蚀试验中,H-NS合金浸泡于人工海水和人工汗液30 d后,根据ASTM-G1计算相应的腐蚀速率(vc):
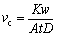 (2)
(2)
式中:K为常数(8.76×104);w为质量损失,g;A为面积,cm2;t为暴露时间,h;D为密度,g/cm3。样品密度采用JL3005SD密度计测定。
试验样品使用铜导线焊接制成工作电极,保留测试面为10 mm×10 mm的正方形,非测试面使用树脂密封。采取标准三电极体系在IM6ex电化学工作站,测量H-NS合金在人工海水和人工汗液腐蚀不同天数的交流阻抗和极化曲线。使用饱和甘汞电极(SCE)作为参比电极,使用铂电极作为辅助电极,电解液分别使用人工海水和人工汗液。所有电化学测试都在开路电位稳定后进行测量。电位动态极化测量电位范围为-0.6~0.4 V,扫描速率为1 mV/s。用CHI660C软件对极化数据进行分析。电化学阻抗谱(EIS)测量交流电位信号为10 mV,频谱在100 kHz到10 mHz之间,在开路电位。利用ZView对EIS数据进行分析。
1.3 微观结构表征
样品在人工海水和人工汗液中后,通过配备能谱仪(EDS)的Nova NanoSEM230扫描电子显微镜(SEM)研究样品的形貌和元素分布。
X射线光电子能谱(XPS)可以描述H-NS样品浸没在人工海水和人工汗中表面生成的腐蚀产物。测试使用了K-Alpha 1063 x射线光电子分光镜和一个真空度为9 mBar的Al-Kα单色光束X射线源的。实验记录了Cu 2p、Zn 2p、Sn 3d和O 1s的高分辨率光电子谱,并用XPSPEAK软件进行分析。
2 实验结果
2.1 抗变色性能
图2所示为H-NS合金在人工海水和人工汗液中腐蚀不同时间的色差变化。经过720 h的腐蚀,在人工海水中合金的色差从16逐渐增长到34,在人工汗液中合金色差增长至26并逐渐稳定。在整个腐蚀过程中,合金在人工海水中的色差始终高于人工汗液,从而可以推断,合金在人工汗液中的抗变色性能优于在人工海水中的抗变色性能。
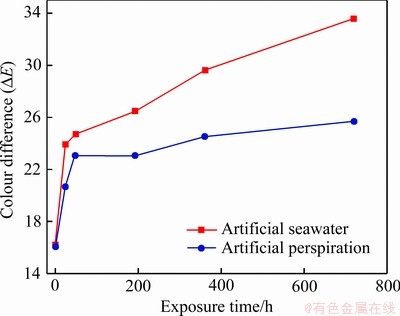
图2 H-Ns合金在人工海水和人工汗液中浸泡不同时间的色差变化
Fig. 2 Variation of colour difference of H-NSl samples exposed in artificial seawater and perspiration for different time
色差与腐蚀时长遵循幂律定律[13]:
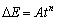
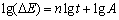 (3)
(3)
式中:常数A和n取决于腐蚀环境和合金成分。
图3所示为色差与腐蚀时间的函数关系。合金在人工海水与人工汗液中的色差变化均较好的拟合于式(3)。在人工海水和人工汗液拟合所得常数n值分别为0.09和0.05,可以看出两种腐蚀介质中,色差与腐蚀时间对数的一次函数人工海水的斜率较大,这意味着合金在人工汗液中有较好的抗变色性能。
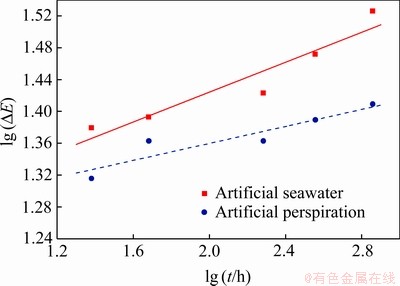
图3 色差与腐蚀时间的函数关系
Fig. 3 Variation of colour difference between gold and designed alloys after exposed in artificial seawater and perspiration for different times
2.2 腐蚀速度测试
为研究H-NS合金在不同腐蚀介质中的腐蚀行为,对合金在两种腐蚀介质中腐蚀不同天数进行动电位极化扫描曲线测试。图4(a)、(b)所示分别为H-NS合金在人工海水和人工汗液中浸泡不同天数实验所得动电位极化扫描曲线。
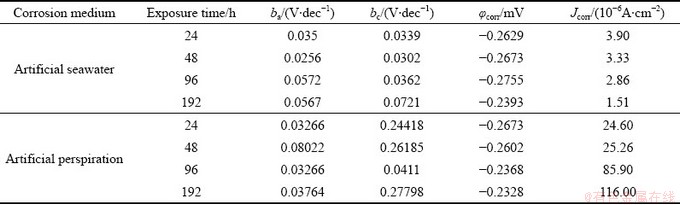
表2所列为H-NS合金在人工海水和人工汗液中腐蚀不同时间的极化曲线拟合参数。表中 Jcorr是腐蚀电流密度,ba和bc分别是阳极和阴极塔菲尔斜率。从表2可以看出,合金在人工海水中的腐蚀电流密度比腐蚀相同时间在人工汗液中测得的腐蚀电流低。且随着腐蚀时间的延长,在人工海水中的腐蚀电流逐渐减少,在人工汗液中的腐蚀电流逐渐增加。这一结果表明合金在人工海水中有较好的耐腐蚀性能。腐蚀720 h后,合金在人工海水和人工汗液中生物平均失重速率分别为0.0176 mm/y和0.1125 mm/y也印证了这一观点。
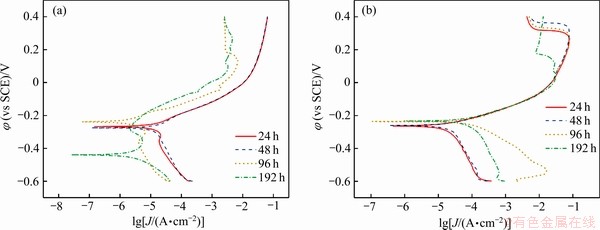
图4 不同腐蚀介质的H-NS合金腐蚀不同时间后的动电位极化曲线
Fig. 4 Polarization curves of H-NS alloy after exposed in artificial seawater(a) and artificial perspiration(b) for different time
表2 在人工海水和人工汗液中腐蚀不同天数的H-NS合金极化曲线拟合参数
Table 2 Electrochemical parameters acquired from polarization curves of H-NS alloys immersed in artificial seawater and perspiration for different time
2.3 腐蚀产物层扫描电镜观察
图5(a)和(c)所示分别为H-NS合金分别在人工海水和人工汗液浸泡1 d后的表面形貌。图5(b)和(d)所示分别为H-NS合金分别在人工海水和人工汗液浸泡四天后侧面的腐蚀形貌。合金在人工海水的腐蚀过程中形成了较为致密的腐蚀产物膜,而在人工汗液的腐蚀过程中,合金表面发生了明显的沿晶腐蚀与剥落[15]。
2.4 腐蚀机理分析
2.4.1 腐蚀产物的X射线能谱分析
采用X射线光电子能谱法测定了H-NS合金在人工海水和人工汗液中腐蚀24 h后腐蚀产物元素在表面的价态。图6所示为样品的宽谱图。腐蚀产物主要元素为Cu、Zn、Ni、Sn和O。图7所示为人工海水和人工汗液中H-NS合金表面腐蚀产物元素化合物含量。在人工海水腐蚀中金属表面主要由铜和锌的氧化物组成,在人工汗液中的金属表面的铜含量与在人工海水中基本不变,锌的氧化物的含量明显下降,而锡的氧化合物的含量明显上升。
2.4.1.1 Cu 2p X射线能谱
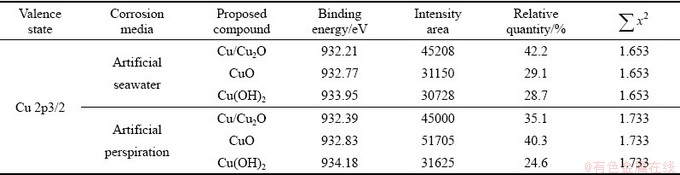
为了解两种腐蚀环境中腐蚀产物种类,对全谱进行了窄谱扫描。图8(a)和(b)分别为H-NS合金放置于人工海水和人工汗液的表面产物的Cu 2p X射线能谱。分峰处理后腐蚀产物主要为Cu/Cu2O、CuO和Cu(OH)2[16]。由图7可知在人工海水中表面腐蚀产物层Cu元素的含量为44.76%, 在人工汗液中表面腐蚀产物层Cu元素的含量为43.05%。由表3铜的化合物的相对含量可计算出人工海水中金属表面CuO的含量明显低于在人工汗液中的含量,Cu2O和Cu(OH)2的含量均高于在人工汗液中的含量。故可以推测在人工海水中铜元素形成的氧化膜比在人工汗液中的氧化膜更加致密。
2.4.1.2 Zn 2pX射线能谱
图9(a)和(b)所示分别为H-NS合金放置于人工海水和人工汗液的表面产物的Zn 2p X射线能谱。分峰处理后腐蚀产物主要为Zn、ZnO、Zn5(CO3)2(OH)6和Zn5(OH)8Cl2・H2O[17]。由图7可知,在人工海水中表面腐蚀产物层Zn元素的含量为47.44%, 在人工汗液中表面腐蚀产物层Zn元素的含量为17.64%。由表4锌的化合物的相对含量可计算出人工海水中金属表面Zn的含量明显低于在人工汗液中的含量,ZnO、Zn5(CO3)2(OH)6和Zn5(OH)8Cl2・H2O的含量均高于在人工汗液中的含量。且在人工汗液中腐蚀产物Zn的化合物的含量显著低于人工海水中的含量,而由文献可知锌的氧化物的积累可以有效抑制黄铜的腐蚀,从而解释了H-NS合金在人工汗液中耐腐蚀性能较差的原因。同时,由于在人工汗液中合金表面没有积累过多的腐蚀产物,从而导致H-NS的色差变化较小也解释了H-NS合金在人工汗液中抗变色性能较好的原因。
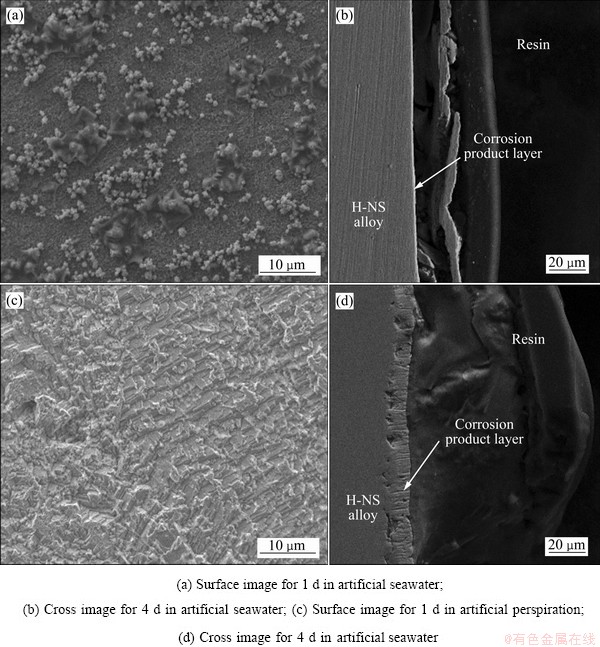
图5 H-NS合金在不同腐蚀介质中腐蚀不同时间的SEM像
Fig. 5 SEM images of samples exposed in different media for different times
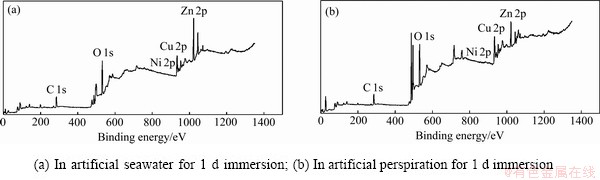
图6 人工海水和人工汗液中H-NS合金表面腐蚀产物层的宽谱图
Fig. 6 Wide spectra of corrosion product layer on surface of CZNS-Al alloy
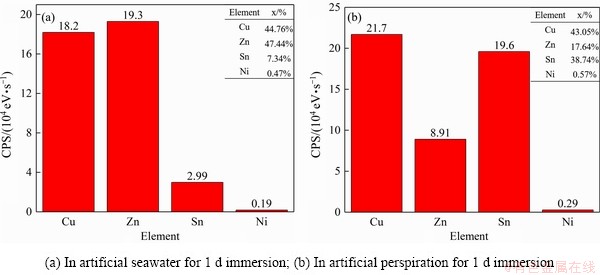
图7 在人工海水和人工汗液中腐蚀1 d后H-NS合金表面腐蚀产物元素化合物含量
Fig. 7 Content of element compounds in surface corrosion products of H-NS alloy in artificial seawater and artificial sweat
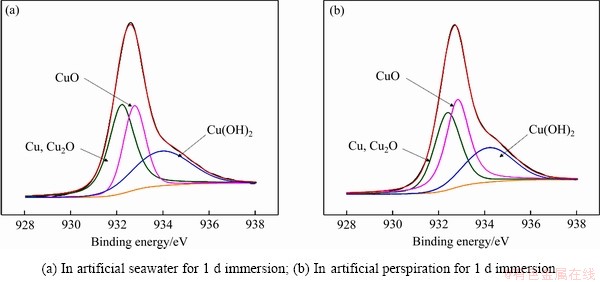
图8 H-NS合金在人工海水和人工汗液中放置1 d后的Cu 2p X射线能谱
Fig. 8 Cu 2p spectra of corrosion product layer on surface of H-NS alloy
表3 H-NS合金在人工海水和人工汗液中腐蚀1 d后含Cu化合物的相对含量
Table 3 Relative quantity of Cu containing compounds in H-NS alloy after being immersed in artificial seawater and artificial perspiration for 1 d
2.4.1.3 Sn 3d X射线能谱
图10(a)和(b)所示分别为H-NS合金放置于人工海水和人工汗液的表面产物的Sn 3d X射线能谱。分峰处理后腐蚀产物主要为Sn、SnO和SnO2[18]。由图7可知,在人工海水中腐蚀产物层的锡化合物的含量为7. 34%,在人工汗液中腐蚀产物层的锡化合物的含量为38.74%。由表5锡的化合物的相对含量可计算出,人工海水中金属表面氧化锡和氧化亚锡的含量明显低于在人工汗液中的含量。表5可知,在人工汗液表面初期大量生成了不稳定的氧化亚锡。
2.4.1.4 Ni 2p3 X射线能谱
图11(a)和(b)所示分别为H-NS合金放置于人工海水和人工汗液中表面产物的Ni 2p3 X射线能谱。分峰处理后腐蚀产物主要为NiO和Ni(OH)2 [19]。由图7和表6可知,在两种腐蚀介质中氧化镍和氢氧化镍的含量基本一致。
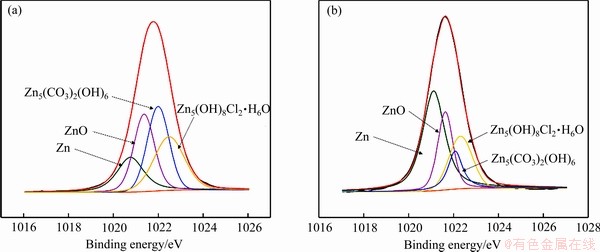
图9 H-NS合金在人工海水和人工汗液中放置1 d后的Zn 2p X射线能谱
Fig. 9 Zn 2p spectra of corrosion product layer on surface of H-NS alloy in artificial seawater(a) and artificial perspiration(b) for 1 d immersion
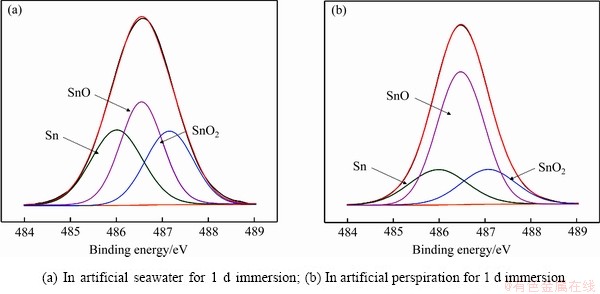
图10 H-NS合金在人工海水和人工汗液中放置1 d后的Sn 3d X射线能谱
Fig. 10 Sn 3d spectra of corrosion product layer on surface of H-NS alloy
表4 H-NS合金在人工海水和人工汗液中腐蚀1 d后含Zn化合物的相对含量
Table 4 Relative quantity of Zn containing compounds in H-NS alloy after being immersed in artificial seawater and artificial perspiration for 1 d
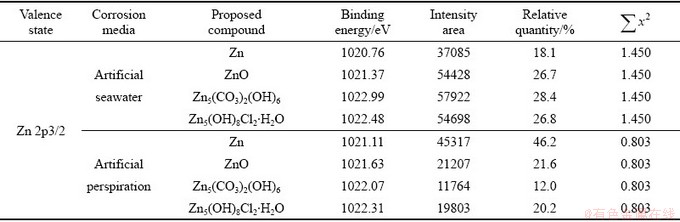
表5 H-NS合金在人工海水和人工汗液中腐蚀1 d后含Sn化合物的相对含量
Table 5 Relative quantity of Sn containing compounds in H-NS alloy after being immersed in artificial seawater and artificial perspiration for 1 d
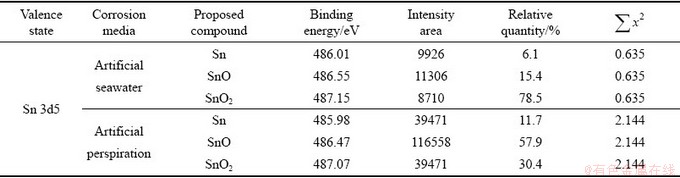
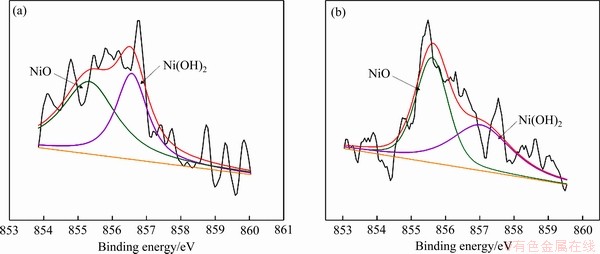
图11 H-NS合金在人工海水和人工汗液中放置1 d后表面产物中Ni 2p3 X射线能谱
Fig. 11 Ni 2p3 spectra of corrosion product layer on surface of H-NS alloy in artificial seawater(a) and artificial perspiration(b) for 1 d immersion
2.4.2 电化学阻抗谱分析
图11所示为H-NS合金在人工海水人工汗液中浸泡1 d和8 d的交流阻抗图谱。在人工海水中,如图12(a)所示H-NS合金的Nyquist图谱在高频部分,随着浸泡时间的延长,半圆弧的半径越来越大,说明随着浸泡时间的延长,阻抗越来越大。从Bode图也可看出(见图12(b)),中频区的 呈现出斜率约为-1的线性关系,这是由于在溶液与电极之间形成了电双层(EDL)[20]。在人工汗液中,如图12(c)所示H-NS合金的Nyquist图谱在高频部分,随着浸泡时间的延长,半圆弧的半径越来越小,说明随腐蚀时间越长,阻抗越小;在低频部分出现45°的线性区域,代表合金的扩散过程[21]。根据扫描电镜观察与XPS分析,结合图12的电化学特征,建立H-NS合金在人工海水和人工汗液中腐蚀的电极反应等效电路如图13所示[20, 22]。
呈现出斜率约为-1的线性关系,这是由于在溶液与电极之间形成了电双层(EDL)[20]。在人工汗液中,如图12(c)所示H-NS合金的Nyquist图谱在高频部分,随着浸泡时间的延长,半圆弧的半径越来越小,说明随腐蚀时间越长,阻抗越小;在低频部分出现45°的线性区域,代表合金的扩散过程[21]。根据扫描电镜观察与XPS分析,结合图12的电化学特征,建立H-NS合金在人工海水和人工汗液中腐蚀的电极反应等效电路如图13所示[20, 22]。
表7所示为H-NS合金浸泡在人工海水中1 d和8 d的交流阻抗谱等效电路参数。随着腐蚀时间的延长,R1值显著提高,R2值有小幅度的升高,这意味着随着腐蚀的进行,在合金表面形成的腐蚀产物逐渐致密[20]。
表8所示为H-Ns合金浸泡在人工汗液中1 d和8 d的交流阻抗谱等效电路参数。随着腐蚀时间的延长,Rl逐渐下降,这代表着合金表面的腐蚀产物膜逐渐破裂,印证了扫描电镜观察到的晶间剥落腐蚀。n1和n2的随着时间的逐渐升高代表着腐蚀产物膜的电容性增加。Rl、Rct和WR的逐渐减少也代表了随着腐蚀时间的增加H-NS的耐腐蚀性能会逐渐下降[23]。
表6 H-NS合金在人工海水和人工汗液中腐蚀1 d后含Ni化合物的相对含量
Table 6 Relative quantity of Ni containing compounds in H-NS alloy after being immersed in artificial seawater and artificial perspiration for 1 d

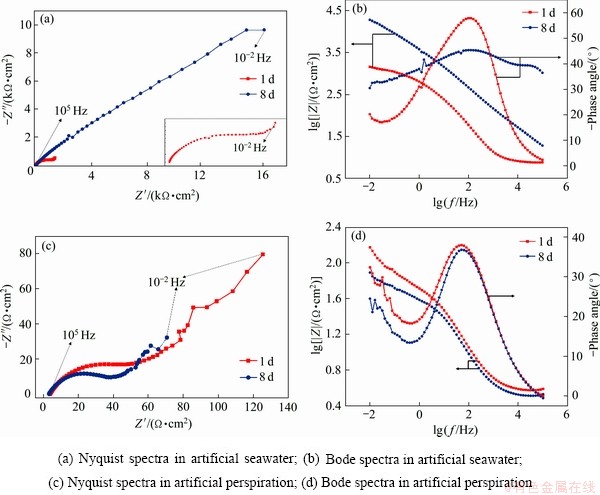
图12 H-NS合金在人工海水和人工汗液中放置1 d和8 d后的Nyquist图和Bode图
Fig. 12 Impedance spectra of H-NS alloy after exposed for different times
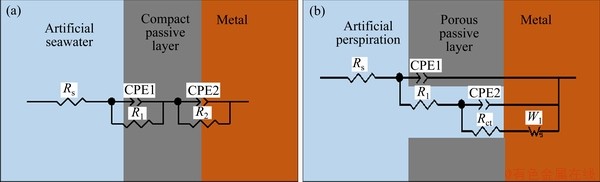
图13 H-NS合金在人工海水和人工汗液中采用的物理模型和相应的等效电路
Fig. 13 Physical models and corresponding equivalent circuits used to fit impedance data of H-NS alloy after being exposed in artificial seawater(a) and artificial perspiration(b) environment
表7 浸泡在人工海水中H-NS合金的交流阻抗谱等效电路参数
Table 7 Elements of equivalent circuit for H-NS alloy after being exposed in artificial seawater for different time

表8 浸泡在人工汗液中H-NS合金的交流阻抗谱等效电路参数
Table 8 Elements of equivalent circuit for H-NS alloy after being exposed in artificial perspiration for different time

3 分析与讨论
该仿金合金在人工海水的腐蚀过程中生成的主要腐蚀产物是较为致密的Cu2O和具有良好耐腐蚀性能的ZnO,Zn5(CO3)2(OH)6和 Zn5(OH)8Cl2・H2O等氧化产物,从而随着腐蚀时间的积累,腐蚀产物层逐渐变厚,抑制腐蚀反应的发生,使合金在具有较好的耐腐蚀作用,但是表面生成的致密的、难溶的氧化产物这也导致合金表面的颜色发生较大变化[24]。在极化曲线测试中,自腐蚀电流代表着金属表面电子转移的难易程度,由于在人工海水中生成了较为致密的腐蚀产物,故在人工海水中自腐蚀电流逐渐减少,电子转移随着腐蚀时间推移变得逐渐困难[25-26]。同时根据EIS分析结果,R1和R2随着时间推移逐渐增大,这代表在腐蚀产物与腐蚀介质界面和金属与腐蚀产物的界面,两个界面的离子交换随腐蚀时间的延长变得困难,这可能是由于合金中氧化亚铜等P型半导体的形成,使得Ni等金属元素很容易加入到这些缺陷中,从而使电子在界面间的转移变得逐渐困难[18]。可以看到,在腐蚀后期R1的值远大于R2,这代表腐蚀后期在腐蚀产物与腐蚀介质界面的传质过程是腐蚀反应的决速步骤。
在人工汗液腐蚀过程中主要腐蚀产物为疏松的CuO和不稳定的SnO,同时发现在合金表面Zn的相对含量远高于在人工海水中的Zn的相对含量,这表明铵根离子加速了对Cu的腐蚀,同时,碱性环境抑制了ZnO,Zn5(CO3)2(OH)6和 Zn5(OH)8Cl2・H2O等氧化产物的生成,从而导致H-NS合金在人工汗液中的耐腐蚀性能较差,但由于合金表面没有过多的氧化产物堆积,故在人工汗液腐蚀后合金金色度较高。在人工汗液中铵根离子的加速腐蚀,在合金表面生成了较为疏松的腐蚀产物,故其极化曲线测试中腐蚀电流逐渐增大,这也意味着腐蚀过程中电子转移逐渐更加容易。在EIS分析中可以看出,由韦伯阻抗产生的WR远大于由Rl和Rct产生的WR。这说明腐蚀反应过程中的扩散过程是反应的决速步骤。
4 结论
1) 仿金H-NS合金在人工海水和人工汗液两种腐蚀介质中,在人工海水中的耐腐蚀性能较好,在人工汗液中的抗变色能力较强。
2) 仿金H-NS合金在人工海水腐蚀初期的腐蚀产物层主要为较为致密的Cu2O和具有良好耐腐蚀性能的ZnO,Zn5(CO3)2(OH)6和 Zn5(OH)8Cl2・H2O等氧化产物,不溶性的腐蚀产物堆积在合金表面减少了活性面积,抑制了反应的进行。在人工汗液中腐蚀初期的主要腐蚀产物主要为疏松的CuO和不稳定的SnO,且Cu对铵根离子十分敏感,易生成疏松的络合物,从而导致腐蚀产物的剥落,加速了腐蚀进程。
3) 在人工海水的腐蚀过程中腐蚀产物会逐渐致密,腐蚀产物层的电容性下降,使合金耐腐蚀性能逐渐提高,该氧化膜两侧界面的传质过程是腐蚀反应发生的决速步骤。在人工汗液的腐蚀过程中,腐蚀产物层不断破裂、溶解、剥离,从而导致合金的耐腐蚀性能下降,而裂纹末端界面的固相扩散决定了腐蚀反应的速率。
REFERENCES
[1] 李 周, 肖 柱, 姜雁斌, 等. 高强导电铜合金的成分设计、相变与制备[J]. 中国有色金属学报, 2019, 29(9): 2009-2049.
LI Zhou, XIAO Zhu, JIANG Yan-bin, et al. Composition design, phase transition and fabrication of copper alloys with high strength and electrical conductivity[J]. The Chinese Journal of Nonferrous Metals, 2019, 29(9): 2009-2049.
[2] 柳 泉, 赵宏达, 刘 革, 等. 装饰用铜锌仿金合金的研究进展[J]. 中国资源综合利用, 2018, 36(11): 123-125.
LIU Quan, ZHAO Hong-da, LIU Ge, et al. Research progress on decorative copper-zinc imitation gold alloy[J]. China Resources Comprehensive Utilization, 2018, 36(11): 123-125.
[3] 唐多光, 周自强, 葛建生, 等. 抗变色仿金合金的研究[J]. 金属科学与工艺, 1991, 10(1): 77-82.
TANG Duo-guang, ZHOU Zi-qiang, GE Jian-sheng, et al. A study of the colour-stable alloy imitating gold[J]. Metal Science & Technology, 1991, 10(1): 77-82.
[4] HOSSEINPOUR S, FORSLUND M, JOHNSON C M, et al. Atmospheric corrosion of Cu, Zn, and Cu-Zn alloys protected by self-assembled monolayers of alkanethiols[J]. Surface Science, 2016, 648: 170-176.
[5] 王吉会, 姜晓霞, 李诗卓. 铜合金在3.5%NaCl+NH3(NH4+)溶液中的腐蚀磨损行为[J]. 金属学报, 1997, 33(12): 1268-1274.
WANG Ji-hui, JIANG Xiao-xia, LI Shi-zhuo. Corrosive wear behaviour of copper alloys in 3.5% NaCl+NH3(NH4+) solution[J]. Acta Metaliurgica Sinica, 1997, 33(12): 1268-1274.
[6] EKERENAM O O, MA A, ZHENG Y, et al. Electrochemical behavior of three 90Cu-10Ni tubes from different manufacturers after immersion in 3.5% NaCl solution[J]. Journal of Materials Engineering and Performance, 2017, 26: 1701-1716.
[7] YUAN S J, PEHKONEN S O. Surface characterization and corrosion behavior of 70/30 Cu-Ni alloy in pristine and sulfide-containing simulated seawater[J]. Corrosion Science, 2007, 49: 1276-1304.
[8] HUTCHISON M J, SCULLY J R. Patina enrichment with SnO2 and its effect on soluble Cu cation release and passivity of high-purity Cu-Sn bronze in artificial perspiration[J]. Electrochimica Acta, 2018, 283: 806-817.
[9] HUTCHISON M J, ZHOU P, OGLE K, et al. Enhanced electrochemical Cu release from commercial Cu-Sn alloys: Fate of the alloying elements in artificial perspiration[J]. Electrochimica Acta, 2017, 241: 73-88.
[10] CHANG T R, HERTING G, JIN Y, et al. The golden alloy Cu5Zn5Al1Sn: Patina evolution in chloride-containing atmospheres[J]. Corrosion Science, 2018, 133: 190-203.
[11] CHANG T R, WALLINDER I O, JIN Y, et al. The golden alloy Cu-5Zn-5Al-1Sn: A multi-analytical surface characterization[J]. Corrosion Science, 2018, 131: 94-103.
[12] CHEN J L, LI Z, ZHU A Y, et al. Corrosion behavior of novel imitation-gold copper alloy with rare earth in 3.5% NaCl solution[J]. Materials & Design, 2012, 34: 618-623.
[13] XIAO Z, LI Z, ZHU A, et al. Surface characterization and corrosion behavior of a novel gold-imitation copper alloy with high tarnish resistance in salt spray environment[J]. Corrosion Science, 2013, 76: 42-51.
[14] 汤泽军. 应用于色差计的两种典型色差公式的对比[J]. 长沙航空职业技术学院学报, 2015, 15(20): 52-55.
TANG Ze-jun. Comparison of two typical color difference formulas for color difference meter[J]. Journal of Changsha Aeronautical Vocational and Technical College, 2015, 15(20): 52-55
[15] GASSA L M, VILCHE J R. Electrochemical study of the corrosion fatigue of copper and alpha brass in ammoniacal copper sulphate solutions[J]. Corrosion Science, 1985, 25(2): 145-157.
[16] COLIN S, BECHE E, BERJOAN R, et al. An XPS and AES study of the free corrosion of Cu-, Ni- and Zn-based alloys in synthetic sweat[J]. Corrosion Science, 1999, 41(6): 1051-1065.
[17] LEE J W, PARK B R, OH S Y, et al. Mechanistic study on the cut-edge corrosion behaviors of Zn-Al-Mg alloy coated steel sheets in chloride containing environments[J]. Corrosion Science, 2019, 160.
[18] ZHANG Y, XIAO Z, ZHAO Y, et al. Effect of thermo-mechanical treatments on corrosion behavior of Cu-15Ni-8Sn alloy in 3.5wt% NaCl solution[J]. Materials Chemistry and Physics, 2017, 199: 54-66.
[19] LUO Q, QIN Z, WU Z, et al. The corrosion behavior of Ni-Cu gradient layer on the nickel aluminum-bronze (NAB) alloy[J]. Corrosion Science, 2018, 138: 8-19.
[20] ZHANG X, PEHKONEN S O, KOCHERGINSKY N, et al. Copper corrosion in mildly alkaline water with the disinfectant monochloramine[J]. Corrosion Science, 2002, 44(11): 2507-2528.
[21] AYAGOU D M D, TRAN T T M, TRIBOLLET B, et al. Electrochemical impedance spectroscopy of iron corrosion in H2S solutions[J]. Electrochimica Acta, 2018, 282: 775-783.
[22] WANG B, XU L, LIU G , et al. Corrosion behavior and mechanism of 3Cr steel in CO2 environment with various Ca2+ concentration[J]. Corrosion Science, 2018, 136: 210-220.
[23] PENG S, XIE S K, XIAO F, et al. Corrosion behavior of spangle on a batch hot-dip galvanized Zn-0.05Al-0.2Sb coating in 3.5 wt.% NaCl solution[J]. Corrosion Science, 2020, 163: 108237.
[24] ZHANG X, LIU X, ODNEVALL WALLINDER I, et al. The protective role of hydrozincite during initial corrosion of a Cu40Zn alloy in chloride-containing laboratory atmosphere[J]. Corrosion Science, 2016, 103: 20-29.
[25] TASIC Z Z, PETROVIC MIHAJLOVIC M B, RADOVANOVIC M B, et al. Cephradine as corrosion inhibitor for copper in 0.9% NaCl solution[J]. Journal of Molecular Structure, 2018, 1159: 46-54.
[26] KONG D, DONG C, NI X, et al. Insight into the mechanism of alloying elements (Sn, Be) effect on copper corrosion during long-term degradation in harsh marine environment[J]. Applied Surface Science, 2018, 455: 543-553.
Corrosion behaviour of Cu-Zn-Ni-Sn imitation-gold copper alloy in artificial seawater and perspiration
YU Xiang-yu1, SHENG Xiao-fei1, ZHOU Tao1, YU Qian1, LI Zhou1, 2, FU Yue1
(1. School of Materials Science and Engineering, Central South University, Changsha 410083, China;
2. State Key Laboratory for Powder Metallurgy, Central South University, Changsha 410083, China)
Abstract: The corrosion behaviours of imitate-gold Cu-Zn-Ni-Sn alloys in artificial seawater and perspiration were investigated by means of colour difference test, static corrosion measurement, scanning electron microscopy analysis, electrochemical impedance measurement and X-ray photoelectron spectroscopy analysis. The corrosion product layer of the alloy in the early stage of artificial seawater corrosion is mainly composed of relatively dense Cu2O and some oxidation products with good corrosion resistance, such as ZnO, Zn5(CO3)2(OH)6 and Zn5(OH)8Cl2・H2O. The mass transfer at the interface on both sides of the oxide film is the rate-determining step of corrosion reaction. The main corrosion products at the initial stage of corrosion in artificial sweat are mainly loose CuO and unstable SnO, which made the corrosion product film loose and easy to peel off. In the corrosion process of artificial perspiration, the corrosion product layer forms in the early stage will crack, and the solid phase diffusion at the crack end interface determined the rate of the corrosion reaction.
Key words: brass alloy; microstructure; electrochemistry; corrosion behaviour
Foundation item: Project(51601227) supported by the National Natural Science Foundation of China; Project (2018JJ3650) supported by the Natural Science Foundation of Hunan Province, China
Received date: 2020-07-10; Accepted date: 2020-11-06
Corresponding author: LI Zhou; Tel: +86-731-88830264; E-mail: lizhou6931@163.com
(编辑 龙怀中)
基金项目:国家自然科学基金资助项目(51601227);湖南省自然科学基金资助项目(2018JJ3650)
收稿日期:2020-07-10;修订日期:2020-11-06
通信作者:李 周,教授,博士;电话:0731-88830264;E-mail:lizhou6931@163.com