文章编号:1004-0609(2012)09-2667-09
耐铅产絮克雷伯氏菌胞外聚合物EPS-07
吸附水中Pb(Ⅱ)的特性
信 欣,姚 力,崔钶,叶芝祥,羊依金,余 静
(成都信息工程学院 资源环境学院,成都 610225)
摘 要:研究抗铅产絮菌株B-07胞外聚合物EPS-07作为吸附剂处理含Pb(Ⅱ)的废水的吸附性能。结果表明:当吸附时间为80 min,pH为5.5,吸附剂用量为0.8 g/L,溶液中Pb(Ⅱ)初始浓度为50 mg/L时,EPS-07对铅离子的吸附平衡容量为61.5 mg/g。吸附等温式能较好地用Langmuir模型表达,吸附动力学很好地符合准二级动力学模型。FT-IR结果表明,EPS-07与Pb(Ⅱ)的作用过程中,主要是羟基、羧基等基团参与了吸附作用。SEM观察显示EPS-07表面结构比较松散,EPS-07与Pb(Ⅱ)作用后, 其表面变得致密并有结晶沉淀物出现。EDS图出现了Pb元素峰,表明 Pb(Ⅱ)被吸附到EPS-07上面。
关键词:生物吸附;克雷伯氏菌;胞外聚合物;Pb(Ⅱ)
中图分类号:X703 文献标志码:A
Sorption characteristics of Pb(Ⅱ) from aqueous solution by
extracellular polymeric substance (EPS-07) of lead-resistant and
producing flocculant strain Klebsiella pneumonia
XIN Xin, YAO Li, CUI Ke, YE Zhi-xiang, YANG Yi-jin, YU Jing
(College of Resource and Environment, Chengdu University of Information Technology, Chengdu 610225, China)
Abstract: The biosorption characteristics of extracellular polymeric substance (EPS-07) of producing flocculant strain B-07 as lead-resistant for the removal of Pb(Ⅱ) from aqueous solution were studied. The results show that the extent of adsorption capacity is 61.5 mg/g when the dosage of EPS-07 is 0.8 g/L, pH=5.5, adsorption contact time is 80 min, initial Pb(Ⅱ) concentration of aqueous solution is 50 mg/L, respectively. The biosorption equilibrium data are better described by Langmuir isotherm model, and the adsorption reaction of Pb(Ⅱ) by EPS-07 follows the second-order kinetic model. The carboxy, hydroxyl groups of EPS-07 are involved in chemical interaction with the Pb(Ⅱ) ions depicted by Fourier transform infrared spectroscopic (FT-IR) results. Moreover, SEM observation indicates that the EPS-07 surface is loose, and then obviously changes to campact after the EPS-07 surface loaded with with Pb(Ⅱ), where cry stalline deposits are deposited on the EPS-07 surface. Also, biosorption of Pb(Ⅱ) is confirmed by EDS analysis, which reveales the presence of Pb(Ⅱ) signals on the EPS-07 surface.
Key words: biosorption; Klebsiella pneumonia; extracellular polymeric substance; Pb(Ⅱ)
当前,由于矿山开采以及冶炼、电镀、纺织、印染、汽车加工制造等行业废水的排放,导致某些地区环境水体重金属严重污染的现象[1-2],传统的处理重金属污染的方法包括化学沉淀、离子交换、吸附法等[3-5],但是它们在处理低浓度时(<100 mg/L)重金属废水时效率低。而生物吸附法可以克服传统方法的弊端,并且生物吸附剂具有来源广、去除效率高、在环境中易于降解无毒等优点,在处理低浓度重金属废水的方法
基金项目:生物地质与环境地质国家重点实验室(BGEG1009);四川省教育厅青年基金资助项目(08zb057)
收稿日期:2011-08-19;修订日期:2011-10-30
通信作者:信 欣,副教授,博士;电话:13568807972;E-mail: xx@cuit.edu.cn
中,应用前景广阔[6-7]。生物胞外聚合物(Extracelluar polymeric substances,EPS) 是一种新型的生物吸附剂,其主要成分包括蛋白质、多聚糖、核酸和脂类等,含有带负电荷的功能基团(如羧基、羟基、氨基等),对不同类型金属离子表现出强烈的亲和性[8]。
国外一些研究表明,EPS可与重金属离子相互作用而达到很好的吸附效果[9-15]。而国内关于EPS对重金的吸附性能研究起步较晚,主要集中在天然水中细菌胞外聚合物[16-17]、硫酸盐还原菌混合菌群胞外聚合物[18]、活性污泥[19-20]、某些细菌和真菌胞外分泌 物[21-23]。不同类型微生物的EPS成分有很大差异,导致其与重金属的相互作用机制亦存在不同。目前国内鲜有耐铅产絮菌株胞外聚合物与重金属废水之间相互关系的研究报道。
因此,本文作者针对课题组筛选的耐铅产絮菌株B-07,采用乙醇提取法提取其胞外聚合物EPS-07,探索其吸附Pb(Ⅱ)的特性和主要影响因素。同时,通过对EPS-07的SEM-EDS、FT-IR分析, 解释EPS-07去除Pb(Ⅱ)的过程机理,为生物吸附法处理低浓度Pb(Ⅱ)废水的应用提供实验依据。
1 材料与方法
1.1 吸附剂的制备
从成都受铅镉污染的土壤中分离出一株产絮抗性菌株克雷伯氏菌(Klebsiella pneumoniae)B-07。其发酵产絮培养基:葡萄糖12 g,酵母膏1 g,NaCl 0.2 g,MgSO4 0.2 g,K2HPO4 1.0 g,KH2PO4 0.5 g,CaCl2 0.1 g,蒸馏水1 L,pH为6.8~7.3。将产絮菌株B-07活化18 h后,按照体积接种比1:100的比例接种到发酵产絮培养基中,在30 ℃、160 r/min条件下培养72 h。经10k r/min离心10 min后取出上清液,与预冷过的无水乙醇按照体积比1:2混匀,混匀后放置在4 ℃ 冰箱里冷却6 h,再次10k r/min离心5 min,用75%的乙醇多次洗涤离心后的沉淀物,在80 ℃ 的烘箱里进行干燥,即可得到胞外聚合物EPS-07,作为本实验的生物吸附剂。
1.2 含Pb(Ⅱ)溶液
将充分烘干的分析纯Pb(NO3)2与去离子水配制成Pb(Ⅱ)浓度为1 000 mg/L模拟含铅废水储备液,实验时根据需要稀释制得实验水样。
1.3 EPS-07对水体中的Pb(Ⅱ)的吸附实验
采用静态吸附的方法研究吸附剂EPS-07对Pb(Ⅱ)的吸附效果。考察不同的吸附时间、pH值和吸附剂投加量对EPS-07吸附水体中Pb(Ⅱ)的影响。每组实验吸附完成后,将EPS-07取出,静置10 min,过滤,利用原子吸收分光光度计测定吸附前后溶液的Pb(Ⅱ)浓度,计算EPS-07对Pb(Ⅱ)的吸附量。计算吸附剂的吸附量计算公式如下:
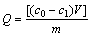 (1)
(1)
式中:Q为一定时间内,EPS-07对废水中Pb(Ⅱ)的吸附量,mg/g;c0为Pb(Ⅱ)的初始浓度,mg/L;c1为吸附后溶液中的Pb(Ⅱ)浓度,mg/L;V为含Pb(Ⅱ)的废水体积,L;m为EPS-07的投加量,g/L。
1.4 吸附等温线
取不同初始浓度的Pb(Ⅱ)模拟废水各100 mL,调节pH=5.5值,分别加入0.08 g的吸附剂EPS-07,在一定温度 (30 ℃)、转速为160 r/min的条件下振荡至吸附平衡;吸附实验完成后,用滤纸过滤瓶中溶液,利用原子吸收分光光度计测定滤液中Pb(Ⅱ)的剩余浓度。利用下式[24]计算平衡吸附量Qe:
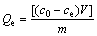 (2)
(2)
式中:Qe为平衡时间时,EPS-07对废水中Pb(Ⅱ)的吸附量,mg/g;c0为Pb(Ⅱ)的初始浓度,mg/L;ce为吸附平衡时溶液中的Pb(Ⅱ)浓度,mg/L;V为含Pb(Ⅱ)的废水体积,L;m为EPS-07的投加量,g/L。
描述吸附平衡过程时常用的模型有Langmuir等温模型(3)和Freundlich等温模型(4)。
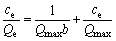 (3)
(3)
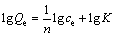 (4)
(4)
式中:ce为吸附平衡时溶液中吸附质的质量浓度,mg/L;Qmax为Langmuir饱和吸附量,mg/g;Qe为平衡吸附量,mg/g;B为与吸附能有关的Langmuir常数;K为Freundlich吸附等温式常数。
1.5 吸附动力学
吸附动力学主要是用来描述吸附剂吸附溶质的速率,吸附速率控制了在固-液界面上吸附质的滞留时间。常用的动力学模型有Lagergren准一级动力学模型(5)和Mckay准二级动力学模型(6)。
 (5)
(5)
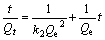 (6)
(6)
式中:Qe为平衡吸附量,mg/g;Qt为t时间的吸附量,mg/g;k1为一级反应速率常数,min-1。k2为二级反应速率常数,min-1。t为吸附时间,min。
1.6 红外、SEM-EDS能谱分析
分别取1mg吸附Pb(Ⅱ)前后的EPS-07样品,与200 mg纯KBr研细混匀,置于模具中,保持干燥,压片,然后通过Thermo spectrometer IR200型红外光谱仪测定红外吸收光谱图;分别取少量的胞外聚合物EPS-07吸附Pb(Ⅱ)前后的样品进行干燥处理,然后将样品用导电胶粘在样品台上,放置能谱仪中进行观察。
2 结果与讨论
2.1 时间对EPS-07吸附Pb(Ⅱ)的影响
吸附剂EPS-07对Pb(Ⅱ)浓度为30、50和70 mg/L的废水中Pb(Ⅱ) 的吸附效果随时间的变化如图1所示。由图1可看出,随着吸附时间的延长,EPS-07对3种废水中Pb(Ⅱ)的吸附量均趋于增大;当吸附时间由20 min增加到80 min时,EPS-07的Pb(Ⅱ)吸附量迅速上升,并且在80 min时,对Pb(Ⅱ)浓度为30、50和70 mg/L的废水中Pb(Ⅱ)的吸附量分别为56.0、61.5

图1 时间对EPS-07吸附Pb(Ⅱ)的影响
Fig. 1 Effect of time on Pb(Ⅱ) adsorption by EPS-07 (Dosage of EPS 0.8 g/L, 30 ℃, pH=5.5, and 160 r/min)
和62.4 mg/g;随着吸附时间继续延长,Pb(Ⅱ)吸附量不再发生明显变化。其原因在于:胞外聚合物是一种非活性体,它对金属离子的吸附主要通过络合、螯合、离子交换等物理-化学作用,官能团通过这种方式同重金属结合不需要耗费大量的能量,反应进行得很快[20]。有一些报道表明,金属离子的生物吸附是一个快速吸附过程。郑蕾[20]在研究3种不同的EPS对Cd2+和Zn2+的吸附时,发现在0~30 min 内的吸附量增加很快,并于60 min 时达到吸附平衡;康春莉[8]在研究胞外多糖和胞外蛋白质对镉的吸附时,发现在前30 min 内的吸附量增加很快。熊芬等[22]研究烟曲霉EPS对Pb2+的吸附时,发现在0~30 min内的吸附量增加很快,而在30~120 min内的吸附量则缓慢上升,在120 min时达到最大吸附量,在180 min时达到吸附平衡。本实验中,吸附剂EPS-07对废水中Pb(Ⅱ)的吸附仍然属于快速吸附,在80 min时达到吸附平衡。
2.2 初始pH值对EPS-07吸附Pb(Ⅱ)的影响
pH值是影响胞外聚合物吸附Pb(Ⅱ)的重要因素之一[25]。pH值对吸附剂EPS-07吸附Pb(Ⅱ)的影响如图2所示。从图2可以看到,在实验范围内,EPS-07对3种废水中Pb(Ⅱ)的吸附规律基本相同。当pH值为2.5时,EPS-07对Pb(Ⅱ)浓度为30、50和70 mg/L的废水中Pb(Ⅱ) 的吸附量最低,分别为29.6、35.8和39.8 mg/g;随着pH值的升高,EPS-07的Pb(Ⅱ)吸附量升高,当pH=5.5时,EPS-07对3种废水中Pb(Ⅱ)的吸附量达到最大,分别为55.8、61.3和63.0 mg/g。这主要是因为EPS-07含有大量羧基、羟基等活性官能团,pH值过低时,溶液中的H+会占据大量这样的活性吸附点位[26],阻止阳离子与吸附活性点之间的接触,H+与被吸附阳

图2 pH值对EPS-07吸附Pb(Ⅱ)的影响
Fig. 2 Effect of pH value on Pb(Ⅱ) adsorption by EPS-07 (Dosage of EPS 0.8 g /L, 30 ℃ and 160 r/min for 80 min)
离子之间的竞争吸附作用导致吸附效果不佳;随着pH值的增加,细胞表面官能团逐渐脱质子化,EPS-07表面暴露的吸附基团增多,金属阳离子与活性电位结合量随之增加;然而,当溶液pH继续增加时,溶液中OH-与Pb(Ⅱ)形成羟基配合物的几率也随之增加,从而削弱胞外聚合物对金属离子的吸附。本实验中,当pH值大于5.5时,投加EPS-07之前废水中就开始出现少量沉淀,导致EPS-07对Pb(Ⅱ)的吸附量下降。因此,本实验中,吸附剂EPS-07吸附水体中Pb(Ⅱ)的最佳pH值为5.5。
2.3 EPS-07投加量对吸附效果的影响
吸附剂EPS-07的投加量对吸附水体中的Pb(Ⅱ)的影响很大。投加量对EPS-07吸附Pb(Ⅱ)的影响如图3所示。从图3可以看到,EPS-07投加量从0.2 g/L增加到0.8 g/L时,对3种废水中Pb(Ⅱ)的吸附量均明显上升,吸附效果明显。原因在于EPS-07投加量的增加带来吸附位点的增多,导致Pb(Ⅱ)吸附量随之增加。当EPS-07投加量为0.8 g/L时,EPS-07对Pb(Ⅱ)浓度为30、50和70 mg/L的废水中Pb(Ⅱ)的吸附量均达到最大,分别为56.1、61.5和63.0 mg/g;继续增加EPS-07投加量时,EPS-07对Pb(Ⅱ)的吸附量呈递减趋势。其原因可能在于EPS-07投加量过大时其未饱和吸附位点也过多,会引起EPS-07自凝聚而导致其吸附有效面积减少。因此,虽然EPS-07投加量过大时,废水中Pb(Ⅱ)被吸附的总量会增加,但单位质量吸附剂的Pb(Ⅱ)吸附量反而减少。本实验中,EPS-07的最佳投加量为0.8 g/L。

图3 EPS-07投加量对吸附Pb(Ⅱ)的影响
Fig. 3 Effects of EPS-07 dosage on Pb(Ⅱ) adsorption (30 ℃, pH=5.5 and 160 r/min for 80 min)
2.4 吸附等温式
吸附等温线是指在一定温度下金属离子在两相界面上进行的吸附过程达到平衡时,它们在两相中浓度之间的关系曲线。Langmuir模型主要用于研究最大单分子层吸附量,Freundlich模型通常能较好地描述水溶液中的吸附过程。当溶液中Pb(Ⅱ)的初始浓度为10、20、30、40、50、60、70、80、90和100 mg/L时,EPS-07吸附水中Pb(Ⅱ)的吸附等温曲线如图4所示。由图4 可知,随着溶液中Pb(Ⅱ)浓度的增大, 吸附剂EPS-07的平衡吸附量也随之增大,并逐渐趋于饱和,但平衡吸附量增大的幅度随Pb(Ⅱ)浓度的不断增加而逐渐减弱;当Pb(Ⅱ)的初始浓度大于50 mg/L时,平衡吸附量趋于稳定。
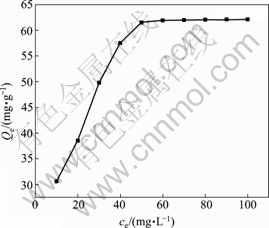
图4 Pb(Ⅱ)初始浓度对EPS-07吸附Pb(Ⅱ)的影响
Fig. 4 Effect of initial Pb(Ⅱ) concentration on Pb(Ⅱ) adsorption by EPS-07 (Dosage of EPS 0.8 g/L, 30 ℃, pH=5.5 and 160 r/min for 80 min)
分别采用Langmuir 等温线模型和Freundlich等温线模型对各实验值进行拟合, 结果如图5、图6和表1所示。Langmuir和Freundlich吸附等温线相关系 数R2分别为0.997和0.859,Langmuir吸附等温线相关系数明显优于Freundlich吸附等温线相关系数。这说明Langmuir模型能更好地拟合吸附剂EPS-07对Pb(Ⅱ)的吸附,Pb(Ⅱ)在胞外聚合物表面的吸附主要以单分子层吸附为主。
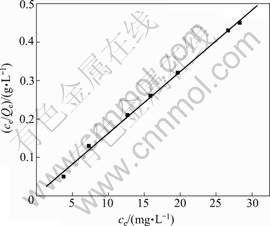
图5 Langmuir吸附等温式
Fig. 5 Langmuir absorption isotherm
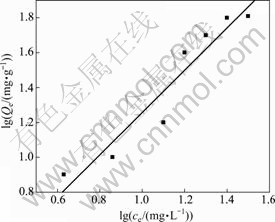
图6 Freundlich 吸附等温式
Fig. 6 Freundlich absorption isotherm
表1 吸附等温式
Table 1 Adsorption isotherm equations

经计算得出胞外聚合物EPS-07对Pb(Ⅱ)的最大吸附容量Qmax为62.5 mg/g。而且另一个重要的吸附平衡参数RL可由式(7)[27]计算得到。
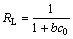 (7)
(7)
式中:b为Langmuir常数;c0为吸附前溶液中Pb(Ⅱ)的最大浓度值,mg/L。RL是无因次参数,当RL>1时,表示吸附不可进行;当0<RL< l时,表示吸附比较容易进行;当RL = 0时,表示吸附是不可逆的。本实验中,吸附剂EPS-07对溶液中Pb(Ⅱ)吸附的RL小于l,说明它对Pb(II)的吸附比较容易进行。
2.5 吸附动力学
吸附剂EPS-07对3种废水中Pb(Ⅱ)的吸附过程分别用准一级和二级动力学模型来拟合,拟合结果见图7和8。由图7和8可知,准二级反应模型的线性相关系数在0.996以上,均优于Lagergren一级反应模型,并且将二级拟合方程计算所得理论平衡吸附量Qcal与实验所得吸附平衡容量Qe相比较可知,实验所得吸附平衡容量Qe更加接近于由准二级反应速率方程计算出来的理论平衡吸附量Qcal(见表2)。因此,EPS-07吸附Pb(Ⅱ)的动力学可近似用二级模型来描述。

图7 准一级动力学模型
Fig. 7 Pseudo first-order plots
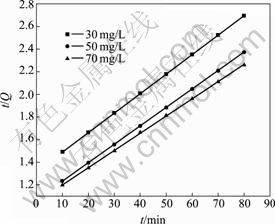
图8 准二级动力学模型
Fig. 8 Pseudo second-order plots
2.6 FT-IR分析
图9所示为吸附剂EPS-07吸附Pb(Ⅱ)前后的红外光谱。由图9谱线a可见,3 400 cm-1处为一较宽的吸收峰,可以判断是由于―OH伸缩振动所致;2 926 cm-1处的吸附峰可能为C―H 不对称伸缩振动所致结果,此区域的吸收峰是糖类的典型特征峰;1 647 cm-1处的吸收峰是由于多糖中的乙酰氨基的C=O键伸缩振动造成;1 391 cm-1处的吸收峰为―COOH振动的结果;1 080 cm-1处的吸收峰是糖环中的C―O伸缩振动的结果。由此可以推断,抗铅产絮菌株胞外分泌物EPS-07的主要成分为多糖,主要含有酰胺基,羧基,羟基等基团。当EPS-07吸附Pb(Ⅱ)后,其红外光谱发生了一些变化(见图9谱线 b)。原来3 400 cm-1处的―OH峰发生了微小偏移,移至3 382 cm-1处,这或许是因为Pb(Ⅱ)与EPS-07的―OH发生络合配位的结果;2 926、1 647和1 391 cm-1处的吸收峰的强度明显减弱,这主要是因为Pb(Ⅱ)与EPS-07的静电吸引和Pb(Ⅱ)与吸附剂中的C=O、―COOH化学吸附作用。1 080 cm-1处的吸收峰不仅强度出现明显的减弱,而且也发生了偏移,可能是EPS-07中的C―O参与了吸附活动。
表2 动力学模型参数
Table 2 Values of parameter of kinetic models
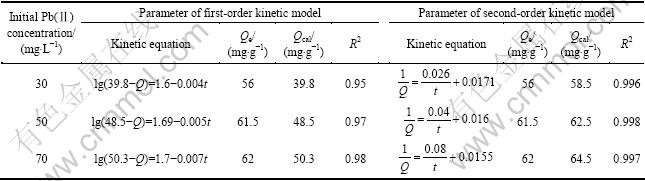
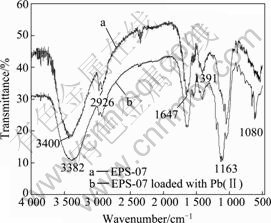
图9 EPS-07吸附Pb(Ⅱ)前后的红外光谱
Fig. 9 FT-IR spectra of EPS-07 before adsorption(a) and after adsorption(b) of Pb(Ⅱ)
综上所述,胞外聚合物EPS-07主要含有羟基、酰胺、羰基等活性基团,在EPS-07与Pb(Ⅱ)的作用过程中, 起主要作用的是多聚糖中的羟基、羧基、C―O和C=O等基团。
2.7 SEM-EDS分析
采用SEM-EDS技术对胞外聚合物EPS-07吸附Pb(Ⅱ)前后进行了表征和元素半定量分析, 结果如图10所示。由图10(a)可见,SEM显示EPS-07表面结构比较松散,而EDS显示除了C、H、O 之外, K、Na 、Mg、Ca、S和P 是EPS-07的主要元素。由图10(b)可见,EPS-07与Pb(Ⅱ)作用后,EPS-07表面变得致密,并有结晶沉淀物出现,EDS显示在2.31 keV 处出现了Pb峰,这说明了Pb(Ⅱ)被吸附到EPS-07上。
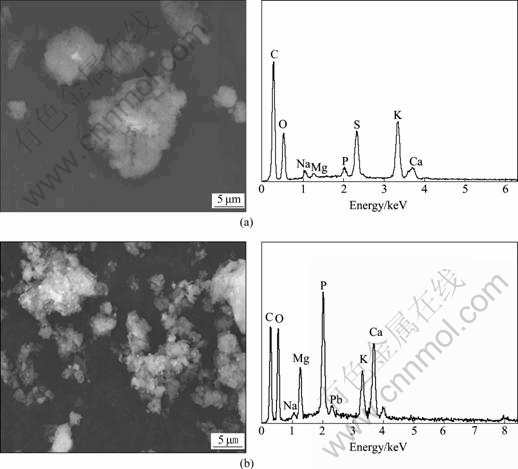
图10 EPS-07吸附Pb(Ⅱ)前后的SEM像和EDS谱
Fig. 10 SEM images and EDS patterns of EPS-07 before(a) and after(b) adsorption of Pb(Ⅱ)
3 结论
1) 以抗铅产絮菌株B-07的胞外聚合物EPS-07作为吸附剂处理含Pb(Ⅱ)的废水;当吸附时间为80 min,pH为5.5,吸附剂用量为0.8 g/L,废水中Pb(Ⅱ)浓度为50 mg/L时,EPS-07对Pb(Ⅱ)的吸附平衡容量为61.5 mg/g。
2) Langmuir模型能更好地拟合胞外聚合物EPS-07对Pb(Ⅱ)的吸附,Pb(Ⅱ)在胞外聚合物表面的吸附主要以单分子层吸附为主。并且,EPS-07对溶液中Pb(Ⅱ)吸附的RL小于l,说明它对Pb(Ⅱ)的吸附比较容易进行。
3) 准二级动力学模型能很好地描述胞外聚合物EPS-07对废水中Pb(Ⅱ)的吸附动力学行为。EPS-07对3种不同Pb(Ⅱ)浓度(30、50和70 mg/L)的溶液的吸附二级动力学模式分别为
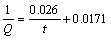 ,
,
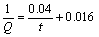 ,
,
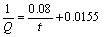 。
。

4) 胞外聚合物EPS-07所含主要成分是多糖类物质,主要含有羟基、酰胺、羰基等活性基团。吸附Pb(Ⅱ)后胞外聚合物EPS-07的―OH基峰发生偏移,2 926、1 647和1391 cm-1处的吸收峰强度明显减弱,1 080 cm-1处的吸收峰强度也明显减弱,并且发生了偏移。EPS-07与Pb(Ⅱ)的作用过程中,可能是羟基、羧基等基团参与了吸附作用。
5) 胞外聚合物EPS-07的表面结构比较松散,与Pb(Ⅱ)作用后, 其表面变得致密,并有结晶沉淀物出现。EDS分析表明Pb(II)被吸附到EPS-07上。
REFERENCES
[1] AMUDA O S, ADELOWO F E, OLOGUNDE M O. Kinetics and equilibrium studies of adsorption of chromium (Ⅵ) ion from industrial wastewater using Chrysophyllum albidum (sapotaceae) seed shells [J]. Colloids and surfaces B: Biointerfaces, 2009, 68: 184-192.
[2] 全桂静, 金 姬. 鞘细菌细胞吸附Cr(Ⅵ)条件的研究[J]. 环境科学与技术, 2009, 32(10): 60-64.
QUAN Gui-jing, JIN Ji. Absorptive condition of chromium by sheathed bacteria [J]. Environmental Science & Technology, 2009, 32(10): 60-64.
[3] ASEM A A, AHMED M D, AHMED M Y. Removal of some hazardous heavy metals from aqueous solution using magnetic chelating resin with iminodiacetate functionality [J]. Separation and Purification Technology, 2008, 61(3): 348-357.
[4] NADIR D, BULENT K, HULUSI B. Sorption of Ni(Ⅱ) ions from aqueous solution by lewatit cation-exchange resin [J]. Journal of Hazardous Materials, 2009, 167(1/3): 915-926.
[5] 范春辉, 张颖超, 张 颖, 韩 雪, CHEFETZ B. 低成本吸附剂稻壳灰对Cr(Ⅵ)去除机制的谱学表征[J]. 光谱学与光谱分析, 2010, 30(10): 2752-2757.
FAN Chun-hui, ZHANG Ying-chao, ZHANG Ying, HAN Xue, CHEFETZ B. Spectroscopic characterization analysis on Cr(Ⅵ) removal mechanism by low-cost adsorbent of rice husk ash [J]. Spectroscopy and Spectral Analysis. 2010, 30 (10): 2752- 2757.
[6] NUHOGLU Y, MALKOC E. Thermodynamic and kinetic studies for environmentally friendly Ni(Ⅱ) biosorption using waste pomace of olive oil factory [J]. Bioresource Technology, 2009, 100(8): 2375-2380.
[7] TUZEN M, SARL A, MENDIL D, ULUOZLUA O D, SOYLAK M, DOGAN M. Characterization of biosorption process of As(Ⅲ) on green algae Ulothrix cylindricum [J]. Journal of Hazardous Materials, 2009, 165(1/3): 566-572.
[8] 康春莉, 苏春彦, 郭 平, 赵宇侠, 董德明. 自然水体生物膜胞外蛋白质吸附铅和镉的研究[J]. 高等学校化学学报, 2006, 27(7): 1245-1246.
KANG Chun-li, SU Chun-yan, GUO Ping, ZHAO Yu-xia, GUO De-ming. Studies on Pb2+ and Cd2+ adsorption by extracellular protein of natural biofilm [J]. Chemical Journal of Chinese Universities, 2006, 27(7): 1245-1246.
[9] ZHANG Dao-yong, WANGJian-long, PAN Xiang-liang. Cadmium sorption by EPSs produced by anaerobic sludge under sulfate-reducing conditions [J]. Journal of Hazardous Materials, 2006, 138(3): 589-593.
[10] HORN H, NEU T R, WULKOW M. Modelling the structure and function of extracellular polymeric substances in biofilms with new numerical techniques [J]. Water Science Technology, 2001, 43(6): 121-127.
[11] JANG A. Adsorption of heavy metals by EPS of activated sludge [J]. Water Science Technology, 2001, 43(6): 41-48.
[12] LEVANKUMAR L, MUTHUKUMARAN V, GOBINATH M B. Batch adsorption and kinetics of chromium (VI) removal from aqueous solutions by Ocimum americanum L. seed pods [J]. Journal of Hazardous Materials, 2009, 161(2/3): 709-713.
[13] MOON S H, PARK C S, KIM Y J, PARK Y l. Biosorption isotherms of Pb(Ⅱ) and Zn(Ⅱ) on Pestan, an extracellular polysaccharide, of Pestalotiopsis sp. KCTC 8637P [J]. Process Biochemistry, 2006, 41(2): 312-316.
[14] STEPHEN I B, WANG J S, LU J F, SIAO F Y, CHEN B H. Adsorption of toxic mercury(II) by an extracellular biopolymerpoly (γ-glutamic acid) [J]. Bioresource Technology, 2009, 100(1): 200-207.
[15] [15] TOURNEY J, NGWENYA B T, FRED MOSSELMANS J W, MAGENNIS M. Physical and chemical effects of extracellular polymers (EPS) on Zn adsorption to Bacillus licheniformis S-86 [J]. Journal of Colloid and Interface Science, 2009, 337(2): 381-389.
[16] 董德明, 康春莉, 李忠华. 天然水中细菌胞外聚合物对重金属的吸附规律[J]. 吉林大学学报: 理学版, 2003, 41(1): 94-96.
DONG De-ming, KANG Chun-li, LI Zhong-hua. The adsorption of heavy metals on extracellular polymers of bacteria in natural water [J]. Journal of Jilin University: Science Edition, 2003, 41 (1):94-96.
[17] 康春莉, 苏春彦, 董德明, 郭 平, 赵宇侠. 自然水体生物膜胞外多糖吸附铅和镉的研究[J]. 吉林大学学报: 理学版, 2005, 41(1): 121-125.
KANG Chun-li, SU Chun-yan, DONG De-ming, GUO Ping, ZHAO Yu-xia. Studies on lead and cadmium adsorption by exopolysaccharide of natural biofilm [J]. Journal of Jilin University: Science Edition, 2005, 41(1): 121-125.
[18] 潘响亮, 王建龙, 张道勇, 王 凡. 硫酸盐还原菌混合菌群胞外聚合物对Zn2+的吸附和机理[J]. 环境科学研究, 2005, 18(6): 53-55.
PAN Xiang-liang, WANG Jian-long, ZHANG Dao-yong, WANG Fan. Zn2+ sorption and mechanism by EPS of mixed SRB population [J]. Research of Environmental Sciences, 2005, 18(6): 53-55.
[19] 杜 伟, 孙宝盛, 吕 英. 胞外聚合物对Cu2+, Cr3+和Ni2+ 的吸附性能研究[J]. 中国给水排水, 2007, 23(13): 98-101.
DU Wei, SUN Bao-sheng, L? Ying. Study on adsorption of Cu2+, Cr3+ and Ni2+ by EPS [J]. China Water & Wastewater, 2007, 23(13): 98-101.
[20] 郑 蕾, 丁爱中, 王金生, 田 禹, 孙德智. 不同组成活性污泥胞外聚合物吸附Cd2+, Zn2+特征[J]. 环境科学, 2008, 29(10): 2850-2855.
ZHENG Lei, DING Ai-zhong, WANG Jin-sheng, TIAN Yu, SUN De-zhi. Adsorption characteristics of Cd2+ and Zn2+ by extracellular polymeric substances with varied constituents from activated sludge [J]. Environmental Science, 2008, 29(10): 2850-2855.
[21] 王远红, 张红波, 罗世田, 刘巍峰, 赵二丽. 胞外聚合物对水中Cd(Ⅱ)的吸附性能研究[J]. 环境工程学报, 2010, 4(10): 2185-2189.
WANG Yuan-hong, ZHANG Hong-bo, LUO Shi-tian, LIU Wei-feng, ZHAO Er-li. Study on adsorption performances of Cd(II) by extracellular biopolymer substances [J]. Chinese Journal of Environmental Engineering, 2010, 4(10): 2185-2189.
[22] 熊 芬, 胡勇有, 银玉容. 烟曲霉胞外聚合物对Pb2+的吸附特性[J]. 环境科学学报, 2009, 29(11): 2289-2294.
XIONG Fen, HU Yong-you, YIN Yu-rong. Biosorption of Pb2+ by extracellular polymeric substances produced by Aspergillus fumigatus [J]. Acta Scientiae Circumstantiae, 2009, 29(11): 2289-2294.
[23] 王 亮, 陈桂秋, 曾光明, 张文娟, 范佳琦, 沈国励. 白腐真菌胞外聚合物及其对菌体吸附Pb2+的影响[J]. 环境科学, 2011, 32(3): 773-778.
WANG Liang, CHEN Gui-qiu, ZENG Guang-ming, ZHANG Wen-juan, FAN Jia-qi, SHEN Guo-li. Extracellular polymeric substances (EPS) of white-rot fungus and their effects on Pb2+ adsorption by biomass [J]. Environmental Science, 2011, 32(3): 773-778.
[24] 戴友芝, 许彩霞. 啤酒酵母对水中Cr(VI)的吸附研究[J]. 湘潭大学学报: 自然科学版, 2007, 29(3): 79-83.
DAI You-zhi, XU Cai-xia. Biosorption of Cr(VI) from aqueous solutions by S. Cerevisiae [J]. Natural Science Journal of Xiangtan University, 2007, 29(3): 79-83.
[25] 董德明, 李 鱼, 花修艺, 张菁菁, 杨 帆. pH对湿地水环境中生物膜吸附铅和镉的影响[J]. 吉林大学学报: 理学版, 2002 , 40 (3): 303-307.
DONG De-ming, LI Yu, HUA Xiu-yi, ZHANG Jing-jing, YANG Fan. Effect of pH on Pb and Cd Adsorption to surface coatings developed in the aquatic environment of wetland [J]. Journal of Jilin University: Science Edition, 2002, 40(3): 303-307.
[26] 郑 蕾, 田 禹, 孙德智. pH 值对活性污泥胞外聚合物分子结构和表面特征影响研究[J]. 环境科学, 2007, 28(7): 1507- 1511.
ZHENG Lei, TIAN Yu, SUN De-zhi. Effects of pH on the surface characteristics and molecular structure of extracellular polymeric substances from activated sludge [J]. Environmental Science, 2007, 28(7): 1507-1511.
[27] HALL K R, EAGLETON L C, ACTRIVOS A, VERMEULEN T. Pore and solid-dif fusion kinetics in fixed-bed adsorption under constant pattern conditions [J]. Industrial and Engineering Chemistry Research Fundamentals, 1966, 5(2): 212-223.
(编辑 何学锋)