DOI: 10.11817/j.issn.1672-7207.2016.08.008
�Ȼ�����-ˮ�ϲ�������ܼ���ZnO���ܽ���Ϊ
��Զ1�����ַ�1�����1, 2����һ��1, 2�����Ӣ1, 2����ƽ��1
(1. ����������ѧ ұ������Դ����ѧԺ������ ������650093��
2. ʡ������������ɫ������Դ������ù����ص�ʵ���ң����� ������650093)
ժҪ�����Ȼ�����(ChCl)��ˮ�ϲ���(H2C2O4��2H2O)Ϊԭ�Ϻϳ��Ȼ�����/ˮ�ϲ�������ܼ�(ChCl/H2C2O4��2H2O DESs)���о�ChCl/H2C2O4��2H2O DESs��������۵�Ĺ�ϵ��1ChCl:1H2C2O4��2H2O DES���ȡ��絼�����¶ȵĹ�ϵ��ZnO��1ChCl:1H2C2O4��2H2O DES�е��ܽ�ȼ��ܽ���Ϊ���о����������1ChCl:1H2C2O4��2H2O DES�ĵ��۵�Ϊ9 �棬��150 �����ھ������ȶ��ԣ����¶ȴ�297 K���ߵ�333 K��1ChCl:1H2C2O4��2H2O DES���ȴ�199.4 mPa��s���͵�35.6 mPa��s���絼�����3.55 mS/cm������15.01 mS/cm��ZnO���ܽ����0.310 mol/L����0.860 mol/L��δ����ZnO����ϵ�е������ӻ����ӽ�ϳ�����������ʽ���ڣ��ܽ���1ChCl:1H2C2O4 ��2H2O DES�е� ZnO����ϵ�еIJ��ᷴӦ���ɿ����ڸ���ϵ��ZnC2O4��
�ؼ��ʣ������ܼ����Ȼ�����/ˮ�ϲ���۵㣻�ȣ��絼�ʣ��ܽ�ȣ�ZnO��ZnC2O4
��ͼ����ţ�TQ151.8 ���ױ�־�룺A ���±�ţ�1672-7207(2016)08-2591-09
Dissolution behavior of zinc oxide in choline chloride-oxalate hydrates deep eutectic solvents
ZHANG Yuan1, LI Linfei1, LI Jian1, 2, HUA Yixin1, 2, XU Cunying1, 2, KE Pingchao1
(1. Faculty of Metallurgical and Energy Engineering,
Kunming University of Science and Technology, Kunming 650093, China;
2. State Key Laboratory of Complex Nonferrous Metal Resources Cleaning Utilization in Yunnan Province,
Kunming 650093, China)
Abstract: Choline chloride/oxalate hydrates deep eutectic solvents(ChCl/H2C2O4��2H2O DESs) were synthesized with choline chloride(ChCl) and oxalate hydrates(H2C2O4��2H2O). The melting point of ChCl/H2C2O4��2H2O DESs as a function of composition, the electrical conductivities and viscosities of 1ChCl:1H2C2O4��2H2O DES as a function of temperature, solubility of ZnO and the form of ZnO in the DES system were researched. The results show that the eutectic point of 1ChCl:1H2C2O4 ��2H2O DES is 9 ��, the DES is thermal stability from room temperature to 150 ��. At 297-333 K, the viscosity of 1ChCl:1H2C2O4��2H2O DES reduces from 199.4 mPa��s to 35.6 mPa��s, the electrical conductivity increases from 3.55 mS/cm to 15.01 mS/cm, and the solubility of ZnO increases from 0.310 mol/L to 0.860 mol/L. There is no ion species form from ZnO combined with any cation or anion species in DES system. ZnO dissolved in the DESs reacts with oxalic acid and generates ZnC2O4.
Key words: deep eutectic solvents; choline chloride/oxalate hydrates; melting point; viscosity; conductivity; solubility; ZnO; ZnC2O4
ͨ��������������������Ի����ˮ��Һ�����ܽ⣬���ھ��ַ����ܼ����Dz��ܽ�ġ�Ȼ��������������ܽ����ܶ��ڽ����ĵ���������ʴ���Լ������Ʊ��ȹ���ȴ�Ǽ�Ϊ��Ҫ�ġ�������ɫ����ͭ��п�ȵ��������ͨ���ᡢ����ܽ⣬�ٽ��е������ȡ�����Ѵ��������ѡ����ȵ���ȡȴ����ø���������Ϊ�����[1-2]��Ϊ�������ε��¶ȣ����Dz���������ĵ��ۻ����罫�����������λ���γ����������Σ��������͵�����Һ�����Ϊ����(����)��ǰ������һ������о�������Ҫ���������������������������[3-5]���˺��о���Χ��չ�������Ľ����Ȼ������ZnCl2[6]��SnCl2[7]��FeCl3[8]��NiCl2[9]��CrCl3��H2O[10]�ȡ�����±����Ҳ������������γ���������������±���������ػ�Ͽ��γ��۵����150 ��Ĺ���[11]�����Ȼ�����(ChCl)������(urea)�����ʵ�����Ϊ1:2���ʱ���γ�����۵�Ϊ12 ��ĵ����ܼ�(deep eutectic solvents��DESs)[12]���������ܼ���ӵ�е��������ӵ�����Һ�����ƣ������в�ͬѰ�����ܼ����ʣ���ϸߵĵ絼�ʡ��Ⱥͱ���������DESs�������ڶ࣬������ɵĻ����ﲻͬ��Ϊ�����(����ChCl)/�����Ȼ�������/ˮ�Ͻ����Ȼ�������/��������Լ�ˮ�Ͻ����Ȼ���/��������4��[12-14]��������������ƣ���������Һ���н�����������ܽ����λ��ѧ��ΪҲ���������ǵ�����[15-16]������DESs�������ͽ�����������ZnO��Cu2O��PbO2�Ⱦ������õ��ܽ����ܣ����Թ����ͽ�����������Al2O3��ȴ�������ܽ�[13]��60 ��ʱChCl/urea DES��ZnO��Cu2O��PbO2���ܽ�ȷֱ�Ϊ8 466��10-6��8 725��10-6��9 157��10-6[17]����ˣ������ڴ����ֵ绡¯�̳���ѡ���Ե���ȡп[18]������п�ڶ�п�����͵�����칤ҵ��һ����Ҫ��������������Ҫ������п��Ϊԭ�ϣ���Ϊ���ô�ͳ�ĸ�ѡ�������Ժ����ؽ�������ʯ���룬ʵ�ָ�ѡ����[19]����������Ȼ��п��������Լ��µ���п��δ��̽�������ǽ�Խ��Խ��������п��Ŀ�����[20]�����������ܼ���������п��ʹ����������ʯ�����α��ܳ����������������ҿ�Һ�̷�������[21]�������ú����ļ����ܼ������������ܼ��ӷ��Դ�����ʧ�����Ҷ����������Բ�����Ա������Ϊ����[21-22]��DESs�����ԭ���á��۸�������ϳɼ��۵�ϵ͡�����Ͷ����ŵ㣬��Ϊһ�����͵���ɫ�ܼ����ܵ��㷺��ע[23-24]�����ǵ�����DESs��ZnO��ѡ�����ܽ��������������Ϊ����п��DZ�ڵĽ����ܼ��������������Ȼ������ˮ�ϲ����Ϲ��ۻ��һ���µ�DES(ChCl/H2C2O4��2H2O)���о�����ϵ���۵㡢�ȡ��絼�ʵ��ﻯ�����Լ�ZnO�ڸ���ϵ�е��ܽ�Ⱥʹ�����̬��
1 ʵ��
1.1 ��Ҫ�������Լ�
��Ҫ�����У�RET basic���ȴ���������(�¹�IKA��˾)��FA1004N�͵�����ƽ(�Ϻ����ܿ�ѧ��������˾)��DZF-6090����ո�����(�Ϻ�����ʵ���豸����˾)��DU-20�͵�����ԡ��(�Ϻ�һ��Ƽ�����˾)��SNB-2��������ת�ȼ�(�Ϻ���ѧ�����о���)��DSSJ-308A�͵絼����(�Ϻ����ܿ�ѧ��������˾)��STA409PCͬ���ȷ�����(�¹��ͳ��������칫˾)��microTOF-Q11������������(�¹�Bruker��˾)��
��Ҫ�Լ��У��Ȼ�����(HOC2H4N(CH3)3Cl��ChCl��99%(������������ͬ)����ҩ���Ż�ѧ�Լ�����˾)����ˮ�Ҵ����ؽᾧ�ᴿ�����˲���353.15 K���¶�����ո���24 h��ˮ�ϲ���(H2C2O4��2H2O������������99%����¤�����ɷ�����˾)������п(ZnO������������99%����¤�����ɷ�����˾)�����Ȼ������ˮ�ϲ��ᰴһ�����ʵ����ȼ��뵽500 mL����ƿ�л�Ͼ��ȣ���50����ԡ���ڼ������γɾ��ȡ�����Һ�壬��Ϊ�Ȼ�����/ˮ�ϲ�������ܼ�(ChCl/H2C2O4��2H2O DESs)��
1.2 ���������
����ëϸ�ܷ��ⶨ�˲�ͬ���ʵ�����ChCl/H2C2O4��2H2O DESs���۵㣬ÿ����ɲ���3�Σ�ȡ3�β��Խ����ƽ��ֵΪ����ɵ��۵�[25]�������ܽ�ƽ�ⷨ�ⶨZnO�����ʵ�����Ϊ1:1��1ChCl:1H2C2O4��2H2O DES�е��ܽ��[26]�������ȼƺ͵絼���Ƿֱ�ⶨ��297~333 K�¶ȷ�Χ��1ChCl:1H2C2O4��2H2O DES���ȼ��絼�ʣ��Լ�1ChCl:1H2C2O4��2H2O DES���ܽⲻͬŨ�ȵ�ZnO����ϵ�ĵ絼�ʡ����õ����������Ƕ��ܽ���0.4 mol/L ZnO��1ChCl:1H2C2O4��2H2O DES���������������������У�1) ����Դ���ࣺESIԴ(˫������©���͵���������Դ)��2) ����Դ�¶ȣ�180 �棻3) ���������٣�4.0 mol/L��4) ��������ѹ��4��104 Pa��5) ������ģʽ������ģʽ������ͬ���ȷ����Ƕ��ܽ��� 0.4 mol/L ZnO��1ChCl:1H2C2O4��2H2O DES��������-���ȷ������¶ȷ�ΧΪ25~400 �棬��������Ϊ10 ��/min������ʱ��Ϊ1 min��
2 ���������
2.1 ChCl/H2C2O4��2H2O DESs���۵�
ChCl��H2C2O4��2H2O����ͬ���ʵ������γɵ�DESs���۵���ͼ1��ʾ����ͼ1���Կ�����ChCl��H2C2O4��2H2O�γɵ�DESs���۵����Ե���ChCl(302 ��)��H2C2O4��2H2O(101 ��)���۵㣬�����ʵ�����Ϊ1:1��1ChCl:1H2C2O4��2H2O DES���۵�Ϊ9 ��(����۵�)����1ChCl:1H2C2O4���۵�(34 ��)��25 ��[13]�������ʵ�������ͬʱ��ChCl/H2C2O4��2H2O DESs���۵����Ե���ChCl/H2C2O4 DESs���۵㡣
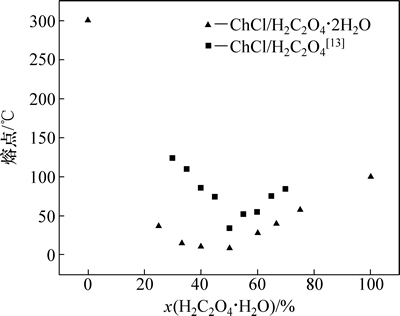
ͼ1 ChCl/H2C2O4��2H2O DESs���۵�����ɵĹ�ϵ
Fig. 1 Melting point of ChCl/H2C2O4��2H2O DESs as a function of composition
��ChCl/H2C2O4��ChCl/H2C2O4��2H2O DESs�У�ChCl��������Cl-�ɷֱ���H2C2O4��H2C2O4��2H2O�γ��������ͼ2��ʾ����ͼ2�ɼ���H2C2O4���ɷ����е��ǻ�(��OH)��Cl-�γ��������H2C2O4��2H2O�����ɷ����е�ˮ��ˮ������Cl-�γ������[H2C2O4��Cl]-��[H2C2O4��2H2O��Cl]-��Ħ�������ֱ�Ϊ125.5 g/mol��143.5 g/mol�����ߵ�������Դ���ǰ�ߵ������
DESs���۵���������������ķ��ӽṹ���������ӵĶԳ��ԡ���������Լ����ӵĵ�ɷֲ��������йء����ӻ������γ����������Խǿ���۵�Խ�ߣ��������ӶԳ���Խ�ͣ��۵�Խ�ͣ�DESs����������ͬʱ�������ӵijߴ�Խ���۵�Խ�ͣ�ͬ������������ͬʱ�������ӳߴ�Խ���۵�Խ�ͣ��������ӵĵ�ɷ�ɢ��Խ���۵�Խ��[27]����ͼ2�ɼ���1ChCl:1H2C2O4 DES�������ӳߴ�С��1ChCl:1H2C2O4��2H2O DES�������ӳߴ磬�����Ǿ�����ͬ�ĵ���������Ch+����͵��º��ߵ������ӵĵ�ɷ�ɢ�ȸ���ʹ��1ChCl:1H2C2O4��2H2O DES���������Ӽ�����������������1ChCl:1H2C2O4��2H2O DES���۵����1ChCl:1H2C2O4 DESs���۵㡣
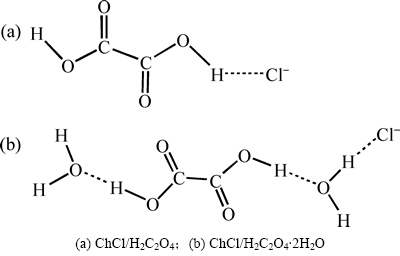
ͼ2 DESs��ϵ��H2C2O4��H2C2O4��2H2O��Cl-�γɵ����
Fig. 2 Hydrogen bonds formed between H2C2O4 and Cl-,and H2C2O4��2H2O and Cl-
2.2 1ChCl:1H2C2O4��2H2O DES����
1ChCl:1H2C2O4��2H2O DES�������¶ȵĹ�ϵ��ͼ3��ʾ����ͼ3�ɼ������¶ȴ�297 K���ߵ�333 K��1ChCl:1H2C2O4��2H2O DES������199.4 mPa��s���͵�35.6 mPa��s����1ChCl:1H2C2O4 DES��������4 280 mPa��s���͵�380 mPa��s[13]����ͬ�¶�ʱ1ChCl:1H2C2O4��2H2O DES���ȱ�1ChCl:1H2C2O4 DES����С�ö࣬�ڵ���ʱ���ֲ���Ϊ���ԡ�
DESs������Ҫ����ṹ��������ȡ������ϵ�е�����ͷ��»��������¶�Ҳ����ϵ���Ȳ�����������Ӱ��[27-28]���¶����ߣ������������Ӽ�ľ����������Ӽ����������������ϵ���ȼ�С����ͼ2�ɼ���2��DES��ϵ�е������Ӷ��ǵ���������Ch+����[H2C2O4��Cl]-���С��[H2C2O4��2H2O��Cl]-�������͵��º��ߵĵ�ɸ�Ϊ��ɢ��ʹ��1ChCl : 1H2C2O4��2H2O DES���������Ӽ����������������������ͬ�¶���1ChCl:1H2C2O4��2H2O DES���ȸ��͡�
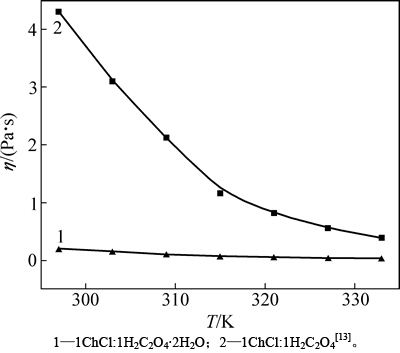
ͼ3 1ChCl:1H2C2O4��2H2O DES�������¶ȵĹ�ϵ
Fig. 3 Viscosity of 1ChCl:1H2C2O4��2H2O DES as a function of temperature
��1ChCl:1H2C2O4��2H2O DES��1ChCl:1H2C2O4 DES�ȵĶ�����1/T��ͼ�������ͼ4����ͼ4�ɼ���ln ����1/T�����Թ�ϵ�����ϰ�������˹��ʽ[29]��
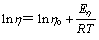 (1)
(1)
ʽ�У���Ϊ�ȣ���oΪ������E��Ϊ�Ȼ�ܣ�RΪĦ�����峣����TΪ����ѧ�¶ȡ�
��ʽ(1)��ͼ4�ɷֱ���1ChCl:1H2C2O4��2H2O DES��1ChCl:1H2C2O4 DES ��E�� �����ϵ��r���������1��
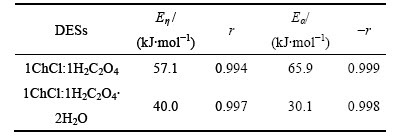
�ɱ�1�ɼ�����1ChCl:1H2C2O4 DES��ȣ�1ChCl:1H2C2O4��2H2O DES��E����С����ϵ���������ܸ��á�E���ͦ�o��ȷ���������Ʋ����ϵ�ڲ�ͬ�¶��µ��ȣ�������Ƶ��ȵ�DESs��

ͼ4 1ChCl:1H2C2O4��2H2O DES��ϵln ����1/T�Ĺ�ϵ
Fig. 4 Plot of ln �� vs 1/T of 1ChCl:1H2C2O4��2H2O DES
��1 1ChCl:1H2C2O4��2H2O DES��1ChCl:1H2C2O4 DES���Ȼ��E���͵絼���E��
Table 1 Activation energies for viscous flow (E��) and conductivity (E��) as DESs
2.3 1ChCl:1H2C2O4��2H2O DES�ĵ絼��
1ChCl:1H2C2O4��2H2O DES�ĵ絼�����¶ȵĹ�ϵ��ͼ5��ʾ����ͼ5�ɼ������¶ȴ�297 K���ߵ�333 K��1ChCl:1H2C2O4��2H2O DES�ĵ絼����3.55 mS/cm����15.01 mS/cm����1ChCl:1H2C2O4 DES�ĵ絼������0.056 mS/cm����0.95 mS/cm[13]����ͬ�¶�ʱ��1ChCl:1H2C2O4��2H2O DES�ĵ絼�ʱ�1ChCl:1H2C2O4 DES�ĵ絼�ʴ�ö࣬�ڽϸ��¶�ʱ����Ϊ���ԡ�
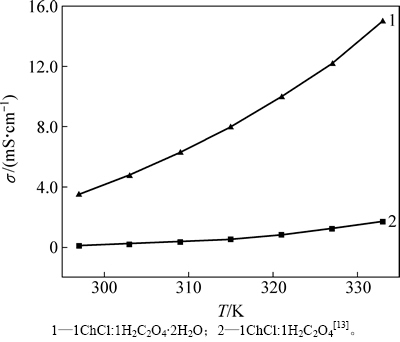
ͼ5 1ChCl:1H2C2O4��2H2O DES�ĵ絼�����¶ȵĹ�ϵ
Fig. 5 Conductivity of 1ChCl:1H2C2O4��2H2O DES as a function of temperature
�絼����DESs�ڵ绯ѧӦ���е�һ����Ҫָ�꣬������DESs�ĵ絼��һ��Ϊ0.1 mS/cm�����¶ȡ��ȡ���Է����������ܼ������ӵ���������ض���ϵ�е�����Ǩ������Ӱ��ϴ��Ե絼�ʲ����ϴ�Ӱ��[30]�������¶ȵ����ߣ�1ChCl:1H2C2O4��2H2O DES ��1ChCl:1H2C2O4 DES�����������������ӣ��˶�������С�������ڵ糡�������µĵ�Ǩ�����ʼӿ죬�ʶ��絼�������⣬����ͬ�¶��£�1ChCl:1H2C2O4��2H2O DES���ȱ�1ChCl:1H2C2O4 DES����С�ö࣬����ԽС�������˶�������ԽС�������ڵ糡�����µ�Ǩ������Խ�ʶ��絼��ҲԽ��
�ֱ���1ChCl:1H2C2O4��2H2O DES��1ChCl:1H2C2O4 DES�ĵ絼�ʵĶ�����1/T��ͼ�������ͼ6����ͼ6�ɼ���ln ����1/T�����Թ�ϵ�����ϰ�������˹��ʽ[29]��
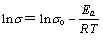 (2)
(2)
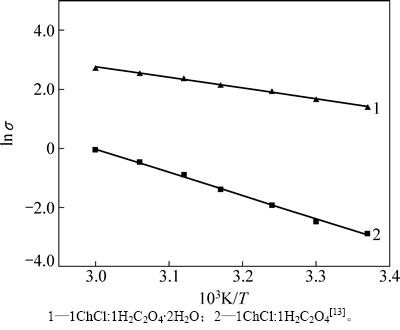
ͼ6 1ChCl:1H2C2O4��2H2O DES��ϵ��ln ����1/T�Ĺ�ϵ
Fig. 6 Plot of ln �� vs 1/T of 1ChCl:1H2C2O4��2H2O DES
ʽ�У���Ϊ�絼�ʣ���oΪ������E��Ϊ�絼��ܡ�
��ʽ(2)��ͼ5�ɷֱ���1ChCl:1H2C2O4��2H2O DES��1ChCl:1H2C2O4 DES��E�������ϵ��(����1)����ͼ5���Կ�����1ChCl:1H2C2O4��2H2O DES��E��С��1ChCl:1H2C2O4 DES��E������ǰ�ߵĵ絼�ʴ��ں��ߵĵ絼�ʣ�����1ChCl:1H2C2O4��2H2O DES�ĵ������ܸ��á�
2.4 1ChCl:1H2C2O4��2H2O DES��ZnO���ܽ��
ͼ7��ʾΪZnO��1ChCl:1H2C2O4��2H2O DES�е��ܽ�ȡ���ͼ7���Կ��������¶ȴ�297 K���ߵ�333 Kʱ��ZnO���ܽ����0.310 mol/L����0.860 mol/L����323 Kʱ��ZnO��1ChCl:1H2C2O4��2H2O DES�е��ܽ��Ϊ0.720 mol/L������1ChCl:1H2C2O4 DES�е��ܽ��0.491 mol/LҪ��[13]�����⣬���¶ȵ��� 317 Kʱ��ZnO��1ChCl:1H2C2O4��2H2O DES�е��ܽ�����¶ȵ���������Ͽ죬���¶Ȼ��������Թ�ϵ�����¶ȸ���317 Kʱ��ZnO���ܽ�����¶ȵ�������������Ƽ�����
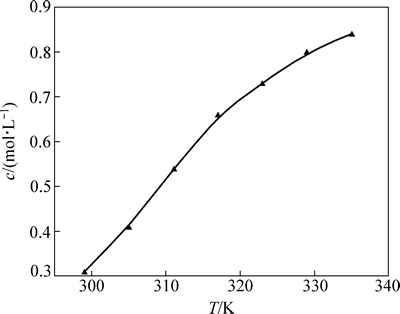
ͼ7 ZnO��1ChCl:1H2C2O4��2H2O DES�е��ܽ��
Fig. 7 Solubility of ZnO in 1ChCl:1H2C2O4��2H2O DES
2.5 ZnOŨ�ȶ�1ChCl:1H2C2O4��2H2O DES���Ⱥ͵絼�ʵ�Ӱ��
1ChCl:1H2C2O4��2H2O DES�зֱ��ܽ���0.1��0.2��0.3��0.4 mol/L ZnO����ϵ���Ⱥ͵絼�ʼ�ͼ8����ͼ8�ɼ������¶ȴ�298 K���ߵ�333 K����ϵ������С�����絼����������ZnOŨ��Ϊ0.4 mol/Lʱ����ϵ������242.5 mPa��s���͵�43.23 mPa��s���絼�����4.0 mS/cm���ߵ�15.3 mS/cm����ͬһ�¶��£���1ChCl:1H2C2O4��2H2O DES��ZnOŨ����0���ӵ�0.4 mol/L����ϵ���������絼��Ҳ��������298 Kʱ����199.4 mPa��s������242.5 mPa��s���絼������3.5 mS/cmС��������4.0 mS/cm���ڽϸ��¶�ʱ���ܽ��˲�ͬŨ��ZnO��1ChCl:1H2C2O4��2H2O DES��ϵ���ȱ����������ͼ8���ɼ����¶ȶԸ�DES��ϵ���Ⱥ͵絼��Ӱ����������ZnOŨ�ȶ����ǵ�Ӱ�첻������
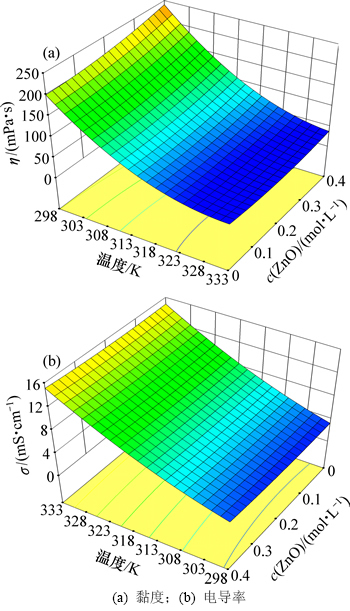
ͼ8 ZnOŨ�ȶ�[1ChCl:1H2C2O4��2H2O]/ZnO��Һ���Ⱥ͵絼�ʵ�Ӱ��
Fig. 8 Conductivity, viscosity of [1ChCl:1H2C2O4��2H2O]/ZnO solution as a function of ZnO concentration
2.6 ��ZnO��1ChCl:1H2C2O4��2H2O DES��������
��1ChCl:1H2C2O4��2H2O DES���ܽ�0.6 mol/L ZnO�Ը���Һ��ϵ���е������������������ͼ9��ʾ������������������ģʽ��ɨ�裬��Ҫ����ʺɱ�m/z�ֱ�Ϊ104��297�����ӷ�(��ͼ9(a))����������ģʽ��ɨ������Ҫ���m/z�ֱ�Ϊ89��174��228��282��315��454��528��593�����ӷ�(��ͼ9(b))��
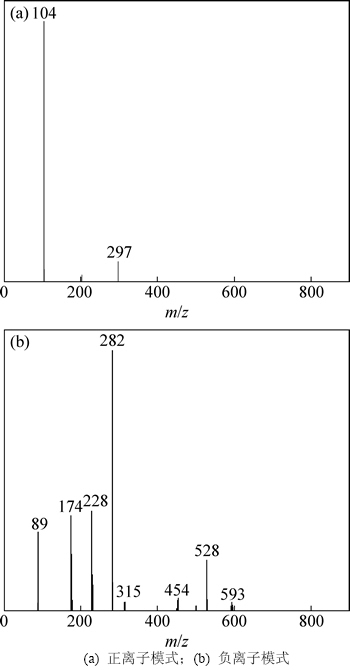
ͼ9 [1ChCl:1H2C2O4��2H2O]/0.6 mol/L ZnO ��Һ��ϵ�ĵ���������ͼ
Fig. 9 ESI-MS of [1ChCl:1H2C2O4��2H2O]/0.6 mol/L ZnO solution
��ͼ9(a)�ɼ���������ģʽ��m/z=104Ϊ���壬�������÷�ΪCh+ (����������)��m/z=297��Ϊ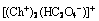 ���Ӵء���ͼ9(b)�ɼ���������ģʽ��m/z=282�Ļ���Ϊ
���Ӵء���ͼ9(b)�ɼ���������ģʽ��m/z=282�Ļ���Ϊ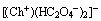 ���Ӵأ�m/z=89Ϊ
���Ӵأ�m/z=89Ϊ ��m/z=174��315��454��593ΪCh+��Cl-ͨ�����Ӽ�ĵ������γɵ�
��m/z=174��315��454��593ΪCh+��Cl-ͨ�����Ӽ�ĵ������γɵ�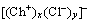 ���͵����Ӵأ�����2��m/z=228Ϊ
���͵����Ӵأ�����2��m/z=228Ϊ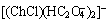 ��m/z=528Ϊ
��m/z=528Ϊ ��
��
��2 [1ChC:1H2C2O4��2H2O]/0.6 mol/L ZnO����Һ��ϵ���������������Ӧ�ĺ��ʱ�
Table 2 Positive ions and negative ions corresponding mass-to-charge ratio of [1ChC:1H2C2O4��2H2O]/0.6 mol/L ZnO solution
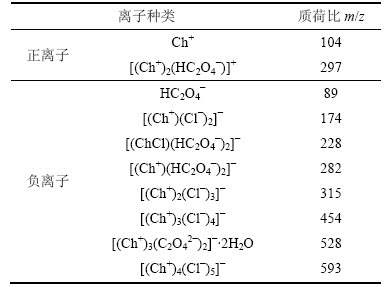
��ChCl/Urea DESs��[Amim]Cl/Urea DESs��ϵ�зֱ��ܽ�һ��Ũ��ZnO�������������ͺ����������������ܽ��ZnO��[ZnClO��Urea]-��̬����[17, 31]��������1ChCl:1H2C2O4��2H2O DES��ϵ���ܽ���ӦŨ�ȵ�ZnO�����������������δ����ZnO����ϵ�е������ӻ����ӽ�ϳ�����������ʽ���ڡ�
2.7 [1ChCl:1H2C2O4��2H2O]/ZnO ��Һ��ϵ���ȷ���
���ܽ�ZnOǰ���1ChCl:1H2C2O4��2H2O DES��Һ��ϵ����TG-DTA�����������ͼ10��ʾ��
��ͼ10(a)�ɼ�����70~150 �淶Χ�����ȷ壬��Ӧ��������ʧ��ԼΪ13.3%������1ChCl:1H2C2O4��2H2O DES��H2O����������13.5%�����Ǻϣ�˵�����¶ȷ�Χ�����ȷ��Ӧ��DES��ʧˮ���̣���150~400 ��ķ�Χ����3�����Ե����ȷ壬���յ�������ʧ�ʴ�91%�������ڴ��¶ȷ�Χ�ڣ�1ChCl:1H2C2O4��2H2O DES�������ȷֽ⡣˵���¶ȳ���70 ���1ChCl:1H2C2O4��2H2O DES����ʧȥˮ��ˮ�����1ChCl:1H2C2O4 DES����������150 ���������ȶ����ڡ���ͼ10(b)�ɼ�������1ChCl:1H2C2O4��2H2O DES���ܽ���0.6 mol/L ZnO����ͼ10(a)�����ƣ���70~150 ��ķ�ΧҲ�����ȷ壬Ϊ����Һ��ϵ��ʧˮ���̣�����150~400 �淶Χ����4�����Ե����ȷ壬ǰ3�����ȷ���ͼ10(a)�е����ƣ�ΪDES���ȷֽ⣻��ͼ10(a)��ͬ���ǣ�320~380 �淶Χ�����ȷ��������������ʷ����˷ֽ⣬���յIJ��ᆳXRD���Է���Ϊ������ZnO����ˣ���ΪZnO����1ChCl:1H2C2O4��2H2O DES�У���������ϵ�еIJ��ᷢ����ѧ��Ӧ������ZnC2O4(�������ߵ�ʵ���о�������ZnC2O4���ܽ���1ChCl:1H2C2O4��2H2O DES��)�������е��о�����[32-33]��ˮ�ϲ���п��108~170 �淶Χ��������ʧ��Ϊ19.5%����ˮ�ϲ���п����������ȥ2��H2O�������Ӧ������п��320~420 �淶Χ��������ʧ��Ϊ37.2%�������п����ͬʱ��ȥCO��CO2�������Ӧ�����ԣ�ͼ10(b)��320~380 �淶Χ�����ȷ��Ӧ��ZnC2O4�����ֽⷴӦ��
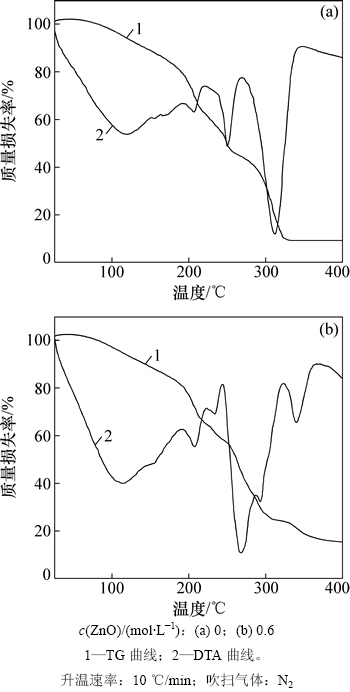
ͼ10 1ChCl:1H2C2O4��2H2O/ZnO DES��TG-DTA����
Fig. 10 TG-DTA curves of 1ChCl:1H2C2O4��2H2O/ZnO DES
Ϊ֤ʵZnO��1ChCl:1H2C2O4��2H2O DES��ϵ�еIJ��ᷴӦ�����������ڸ���ϵ��ZnC2O4����ZnO����1ChCl:1H2C2O4��2H2O DES������ϵ�м���10�������ˮϡ�ͣ�������ɫ����������ˡ�ϴ�Ӻ��������XRD���Է����������ͼ11��ʾ����ͼ11�ɼ������ð�ɫ������ΪZnC2O4��
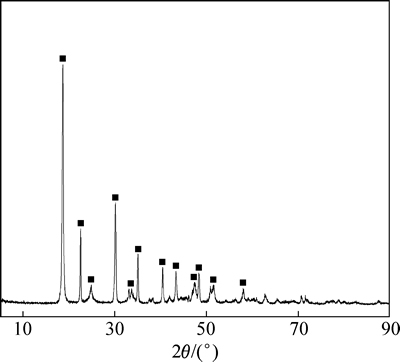
ͼ11 [1ChCl:1H2C2O4��2H2O]/ZnO DES��ˮϡ�����ó������XRD��
Fig. 11 XRD pattern of precipitate formed from [1ChCl:1H2C2O4��2H2O]/ZnO DES diluted with water
ZnO����1ChCl:1H2C2O4��2H2O DES����H2C2O4��Ӧ�γ���ZnC2O4���ܽ���1ChCl:1H2C2O4��2H2O DES�У���һ��֤ʵͼ10(b)��320~380 �淶Χ�����ȷ���ZnC2O4�����ֽ⡣�ȷ�����XRD���Խ��������1ChCl:1H2C2O4��2H2O DES�Լ��ڼ���һ����ZnO����150 ���������ȶ��ģ�ZnO����ϵ��Ӧ������ZnC2O4��
3 ����
1) ChCl/H2C2O4��2H2O DES�ĵ��۵�Ϊ9 �棬��ChCl/H2C2O4 DES�ĵ��۵�(34 ��)��25 �棬˵��ǰ�ߵĵ���Һ̬��Χ������
2) 1ChCl:1H2C2O4��2H2O DES��150 �����ھ������ȶ��ԡ�
3) �����¶ȴ�297 K���ߵ�333 K��1ChCl:1H2C2O4��2H2O DES���ȴ�199.4 mPa��s���͵�35.6 mPa��s��������ͬ�¶�ʱ�����ȱ�1ChCl:1H2C2O4 DES����С�öࡣ
4) �����¶ȴ�297 K���ߵ�333 K��1ChCl:1H2C2O4��2H2O DES�ĵ絼�ʴ�3.55 mS/cm������15.01 mS/cm��������ͬ�¶�ʱ���ĵ絼�ʱ�1ChCl:1H2C2O4 DES�ĵ絼�ʴ�öࡣ
5) �����¶ȴ�297 K���ߵ�333 K��ZnO��1ChCl:1H2C2O4��2H2O DES�е��ܽ����0.31 mol/L����0.86 mol/L��������ͬ�¶�ʱ��ZnO��1ChCl:1H2C2O4��2H2O DES�е��ܽ�ȴ�����1ChCl:1H2C2O4 DES�е��ܽ�ȡ�
6) ZnO����1ChCl:1H2C2O4��2H2O DES��δ����ϵ�е������ӻ����ӽ���γ��������֣���������ϵ�еIJ��ᷴӦ�����˿����ڸ���ϵ��ZnC2O4��
�ο����ף�
[1] CHEN G Z, FRAY D J, FARTHING T W. Direct electrochemical reduction of titanium dioxide to titanium in molten calcium chloride[J]. Nature, 2000, 407(9): 361-364.
[2] ��͢��, ����ϲ, ����־, ��. ��ұ����[M]. ����: ��ѧ������, 2014: 3-4.
ZHANG Tingan, ZHU Wangxi, L Guozhi, et al. Aluminium metallurgy technology[M]. Beijing: Science Press, 2014:3-4.
Guozhi, et al. Aluminium metallurgy technology[M]. Beijing: Science Press, 2014:3-4.
[3] LI B, FAN C, CHEN Y, et al. Pulse current electrodeposition of Al from an AlCl3-EMIC ionic liquid containing NdCl3[J]. Electrochemistry, 2010, 78(6): 523-525.
[4] ROBINSON J, OSTERYOUNG R A. An electrochemical and spectroscopic study of some aromatic hydrocarbons in the room temperature molten salt system aluminum chloride- n-butylpyridinium chloride[J]. Journal of the American Chemical Society, 1979, 101(2): 323-327.
[5] HOLBREY J D, SEDDON K R. The phase behaviour of 1-alkyl-3-methylimidazolium Tetrafluoroborates; ionic liquids and ionic liquid crystals[J]. Journal of the Chemical Society, Dalton Transactions, 1999(13): 2133-2140.
[6] HSIU S I, HUANG J F, SUN I W, et al. Lewis acidity dependency of the electrochemical window of zinc chloride�C1-ethyl-3-methylimi-dazolium chloride ionic liquids[J]. Electrochimica Acta, 2002, 47(27): 4367-4372.
[7] WASSERSCHEID P, KEIM W. Ionic liquids-new ��solutions�� for transition metal catalysis[J]. Angewandte Chemie International Edition, 2000, 39(21): 3772-3789.
[8] SHANG S, LI L, YANG X, et al. Synthesis and characterization of poly (3-methyl thiophene) nanospheres in magnetic ionic liquid[J]. Journal of Colloid and Interface Science, 2009, 333(1): 415-418.
[9] ABBOTT A P, EL TTAIB K, RYDER K S, et al. Electrodeposition of nickel using eutectic based ionic liquids[J]. Transactions of the Institute of Metal Finishing, 2008, 86(4): 234-240.
[10] ABBOTT A P, AL-BARZINJY A A, ABBOTT P D, et al. Speciation, physical and electrolytic properties of eutectic mixtures based on CrCl3��6H2O and urea[J]. Phys Chem, 2014, 16: 9047-9055.
[11] GAMBINO M, BROS J P. Capacite calorifique de l��uree et de quelques melanges eutectiques a base d'uree entre 30 et 140 ��[J]. Thermochimica Acta, 1988, 127: 223-236.
GAMBINO M, BROS J P. The heat capacity of urea and some urea based eutectic mixtures between 30 to 140��[J]. Thermochimica Acta, 1988, 127: 223-236.
[12] ABBOTT A P, CAPPER G, DAVIES D L, et al. Novel solvent properties of choline chloride/urea mixtures[J]. Chem Commun, 2003 (1): 70-71.
[13] ABBOTT A P, BOOTHBY D, CAPPER G, et al. Deep eutectic solvents formed between choline chloride and carboxylic acids: versatile alternatives to ionic liquids[J]. Journal of the American Chemical Society, 2004, 126(29): 9142-9147.
[14] XING S, ZANELLA C, DEFLORIAN F. Effect of pulse current on the electrodeposition of copper from choline chloride-ethylene glycol[J]. Journal of Solid State Electrochemistry, 2014, 18(6): 1657-1663.
[15] DAI S, SHIN Y S, TOTH L M, et al. Comparative UV-Vis studies of uranyl chloride complex in two basic ambient- temperature melt systems: the observation of spectral and thermodynamic variations induced via hydrogen bonding[J]. Inorganic Chemistry, 1997, 36(21): 4900-4902.
[16] BELL R C, CASTLEMAN A W, THORN D L. Vanadium oxide complexes in room-temperature chloroaluminate molten salts[J]. Inorganic Chemistry, 1999, 38(25): 5709-5715.
[17] ABBOTT A P, CAPPER G, DAVIES D L, et al. Selective extraction of metals from mixed oxide matrixes using choline-based ionic liquids[J]. Inorganic Chemistry, 2005, 44(19): 6497-6499.
[18] ABBOTT A P, CAPPER G, DAVIES D L, et al. Processing metal oxides using ionic liquids[J]. Mineral Processing and Extractive Metallurgy, 2006, 115(1): 15-18.
[19] ��ޱ, ͯ��. ��ѡ��п�������п��IJ��ռ��о���״����չ[J]. ���������ѡ��, 2007, 44(8): 25-27.
CHEN Wei, TONG Xiong. Review on research progress of sphalerite and marmatite floation an its collector[J]. Metallic Ore Dressing Abroad, 2007, 44(8): 25-27.
[20] ��־��, ������, ������, ��. MACA ��ϵ��ѭ��������Ʒλ����п���Ʊ����п[J]. �й���ɫ����ѧ��, 2013, 23(12): 3455-3461.
XIA Zhimei, YANG Shenghai, TANG Moteng, et al. Cycle leaching of low grade zinc oxide ores in MACA system for preparing zinc[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(12): 3455-3461.
[21] �����, κ��, ����, ��. �߹�����п���ѹ�������[J]. �й���ɫ����ѧ��, 2009, 19(9): 1678-1683.
LI Cunxiong, WEI Chang, FAN Gang, et al. Pressure acid leaching of high silicon zinc oxide ore[J]. The Chinese Journal of Nonferrous Metals, 2009, 19(9): 1678-1683.
[22] ������, ����, �μ�ǿ, ��. ����淋��±����е�Ʒλ����п��[J]. �����о�ѧ��, 2012, 26(4): 396-401.
SHEN Xiaoyi, SUN Yi, SONG Jiqiang, et al. Low grade zinc ore by low temperature roasting using (NH4)2SO4[J]. Chinese Journal of Materials Research, 2012, 26(4): 396-401.
[23] ��ӯӯ, ½С��, ����, ��. ����������ܼ������Լ�Ӧ��[J]. ��ѧ��չ, 2013, 25(6): 881-891.
ZHANG Yingying, LU Xiaohua, FENG Xin, et al. Properties and applications of choline-based deep eutectic solvents[J]. Progress in Chemistry, 2013, 25(6): 881-891.
[24] DURAND E, LECOMTE J, VILLENEUVE P. Deep eutectic solvents: synthesis, application, and focus on lipase-catalyzed reactions[J]. European Journal of Lipid Science and Technology, 2013, 115(4): 379-385.
[25] ����ƽ. ��ѧƷ�۵�IJⶨ[J]. �й�����ó��, 2013, 5(12): 288-289.
SONG Leping. Determination of chemical substance[J]. China Chemical Trade, 2013, 5(12): 288-289.
[26] ����ҫ, ����. �����ܽ�Ȳⶨ�����Ľ����о���չ[J]. ҩ�������־, 2010, 30(4): 761-766.
HU Chengyao, HUANG Pei. Recent research and development on determination solid solubility[J]. Chinese Journal of Pharmaceutical Analysis, 2010, 30(4): 761-766.
[27] ��ֹ��, ����Դ, ����, ��. ����Һ��1-��3-�һ������ķ������κ�1, 2-����-3-�һ������ķ������ε�����ѧ�͵絼�����о�[J]. ��ѧ�Լ�, 2013, 35(8): 693-696.
WU Zhijing, ZHANG Xinyuan, YANG Yang, et al. Thermodynamic and electrical conductivity properties of ionic liquids 1-ethyi-3-Methyilimidazolium tetrafluorobo-rate and 1, 2-dimethyl-3-ethyllimidazolium tetrafluorrobo-rate[J]. Chemical Reagents, 2013, 35(8): 693-696.
[28] LI C P, LI Z, ZOU B X, et al. Density, viscosity and conductivity of protic ionic liquid N, n-dimethylethanol- ammonium propionate[J]. Acta Phys Chim Sin, 2013, 29(10): 2157-2161.
[29] LIU Q S, YAN P F, YANG M, et al. Dynamic viscosity and conductivity of ionic liquids [Cnpy][NTf2](n=2, 4, 5)[J]. Acta Physico-Chimica Sinica, 2011, 27(12): 2762-2766.
[30] ����ٻ, ��Ƽ, ��С��, ��. �廯1-��ϩ��-3-�����������Һ��ĵ绯ѧ����[J]. ����ѧ��, 2013, 64(11): 4153-4160.
LI Xiaoqian, GUAN Ping, HU Xiaoling, et al. Electrochemical properties of 1-vinyl-3-alkylimidazole bromide ionic liquids[J]. CIESC Journal, 2013, 64(11): 4153-4160.
[31] ZHENG Y, DONG K, WANG Q, et al. Electrodeposition of zinc coatings from the solutions of zinc oxide in imidazolium chloride/urea mixtures[J]. Science China Chemistry, 2012, 55(8): 1587-1597.
[32] �����, ��ϴ, ������, ��. ˮ�ϲ���п�ȷֽⷴӦ����ѧ�������߷��о�[J]. �人��ѧѧ��(��ѧ��), 2004, 50(6): 673-677.
TANG Wanjun, YANG Xi, LIU Yuwen, et al. The main curve method research of Zinc oxalate hydrate decomposition reaction kinetics[J]. Journal of Wuhan University (Natural Science Edition), 2004, 50(6): 673-677.
[33] ӡ����, ����, ��Ծ��, ��. �Զ�ˮ�ϲ���пΪǰ�����Ʊ���������п[J]. ������ѧѧ��(��Ȼ��ѧ��), 2005, 26(6): 585-587.
YIN Wanzhong, DING Yazhuo, HAN Yuexin, et al. The preparation of nano Zinc oxide precursor by Zinc oxalate dehydrate[J]. Journal of Northeastern University (Natural Science), 2005, 26(6): 585-587.
(�༭ ����ƽ)
�ո����ڣ�2015-08-24�������ڣ�2015-11-13
������Ŀ(Foundation item)�������ص�����о���չ�滮(973�ƻ�)��Ŀ(2014CB643404)��������Ȼ��ѧ����������Ŀ(51274108��21263007) (Project(2014CB643404) supported by the National Basic Research Development Program (973 Program) of China; Projects(51274108, 21263007) supported by the National Natural Science Foundation of China)
ͨ�����ߣ���ᣬ���ڣ�˶ʿ����ʦ��������ɫ����ұ���о���E-mail��kglj1010@163.com