DOI: 10.11817/j.issn.1672-7207.2016.07.002
植物修复收获物热解制备生物炭过程中重金属的稳定性研究
孙阳,刘亚男,郭朝晖,侍维
(中南大学 冶金与环境学院,湖南 长沙,410083)
摘要:基于重金属污染土壤植物修复过程中产生大量含重金属的生物质收获物,以含重金属芦竹收获物为研究对象,通过在芦竹收获物中添加化学固定材料,研究其热解制备生物炭过程中As,Cd和Pb等重金属的稳定与富集特征。研究结果表明:热解过程中生物质中重金属主要富集在生物炭中,其质量分数及存在形态明显受热解温度、热解时间、固定材料种类及添加量等因素影响;在250 ℃下添加0.5%(质量分数,下同)的NaOH、热解0.50 h,生物炭产率达到86%;芦竹生物质热解制备生物炭过程中As的稳定适宜条件为在300 ℃添加2% NaOH,热解2.00 h;Cd的稳定适宜条件为在250 ℃添加5% FeCl3,热解0.50 h;Pb的稳定适宜条件为在400 ℃添加5% CaCO3,热解1.00 h;添加FeCl3热解得到的生物炭比表面积达到0.31 m2/mg,重金属固定率提高;添加固定材料NaOH后热解制备的生物炭中As主要以残渣态存在,添加CaCO3,Al2O3和FeCl3等固定材料后热解制备的生物炭中As主要以可氧化态存在;添加NaOH,CaCO3,Al2O3和FeCl3等固定材料后热解制备的生物炭中Cd主要以残渣态存在,Pb主要以可氧化态存在。
关键词:植物修复;芦竹收获物;热解;重金属
中图分类号:X383;S795.8 文献标志码:A 文章编号:1672-7207(2016)07-2189-07
Stabilization on heavy metals of biochar from phytoremediation harvested biomass in pyrolysis processing
SUN Yang, LIU Yanan, GUO Zhaohui, SHI Wei
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: Considering that a large amounts of biomass harvested containing heavy metals will be produced by phytoremediation for metal contaminated soil, the harvested biomass of giant reed containing heavy metals was selected, and the stability and enrichment characteristics of As, Cd and Pb in the pyrolysis process for biochar were studied by adding chemicals. The results show that the heavy metals in biomass are mainly enriched in biochar, and the amount and speciation of heavy metals in biochar are affected deeply by temperature of pyrolysis, pyrolysis time, the kind and amount of chemicals added. The percentage of biochar arrives at 86% when biomass is pyrolysed for 0.5 h by adding 0.5% NaOH of 250 ℃. The optimized stability conditions for As in biochar is pyrolysed for 2.00 h by adding 2% NaOH at 300 ℃, and for Cd in biochar is pyrolysed for 0.50 h by adding 0.5% FeCl3 at 250 ℃, for Pb in biochar is pyrolysed for 1 h by adding 5% CaCO3 at 400 ℃, respectively. The specific surface area of biochar reaches 0.31 m2/mg by adding FeCl3 and the stability capacity of heavy metals in biochar significantly increases. According to the BCR sequential extraction procedure, the speciation of As in biochar exists mainly in residual form from the pyrolysis by adding NaOH while those of As in biochar exists mainly in oxidizable form by adding CaCO3,Al2O3 and FeCl3. The speciation of Cd in biochar exists mainly in residual form, and that of Pb in biochar exists mainly in oxidizable form with adding stable agents including NaOH, CaCO3, Al2O3 and FeCl3.
Key words: phytoremediation; biomass harvested of giant reed; pyrolysis; heavy metal
近年来,重金属污染土壤植物修复技术的工程应用越来越受到广泛关注。随着植物修复技术大规模的工程应用,如何科学处理处置修复过程中产生的含重金属生物质收获物已成为该技术的瓶颈问题之一。利用焚烧法[1-2]、灰化法[3]、堆肥法[4]、压缩填埋法[5]、植物冶金[6-8]、液相萃取法[9]、高温分解法[10-13]等对其进行处置取得了一系列研究成果。焚烧法可使生物质最大限度减量,同时便于运输和贮存[14];灰化法能将生物质有效减量并回收其中重金属[15],但这2种方法处理的生物质中重金属在灰分中残留量仅在 10%以下,大量Cd 和Pb等重金属进入到烟气中而造成二次污染[16]。堆肥法可使生物质减量,并且其设备占地面积小,反应过程易受控制,不受气候条件影响,但该方法处理周期长,投入成本较高[9, 17]。压缩填埋法与堆肥法相似,但残留的生物质及其渗滤液处置仍是目前的一个难题[17]。更为重要的是,堆肥法和压缩填埋法并没有解决其中重金属的潜在污染问题。植物冶金可以使金属得到回收,获得经济利益,但其处理步骤繁琐,工艺流程复杂[17]。液相萃取法可有效地提取生物质中重金属,但目前仍局限在实验室研究阶段[9]。高温分解法也称热解法[18],该方法能够将生物质原料转化为生物炭(同时获得部分合成气和生物油),实现含重金属生物质的体积减少,同时作为以资源再利用[19],是解决含重金属生物质收获物的一种比较合适的途径。生物炭可以作为生物质能源综合利用,同时具有很强的吸附能力[20],是目前研究的前沿热点之 一[21]。本文选取重金属污染土壤修复植物芦竹收获物为原料,探讨热解条件和几种外加固定材料对芦竹生物质热解制备生物炭过程中As,Cd和Pb等重金属的稳定调控作用,以期在生物质热解过程中重金属主要富集在生物炭中,防止重金属二次污染。
1 材料与方法
1.1 实验材料
在某典型冶炼区污染土壤田间植物修复示范区收获芦竹生物质。将收集的芦竹生物质依次用自来水和去离子水冲洗干净,用不锈钢刀具将其剪(切)碎至长 1 cm左右,混合均匀,于105 ℃下在烘箱中杀青0.50 h,再在60 ℃下烘干至恒定质量,粉碎备用。其中,芦竹收获物中As,Cd和Pb质量分数依次为18.72,30.68和63.10 mg/kg。
1.2 实验设计
通过设定不同的热解温度和热解时间对上述芦竹收获物粉末进行热解。为提高芦竹生物质中重金属在生物炭中稳定效果,选取本课题组前期筛选出的NaOH,CaCO3,Al2O3 和FeCl3这4种材料作为生物质中重金属固定材料添加到芦竹粉末中同时进行热解。按照热解温度(250,300,350和400℃)、热解时间(0.50,1.00,1.50和2.00 h)、固定材料种类(NaOH,CaCO3,Al2O3和FeCl3)及其添加量(质量分数分别为0.5%,1.0%,2.0%和5.0%) 4个因素,采用L16(45)正交表进行芦竹生物质热解制备生物炭实验设计。具体步骤如下:取10 g芦竹粉末于密封性好、直径为5 cm的新铝盒中,按照L16(45)正交表在芦竹粉末中添加相应固定材料,充分混匀后将铝盒盖紧(实现生物质在缺氧条件下热解),放入马弗炉中热解。待反应结束后,迅速取出铝盒置于干燥箱中冷却至室温后称质量,将制备的生物炭用自封口塑料样品密封袋装袋备用。同时,在不添加固定材料的相同热解条件下制备生物炭。所有实验处理重复2次。
1.3 分析与测试
芦竹收获物热解制得的生物炭产率通过直接称质量和计算得到;生物炭采用硝酸-高氯酸微波消解[22];生物炭中As,Cd和Pb等重金属的组分形态采用BCR连续提取法提取[23];生物炭中As,Cd和Pb等重金属稳定性参照HJ 557―2010“固体废物浸出毒性浸出方法-水平振荡法”进行评估[24]:在室温下,采用水浸(pH=5.5)和酸浸(pH=2.5),取0.2 g生物炭离心管中,分别加入20 mL蒸馏水和酸化后的蒸馏水,置于恒温水浴振荡箱中振荡24.00 h,离心过滤即得浸出液,消解液、连续提取液和浸出液中As质量分数采用原子荧光法(AFS-2202E双道原子荧光,北京海光仪器公司)测定,Cd和Pb质量分数采用原子吸收仪(AA-6800 Shimadzu,Japan)测定。生物炭的比表面积采用激光粒度分析仪测定,生物炭表面孔结构采用扫描电镜(KYKY2800 岛津)测定。
2 结果与分析
2.1 芦竹收获物热解制取生物炭产率
含重金属芦竹生物质收获物可以顺利实现热解。表1所示为芦竹生物质热解制备生物炭正交分析结果。从表1可以看出:在实验热解条件下,芦竹收获物制备生物炭产率达35%~86%;随着热解温度升高和热解时间延长,芦竹收获物制备出的生物炭产率明显降低至30%~40%。正交实验结果表明:热解温度对生物炭产率影响显著,其次依次为热解时间和外加固定材料比例。其中,适宜的热解条件为在250 ℃下添加质量分数为0.5%的NaOH、热解0.50 h,其生物炭产率达到86%。王秦超等[25]的研究表明:在温度为250~300 ℃条件下热解,生物质炭的表观体积比原料生物质小,外形收缩,颜色随温度升高加深,显著改善生物质炭表面的疏水性和研磨特性;升高热解温度和延长热解时间,生物炭产率明显降低。杨海平等[26]也发现,在300~600 ℃下,生物质炭量随着热解温度升高从36.7%下降到28.5%。在生物质热解反应过程中,金属盐的添加对反应具有促进作用,在一定范围内热解转化率随其添加量的增加而增加,且使反应速度提高[27]。上述研究结果与本研究的含重金属芦竹生物质热解制备生物炭结果相一致。
2.2 生物炭中As,Cd和Pb的固定率
表2所示为生物炭中As,Cd和Pb的固定率。从表2可以看出:生物炭中As固定率只有8%~37%;影响生物炭中As固定率的因素依次为固定材料种类、热解时间、热解温度和固定材料添加量。正交实验结果表明有利于生物炭中As的固定条件为:选用NaOH作为固定材料,添加质量比为2%,热解温度为300 ℃,热解时间为2.00 h。
生物炭中Cd的固定率达到65%~97%,影响生物炭中Cd固定率的影响因素依次为热解温度、固定材料比例、热解时间和固定材料种类。正交试验结果表明有利于生物炭中Cd固定条件为:选用FeCl3作为固定材料,添加质量比为5%,热解温度为250 ℃,热解时间为0.50 h。
生物炭中Pb的固定率也较低,只有23%~59%。影响生物炭中Pb固定率的影响因素依次为热解温度、固定材料种类、热解时间和固定材料添加比例。正交实验结果表明有利于生物炭中Pb的固定条件为:选用CaCO3作为固定材料,添加质量比为5%,热解温度为400 ℃,热解时间为1.00 h。
上述研究结果表明,生物炭中不同重金属的固定条件存在明显的差异,针对不同的重金属污染元素,需要有相应的适宜固定条件。
2.3 生物炭的基本特性
将添加不同固定材料,优化条件下制备的生物炭进行电镜扫描分析,结果见图1。从图1可以看出热解过程中添加不同外加固定材料前后生物炭的表面特征:不加固定材料的生物炭孔隙较小且分散,孔隙有大量的生物油吸附;添加固定材料后生物炭的表面空隙结构得到明显改善;添加NaOH后,热解制备的生物炭孔隙结构丰富,但孔径较小,且孔隙上附着有生物油;而添加固定材料FeCl3后热解制备的生物炭部分孔隙结构发达,但大部分孔隙结构不完整,存在不同程度的塌陷;孔内吸附有生物油吸附,但孔径较添加固定材料NaOH后热解制备的生物炭的孔径大;添加固定材料CaCO3后,热解制备的生物炭孔隙结构发达,孔径不均匀,具有明显的介孔材质特性;添加固定材料Al2O3后热解制备的生物炭孔隙结构发达,孔径不一,但存在不同程度的塌陷,表面吸附有生物油。上述生物炭表面结构的特性表明:由于添加不同的外加固定材料,生物炭的孔隙结构差异显著,外加固定材料不仅可以在生物质热解制备生物炭过程中稳定重金属,而且可以改善生物炭的孔隙结构。
表1 芦竹生物质热解制备生物炭正交分析
Table 1 Orthogonal analysis results for biochar prepared from giant reed biomass by pyrolysis
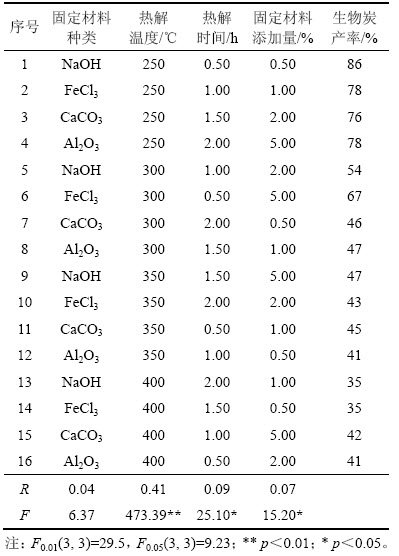
表2 生物炭中As,Cd和Pb的固定率
Table 2 Stabilization rate of As, Cd and Pb in biochar

通过激光粒度分析仪测定发现:在热解过程中添加FeCl3得到的生物炭比表面积明显增大,达到0.31 m2/mg,明显大于在热解过程中添加NaOH,CaCO3和Al2O3所得生物炭的比表面积,其相应的比表面积依次为0.13,0.13和0.21 m2/mg。这与表2中相应的Cd固定率较高的生物炭的比表面积一致。上述结果表明,Cd的固定可能与生物炭的比表面积有关。
将适宜热解条件下制备出的生物炭中的重金属进行连续提取,结果见图2。从图2可以看出:添加固定材料NaOH后热解制备的生物炭中As主要以残渣态存在,质量分数为58.3%, 其次为可氧化态,质量分数为35.1%。添加其他固定材料热解制备的生物炭中As主要以可氧化态存在,质量分数为42.0%~ 59.6%;添加固定材料后FeCl3热解制备的生物炭中Cd主要以残渣态存在,质量分数为45.7%。其次为可氧化态,质量分数为29.8%。 添加其他固定材料热解制备的生物炭中Cd主要以残渣态存在,其质量分数范围为45.8%~51.6%。添加固定材料CaCO3热解制备的生物炭中的Pb主要以氧化态形式存在,质量分数为47.5%。其次为酸提取态,质量分数为19.5%。添加其他固定材料热解制备生物炭中Pb主要以氧化态形式存在,其质量分数范围为54.6%~85.6%。
与未添加固定材料生物炭相比,添加固定材料后,生物炭中Cd可氧化态,酸提取态质量分数增加,残渣态减少,Cd 的4种形态整体变化不大;Pb 的4种形态变化程度不一,FeCl3的添加使得Pb可氧化态大幅度升高,残渣态Pb质量分数降低,NaOH和Al2O3的添加使得酸提取态质量分数有所增大;添加固定材料后可氧化态As质量分数均得到提高,FeCl3,CaCO3和Al2O3使得As残渣态质量分数降低,NaOH通过As的残渣态质量分数增大这一机理使得As得到固定;FeCl3通过提高Pb可氧化态质量分数使Pb得到固定。

图1 添加不同固定材料热解后生物炭的电镜照片
Fig. 1 SEM images of biochar prepared by adding fixed material

图2 添加固定材料热解制备的生物炭中As,Cd和Pb的赋存形态
Fig. 2 Speciation of As, Cd and Pb in biochar pyrolysised by adding fixed material
上述结果表明:添加不同固定材料后热解制备的生物炭中Cd主要以残渣态存在,Pb主要以可氧化态存在,As主要以残渣态和可氧化态2种形态存在。固定材料对生物质中重金属的固定作用通过提高残渣态的质量分数和降低可氧化态的质量分数得到实现,且添加不同固定材料后,Cd各种形态所占百分比变化不明显。添加固定材料NaOH后,热解制备的生物炭中As残渣态质量分数和Pb的残渣态质量分数明显提高,表明NaOH是含重金属生物质热解制备生物炭过程中比较适宜的重金属固定材料。
3 结论
1) 芦竹收获物热解制备生物炭产率可达到35%~86%,热解温度对生物炭产率影响显著。在250 ℃时添加质量分数为0.5%的NaOH、热解0.50 h,其生物炭产率可达86%。
2) 利用含重金属的生物质热解制备生物炭,生物炭中As最适宜的固定材料为NaOH,添加质量分数为2%,热解温度为300 ℃,热解时间为2.00 h;生物炭中Cd最适宜的固定材料为FeCl3,添加质量分数为5%,热解温度为250 ℃,热解时间为0.50 h;生物炭中Pb最适宜的固定材料为CaCO3,热解温度为400 ℃,添加质量分数为5%,热解时间为1.00 h。在热解过程中添加FeCl3得到的生物炭比表面积达到0.31 m2/mg,生物炭比表面积显著增加促进了其中重金属固定率提高。
3) 添加不同固定材料后热解制备出的生物炭中重金属进行连续提取,添加固定材料NaOH后热解制备的生物炭中As主要以残渣态存在,其次为可氧化态;添加其他固定材料热解制备的生物炭中As主要以可氧化态存在;添加不同固定材料后热解制备的生物炭中Cd主要以残渣态存在而生物炭中Pb主要以可氧化态存在。NaOH是含重金属生物质热解制备生物炭过程中比较适宜的重金属固定材料。
参考文献:
[1] YAN X L, CHEN T B, LIAO X Y, et al. Arsenic transformation and volatilization during incineration of the hyperaccumulator Pterisvittata L[J]. Environmental Science & Technology, 2008, 42(5): 1479-1484.
[2] LU S, DU Y, ZHONG D, et al. Comparison of trace element emissions from thermal treatments of heavy metal hyperaccumulators[J]. Environmental Science & Technology, 2012, 46(9): 5025-5031.
[3] BARBAROUX R, PLASARI E, MERCIER G, et al. A new process for nickel ammonium disulfate production from ash of the hyperaccumulating plant Alyssummurale[J]. Science of the Total Environment, 2012, 423(8): 111-119.
[4] CAO X, MA L, SHIRALIPOUR A, et al. Biomass reduction and arsenic transformation during composting of arsenic-rich hyperaccumulator Pterisvittata L[J]. Environmental Science and Pollution Research, 2010, 17(3): 586-594.
[5] GHOSH M, SINGH S P. A review on phytoremediation of heavy metals and utilization of its byproducts[J]. Applied Ecology and Environmental Research, 2005, 3(1): 1-18.
[6] ANDERSON C W N, BROOKS R R, CHIARUCCI A, et al. Phytomining for nickel, thallium and gold[J]. Journal of Geochemical Exploration, 1999, 67(1/2/3): 407-415.
[7] SHEORAN V, SHEORAN A S, POONIA P. Phytomining: a review[J]. Minerals Engineering, 2009, 22(12): 1007-1019.
[8] SHEORAN V, SHEORAN A S, POONIA P. Phytomining of gold: a review[J]. Journal of Geochemical Exploration, 2013, 128: 42-50.
[9] 李宁, 吴龙华, 孙小峰, 等. 修复植物产后处置技术现状与展望[J]. 土壤, 2005, 37(6): 587-592.
LI Ning, WU Longhua, SUN Xiaofeng, et al. Techniques for disposal or reuse of phytoremediating plants-present and future[J]. Soils, 2005, 37(6): 587-592.
[10] KOPPOLU L, CLEMENTS L D. Pyrolysis as a technique for separating heavy metals from hyperaccumulators. Part Ⅰ: Preparation of synthetic hyperaccumulator biomass[J]. Biomass and Bioenergy, 2003, 24(1): 69-79.
[11] KOPPOLU L, AGBLEVOR F A, CLEMENTS L D. Pyrolysis as a technique for separating heavy metals from hyperaccumulators. Part Ⅱ: Lab-scale pyrolysis of synthetic hyperaccumulator biomass[J]. Biomass and Bioenergy, 2003, 25(6): 651-663.
[12] KOPPOLU L, PRASAD R, DAVIS CLEMENTS L. Pyrolysis as a technique for separating heavy metals from hyperaccumulators. Part Ⅲ: Pilot-scale pyrolysis of synthetic hyperaccumulator biomass[J]. Biomass and Bioenergy, 2004, 26(5): 463-472.
[13] LIU W J, TIAN K, JIANG H, et al. Selectively improving the bio-oil quality by catalytic fast pyrolysis of heavy-metal-polluted biomass: take copper (Cu) as an example[J]. Environmental Science & Technology, 2012, 46(14): 7849-7856.
[14] DEMIRBAS A. Combustion characteristics of different biomass fuels[J]. Progress in Energy and Combustion Science, 2004, 30(2): 219-230.
[15] SAS-NOWOSIELSKA A, KUCHARSKI R, MAKOWSKI E, et al. Phytoextraction crop disposal: An unsolved problem[J]. Environmental Pollution, 2004, 128(3): 373-379.
[16] 邢前国, 潘伟斌. 富含Cd、Pb植物焚烧处理方法的探讨[J]. 生态环境, 2004, 13(4): 585-586, 600.
XING Qianguo, PAN Weibin. On incineration of plants with high concentration of cadmium and lead[J]. Ecology and Environment, 2004, 13(4): 585-586, 600.
[17] 刘维涛, 倪均成, 周启星, 等. 重金属修复植物有害生物量的处理技术研究进展[C]// 农业环境与生态安全―第五届全国农业环境科学学术研讨会论文集. 2013: 417-428.
LIU Weitao, NI Juncheng, ZHOU Qixing, et al. Research progress of disposal technology for hazardous biomass of heavy metal remediation plants[C]// The Security of Agriculture Environment and Ecology: The Fifth Session of the National Agricultural Academic Conference on Environmental Science. 2013: 417-428.
[18] DEMIRBAS A, ARIN G. An overview of biomass pyrolysis[J]. Energy Sources, 2002, 24(5): 471-482.
[19] LIEVENS C, YPERMAN J, VANGRONSVELD J, et al. Study of the potential valorisation of heavy metal contaminated biomass via phytoremediation by fast pyrolysis. Part Ⅰ: Influence of temperature, biomass species and solid heat carrier on the behaviour of heavy metals[J]. Fuel, 2008, 87(10/11): 1894-1905.
[20] CAO X D, MA L, GAO B, et al. Dairy-manure derived biochar effectively sorbs lead and atrazine[J]. Environmental Science & Technology, 2009, 43(9): 3285-3291.
[21] 戴静, 刘阳生. 生物炭的性质及其在土壤环境中应用的研究进展[J]. 土壤通报, 2013, 44(6): 1520-1525.
DAI Jing, LIU Yangsheng. Review of research on the properties of biochar and its applications in soil[J]. Chinese Journal of Soil Science, 2013, 44(6): 1520-1525.
[22] 夏娟娟, 钟慧琼, 赵增立, 等. 修复植物热解过程中重金属元素迁移行为的研究[J]. 生态环境学报, 2010, 19(7): 1696-1699.
XIA Juanjuan, ZHONG Huiqiong, ZHAO Zengli, et al. Study on transfer behavior of heavy metals during pyrolysis of phytoremediating plant[J]. Ecology and Environmental Science, 2010, 19(7): 1696-1699.
[23] RAURET G, LOPEZ-SANCHEZ J F, SAHUQUILLO A, et al. Improvement of the BCR three step sequential extraction procedure prior to the certification of new sediment and soil reference materials[J]. Journal of Environmental Monitoring, 1999, 1(1): 57-61.
[24] HJ 557―2010, 固体废物浸出毒性浸出方法―水平振荡法[S].
HJ 557―2010, Solid waste-Extraction procedure for leaching toxicity-Horizontal vibration method[S].
[25] 王秦超, 卢平, 黄震, 等. 生物质低温热解炭化特性的实验研究[J]. 中国电机工程学报, 2012, 32(S1): 121-126.
WANG Qinchao, LU Ping, HUANG Zhen, et al. Experimental study on low temperature pyrolysis of biomass[J]. Proceeding of the CSEE, 2012, 32(S1): 121-126.
[26] 杨海平, 陈汉平, 晏蓉, 等. 温度对生物质固定床热解影响的研究[J]. 太阳能学报, 2007, 28(10): 1152-1157.
YANG Haiping, CHEN Hanping, YAN Rong, et al. The influence of temperature on biomass pyrolysis in fixed bed[J]. Acta Energiae Solaris Sinica, 2007, 28(10): 1152-1157.
[27] 杨凯. 金属盐催化生物质热解动力学特性研究[J]. 环境保护与循环经济, 2011, 31(10): 50-55.
YANG Kai. The research of dynamic characteristics of metal salts catalytic biomass pyrolysis[J]. Environmental Protection and Cycle Economy, 2011, 31(10): 50-55.
(编辑 陈灿华)
收稿日期:2015-07-22;修回日期:2015-09-18
基金项目(Foundation item):国家自然科学基金资助项目(21577176,41271330) (Projects(21577176, 41271330) supported by the National Natural Science Foundation of China)
通信作者:郭朝晖,博士,教授,主要从事重金属污染土壤生态修复与固体废物无害化资源化研究;E-mail: zhguo@csu.edu.cn