ϡ�н��� 2013,37(03),461-467
�ڻ����Ȼ�����������ѧ����
���� ��� ��һ�� ���ǹ� ��־ ����
����������ѧұ������Դ����ѧԺ
����ʡ������ɫ������Դ������ù����ص�ʵ������������
ժ Ҫ��
ͨ������ѧ����,���Ƴ�Au-Te-Cl-H2OϵE-pHͼ,��������ڻ�����������������ϵ�пɱ��ܽ����ڻ����Ȼ�������,������AuCl4-���ڻ���,����ҺpH<3.7ʱ,Te(��)�Ļ�����ΪHTeO2+;��pH>3.7ʱ���Բ����Ե�H2TeO3���ڡ�ͬʱ̽����AuCl4-��ȷֱ�Ϊ1��10-4,1��10-2,1ʱ,��Au-Cl-H2OϵE-pHͼ��AuCl4-��Au(OH)3�ȶ������Ӱ�졣�������,AuCl4-���Խ��,���ȶ�����Խխ,���γ�Au(OH)3��pHֵԽ�͡�
�ؼ��ʣ�
�ڻ��� ;������ ;E-pHͼ ;�Ȼ����� ;
��ͼ����ţ� TF831
����飺 ����(1986-),Ů,���ϴ�����,˶ʿ�о���;�о�����:��ɫ����ұ��; ���(E-mail:kglj1010@163.com);
�ո����ڣ� 2013-01-09
���� ������Ȼ��ѧ������Ŀ(51274108)����; ����������ѧ2009����л���(KKZ4200727003)����;
Thermodynamic Analysis of Gold Telluride Chlorination Leaching Process
Abstract��
Pourbaix diagrams(potential/pH diagrams) for Au-Te-Cl-H2O system were presented based on the principle and calculation of thermodynamic analysis.It could be confirmed that chlorination leaching of gold telluride was feasible,AlCl-4 and telluride(��) would be generated.When pH<3.7,telluride(��) existed as HTeO+2;while,telluride(��) was insoluble H2TeO3 when pH>3.7.The effects of AlCl-4 activities(1��10-4,1��10-2,1) on the stable region of AlCl-4 and Au(OH)3 were discussed.The Pourbaix diagrams showed that the bigger the AlCl-4 activities were,the narrower the stable range of AlCl-4 and the lower the pH value to form Au(OH)3 was.
Keyword��
gold telluride;copper anode slime;pourbaix diagrams;chlorination leaching;
Received�� 2013-01-09
Ŀǰ, �ҹ��ѳ�Ϊȫ���һ������
[1 ,2 ]
, �ƽ��ܲ�����1/4(����ƽ����Ϊ13%)Ϊ������, �������Ʒ��Ҫ����ͭ�� Ǧ����ɫ����ұ�����������������ࡣ ������ɫ����ұ�����ղ�������, ͭ�� Ǧ����ɫ������������, ��ұ��Ʒ��ͭ�� Ǧ���������Ҳ����������, 2006�������������괦����Ϊ55000��
[3 ]
�� ��ͭ���������ۺϻ��ս� ���� ���� �ڵ��м�Ԫ��һֱ�ܵ��㷺���Ӻͳ����о�
[4 ,5 ,6 ,7 ,8 ,9 ,10 ,11 ,12 ,13 ]
�� ͭ���������һ��Ϊ0.3%��1.0%(ռ����ͭ��������������), ͨ����Au, Ag, Cu, Se, Te, Pb, As, Sb, Bi, Fe, Ni, S������Ԫ�ص�
[14 ]
, ����Ƚϸ��ӡ� Ŀǰ��ͭ���������ۺϻ��ս� �����м�Ԫ�صķ����϶�, ��Ҫ��: ��-��ⷨ���ա� ѡ��-ұ�����Ϲ��ա� ȫʪ���������յ�
[15 ,16 ,17 ,18 ,19 ,20 ]
�� ͭ����������ڵķ�����Ҫ��: ����շ��� ��ѹ������� ����������� ҺĤ���뷨�� �ܼ���ȡ���� ����� ͭ�ۻ�ԭ����
[21 ]
��
ͭ�������н�Ĵ�����ʽ��Ҫ�ǵ��ʽ�(Au0 )���ڻ���(AuTe2 ), ����ij��ͭ��������Au0 ��AuTe2 �����ֱ�Ϊ0.3165%��748.32 g��t-1
[22 ]
�� �ڻ�-��ⷨ������, ���������ữ���մ���������ʱ, AuTe2 ��תΪTeO2 ���ͷų�Au0 ; ��ʪ�����մ���������(���Ȼ�����)ʱ, Au0 ���Ȼ�����������-��λ�Ĺ���, ��������λȡ�������ɵĽ����������ȶ��������ض��Ľ�������
[23 ,24 ,25 ]
�� ͨ��Au0 �Ȼ�������Au-Cl-H2 Oϵ��λ-pHͼ, ������ѧ�Ƕ�ȷ��Au0 �Ȼ������Է����еķ�Ӧ�����Լ���Ӧ��ϵ�и������ȶ����ڵ�����
[26 ]
�� ����ͨ������ѧ����, ���Ƴ�AuTe2 �Ȼ������ĵ�λ-pHͼ, ���������Ȼ�����������, AuTe2 �Ȼ������������γɵĸ����ּ����ȶ�����, ΪAuTe2 ���Ȼ������ṩ�������ݡ�
1 ���ڻ����Ȼ��������̵�����ѧ����
����Ȼ�������ָ�������� ������(��)�� �������Ƽ�˫��ˮ����һ����Ϊ������, ��HCl-NaCl��Һ��H2 SO4 -NaCl��Һ���ܽ��
[27 ]
��
��ı��缫��λΪ
[25 ]
Au+ +e=Au E
0 A u + / A u =1.691 V (1)
Au3+ +3e=Au E
0 A u 3 + / A u =1.498 V (2)
��E
0 A u + / A u ��E
0 A u 3 + / A u ����, ����ˮ��Һ�н��ȶ�, ������������Һ��Ҫ�ߵ缫��λ���������� ���������� ������(��) �ʹ�������Ϊ������ʱ, ���������µı��缫��λ�ֱ�Ϊ
Cl2 +2e=2Cl- E
0 C l 2 / C l - =1.36 V (3)
ClO- 3 +6H+ +6e=Cl- +3H2 O E
0 C l �� - 3 / C l - =1.45 V (4)
HClO+H+ +2e=Cl- +H2 O E
0 �� C l �� / C l - =1.49 V (5)
�ӱ��缫��λ����, ������ ������(��) �ʹ���������Ϊ��������������ʹ���ʽ�����, ������Һ�д���������ʱ, ������������������������ȶ���AuCl- 4 ��AuCl- 2 , ʹ���ܽ�����缫��λ�����½�
[26 ]
�� ���������µı��缫��λΪ
AuCl- 2 +e=Au+2Cl- E
0 A u C l - 2 / A u =1.13 V (6)
AuCl- 4 +3e=Au+4Cl- E
0 A u C l - 4 / A u =0.99 V (7)
��ʽ(6)��(7)��֪, ���Ȼ��ܽ������, ����ѧ�ϸ���������AuCl- 4 ���ֵ���̬���ڡ� ��״̬��, ���������ӵ���Һ��, ֻҪ�������ı��缫��λ����0.99 V, ���ɽ����ʽ�����ΪAuCl- 4 �� ��������������Һ�ܽⵥ�ʽ�ʱ�ķ�Ӧʽ����
2Au+ClO- 3 +6H+ +7Cl- =2AuCl- 4 +3H2 O (8)
�ڻ���Ϊ��б����, �ʰ�ɫ�����ɫ; ��Au-Te��Ԫ��ͼ��, �������γ�Ψһ�ȶ��Ļ�����AuTe2
[28 ]
; X�����չ����о��������, AuTe2 �н�Ļ��ϼ�Ϊ+1��
[29 ,30 ]
�� AuTe2 ����HNO3 �γɺ�ɫ��ij���; ��ŨH2 SO4 �м��ȳ����ɫ
[31 ]
; �ڳ��õĽ��������軯� ���弰�����������Һ��, AuTe2 �Ƚ��Ѵ���, ͬʱ����AuTe2 �ڽ�������в���TeO
2 - 3 , �����ƽ���������, ��˽���Ч�������롣 ��AuTe2 �Ľ���ڽ���ǰ�����Ԥ����, �籺�ա� ��ѧ������ ��ѹ�����ϸ��������Ԥ�ȷֽ�AuTe2
[32 ,33 ,34 ]
�� ����ѧ����
[35 ]
�͵绯ѧ�о��������, ��1 mol��L-1 ��������Һ��, ���缫��λ����0.5 Vʱ, AuTe2 �е��ڱ�����ΪTe(��), ͬʱ���������Au0 , pH<2ʱ, ��ҪΪHTeO+ 2 , pH>2ʱ, ��ҪΪH2 TeO3 ����
[36 ]
��
�ڻ����Ȼ�������ӦΪ:
pH<2��ˮ��Һ
3AuTe2 +4ClO- 3 +6H+ =3Au+6HTeO+ 2 +4Cl- (9)
pH>2��ˮ��Һ
3AuTe2 +4ClO- 3 +6H2 O=3Au+6H2 TeO3 +4Cl- (10)
AuTe2 �Ȼ�����ʱ�������ɵ��ʽ�Au0 , Au0 ��һ������������AuCl- 4 ��ʽ������Һ�� ���AuTe2 �Ȼ��������ܷ�Ӧ����Ϊ
6AuTe2 +11ClO- 3 +30H+ +13Cl- =6AuCl- 4 +12HTeO+ 2 +9H2 O (11)
6AuTe2 +11ClO- 3 +18H+ +13Cl- +3H2 O=6AuCl- 4 +12H2 TeO3 (12)
��1Ϊ298.15 K����Ҫ���ʵ����ɼ���˹������
[37 ]
�� �Ա�1�е����ݼ����298.15 Kʱ, ��Ӧ(11)��(12)�ı�����˹�����ֱܷ�Ϊ-4549.46��-4803.36 kJ��mol-1 , ����AuTe2 �ܱ������������γɽ�����Һ��
2 Au-Te-Cl-H2O��E-pHͼ
��ʪ��ұ�������, �ض��ķ�Ӧ������, E-pHͼ��ֱ�۵ط�ӳ�������ȶ����ڵ�����͵缫��λ, Ϊ������ ������ ����ṩ����ѧ����
[39 ,40 ,41 ,42 ,43 ]
��
����Au-Te-Cl-H2 Oϵ����Ҫ�ķ�Ӧ����ʽ, ��298.15 K�������ϵ�и���Ӧƽ���E��pH��ϵʽ, ����2��ʾ��
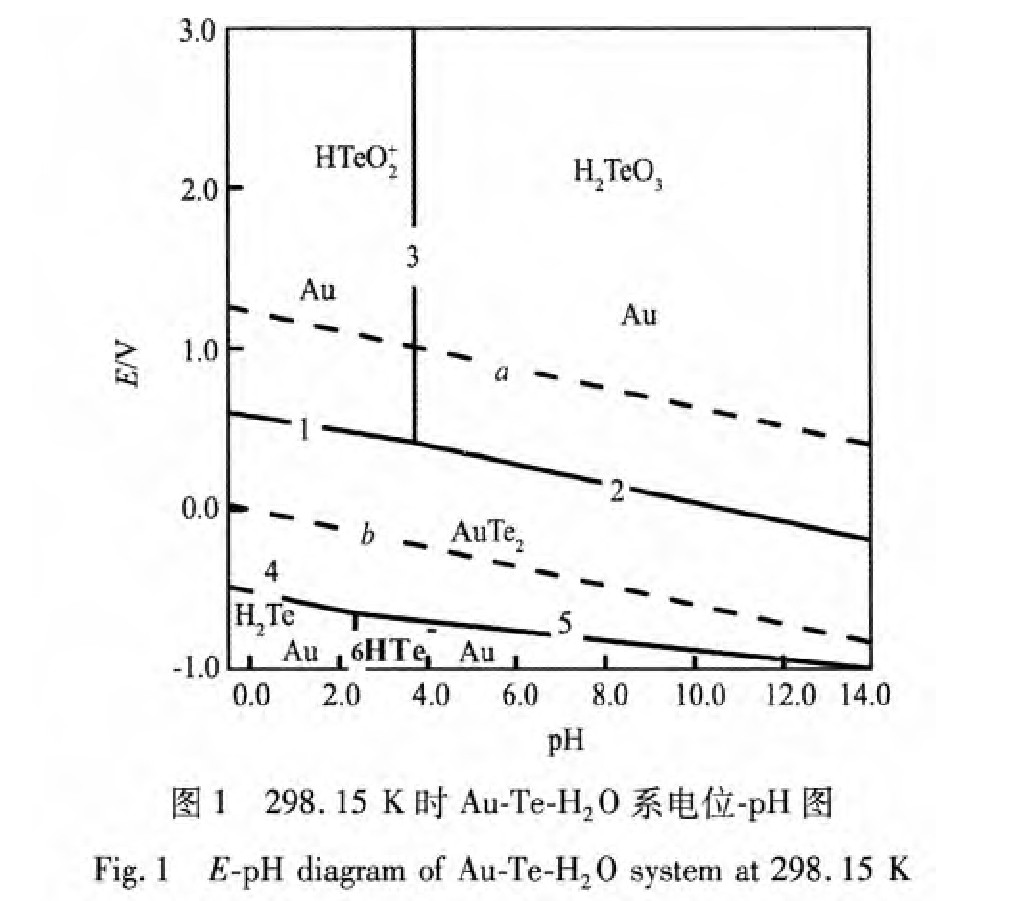
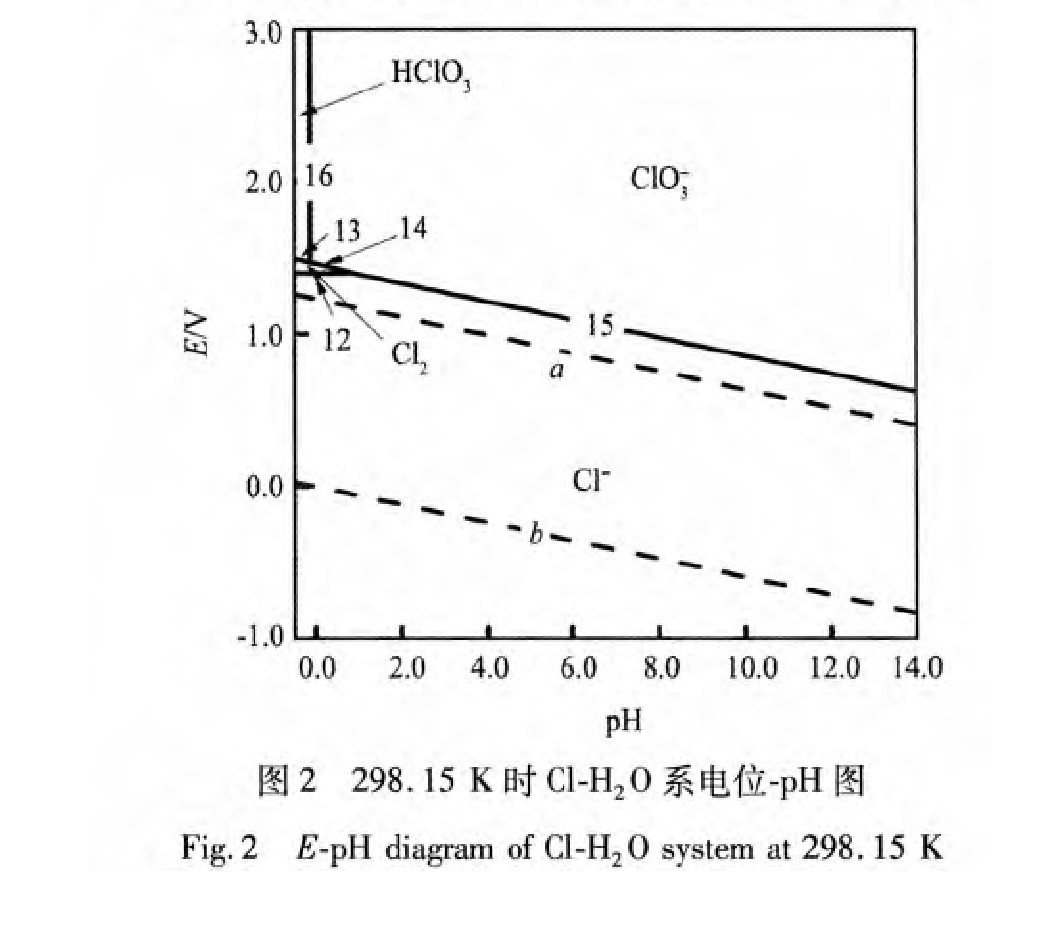
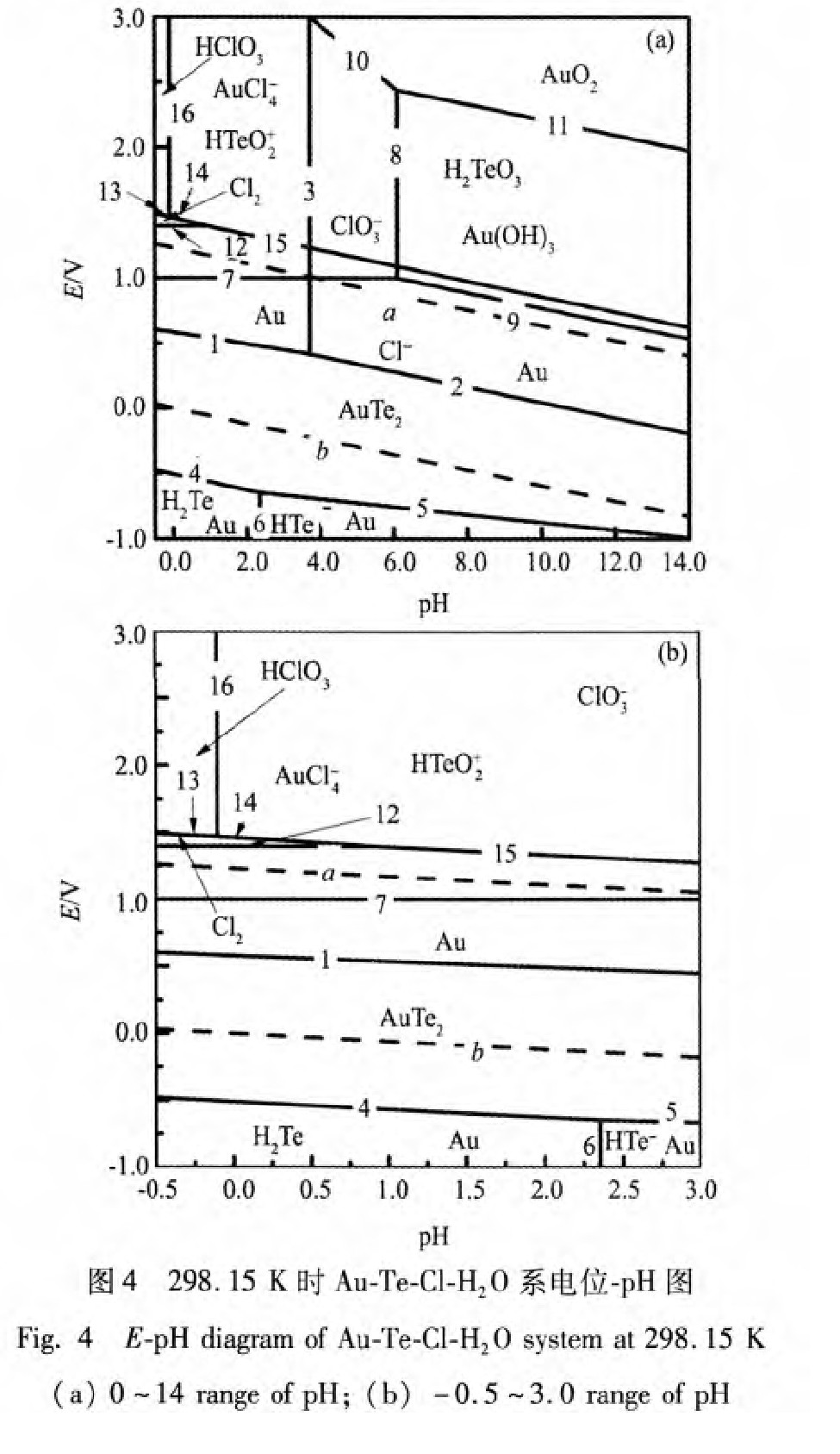
���ձ�2��ƽ���ϵʽ, �ֱ���Ƴ�Au-Te-H2 Oϵ��Cl-H2 Oϵ��E-pHͼ, ��ͼ1��2, ����a HTeO+ 2 , a H2 Te , a HTe- , a Cl- , pCl2 , a HClO3 ��a ClO- 3 ��Ϊ1; Au-Cl-H2 OϵE-pHͼ��ͼ3, ����a AuCl- 4 �ֱ�Ϊ1��10-4 , 1��10-2 , 1, ��������ֵĻ�Ⱦ�Ϊ1�� Au-Te-Cl-H2 OϵE-pHͼ��ͼ4(a), ���и����ֵĻ�Ⱦ�Ϊ1�� ����Ȼ�����ͨ������Һ���������Ի�����, ��˻���pH��ΧΪ-0.5��3.0��Au-Te-Cl-H2 Oϵ�ֲ�E -pHͼ, ��ͼ4(b)��ʾ��
��1298.15 KʱAu-Te-Cl-H2Oϵ��Ҫ���ʵı�����˹������
Table 1 G �� values of of substances in Au-Te-Cl-H 2 O system at 298.15 K
Substances
G �� /-1 )Substances
G �� /-1 )Substances
G �� /-1 )
Au
-14.1628
H2 Te
35.7983
H2 O
-306.683
H+
6.238344
HClO3
-146.976
H2 TeO3
-619.901
AuCl- 4
-407.994
HTe-
42.99478
Cl2
-59.6136
AuTe2
-60.8241[38]
ClO- 3
-153.8
Au(OH)3
-481.817
HTeO+ 2
-328.139
Cl-
-190.217
AuO2
114.9665[26]
e
-25.702
��2 298.15 Kʱ Au-Te-Cl-H2O��ϵ�ķ�Ӧʽ��E-pH����ʽ
Table 2 Equilibrium reactions of Au-Te-Cl-H 2 O system and E -pH equations at 298.15 K
Nos.
Reactions
Equations
a
O2 +4H+ +4e=2H2 O
E =1.229-0.0592pH
b
2H+ +2e=H2
E =-0.0592pH
1
Au+2HTeO+ 2 +6H+ +8e=AuTe2 +4H2 O
E =0.582-0.0444pH+0.0148lga HTeO+ 2
2
Au+2H2 TeO3 +8H+ +8e=AuTe2 +6H2 O
E =0.636-0.0592pH
3
H2 TeO3 +H+ =HTeO+ 2 +H2 O
pH=3.706-lga HTeO+ 2
4
AuTe2 +4H+ +4e=2H2 Te+Au
E =-0.508-0.0592pH-0.0296lga H2 Te
5
AuTe2 +2H+ +4e=2HTe- +Au
E =-0.578-0.0296pH-0.0296lga HTe-
6
H+ +HTe- =H2 Te
pH=2.353-lga H2 Te +lga HTe-
7
AuCl- 4 +3e=Au+4Cl-
E =1.001+0.0197lga AuCl- 4 -0.0789lga Cl-
8
Au(OH)3 +3H+ +4Cl- =AuCl- 4 +3H2 O
pH=6.077+1.333lga Cl- -0.333lga AuCl- 4
9
Au(OH)3 +3H+ +3e=Au+3H2 O
E =1.361-0.0592pH
10
AuO2 +4H+ +4Cl- +e=AuCl- 4 +2H2 O
E =3.883-0.2368pH+0.2368lga Cl- -0.0591lga AuCl- 4
11
AuO2 +H+ +H2 O+e=Au(OH)3
E =2.805-0.0592pH
12
Cl2 +2e=2Cl-
E =1.396+0.0296lgp Cl2 -0.0592lga Cl-
13
2HClO3 +10H+ +10e=Cl2 +6H2 O
E =1.462-0.0592pH-0.00592lgp Cl2 +0.0118lga HClO3
14
2ClO- 3 +12H+ +10e=Cl2 +6H2 O
E =1.461-0.0710pH+0.0118lga ClO- 3 -0.00592lgp Cl2
15
HCl- 3 +6H+ +6e=Cl- +3H2 O
E =1.450-0.0592pH+0.00987lga HClO- 3 -0.00987lga Cl-
16
ClO- 3 +H+ =HClO3
pH=-0.103-lga HClO3 +lga ClO- 3
3 �� ��
��ͼ1�ɼ�, ������Ϊ���������Ȼ�������ϵ��, AuTe2 �е��ڱ������γ�Te(��)�Ļ�����, ���Ե��ʽ��������; ����ҺpH<3.7ʱ����HTeO+ 2 ,pH>3.7ʱ������H2 TeO3
[36 ]
��
��ͼ3�ɼ�, ����������������, ���ʽ��������Ȼ�������Һ���γ�AuCl- 4 ; ���ʽ���������������Һ���γ�Au(OH)3 , ��˽���Ȼ�����ͨ��ѡ��������Һ��ϵ; a AuCl- 4 ���ֱ�Ϊ1��10-4 , 1��10-2 , 1ʱ, AuCl- 4 ת��ΪAu(OH)3 ������pHֵ�ֱ�Ϊ7.40, 6.74��6.08, ����a AuCl- 4 ������ʱ, a AuCl- 4 ���ȶ�����խ, Ҳ����AuCl- 4 �ȶ�����������AuCl- 4 ��Ũ�ȵ�����Ӱ�졣
��ͼ4(a)�ɼ�, ��������������Һ��ϵ�����ȶ����ڵ�����, ������ѧ�Ƕ�˵��AuTe2 ���Ȼ��������п����ԡ� ������ϵ��, ����������ɵ������Խ�ȶ�, �������ڽ�Ľ���, AuCl- 4 ���ȶ�����Ϊ1��1026 , ���ѡ��������Ϊ������ʱ, ����������Һ��ϵ�����γ�AuCl- 4 ������Һ
[23 ]
��
�ۺ�ͼ1��ͼ4��E -pHͼ�������Կ���, AuTe2 ��������������Һ�пɱ�����, �γ�Te(��)�Ļ������AuCl- 4 �� ʵ�ʽ���������, ��pH<1��������+�Ȼ���Ϊ������, ��ͼ4(b)��ʾ, AuTe2 ��������ȫ���Ȼ�������Ӧ, ����AuCl- 4 ��HTeO+ 2 ��
4 �� ��
1. ͨ������ѧ����, ���Ƴ�298.15 KʱAu-Te-Cl-H2 Oϵ�ĵ�λ-pHͼ, ����AuTe2 ��������������Һ�н����ǿ��е�, ����ΪTe(��)�Ļ�����͡�
2. ����ҺpH<3.7ʱ, Te(��)�Ļ������Կ��ܵ���ʽ����, ��pH>3.7ʱ���Բ����ԵĴ��ڡ�
3. �������ʱ, �ȶ������խ, ���γ�Au(OH)3 ������pH����С, �ȶ�����������Ũ�ȵ�����ѧ����Ӱ�졣
�����
[1] Zhang Y T.Development status and future prospect ofChina's gold industry[J].Gold,2011,32(6):1.(������.�й��ƽ�ҵ��չ��״��δ��չ��[J].�ƽ�,2011,3(6):1.)
[2] Zhou Y K.Development of associated gold/sliver ex-traction technology in China[J].Chinese Journal ofRare Metals,1996,20(3):217.(��һ��.�ҹ�����������ȡұ������չ[J].ϡ�н���,1996,20(3):217.)
[3] Green M A.Improved estimates for Te and Se availa-bility from Cu anode slimes and recent price trends[J].Prog.Photovolt.Res.Appl.,2006,14:743.
[4] Syed S.A green technology for recovery of gold fromnon-metallic secondary sources[J].Hydrometallurgy,2006,82:48.
[5] Wang X L,Zhang X H.Discussion on process for trea-ting copper anode Slime[J].Mining&metallurgy,2005,14(4):46.(��С��,��꿺�.ͭ�����ദ�����յ�̽��[J].��ұ,2005,14(4):46.)
[6] Li H R,Chen J H,Xu Q X,He X C,Zhai Z B.Goldrecovery by chloridization leaching of lead anode slime[J].Journal of Kunming University of Science andTechnology(Science and Technology),2011,36(5):14.(���,�¼һ�,������,������,���б�.�Ȼ�����Ǧ��������ս���о�[J].����������ѧѧ��(��Ȼ��ѧ��),2011,36(5):14.)
[7] Zheng Y J,Wang B,Shi J Y,Sun Z M,Liu Z C.Pretreatment of copper anode slime for concentrating goldand silver[J].Journal of Central South University,2010,41(3):865.(֣�Ž�,����,ʷ��Զ,������,���ѳ�.ͭ������Ԥ���������������о�[J].���ϴ�ѧѧ��,2010,41(3):865.)
[8] Xia G X,Shi W,Fang Z Y.Hydrometallurgicalprocess study on treating copper anodic slurry[J].Nonferrous metals(Extractive Metallurgy),2002,(1):29.(�Ĺ���,ʯΰ,������.ͭ������ȫʪ�����������о�[J].��ɫ����(ұ������),2002,(1):29.)
[9] Wang A R.Research on optimization process for leac-hing of gold from copper slime[J].Hydrometallurgy ofChina,2007,26(1):44.(������.��ͭ��������ʪ����ȡ��Ĺ����Ż��о�[J].ʪ��ұ��,2007,26(1):44.)
[10] Translated selectively by Wang Y H.A new hydromet-allurgical process for treating copper anode slimes[J].China Nonferrous Metallurgy,2009,(3):8.(������ժ��.ʪ������ͭ��������·���[J].�й���ɫұ��,2009,(3):8.)
[11] Guo X Y,Xiao C M,Zhong J Y,Tian Q H.Behaviorsof precious metals in process of copper anode slime treat-ment[J].The Chinese Journal of Nonferrous Metals,2010,20(5):990.(��ѧ��,Ф��÷,�Ӿ�ѿ,���컪.ͭ�����ദ�������й��������Ϊ[J].�й���ɫ����ѧ��,2010,20(5):990.)
[12] Quinet P,Proost J,Van A L.Recovery of preciousmetals from electronic scrap by hydrometallurgical pro-cessing routes[J].Min.Metall.Process,2005,22(1):17.
[13] Sheng P P,Etsell T H.Recovery of gold from comput-er circuit board scrap using aqua regia[J].Waste Man-age.Res.,2007,25(4):380.
[14] Zhong P,Huang Z Q.The present situation of the re-search on gold chlorinationis reviewed[J].JiangxiChemical Industry,1996,(4):16.(��ƽ,����Ȫ.�Ȼ�����빤�յ��о���Ӧ��[J].��������,1996,(4):16.)
[15] Cui J,Zhang L.Metallurgical recovery of metals fromelectronic waste:a review[J].J.Hazard.Mater,2008,158:228.
[16] Fleming C A.Hydrometallurgy of precious metals re-covery[J].Hydrometallurgy,1992,30:127.
[17] Yap C Y,Mohamed N.An electro-generative processfor the recovery of gold from cyanide solutions[J].Chemosphere,2007,67:1502.
[18] Syed S.Recovery of gold from secondary sources��areview[J].Hydrometallurgy,2012,115-116:30.
[19] Kang L W,Wang Q Y.Discussion on hydrometallurgi-cal process for copper anode slime[J].World Nonfer-rous Metal,2011,(11):52.(������,������.ͭ������ʪ���������ճ�̽[J].������ɫ����,2011,(11):52.)
[20] B��nyamin D��nmez,Zafer Ekinci,Cafer C elik,Sabri Colak.Optimisation of the chlorination of gold in decop-perized anode slime in aqueous medium[J].Hydromet-allurgy,1999,52:81.
[21] Zheng Y J,Sun Z M.Progress in recovery of telluriumfrom copper anode slime and preparation of new materialswith tellurium[J].Chinese Journal of Rare Metals,2011,35(4):593.(֣�Ž�,������.ͭ�������л����ڼ����²����Ʊ�������չ[J].ϡ�н���,2011,35(4):593.)
[22] Sun Z.Handbook of Heavy Non-Ferrous Metal Smel-ting Design:About Sn,Te,Hg and Noble Mental[M].Beijing:Metallurgical Industry Press,1995.703.(��پ.����ɫ����ұ������ֲ�:����������[M].����:ұ��ҵ������,1995.703.)
[23] Wang Z K,Chen D H,Chen L.The analysis of goldleaching systems based on thermodynamics[J].Chinesejournal of Nonferrous Metals(Extractive Metallurgy),2006,(3):36.(���ο�,�¶���,����.��������ѧ������ϵ����[J].��ɫ����(ұ������),2006,(3):36.)
[24] Wang Z K,Ye C L,Fan S L,Chen D H.Eh-pH dia-grams and thermodynamic analysis of gold leaching sys-tems[J].Chinese Journal of Nonferrous Metals(Ex-tractive Metallurgy),2008,(3):37.(���ο�,Ҷ����,��˳��,�¶���.������ϵ�ĵ�λ-pHͼ��������ѧ����[J].��ɫ����(ұ������),2008,(3):37.)
[25] Wang Z K,Chen D H,Chen L.Thermodynamic anal-ysis of common regularities for gold chlorination[J].Chinese Journal of Rare Metals,2006,30(5):703.(���ο�,�¶���,����.����ѧ�����Ȼ�������ϵ����[J].ϡ�н���,2006,30(5):703.)
[26] Kim C S,Zhang T A,Mou W Z,Zheng D L,Zeng Y,Jiang X L.Thermodynamics of gold chlorination leac-hing process[J].Chinese Journal of Rare Metals,2012,36(1):129.(��ʯ,���Ӱ�,IJ����,֣��¼,����,��Т��.Һ�Ȼ��������������ѧ[J].ϡ�н���,2012,36(1):129.)
[27] Yang T Z.Noble Metals Metallurgy and Product Pro-cessing[M].Changsha:Central South University ofPress,2005.(������.�����ұ��Ʒ��ӹ�[M].��ɳ:���ϴ�ѧ������,2005.)
[28] Okamoto H,Massalskl T B.The Au-Te(gold-telluri-um)system[J].Bulletin of Alloy Phase Diagrams,1984,5(2):172.
[29] Ettema A,Stegink T A,Haas C.The valence of Au inAuTe2 and AuSe studied by X-ray absorption[J].Spec-troscopy Solid State Communications,1994,90(3):211.
[30] Schutte W J,Deboer J L.Valence fluctuations in theincommensurately modulated structure of calaveriteAuTe2[J].Acta Crystallographica Section B,1988,44(5):486.
[31] Cai C J.The Handbook of Identification of Gold Miner-als[M].Beijing:Atomic Energy Press,1993.1.(�̳���.���������ֲ�[M].����:ԭ���ܳ�����,1993.1)
[32] Jing Z.Mechanism and kinetics of mineral transforma-tion under hydrothermal conditions:calaverite to metallicgold[J].American Mineralogist,2009,94:1541.
[33] Jing Z.A novel pre-treatment of calaverite by hydro-thermal mineral replacement reactions[J].Minerals En-gineering,2010,23:451.
[34] Climo M.Biooxidation as pre-treatment for a telluride-rich refractory gold concentrate[J].Minerals Engineer-ing,2000,13(12):1219.
[35] Zhdanov S I.Standard Potentials in Aqueous Solution(Edited by A.J.Bard,R.Parsons and J.Jordan),IUPAC 115.Marcel Dekker,New York,1985.
[36] Jayaasekera S.The electrochemical oxidation of goldtelluride in perchloric acid solutions[J].ElectrochimicaActa,1996,41(6):879.
[37] Yang X W.Handbook of Thermodynamic Data in A-queous Solutions at High Temperature[M].Beijing:Metallurgical Industry Press,1983.523.(������.����ˮ��Һ����ѧ���ݼ����ֲ�[M].����:ұ��ҵ������,1983.523.)
[38] Ye D L,Hu J H.The Applied Handbook of the Ther-modynamics of Organic Compounds[M].Beijing:Met-allurgical Industry Press,2002.120.(Ҷ����,������.ʵ����������ѧ�����ֲ�[M].����:ұ��ҵ������,2002.120.)
[39] Zhao Z W,Liu D X.Thermodynamic analysis on theleaching process of molybdenite with oxygen fugacity-pHdiagram[J].China Molybdenum Industry,2009,33(1):18.(����ΰ,����ѧ.ʹ�����ݶ�-pHͼ�Ի�Կ��������̵�����ѧ����[J].�й���ҵ,2009,33(1):18.)
[40] Qiu W S,Li Y J,Zhao Z W,Huo G S,Xi X M,ChenP P.E-pH diagram of Li-Ti-H2O system at 298.15 Kand synthesis of Li4Ti5O12[J].The Chinese Journal ofNonferrous Metals,2010,20(11):2260.(����˳,�����,����ΰ,������,ϰС��,������.298.15K��Li-Ti-H2Oϵ��λ-pHͼ��Li4Ti5O12�ĺϳ�[J].�й���ɫ����ѧ��,2010,20(11):2260.)
[41] Yang X W,Qiu D F.Hydrometallurgy[M].Beijing:Metallurgical Industry Press,1998.96.(������,��ެ.ʪ��ұ��[M].����:ұ��ҵ������,1998.96.)
[42] Zhao Z W,Huo G S.Thermodynamic analysis of Li-Mn-H2O system[J].The Chinese Journal of NonferrousMetals,2004,14(11):1926.(����ΰ,������.Li-Mn-H2Oϵ����ѧ����[J].�й���ɫ����ѧ��,2004,14(11):1926.)
[43] Zhao Z W,Liu X H.Thermodynamic analysis of Li-Fe-P-H2O system[J].The Chinese Journal of Nonfer-rous Metals,2006,16(7):1257.(����ΰ,�����.Li-Fe-P-H2Oϵ����ѧ����[J].�й���ɫ����ѧ��,2006,16(7):1257.)