���±��: 1004-0609(2006)03-0530-06
��������Ⱦ��·�绯ѧ��ԭ����
������1, ������2, �ܹ���2
(1. �人�Ƽ���ѧ ����ұ����Դ����ʡ�������������ص�ʵ����, �人 430081;
2. �����Ƽ���ѧ ұ������̬����ѧԺ, ���� 100083)
ժ Ҫ: �ڿɿ�����ұ������ָ���·�չ����������Ⱦ��·�绯ѧ��ԭ�·����� �������������ӵ���������Ĥʱ��������������ֱ����ȡ�����ĵ绯ѧ��ԭԭ���� ���õ�ص�Ч��·, �Ƚ��������ڶ�·�� ��·�����µ绯ѧ��ԭʱ���������ص�, ������������ԭʱӰ�������������ء� �������: ���·��·�� ���͵�·���ܵ��衢 ѡ�ø�ǿ�Ļ�ԭ������������Ͻȴ�ʩ�������������ӵ���, ��������绯ѧ��ԭ�ٶȡ� ʵ������̼������Һ����ԭ��, ����������ֵ��: ʯī��|[O]Fe+C����|ZrO2(MgO)|FeO(slag)|����; ʯī��|[O]Fe+C����|ZrO2 (MgO)| FeO(slag)+Cu(l)||��˿, ��CaO-SiO2-Al2O3-FeOϵ�����зֱ�õ��˴�������̼���Ͻ�
�ؼ���: �ɿ�����ұ��; �绯ѧ��ԭ; ����; �����ӵ���; �����; ����Ⱦ ��ͼ�����: TF111.5
���ױ�ʶ��: A
Unpolluted short circuit electrochemical reduction analysis for molten oxide slags
GAO Yun-ming1, GUO Xing-min2, CHOU Kuo-chih2
(1. Key Laboratory for Ferrous Metallurgy and Resources Utilization of Ministry of Education,
Wuhan University of Science and Technology, Wuhan 430081, China;
2. School of Metallurgical and Ecological Engineering,
University of Science and Technology Beijing, Beijing 100083, China)
Abstract: According to a new idea of the metallurgy with controlled oxygen flow, the unpolluted short circuit electrochemical reduction technique for molten oxide slags was developed. The electrochemical reduction principle of direct extraction of metal from molten oxide slags using oxygen ionic conductor as separate membrane was analysed. By means of equivalent circuit, oxygen ionic current characteristics in the open circuit mode and short circuit mode were compared; the effects on oxygen ionic current in electrochemical reduction process were discussed. The results show that oxygen ionic current may get large and the electrochemical reduction reaction rate will increase when the external circuit has a short circuit, total resistance of the circuit decreases, a stronger reducing agent was selected, the cathode-alloying is employed, and so on. In the present experiment the carbon saturated iron melt is used as the reducing agent and the following galvanic cells were assembled: graphite rod |[O]Fe-C saturated |ZrO2(MgO)|(FeO)(slag)| iron rod, graphite rod|[O]Fe-C saturated |ZrO2 (MgO)|Cu(l)+(FeO)(slag)|Mo wire. Pure iron and carbon-free ferroalloy were obtained respectively from CaO-SiO2-Al2O3-FeO molten slags by means of the above cells mentioned.
Key words: metallurgy with controlled oxygen flow; electrochemical reduction; molten oxide slags; oxygen ionic conductor; zirconia; pollution-free
��ͳ�ĸ�������������һϵ�еĻ�ԭ���������������, �����϶��������Ĵ��ݹ���, �����ڷ�Ӧ� ����ֱ�ӽӴ�, �������ִ��ݹ����ڷ�Ӧϵͳ�в����γ�������ϣ������������������ ���, ��ͳ��������������������һϵ������, �����ܺĸ�, Ч�ʵ�, ��Ʒ������Ⱦ, ������Ⱦ�ȡ� ұ��Ӧ���е绯ѧ����, ������������������Ĵ��ݹ������γɷ����Ե�����, ʹ�������������뷴Ӧ���������Ӧ, һ�����ͨ����������������������ԭ��Ӧ, �����������ԭ�������; ��һ����, �ɱ����Ʒ�ܵ���Ⱦ�� ����, ��ͳұ���е�ȱ�㶼�ܵõ����ƻ���⡣ ��������Ⱦ�ĵ绯ѧұ�����Գ�Ϊ���ɿ�����ұ��, ����ұ�����е�һ�������
��̬�����ӵ���(����ZrO2����������)�ڸ����¶������Ӿ��к�ǿ��ѡ������, ���������ȶ�, �ܹ�����һ������״��ǿ�ȡ� ���, ��������Ϊ���������Ľ��ʡ� ͨ�������ӵ���ʵ���������������Ķ���Ǩ�ƿ��Բ������÷����ض�·��[1]�� Ŀǰ, ���÷���Ӧ���ڽ������������[2, 3]��Ӻ��б���ȡ������������������ֱ����ȡ�����[4]�� þ[5-7]�� ��[6]�ȡ� ��ض�·�������Ӧ���ڽ������������[8-14]�� ��������[15]��ͨ��ʵ��֤ʵѡ��̼������Һ����ԭ��, ���õ�ض�·�����ԴӺ�FeO������(CaO-SiO2-Al2O3-FeOϵ)��ֱ����ȡ������ Ϊ��չ�ɿ�����ұ���еĻ�ԭ����, �����������õ�ص�Ч��·, �о������������ӵ��������������Ⱦ��·��ԭ���·���, ϵͳ����������Ⱦ��·�绯ѧ��ԭʱӰ��������������, ����ʵ����֤���йط�����
1 �����绯ѧ��ԭԭ��
1.1 �����绯ѧ��ԭԭ��
�������������, ��ʼ����ֻ����Ԫ�ز���绯ѧ����, ��������������, ���ڽ��������ǵ��ӵ���, ������������ʻ������仯�� ��������������, ����������������֮�����ƽ��, ����Ϊ�����Ǻ��������ӵĵ����(��������), �ڻ�ԭ������, ���������ʲ��Ϸ����仯�� ���, �������ӵ�������������ԭԭ�����������������ͬ��
���������ӵ���(�粿���ȶ��������Ĥ)����������(����ѡ��̼������Һ����ԭ��)������������(������������ΪFeO)����, ���ԭ�����ϵ(��ͼ1��ʾ), ��������������·ʱ, �����Ʋ�������, ������������(O2-)ͨ�������ӵ������������Ǩ��, ��������(M2+)��������Ǩ��, �ڵ缫���ֱ����缫��Ӧ, �պϻ�·���е�������ͨ���� ���������е������ѳ�, ����ؽ�������ԭ������ ���������пɻ�ԭ�������ӵ��������ʹ�õ���������, ���������ô�������Ͻ�(�紿������̼���Ͻ�)��

ͼ1 �����绯ѧ��ԭ�Ĺ���ԭ��ʾ��ͼ
Fig.1 Schematic of principle of electrochemical reduction for molten oxide slags
1.2 ��Ч��·����
1.2.1 ��Ч��·
�ڹ������ʵ��й��о���, Ϊ��������ķ���, �������õ�ص�Ч��·[16]�� ���ǵ���ֱ����·�е��Ԫ����������·, ����Ԫ����������·, ���ɽ���˫���������������ĵ��ݡ� ��о��ɺ��ԡ� �����ӵ��������������Ӻ͵��ӵĻ�ϵ���, �ڵ�ص�Ч��·��, ��Ӧ�������ӵ������Rion�͵��ӵ������Re�� Ϊ�������, ��ԭ����������ӵ�����������ֱ�ﵽƽ��, ����������ѹΪp(O2)��, ��һ������ѹΪp(O2)���� �ڶ�·��ԭ������, ����ѡ��̼������Һ����ԭ��, ������FeOΪ���������, ��p(O2)��(������)>p(O2)��(��̼�����)�� ��Nernst����, ��֪

ʽ�� EnΪԭ���Nernst�綯��, V; RΪĦ�����峣��, R=8.314J/(mol��K); TΪ����ѧ�¶�, K; nΪ�缫��Ӧʽ�вμӷ�Ӧ�ĵ�����, �˴�n=4; FΪ�����ڳ���, F=96500C/mol�� ���õ�ص�Ч��·, �ɻ�ø���������ʽ, �ݴ˿��Է��������绯ѧ��ԭ���̵��ص㡣
1.2.2 ���·��·��ԭ
��ԭ��ص����·�պ�, �༴��·ʱ, �����绯ѧ��ԭ��Ӧ���Է�����, ��Ч��·��ͼ2��ʾ�� ͼ2��, RexΪ���·����, ��; Iion�� Ie�� Iex�ֱ�Ϊͨ�������ӵ���������ӵ����� ���ӵ����Լ����·����, A�� �ɻ��������·����, �������µ�ʽ:


ͼ2 ԭ��ض�·��ԭ��Ч��·
Fig.2 Reduction equivalent circuit of galvanic short circuit method
����ʽ(2)~(4), �ɵ�

��ʽ(5)~(7)��֪, �ڶ�·��ԭ������, ��������������ı䡣 ���滹ԭ�IJ��Ͻ���, �����е��������Ũ�Ȳ��Ͻ���, ��Ӧ����ѹp(O2)��Ҳ���ϼ�С, ����En���ϼ�С, ����Ҳ���ϼ�С�� ��p(O2)��=p(O2)��ʱ, En=0, ����Ҳ�½�Ϊ0, ������·��ԭֹͣ�� ��·��ԭʵ���ͨ���ⶨ���·����Iex�ı仯���������ԭ��״����
1.2.3 ���·��·��ԭ
�����·��·ʱ, ���������ӵ�����еĵ��ӵ絼, ԭ����ڲ���·, �����ӵ��屾��Ҳ���γ�һ�պϻ�·, ��Ч��·��ͼ2�����߿�����ʾ�� ��֪

��ʱ, �����ӵ�������ӵ�����ȡ� ���, ������, ԭ��ؽ����������ӵ��屾���ĵ��ӵ�����Ҳ�ܻ�ԭ������ ����ԭ������·��·ʱ������ֵҲ���ɶ�·ʱ�ĵ�������ʽ����, ���, ԭ������·��·��ԭ����Ϊ��·��ԭ(Rex����)ʱ��һ����������� ���·��·ʱ�ĵ���V�ɱ�ʾΪ
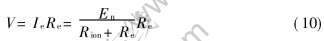
��·��ԭʵ���ͨ���ⶨ��·���Ƶı仯���������ԭ��״����
2 ʵ��
ʵ����ϵѡCaO-SiO2-Al2O3-FeO, ����ĸ�����(��������)Ϊ: 37%CaO, 43%SiO2, 20%Al2O3, ���۵�(1538K)�ϵ͡� ĸ����CaCO3(������)�� SiO2(������)�� Al2O3(������)���������Ⱥ���1623K��������ڸ����������ۻ��õ�; FeO��FeC2O4��2H2O(��ѧ��)����������������������µ�1673K�ۻ���ȡ����ˮ�м����Ʊ��õ��� ���趨������ȡһ������ĸ����FeO, ���Ⱥ���Ϊ�绯ѧʵ�������� �������õ�̼������Һ(�������30mm), �ɸߴ���(����99.9%)������ʯī��һ����ʯī����(��̼99.9%)���ۻ��õ��� ����һ�˷�յ�MgO�����ȶ�������ﯹ�(�ھ�12mm, �⾶14mm, ��58~60mm)��������̼������Һ֮��ĸ���Ĥ�� ������(����99.3%)��ͭ����(��ͭ99.95%)�������������� ʹ������������, �ɻ�ô���, �о����������Ϊ1ʱ�����绯ѧ��ԭ��Ϊ�� ��ͭ��Һ̬����, �ɵõ����۵��Cu-Fe�Ͻ�, �о���������������绯ѧ��ԭ��Ϊ�� ʯī��(���״�, ֱ��10mm, ��300mm)���������ߡ� ����ͭ����ʱ, ��˿(��Mo99.99%, ֱ��1.5mm)����������, �����ܽ���ͭ���塣 ���������е���˿ǰ��������ϸ������, �Ա�����˿ֱ���������Ӵ��� �ɺ���ͭ��������FeO֮��ķ�Ӧ[17]�� ��������˿ʹ��ǰ����ϸɰֽ��ĥ, ȥ������Ĥ, ����С���衣
ʵ����˫����˿¯�ڽ���, ����¯���ڳĽӵص���Ƭ, �����ӵ���Ҳ���ýӵص�������, �����������źš� ʵ��װ�ÿɲμ�����[15]�� ͨ��ǰ����װ̼������̼�Ͻ��ʯī�������ں��´����ĸ�������(�ھ�41mm, �⾶45mm, ��75mm)��, �ڸߴ����(��벸���99.9993%)������, ��˿¯��4K/min���������¶ȡ� ʵ�����������������, һ��Ϊ��̬����; ��һ��ΪҺ̬ͭ����(4g)�� ʵ��ʱ��װ��2.1g����, ��ͨ��Ar������������ﯹܻ����½���������, ֱ������ﯹܷ�ն�����̼������Һ�Ϸ�10mm���Ҵ�, ����20min�� ͬʱ�缫����Ҳ����������Һ���Ϸ�10mm���� ����CHI1140�͵绯ѧ������, ���������������缫����֮�䡣 �����������, ��������(�����缫����)��������, ������˿�缫������������Һ̬ͭ�缫�Ӵ�, �������ﯹܰ��ء� Ȼ��Ѱ��ؽ��뵽��̼������, ���ԭ�����ϵ�� ��ʵ���е�صĹ���Ϊ
��: ʯī��|[O]Fe+C����|ZrO2(MgO)|FeO(slag)|����;
��: ʯī��|[O]Fe+C����|ZrO2(MgO)|FeO(slag)+Cu(l)||��˿
Ϊʹ������ֱ��ͨ������ﯹܵ�����������̼�����зŵ�, ����ﯹ�����Һ�������ƽ�� ���õ绯ѧ�����Dzɼ�����������ź�, ����������� ʵ�鰲������:
1) ��·��ԭʵ�顣 ���õ绯ѧ������, �����·��·, ͬʱ����¼������·��ԭʱ�����·������ʱ��Ĺ�ϵ���ߡ�
2) ��·��ԭʵ�顣 ͨ���绯ѧ����������¼��FeO��������·��ԭʱ�Ŀ�·������ʱ��Ĺ�ϵ����(���·��·)��
�����·���������·����ֵ�㹻С�ұ仯����ʱ, �Ͽ���·, ����ʵ�顣 ͬʱ, Ϊ�ų����� (���������ܽ�������� ��������Ԫ�صĻ�ԭ�Լ��缫�����ȵ��ơ� �ȵ�����)�ͶԱ�, �����˸���������ĸ��(����FeO)�Ŀհ�ʵ�顣
ʵ���, �Բ���ʵ���������ȫ����ѧ����, ͨ��LEICA MPS60�������������۲�, ����CAMBRIDGE S250-MK2��ɨ��羵���е���̽����������
3 ���������
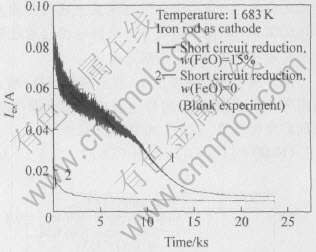
ͼ3��ʾΪ���õ�آ�(����������)ʱ, ���õ�ض�·����CaO-SiO2-Al2O3-FeO�������������·������ʱ��ı仯���ߡ� ������FeO��ʼ��������w(FeO)=15%, ͼ��w(FeO)=0Ϊ�հ�ʵ�����ߡ� ��ʱ, �绯ѧ��ӦΪ

ͼ3 ���·��·������ʱ��ı仯
Fig.3 Variations of external short circuit current with time
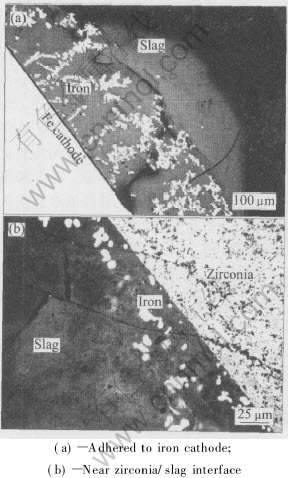
ͼ4��ʾΪʵ�����Ʒ�Ķ���ͼ�� ��ͼ4�п�֪, ������������������֦��(��������ⷶΧ��, ������Ϊ����), �������·��·��ԭ�Ľ��; �������(�����ӵ���)Ĥ���������渽��Ҳ������
ͼ4 ʵ�����Ʒ������
Fig.4 Cross sections of residual specimens
��������, �������������Ĥ�������ӵ����Զ������Ļ�ԭ���á� �����绯ѧ��ԭ�����������湲ͬ���õĽ��, �����ӵ���Ϊ���·������ͨ�������Ĥ�ĵ��ӵ���֮��, ������ʽ(2)��
ͼ5��ʾΪ���õ�آ�(Һ̬ͭ������)ʱ, ������FeO�绯ѧ��ԭ�����·������·������ʱ��ı仯���ߡ� ��ʱ, �绯ѧ��ӦΪ
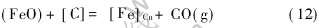
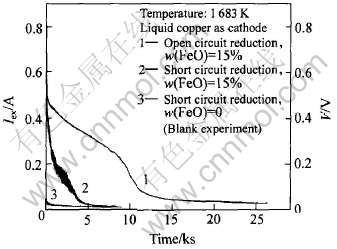
ͼ5 ������·��ԭ�� ��·��ԭ�ĶԱ�
Fig.5 Comparison between short circuit and open circuit reduction
��������·��ԭ������, ��·����V�ɴ�С, ֱ������ֵ(���缫���ߵ��ȵ��Ƶ�); ��������·��ԭ������, ���·����Ҳ�ɴ�С, ��˵��������FeO�����ڲ��Ͻ��͡� ����·���ƻ����·�����ﵽ����ֵʱ, �ڽϳ�һ��ʱ���ڱ仯������, ����Ϊ��ԭ���������� ʵ���, �ɷ��ֲ�����ɫ��ס� ��ѧ����Ҳ����, ����������ȫ���������ֱ�Ϊ0.12%��0.21%�� ���Կ���, ���·��·ʱ�����·��·(Iex=0)ʱ����ʱ��ҪС�ö�, ����ǰ�ߵĻ�ԭ�ٶȱȺ��߿�öࡣ ������ȫ��������ﯹܱ����ĵ��ӵ���������������������ﯹ���Ǩ�Ʋ����ĵ糡��
�����绯ѧ��ԭ�ٶ���ͨ�������ӵ������������С������ء� ��ʽ(5)�� (6)��֪, �����ӵ��������·�����ı仯������һ�µġ� ʽ(5)���Ա任Ϊ
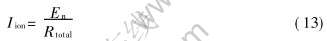
ʽ�� RtotalΪ��·���ܵ���, ���� Rtotal�ɱ�ʾΪ

ʽ�� LΪ�����ӵ���ĺ��, m; AΪ�����ӵ������Ч���, m2; ��ion�� ��e�ֱ�Ϊ�����ӵ���������ӵ絼�ʺ͵��ӵ絼��, S/m��
�ɼ�, �ڹ���ԭ��������, ����Rtotal������En, ��������Iion��
���, ��Ҫ��������ӵ���(�����·����), �ӿ�������ԭ�ٶ�, ���Զ���ϵ����ɲ��ֱַ��ȡ���´�ʩ:
1) ���·��·�� ���·��·�ɽ����ܵ���, ��·��ԭ�ȿ�·��ԭ��; ���·��·����ԽСԽ�á� �������·�����ȡ�Ĵ�ʩ����: ѡ�ô֡� �̡� �絼�ʴ�IJ���ͨ��������·��������������; ��С��·�нӴ�����ȡ�
2) ���������ӵ������ӵ��衢 ���ӵ��衣 ������������ӵ��������ӵ絼�ʡ� ���ӵ絼��(�����û�ϵ���); ��С�����ӵ�����; ����Ӵ������
3) ����Nernst�綯�ơ� ʹ�ø�ǿ�Ļ�ԭ��, ���Ͳο�̬������ѹ, �����Nernst�綯��; �����ȡ�������������Ͻ�, Ҳ�����Nernst�綯�ơ� ����, �¶ȡ� �����е�������ʵ�Ũ�ȵ�����Ҳ��Ӱ��Nernst�綯�ơ�
������ʩ��һ���̶��Ͼ������������ӵ����� �������ӵ�������һ���̶Ⱥ�, �����еĴ��ʻ��ڽ������������ӵ����Ľ�һ�����, ����ǰ��������ϵʽ��δ�ܵõ���ӳ�� Ϊ����������������绯ѧ��ԭȫ����, �˽ԭ�����е����ı仯����, Ӧ�ۺϿ��������еĴ��ʻ�����缫��Ӧ���ڡ� �������һ���о���
4 ����
1) ���������������������Ⱦ��·�绯ѧ��ԭ�·���, �ḻ�ͷ�չ�˿ɿ�����ұ���еĻ�ԭ������ ʹ�øõ绯ѧ��ԭ����, �ɴ�������������ֱ����ȡ��������Ͻ�
2) ���õ�ص�Ч��·���������绯ѧ��ԭ����, �� ����, �����ܷ�ӳ�����绯ѧ��ԭ���̵���ҪӰ�����ء� ͨ�������й�����, ���Կ�����������
3) ���·��·�� ���͵�·���ܵ��衢 ѡ�ø�ǿ�Ļ�ԭ������������Ͻ�, �������������ӵ���, ��������绯ѧ��ԭ�ٶȡ�
REFERENCES
[1]������, ������, �ܹ���. ��������Ĥ��ұ���ϵ�Ӧ����ǰ��[A]. ұ���о�[C]. ����: ұ��ҵ������, 2002. 307-319.
GAO Yun-ming, GUO Xing-min, CHOU Kuo-chih. Applications and foreground of oxygen ion permeable membrane in chemical metallurgy[A]. Metallurgy Investigation[C]. Beijing: Metallurgical Industry Press, 2002. 307-319.
[2]Fischer W A, Janke D. Electrolytic deoxidation of liquid melts at 1600��[J]. Scr Metall, 1972, 6(10): 923-928.
[3]Oberg K E, Friedman L M, Boorstein W M, et al. Electrochemical deoxidation of induction-stirred copper melts[J]. Metall Trans, 1973, 4(1): 75-82.
[4]Semkow K W, Sammells A F. The indirect electrochemical refining of lunar ores[J]. J Electrochem Soc, 1987, 134(8): 2088-2089.
[5]Krishnan A, Lu X G, Pal U. Solid oxide membrane process for magnesium production directly from magnesium oxide[J]. Metall Mat Trans B, 2005, 36(4): 463-473.
[6]Pal U, Krishnan A, Lu X G. Solid oxide membrane (SOM) technology for cost effective and environmentally sound production of metals and alloys directly from their oxides and ore concentrates[J]. JOM, 2004, 56(11): 245.
[7]Woolley D E, Pal U, Kenney G B. Electrowinning magnesium metal from MgCl2-NdOCl melt using solid-oxide-oxygen-ion-conducting membrane technology[J]. High Temp Mater Processes, 2001, 20(3-4): 209-218.
[8]Iwase M, Tanida M, Mclean A, et al. Electronically driven transport of oxygen from liquid iron to CO+CO2 gas mixtures through stabilized zirconia[J]. Metall Trans B, 1981, 12(9): 517-524.
[9]Yuan S, Pal U, Chou K C. Deoxidation of molten metals by short circuiting yttria-stabilized zirconia electrolyte cell [J]. J Electrochem Soc, 1994, 141(2): 467-474.
[10]Yuan S, Pal U, Chou K C. Modeling and scaleup of galvanic deoxidation of molten metals using solid electrolyte cells[J]. J Am Ceram Soc, 1996, 79(3): 641-650.
[11]Soral P, Pal U, Larson H R, et al. A pilot-scale trial of an improved galvanic deoxidation process for refining molten copper[J]. Metall Mat Trans B, 1999, 30(4): 307-321.
[12]������, Ф��, ���, ��. һ������Ⱦ��������[J]. ����ѧ��, 1999, 35(3): 316-319.
HU Xiao-jun, XIAO Li, LI Fu-shen, et al. An unpolluted deoxidation way[J]. Acta Metallurgica Sinica, 1999, 35(3): 316-319.
[13]���, ³�۸�, ��ӽ�, ��. ��Һ�Ĺ�����������Ⱦ����[J]. ����ѧ��, 2003, 39(3): 287-292.
LI Fu-shen, LU Xiong-gang, JIN Cong-jun, et al. Unpolluted deoxidation in steel melts with solid electrolyte[J]. Acta Metallurgica Sinica, 2003, 39(3): 287-292.
[14]���, ��ӽ�, ³�۸�, ��. ��Һ������������������ʱ�Ķ�����������[J]. ����ѧ��, 2004, 40(7): 673-676.
LI Fu-shen, JIN Cong-jun, LU Xiong-gang, et al. Oxygen rerising phenomenon during deoxidation with solid electrolyte deoxidation units in steel melts[J]. Acta Metallurgica Sinica, 2004, 40(7): 673-676.
[15]GAO Yun-ming, GUO Xing-min, CHOU Kuo-chih. Pure metal extraction from molten oxide slag by short-circuit galvanic cell [J]. J Univ Sci Technol Beijing, 2004, 11(4): 306-309.
[16]������. ұ��������ѧ�о�����[M]. ����: ұ��ҵ������, 2002. 150.
WANG Chang-zhen. Research Methods of Physical Chemistry in Metallurgy[M]. Beijing: Metallurgical Industry Press, 2002. 150.
[17]Sato K, Aragane G, Hirose F, et al. Reducing rate of iron oxide in molten slag by carbon molten iron[J]. Transactions ISIJ, 1984, 24: 808-815.
������Ŀ: ������Ȼ��ѧ����������Ŀ(50274008, 50574011); ����ʡ��Ȼ��ѧ����������Ŀ(2005ABA019)
�ո�����: 2005-07-04; ������: 2005-10-12
�����: ������(1969-), ��, ������, ��ʿ
ͨѶ����: ������, ������, ��ʿ; �绰: 027-68862223; E-mail:gym_1@sina.com
(�༭�°���)