文章编号:1004-0609(2007)04-0629-07
高温下锂离子电池电解液与电极的反应
胡传跃1,李新海2,郭 军1,汪形艳1,易 涛1
(1. 湖南人文科技学院 化学与材料科学系,娄底 417000;
2. 中南大学 冶金科学与工程学院,长沙 410083)
摘 要:采用DSC和XRD方法研究了1 mol?L-1 LiPF6电解液的热行为,发现EMC和H2O降低了1 mol?L-1 LiPF6 电解液(溶剂为EC\DML,质量比为1?1)的热稳定性。电解液热分解反应是EMC分解生成DEC和DMC,而DEC和DMC与LiPF6的分解产物PF5发生系列化学反应,释放大量反应热与气体。由于可燃性电解液与Li0.5CoO2 的热分解产物O2之间发生燃烧反应,使Li0.5CoO2发生复杂的热分解反应。高温下电解液与LiC6电极的热反应主要是:固体电解质膜(SEI膜)的碎裂反应,LiC6与粘结剂和电解液之间的反应。热反应主要发生在石墨的表面,而石墨的晶形结构在160 ℃热反应前后没有变化。
关键词:电解液;锂离子电池;DSC
中图分类号:O 646; TM 912 文献标识码:A
Reactions between electrolyte and electrode of lithium ion batteries at elevated temperature
HU Chuan-yue1, LI Xin-hai2, GUO Jun1, WANG Xing-yan1, YI Tao1
(1. Department of Chemistry and Material Science, Hunan Institute of Humanities,Science and Technology, Loudi 417000, China;
2. School of Metallurgy Science and Engineering, Central South University, Changsha 410083, China)
Abstract: Reactions between Li0.5CoO2 electrode and 1 mol?L-1 LiPF6 electrolyte at elevated temperature for lithium ion batteries were studied with differential scanning calorimeter (DSC) and X-ray diffraction (XRD). The results show that the thermal stability of 1 mol?L-1 LiPF6 ethylene carbonate (EC)-dimethyl carbonate(DMC)(1?1, mass ratio) electrolyte decreases by the impurity H2O and ethylmethyl carbonate (EMC) solvent. DEC and DMC are produced from the thermal decomposition reaction of EMC. A large amount of gases and heat are produced through series of chemical reactions among DEC and DMC and PF5 from decomposition of LiPF6. In the presence of sufficient electrolyte, the decomposition reactions of Li0.5CoO2 proceeds in a clear stepwise manner through solid phases as a function of temperature. Electrolyte combustion reactions take place due to the evolved oxygen from the decomposition of Li0.5CoO2 that releases large amounts of heat. The thermal reactions between electrolyte and LiC6 electrode of lithium ion batteries at elevated temperature includes the chipping reaction of solid electrolyte interface (SEI) film, the reaction between electrolyte and LiC6 and the reaction between adhesives and LiC6. However, the crystal structure of graphite does not change after thermal reaction at 160 ℃.
Key words: electrolytes; lithium-ion batteries; differential scanning calorimeter
由可逆嵌入与脱嵌的炭素材料如石墨、石油焦等取代金属锂制备锂离子电池,提高了电池的循环寿命与快速充电能力,提高了电池的安全性[1-3]。目前,人们对锂离子电池的电解质和电极材料进行了大量研究[1, 4-16],但关于锂离子电池安全性的研究较少。在此,本文作者针对锂离子电池在过充电过程中电池内部形成的高温现象,采用差示扫描量热方法研究电解液及其在电池正极与负极热反应过程中的行为,以揭示锂离子电池在过充电时有关电解液热行为的规律。
1 实验
1.1 仪器和试剂
仪器为:差示扫描量热仪(MDSC 2910型);BS9300锂离子电池综合测试仪(广州擎天有限公司制造);真空干燥箱(DZG-404型,天津天宇技术实业有限公司制造);手套箱(MB150B-G,德国MBRAUN公司制造)。
试剂为:聚偏二氟乙烯(PVDF);乙炔碳黑;石墨;LiCoO2;电解液1 mol?L-1 LiPF6 EC-DMC-EMC(溶剂的质量比为m(EL)?m(DML)?m(EML)= 1?1?1)。
1.2 DSC测试
将PVDF、乙炔黑与LiCoO2按一定的质量比混合均匀制备LiCoO2电极,另将石墨与PVDF按一定质量比制备石墨电极。以厚度为0.3 mm的锂箔作对电极,制备Li/LiCoO2与Li/graphite的CR2025电池,电解液采用1 mol?L-1 LiPF6 EC-DMC-EMC。Li/LiCoO2电池以1.3×10-4 mA?mm-2的电流密度充电至4.2 V,然后在4.2 ~2.75 V之间循环5次,最后,以4.2 V恒压充电至电流密度接近0 mA?mm-2,稳定电极达到4.2 V,使LiCoO2转变为Li0.5CoO2。Li/graphite 电池以1.3×10-4 mA?mm-2的电流密度充电至0 V,然后在0~1.5 V之间循环5次,最后以5×10-4 mA?mm-2的电流密度充电至0 V,石墨形成LiC6结构。
将以上制备的电池在手套箱中拆开,用不锈钢刮刀分别在LiCoO2电极与石墨电极上获取Li0.5CoO2与LiC6粉末样品,并迅速制备成DSC样品,整个过程在15 min内完成。对制好的样品在20 min内开始进行DSC测量。将Li0.5CoO2电极粉末以DMC溶剂浸泡48 h,过滤,重复2次,于100 ℃的真空中放置36 h,然后在手套箱中制备DSC样品。向经DMC溶剂浸提处理的Li0.5CoO2粉末中加入EC-DMC-EMC混合溶剂制备DSC样品。
将石墨粉于真空150 ℃处理24 h在手套箱中制备纯石墨粉DSC样品。制备的DSC样品质量一般为5~8 mg。在套箱中称量误差约为±1 mg。
1.3 XRD与SEM分析
将首次循环后的4.2 V锂离子电池在手套箱中拆开,重新组装成LiC6-电解液电池和Li0.5CoO2-电解液实验电池。对实验电池进行高温实验后,采用XRD方法分析正极和负极的成分。
解剖经140,145或150 ℃高温实验前后的锂离子电池,取出正极片,刮取正极粉,然后进行形貌测试。
2 分析与讨论
2.1 电解液的热稳定性
图1所示为水质量分数对电解液热稳定性的影响,电解液体系为1.0 mol?L-1 LiPF6 EC-DMC(1?1)。电解液样品a的水质量分数为5.85×10-3,样品b的水质量分数为8×10-6。由图1可以看出,2种电解液样品的放热峰位于230~285 ℃之间,其中水质量分数为5.85×10-3的电解液放热峰在257 ℃处,反应起始温度为240 ℃;而水质量分数为8×10-6的电解液放热峰在272 ℃处,反应起始温度为255 ℃。这说明电解液的水质量分数愈大,电解液的热稳定性就愈低。

图1 水对1.0 mol?L-1 LiPF6 EC-DMC(1?1)电解液热稳定性的影响
Fig.1 Influence of H2O on thermal stability of 1.0 mol?L-1 LiPF6 EC-DMC(1?1, mass ratio) electrolyte
2.2 电解液的热反应
纯LiPF6与1 mol?L-1 LiPF6 EC-DMC-EMC电解液的DSC曲线如图2所示。其中图2(a)所示为LiPF6在100~350 ℃时的DSC曲线。可见,DSC曲线在195 ℃左右出现第1个较弱的吸热峰,该峰为LiPF6的熔解峰,是可逆的;自250 ℃左右开始出现第2个吸热峰,表明LiPF6自250 ℃开始热分解。可见,纯LiPF6直到250 ℃仍是热稳定的。
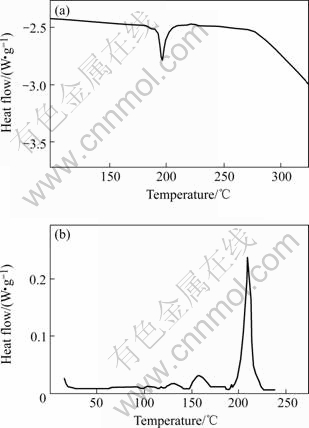
图2 LiPF6和1 mol?L-1 LiPF6 EC-DMC-EMC电解液的DSC曲线
Fig.2 DSC curves of LiPF6 (a) and 1 mol?L-1 LiPF6 EC-DMC-EMC (1?1?1, mass ratio) electrolytes (b)
图2(b)所示为1 mol?L-1 LiPF6EC-DMC-EMC电解液在0~300 ℃的DSC曲线。可以看出,DSC曲线在125~250 ℃的温度范围内有3个放热峰,其中第1个放热峰与第2个放热峰都非常弱,它们的反应热可忽略不计,这2个峰可能与反应(1)~(3)相关。因为在电解液中,尤其是当电解液中存在痕迹水时,LiPF6极易转变成LiF和HF。第3个放热峰较强,位于215 ℃左右。根据Edstrom等[14]对含LiPF6的(CH3)2CHOCOOCH(CH3)2溶液的热分解产物的研究结果,此时生成的产物有:(CH3)2CHF, CH3CH=CH2,(CH3)2CHOH, CO2和(CH3)CHO(CHCH3)2。由此可推断第3个放热峰可能是在LiPF6存在下,EMC与DMC溶剂分子发生了系列复杂的热分解反应,如式(4)~(12)所示。

将图2(b)中的DSC曲线与图1中1 mol?L-1 LiPF6 EC-DMC(溶剂质量比为1?1,水质量分数为8×10-6)电解液的DSC曲线对比可以看出,EMC溶剂降低了1 mol?L-1 LiPF6 EC-DMC电解液的热稳定性,说明有机电解液的热稳定性不仅与电解液的质子溶剂杂质有关,而且与有机混合溶剂的组成有关。
2.3 电解液在Li0.5CoO2热反应中的行为
图3所示为Li0.5CoO2的DSC曲线,其中图3(a)所示是经DMC溶剂浸提并干燥的Li0.5CoO2试样的DSC曲线。Li0.5CoO2电极粉末用溶剂浸提并真空烘干,除去电极中残留的电解质LiPF6与有机溶剂分子,消除它们对Li0.5CoO2热分解反应的影响。另外,试样中仍存在制备电极时所加入的少量PVDF粘结剂与乙炔黑导电剂,但PVDF与乙炔黑的热稳定性很高,到350 ℃仍是热稳定的,且PVDF不可燃烧。由图3(a)可知,DSC曲线在165 ℃左右存在1个吸热峰,该峰是PVDF的熔解峰;Li0.5CoO2自200 ℃左右开始分解,峰温为279 ℃,反应原理为:

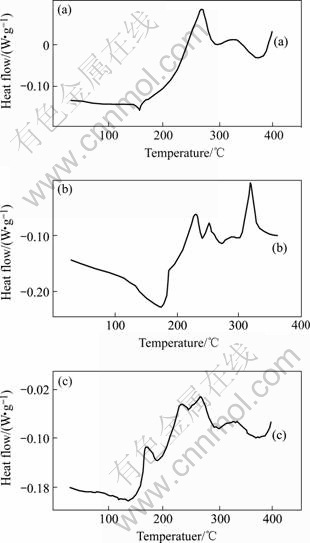
图3 Li0.5CoO2, 含足量EC-DMC-EMC混合剂的Li0.5CoO2和含电解液1 mol/L LiPF6 EC-DMC-EMC的Li0.5CoO2的DSC曲线
Fig.3 DSC curves of Li0.5CoO2 (a), Li0.5CoO2 with enough mixture solvents of EC-DMC-EMC (b) and Li0.5CoO2 with 1 mol/L LiPF6 EC-DMC-EMC electrolyte (c)
图3(b)的试样是经溶剂浸提和干燥的Li0.5CoO2,同时加入足量EC-DMC-EMC混合溶剂(以CnHmOx表示),保证存在足够的溶剂可与Li0.5CoO2的分解产物发生反应。因为没有锂盐时,纯有机溶剂的稳定性高,很难分解。由图3(b)可看出,加入EC-DMC-EMC混合溶剂后,Li0.5CoO2的热分解反应与图3(a)所示的纯Li0.5CoO2的热分解反应存在明显的差别。加入有机溶剂后,Li0.5CoO2的DSC曲线上存在2个放热峰,并且第1个放热峰是分裂的双峰,第2个放热峰对应温度在300 ℃以上。分裂的双峰可能是由于Li0.5CoO2分解释放的氧气导致有机溶剂燃烧,释放大量的热和气体。这种燃烧热导致分解产物Co3O4继续分解,如式(14)和(15)所示。与第2个放热峰相关的反应则较复杂,可能是CoO继续分解,或者CoO和LiCoO2分别与燃烧产物CO2反应生成Li2CO3和Co等。
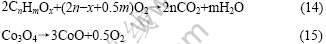
图3(c)的试样为新制备的、没有用溶剂浸提的Li0.5CoO2。样品中残留EC、DMC与EMC有机溶剂及LiPF6。由图3(c)可知,DSC曲线在173 ℃附近有1个较小的放热峰,根据图1所示结果,可认为该放热峰与残留的电解液热分解反应相关;从210℃左右开始出现第2个放热峰,是1个很弱的分裂峰,其原因可能是样品中电解液的含量少,释放的燃烧热较小,不足以使Co3O4完全分解生成CoO,反应生成物可能是Co3O4、LiCoO2及少量CoO等混合物。
根据以上分析可知,LiCoO2型锂离子电池过充电至爆炸时,1 mol?L-1 LiPF6 EC-DMC-EMC电解液及其分解产物因Li1-xCoO2(0.5≤x<1)分解释放的氧气发生燃烧,释放大量的热和气体。热稳定性实验结果表明,电解液-Li0.5CoO2电池在140 ℃是安全,在145 ℃就会发生爆炸。
图4所示为LI0.5CoO2与电解液高温反应后的XRD谱。可以看出,Li0.5CoO2电极与1 mol?L-1 LiPF6 EC-DMC-EMC电解液在145 ℃反应后,XRD谱中存在LiCoO2、Co3O4和CoO的典型X射线衍射峰,表明Li0.5CoO2发生了如式(13)和(15)的热分解反应。Li0.5CoO2电极与电解液在 140 ℃反应前后,其XRD谱中均出现典型的LiCoO2的XRD衍射峰,经140 ℃反应后,LiCoO2所有的特征衍射峰均发生了明显的宽化,但衍射峰位和峰强度基本没有改变。图5所示为Li0.5CoO2与电解液高温反应前后的SEM像。可以看出,反应前的Li0.5CoO2正极材料颗粒表面光滑整洁,结晶仍十分完整;经140 ℃高温反应后,材料颗粒表面更加光滑,而且颗粒表面粘附了一层细小的物质。由XRD和SEM结果可知,正极材料和电解液间可能发生了某些反应,但LiCoO2经140 ℃高温反应后,材料结构没有发生变化,只是晶粒细化了。

图4 Li0.5CoO2与电解液高温反应后的XRD谱
Fig.4 XRD patterns of Li0.5CoO2 electrode in presence of 1 mol?L-1 LiPF6 EC-DMC-EMC electrolyte after reaction at 145 ℃ (a), before reaction at 140 ℃(b) and after reaction at 140 ℃(c)

图5 高温下与电解液反应后Li0.5CoO2电极材料的SEM像
Fig.5 SEM photographs of Li0.5CoO2 electrode in presence of 1 mol?L-1 LiPF6 EC-DMC-EMC electrolyte before reaction at 140 ℃ (a) and after reaction at 140 ℃ (b)
结合DSC实验结果,可以认为电解液在130~200 ℃范围内的热反应所释放的热量较小,分解产生的气体少,而Li0.5CoO2在190 ℃以上才开始分解。因此,当温度高于190 ℃时,Li0.5CoO2分解释放的O2可以导致可燃性电解液燃烧,释放大量的燃烧热和气体,电池内部温度迅速增大,导致Li0.5CoO2向生成金属Co方向分解并释放更多氧气,从而引发一系列复杂反应,最终导致电池发生爆炸。因此,电解液的燃烧反应是导致锂离子电池安全性问题的主要因素之一。
2.4 电解液在LiC6电极热反应中的行为
图6所示为未充电纯石墨粉及LiC6/石墨电极的DSC曲线。其中图6(a)所示为未充电的纯石墨粉在空气气氛下的DSC结果,石墨粉的DSC曲线在341 ℃有1个放热峰,反应起始温度为256 ℃,说明石墨在256 ℃前都是热稳定的。若在惰性气氛下,石墨在400 ℃仍没有任何反应发生。图6(b)所示是LiC6/石墨电极在氩气氛中的DSC曲线。可以看出,在100~300 ℃范围内存在2个放热峰:第1个放热峰表征的是电极表面固体电解质膜(SEI膜)碎裂的热分解反应,因锂离子电池中SEI膜是一种离子导体薄膜(电子绝缘),是在锂离子电池首次充电过程中由电解液反应生成的不溶物附着于电极表面形成的;第2个放热峰表征的是LiC6与粘结剂及电极中残留的电解液之间的热反应,反应剧烈程度受粘结剂和电解液的性质及质量的影响[17-18]。考虑到锂离子电池是贫液体系,电极制备工艺总是采用尽可能少的粘结剂以提高电池的比能量,因此,第2个峰的反应热比SEI膜热分解反应热小得多。因为实验中没有氧气,故不能发生与电解液相关系列燃烧反应。此外,锂离子电池SEI膜在循环过程中逐渐增厚,电池循环次数愈多,电池负极热分解释放的热也愈多。
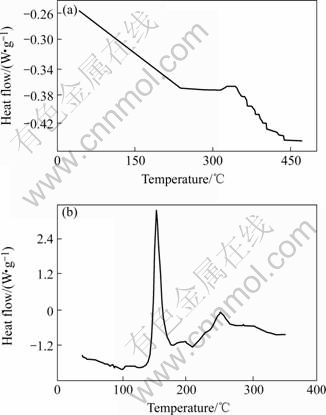
图6 纯石墨和含电解液1 mol?L-1 LiPF6 EC-DMC-EMC的LiC6/石墨电极的DSC曲线
Fig.6 DSC curves of pure graphite (a) and LiC6/graphite electrode (b) in presence of 1 mol?L-1 LiPF6 EC-DMC-EMC electrolyte
热稳定性实验结果表明,电解液-LiC6电池在160 ℃时是安全的,在165 ℃时则发生爆炸。图7所示为LiC6电极与1 mol?L-1 LiPF6 EC-DMC-EMC电解液在160 ℃反应前后的XRD谱。可以看出,在160 ℃高温反应前后,碳材料所有特征衍射峰的峰位、峰强度以及半峰宽都没有明显改变,说明碳材料的晶形结构在160 ℃高温下几乎没有变化。XRD分析结果表明,碳负极热分解反应主要发生在碳的表面,因而碳材料的晶形结构并没有发生变化;反应受锂离子在碳材料层状结构中的扩散速率控制,这与Hossain等[19] 对中间相碳微球的研究结果一致。因此,电解液与LiC6电极的反应主要是碳电极表面SEI膜的碎裂反应,电解液与粘结剂的反应以及与嵌入碳材料中的锂之间的反应。
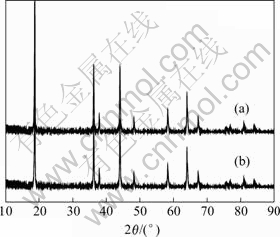
图7 LiC6电极与电解液于160 ℃反应前后的XRD谱
Fig.7 XRD patterns of LiC6 electrode in presence of 1 mol?L-1 LiPF6 EC-DMC-EMC electrolyte before reaction at 160 ℃ (a) and after reaction at 160 ℃ (b)
3 结论
1) H2O和EMC降低了1 mol?L-1 LiPF6 EC-DMC (溶剂为EC、DML,质量比为1?1)电解液的热稳定性。
2) 1 mol?L-1 LiPF6 EC-DMC-EMC (溶剂为EC、DML、EML,质量比为1?1?1)电解液的可能热分解反应机理为:EMC分解生成DEC与DMC, DEC和DMC与LiPF6的分解产物PF5发生了复杂的化学反应。
3) 在1 mol?L-1 LiPF6 EC-DMC-EMC (溶剂为EC、DML、EML,质量比为1?1?1)电解液中,Li0.5CoO2的分解反应为:6Li0.5CoO2→3LiCoO2+Co3O4→3LiCoO2+3CoO,电解液发生燃烧反应。
4) 高温下电解液与LiC6电极的热反应是SEI膜的碎裂反应以及LiC6与粘结剂和电解液之间的反应,反应主要发生在石墨的表面,石墨的晶形结构在160 ℃热反应前后没有变化。
REFERENCES
[1] Biensan P, Simon B, Peres J P, Guibert A D, Broussely M, Bodet J M, Perton F. On safety of lithium-ion cells[J]. J Power Sources, 1999, 81/82: 906-912.
[2] Nazri G A, Conell R A, Julien C. Preparation and physical properties of lithium phosphide-lithium chloride, a solid electrolyte for solid sate lithium batteries[J]. Solid State Ionics, 1996, 86/88: 99-105.
[3] 李义兵, 陈白珍,胡拥军,李致高,陈 亚,金基明. Li-Mn-Al-O锂离子正极材料的合成及其性能[J]. 中南大学学报:自然科学版, 2006, 37(5): 913-918.
LI Yi-bing, CHEN Bai-zhen, HU Yong-jun, LI Zhi-gao, CHEN Ya, JIN Ji-ming. preparation and property of Li-Mn-Al-O cathode material for lithium batteries[J]. Journal of Central South University: Science and Technology, 2006, 37(5): 913-918
[4] Tobishima S I, Takei K, Sakurai Y, Yamaki J I. Lithium ion cell safety[J]. J Power Sources, 2000, 90: 188-195.
[5] 胡传跃,李新海,王志兴,郭华军. 锂离子电池电解液过充添加剂的行为 [J]. 中国有色金属学报,2004, 14(12): 2125-2130.
HU Chuan-yue, LI Xin-hai, WANG Zhi-xing, GUO Hua-jun. Behavior of overcharging additions for electrolyte used in Li-ion batteries[J]. The Chinese Journal of Nonferrous Metals, 2004, 14(12): 2125-2130.
[6] Yoshiyasu S, Kiyonami T, Akira N. Thermal behaviors of lithium-ion cells during overcharge [J]. J Power Sources, 2001, 97/98: 693-696.
[7] Carlos J, Reis R. Thermodynamic analysis of the symmetry factor and the transfer coefficient in electrode kinetics [J]. J Electrocheml Soc, 1997, 144(7): 2404-2409.
[8] Takano K, Saito Y. Entropy changes in lithium ion cells on charge and discharge [J]. Journal of Applied Electrochemistry, 2002, 32(1): 251-258.
[9] Selman S R, Hallaj S A, Uchida I, Hirano Y. Cooperative research on safety fundamentals of lithium batteries [J]. J Power Sources, 2001, 97/98: 726-732.
[10] Atsuhiro F, Yoshinori K, Katsunori Y, Toshiyuki N, Ikuo Y. Thermal simulation of large-scale lithium secondary batteries using a graphite-coke hybrid carbon negative electrode and LiNi0.7Co0.3O2 positive electrode[J]. J Power Sources, 2002, 104: 248-252.
[11] Gerardine G B, White T E, Zhang Z M. Thermal stability of LiPF6-EC: EMC electrolyte for lithium-ion batteries[J]. J Power Sources, 2001, 97/98: 570-575.
[12] Kawamura T, Kimura A, Egashira M, Okada S, Yamaki J I. Thermal stability of alkyl carbonate mixed-solvent electrolytes for lithium ion cells[J]. J Power Sources, 2002, 104: 260-264.
[13] Yamaki J I, Takatsuji H, Kawamura T, Egashira M. Thermal stability of graphite anode with electrolyte in lithium-ion cells[J]. Solid State Ionics, 2002, 148: 241-245.
[14] Edstrom K, Andersson A M, Bishop A, Fransson L, Lindgren J, Hussenius A. Carbon electrode morphology and thermal stability of the passivation layer[J]. J Power Sources, 2001, 97/98: 87-91.
[15] 赵铭姝,汪 飞,宋晓平. 锂离子电池正极材料锰钴酸锂表征与分解动力学[J]. 中国有色金属学报,2005, 15(9): 1396-1402.
ZHAO Ming-shu, WANG Fei, SONG Xiao-ping. Synthesizing kinetics and characteristics of LiMnCoO4 using as lithium-ion battery cathode material[J]. The Chinese Journal of Nonferrous Metals, 2005, 15(9): 1396-1402.
[16] 尹笃林,范长冷,徐仲榆. 尖晶石LiMn2O4和LiCoO2与电解液的相容性[J]. 中国有色金属学报,2006, 16(10): 1799-1805.
YIN Du-lin, FAN Chang-ling, XU Zhong-yu. Compatibilities of electrolytes with spinel LiMn2O4 and LiCoO2[J]. The Chinese Journal of Nonferrous Metals, 2006, 16(10): 1799-1805.
[17] Gerardine G B, Talph E W, Zhang Z M. Thermal stability of LiPF6-EC: EMC electrolyte for lithium-ion batteries [J]. J Power Sources, 2001, 97/98: 570-575.
[18] 胡传跃,李新海,王志兴,罗文斌. 材料对锂离子电池热稳定性的影响[J]. 中南大学学报:自然科学版, 2005, 36(4): 587-593.
HU Chuan-yue, LI Xin-hai, WANG Zhi-xing, LUO Wen-bin. Influence of materials on thermal stability of lithium-ion batteries[J]. Journal of Central South University: Science and Technology, 2005, 36(4): 587-593.
[19] Hossain S, Kim Y K, Saleh Y, Loutfy R. Comparative studies of MCMB and C-C composite as anodes for lithium-ion battery systems [J]. J Power Sources, 2003, 114: 264-276.
收稿日期:2006-09-26;修订日期:2007-01-08
通讯作者:胡传跃,讲师,博士;电话:0738-8325065;E-mail: huchuanyue@vip.sina.com.cn
(编辑 陈灿华)