网络首发时间: 2015-04-07 09:25
稀有金属 2015,39(07),666-672 DOI:10.13373/j.cnki.cjrm.2015.07.015
四氯化钛精制除钒试剂的制备及应用研究
李亮 李开华 苗庆东 程晓哲 何安西 孙朝晖
攀钢集团研究院有限公司钒钛资源综合利用国家重点实验室
摘 要:
TiCl4是海绵钛与氯化法钛白的生产原料,粗TiCl4精制除钒是确保TiCl4质量的重要环节。为稳定制备粗钛除钒试剂质量及优化粗钛除钒效果,结合我国攀西地区高钙镁钛渣氯化所得粗TiCl4的原料特点,对粗TiCl4铝粉除钒试剂的制备原理进行了热力学分析,并考察了铝粉含量、氯气浓度、停止通氯温度、反应最高温度持续时间对除钒试剂制备过程的影响,获得了除钒试剂稳定制备的优化工艺参数;同时开展了工艺优化验证实验与除钒应用实验研究。热力学分析结果表明:温度为25~140℃时,Al粉与精TiCl4能够在通氯条件下反应生成低价钛除钒试剂,控制温度为90~150℃时,能使溶于粗TiCl4中的VOCl3转变为不溶于TiCl4的VOCl2沉淀除去。实验研究表明:当铝粉悬浮液中铝含量为30~35 g・L-1,Cl2浓度为85%~90%、停止通氯温度为105℃、反应器内最高温度持续时间为8~10 min时,能稳定制备质量较佳除钒试剂,在最优工艺条件下制备所得除钒试剂中TiCl3含量为8.24%~9.24%,Al Cl3含量为2.67%~3.68%,质量稳定且除钒效果好,该除钒试剂能将粗TiCl4中VOCl3含量由0.0963%~0.1116%降低至0.0003%。
关键词:
四氯化钛精制;铝粉除钒;三氯化钛;稳定制备;
中图分类号: TQ134.11
作者简介:李亮(1986-),男,四川广安人,硕士研究生,研究方向:海绵钛冶金、真空冶金、钒钛资源的综合利用;E-mail:254324378@qq.com;;何安西,教授级高级工程师;电话:0212-3380801;E-mail:Heanxi56@163.com;
收稿日期:2014-02-25
基金:国家科技部重点基础研究发展计划(973计划)项目(2013CB632606)资助;
Preparation and Application of Vanadium Removing Reagent in Refining Crude TiCl4
Li Liang Li Kaihua Miao Qingdong Cheng Xiaozhe He Anxi Sun Chaohui
State Key Laboratory of Vanadium and Titanium Resources Comprehensive Utilization,Pangang Group Research Institute Co. ,Ltd.
Abstract:
Pure TiCl4 is raw material for titanium sponge and pigment grade TiO2 production. Removing vanadium from crude TiCl4 is an important process to ensure the quality of TiCl4. According to the characteristic of crude TiCl4 which was produced from titanium slag with high calcium and magnesium in Panxi region of China,preparation principle of vanadium removing reagent was analyzed from the perspective of thermodynamics to optimize vanadium impurities removal from crude TiCl4 and stablize the quality of vanadium removing reagent. Influences of Al powder content,concentration of chlorine gas,stop temperature of Cl2 and maximum temperature duration preparation process were investigated to obtain the optimal and stable preparation process parameters of vanadium removing reagent. Process optimization and application experiments of vanadium removing reagent were also carried out. Thermodynamic analysis results showed that low valence titanium slurry could be produced when Al powder and Cl2 were added in pure TiCl4 at 25 ~ 140 ℃.VOCl3 dissolved in crude TiCl4 could transform into VOCl2 precipitation which was insoluble to TiCl4 at 90 ~ 150 ℃,and thus VOCl3 was removed from crude TiCl4. Experimental research showed that high quality and stable vanadium removing reagent could be obtained when Al powder content in suspension liquid was 30 ~ 35 g・L- 1,Cl2 concentration was 85% ~ 90%,stop temperature of Cl2 was 105℃,and maximum temperature duration time was 8 ~ 10 min. TiCl3 and Al Cl3 contents in low valence titanium slurry which was produced under optimal conditions were 8. 24% ~ 9. 24% and 2. 67% ~ 3. 68%,respectively. VOCl3 content in crude TiCl4 could be reduced from 0. 0963% ~ 0. 1116% to 0. 0003% after vanadium removing operation.
Keyword:
TiCl4 purification; vanadium removal by adding Al powder; titanium trichloride; stability of preparation process;
Received: 2014-02-25
钛因具有熔点高、密度小、耐磨损、抗腐蚀等优异性能,被广泛应用于航空航天、石油化工、能源、交通运输、医学等领域[1,2,3]。纯净的Ti Cl4是海绵钛与氯化法钛白生产的原料,Ti Cl4还可作为制备纳米Ti O2的原料,在钛工业生产过程中占有重要地位[4,5]; 目前工业上制备四氯化钛主要采用沸腾氯化法与熔盐氯化法[6,7,8,9]。通过熔盐氯化法生产的粗Ti Cl4中含有钒、硅、铝、铁等氯化物杂质, 还原制备海绵钛之前需通过精制工序对粗Ti Cl4进行除杂处理[10~11]。粗Ti Cl4中硅、铝、铁等杂质氯化物分别可采用蒸馏与精馏去除,而钒杂质则需采用化学法才能得以去除[3]。
目前工业上粗Ti Cl4精制除钒的主要方法有铜丝除钒法、硫化氢除钒法、有机物除钒法、铝粉除钒法[12]; 其中铝粉除钒具有铝粉用量小、能处理高钒粗Ti Cl4、对设备无腐蚀、除杂产品易与残渣分离等优点,且可从除钒残渣中综合回收钒,是含钒粗Ti Cl4除钒方法的较佳选择。“两步法”铝粉除钒技术自20世纪70年代起在前苏联进入工业化应用阶段,但有关铝粉除钒的设备结构、工艺参数至今仍属保密范围[13]; 国内北京有色金属研究总院邓国珠等开发了“一步法”[12],但“一步法”铝粉除钒要求粗Ti Cl4中不存在干扰生成3Ti Cl3・Al Cl3反应的杂质[12]。针对我国攀西地区高钙镁钛渣熔盐氯化法生产所得粗Ti Cl4,因其固相物杂质含量较高,目前采用由乌克兰引进的“两步法”铝粉除钒法,该法需间歇制备低价钛除钒试剂。为提升粗Ti Cl4除钒效果、稳定低价钛除钒试剂质量,本文针对我国攀西地区高钙镁钛渣氯化所得粗Ti Cl4的原料特点,开展了除钒试剂制备原理分析、制备工艺条件优化及应用研究。
1实验
1. 1原理铝粉除钒试剂的获得需将铝粉加入精Ti Cl4中,并通入Cl2使部分铝粉氯化生成Al Cl3,在Al Cl3的催化作用下,铝粉与Ti Cl4反应生成Ti Cl3。为避免杂质气体对制备过程的干扰, 反应过程常在N2保护条件下进行。制备过程相关反应如式( 1) ,( 2) 所示:

制备所得的低价钛以3Ti Cl3・Al Cl3络合物形态存在[14]。根据相关热力学数据[13],可计算得出反应( 1) ,( 2) 的吉布斯自由能,图1为反应( 1) , ( 2) 的 ΔGθ-T关系图。
由图1可知: 当温度在25 ~ 140 ℃之间时,反应( 1) 的 ΔGθ值为 - 1236. 3 ~ - 1194. 6 k J・mol- 1, 反应( 2) 的 ΔGθ值为 - 364. 6 ~ - 341. 5 k J・mol- 1, 均小于零。因此,在此温度条件下反应( 1) ,( 2) 均能发生,且在相同温度条件下反应( 1) 的 ΔGθ值比反应( 2) 小,反应( 1) 将先于反应( 2) 发生,Al Cl3将优先生成。
Gerhard[14]认为参与除钒反应的主要是络合物3Ti Cl3・Al Cl3中的Ti Cl3,在有Al Cl3作为催化剂存在的条件下,Ti Cl3将与粗Ti Cl4中VOCl3反应生成不溶于Ti Cl4的VOCl2沉淀,进而采用蒸馏的方法可将其分离去除。实际生产中除钒过程常在蒸馏釜中完成,发生的反应如式( 3) 所示:
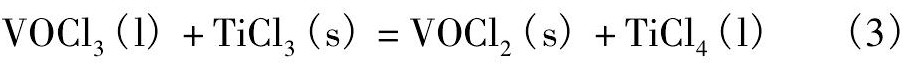
反应( 3) 的 ΔGT-T的关系可由HSC软件计算得出[15],其计算结果如图2所示。
由图2可知: 在90 ~ 150 ℃的温度范围内,反应( 3) 的 ΔGθ均为负值。热力学计算表明反应( 3) 能够发生,且温度越低反应发生的趋势越大; 为保证生成的VOCl2沉淀能与Ti Cl4实现较好分离,可选择大于Ti Cl4的沸点温度作为除钒作业的工作温度,即除钒过程的温度应大于136 ℃。
与此同时,铝粉除钒生成的Al Cl3将与Ti OCl2发生反应,在除钒的同时可去除溶于粗Ti Cl4中的Ti OCl2,其化学反应如式( 4) 所示[12]:

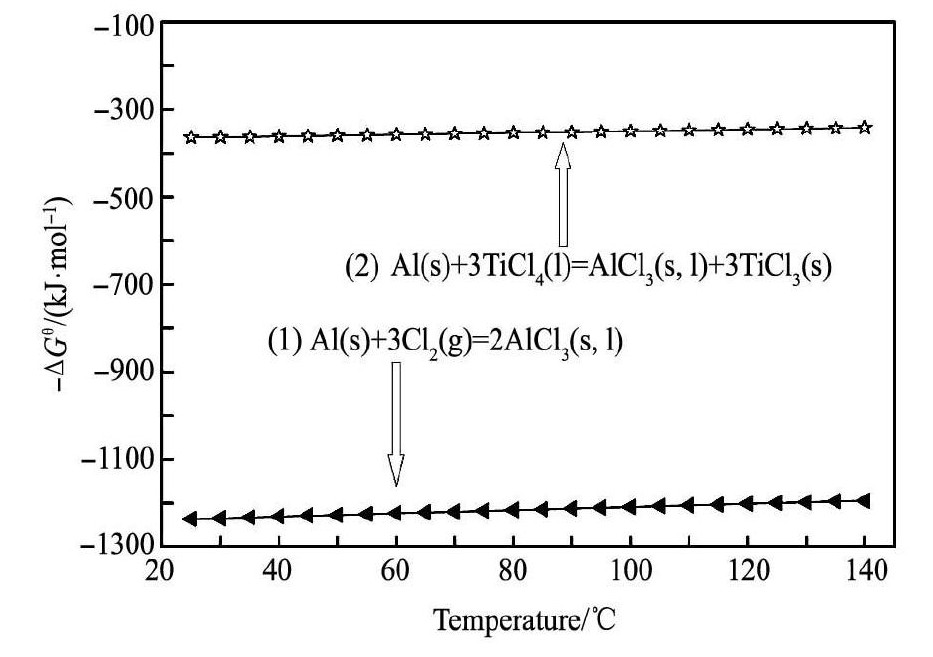
图1 反应( 1) 和( 2) 的 ΔGθ-T 关系图 Fig.1 Relationship between ΔGθand T of Reactions ( 1) and ( 2)

图2 反应( 3) 的 ΔGθ-T 关系图 Fig.2 Relationship between ΔGθand T of Reaction( 3)
热力学分析结果表明: 铝粉与精Ti Cl4在通氯条件下能够制备获得Ti Cl3除钒浆液,温度为90 ~ 150 ℃ 时能使溶于粗Ti Cl4中的VOCl3转变为不溶于Ti Cl4的VOCl2沉淀除去,同时可除去溶于粗Ti Cl4中的Ti OCl2。
1. 2方法除钒试剂制备流程主要包括铝粉悬浮液制备和低价钛除钒浆液制备两大工序。图3为除钒试剂制备流程及设备示意图。实验所用的原料Cl2,N2,Ti Cl4及铝粉的质量指标列于表1。
实验过程中首先向铝粉悬浮液混合罐中加入一定液位的精Ti Cl4,待混合罐内压力达到 - 150 Pa时,吸入一定量铝粉; 当铝粉加入完成后,启动搅拌器进行搅拌3 ~ 4 min时间,完成铝粉悬浮液的制备。
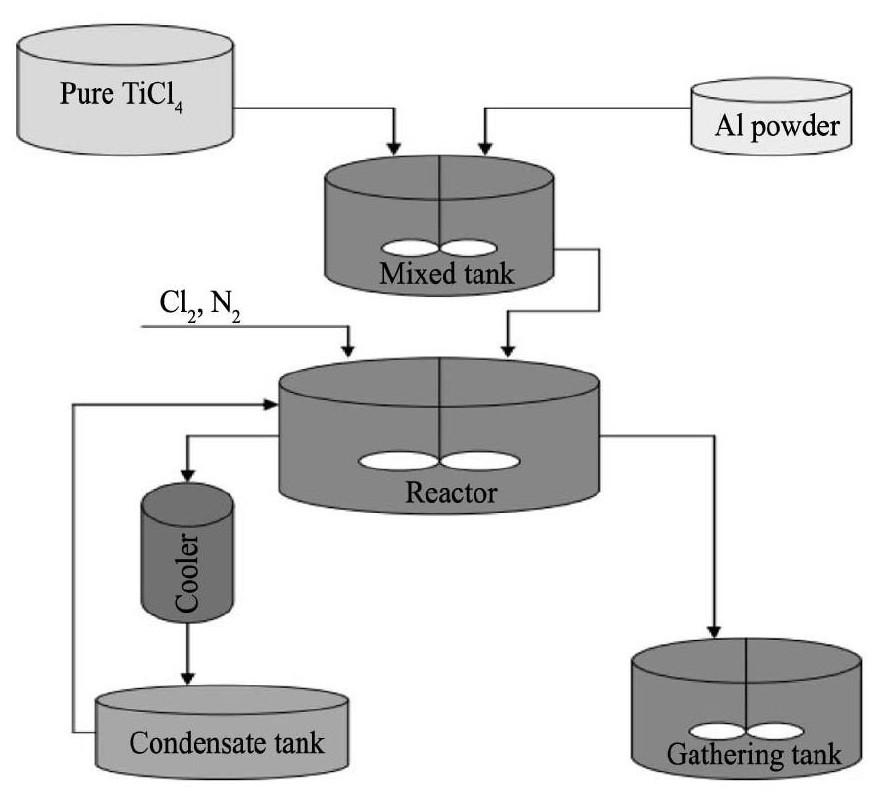
图3 除钒试剂制备流程图 Fig.3 Flow chart of vanadium remove reagent preparation
表1 除钒试剂制备所需原料质量指标 Table 1 Quality indicators of raw material 下载原图

表1 除钒试剂制备所需原料质量指标 Table 1 Quality indicators of raw material
向除钒试剂制备反应器中补充一定液位的精Ti Cl4,并通入氮气进行保护; 向反应器内加入一定量的铝粉悬浮液,搅拌4 ~ 5 min后通入氯气使除钒试剂制备反应自动发生,同时释放大量反应热; 待反应器温度升至80 ~ 120 ℃ 时,停止通入Cl2。 当反应罐内温度不再上升,且罐内液位不再下降, 标志反应已结束。此时,向反应器补加一定量精Ti Cl4液体,并搅拌5 ~ 10 min,打开排料阀将制备好的除钒试剂放至收集罐中待用,并取样化验。
制备所得除钒试剂中Al含量通过电感耦合等离子体发射光谱仪( ICP-AES) 进行检测,Ti3 +含量则通过硫酸高铁铵滴定法测定。
2结果与讨论
2. 1铝粉含量的影响虽然除钒试剂的有效成分是Ti Cl3,但试剂中Ti Cl3的含量不宜过高,否则将给使用带来不便。实验发现,含Ti Cl36% ~ 10% 、 Al Cl3< 5% 的除钒试剂具有较好的流动性,便于输送和使用。
铝粉悬浮液中铝粉的含量直接影响到除钒试剂中Al Cl3,Ti Cl3的含量,图4为不同铝含量的悬浮液制备所得除钒试剂的实验结果。
由图4可知,除钒试剂中Al Cl3,Ti Cl3的含量随悬浮液中铝粉含量的变化而有所波动。悬浮液中铝粉含量由26增至35 g・L- 1,除钒试剂中Ti Cl3含量由7. 9% 增至9. 4% ,之后继续升高悬浮液中铝粉含量,除钒试剂中Ti Cl3含量呈下降趋势。然而,除钒试剂中Al Cl3的含量却是随悬浮液中铝粉含量的升高而缓慢增大,其值仅由3. 80% 增至4. 48% 。由热力学分析结果可知,反应( 1 ) 先于反应 ( 2) 发生。当体系内铝粉过量时,反应( 2) 发生的同时,反应( 1) 仍将长时间进行,导致生成的Al Cl3含量有所增加。图4结果显示,选择悬浮液中铝粉含量为30 ~ 35 g・L- 1,可维持除钒试剂中Ti Cl3含量在较高水平,同时Al Cl3含量相对较低,即使用铝粉含量为30 ~ 35 g・L- 1的悬浮液时能获得较好质量的除钒试剂。
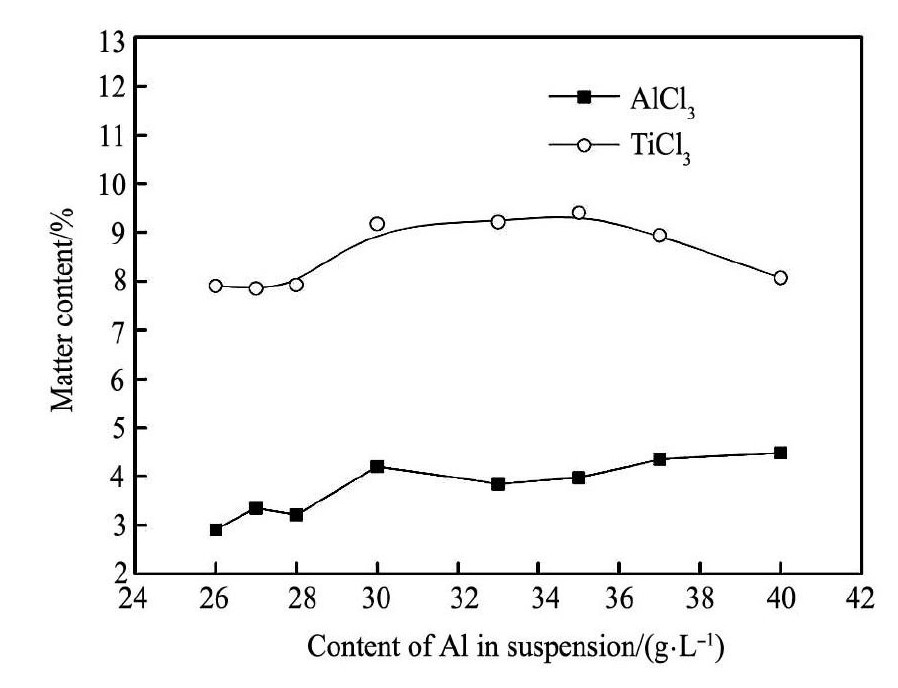
图4 铝含量对除钒试剂中 Al Cl3,Ti Cl3含量的影响 Fig.4 Effect of Al content in suspension on Al Cl3and Ti Cl3 contents in vanadium removing reagent

图5 氯气浓度对除钒试剂中 Al Cl3含量的影响 Fig.5 Effect of Cl2concentration on Al Cl3content in vanadium removing reagent
2. 2氯气浓度的影响当氯气浓度较高时,通氯的同时带入除钒试剂制备系统的O2,N2,CO2等杂质气体较少,反应过程中生成的Al Cl3含量相对较多; 而充足的Al Cl3含量在低价钛生成的反应发生过程中能有效实现催化作用,且能将溶解在Ti Cl4中的Ti OCl2转化为Ti Cl4。由于工业生产过程中常采用海绵钛厂镁电解车间产生的阳极氯气或与液氯蒸发氯气混合所得气体作为除钒试剂制备的反应氯气,这就不可避免地会出现氯气浓度相同但杂质浓度不同的情况,杂质浓度的变化必将导致除钒试剂质量的波动。图5和6分别为不同氯气浓度条件下制备得到的除钒试剂中Al Cl3,Ti Cl3含量的变化情况。
图5与6均表明,氯气浓度变化将直接引起除钒试剂中Al Cl3,Ti Cl3含量的波动。当氯气浓度低于80% 时,制备所得除钒试剂中Ti Cl3含量相对较高,其含量平均为9. 2% 。同时,试剂中Al Cl3含量也较高,平均为3. 5% ; 此种高Ti Cl3含量的除钒试剂浆液虽对除钒有利,但增加了Ti Cl4精制系统去除Al Cl3的难度。氯气浓度为85% ~ 90% 时,除钒试剂中Ti Cl3含量在8. 59%~ 9. 96% 间波动,平均为9. 06% ,满足生产的需要,且除钒试剂中Al Cl3含量相对较低,平均为3. 04% 。此类试剂既有利于除钒的进行,又降低了系统除铝的难度与负荷。当氯气浓度大于90% 时,Ti Cl3含量与Al Cl3含量均较低,难以满足除钒反应的要求。因此,控制氯气浓度为85% ~ 90% 有利于制备获得高质量的除钒试剂。

图6 氯气浓度对除钒试剂中 Ti Cl3含量的影响 Fig.6 Effect of Cl2concentration on Ti Cl3content in vanadium removing reagent
2. 3停氯温度的影响由于反应( 1 ) 和 ( 2 ) 均为放热反应,向反应器通入氯气后的除钒试剂制备过程中期处于强反应放热阶段,此时反应罐内温度将持续升高,通过除钒试剂制备过程中最高反应温度及其高温持续时间长短可有效判断除钒试剂制备控制过程的优劣,且通氯停止温度对试剂中Al Cl3,Ti Cl3含量具有直接影响; 根据热力学的计算结果,选择97 ~ 120 ℃作为停止通氯温度进行实验,实验结果列于表2。
表2 不同停氯温度的对除钒试剂制备过程影响 Table 2 Influences of stop temperature of Cl2on preparation process of vanadium removing reagent 下载原图

表2 不同停氯温度的对除钒试剂制备过程影响 Table 2 Influences of stop temperature of Cl2on preparation process of vanadium removing reagent
由表2结果可知: 当停止通氯温度分别120, 110,105,97 ℃ 时,反应器内最高温度均能达到131 ℃ 以上,停氯温度越低反应器内最高温度相对越高,但反应罐内最高温度相差较小。停止通氯温度高时,最高温度持续时间相对较长。当停止通氯温度为105 ℃ 时,除钒试剂矿浆中Ti Cl3含量为9. 36% ,Al Cl3含量为3. 45% ,Ti Cl3含量相对较高,且Al Cl3含量满足 < 5% 的质量要求,其制备效果较好。因此,实际生产过程中可选择105 ℃作为停止通氯的温度。
2. 4高温持续时间的影响除钒试剂制备反应器内的高温持续时间直接反映反应放热量和反应完成程度。因此,生产过程中将其作为除钒试剂制备过程优劣重要判断标准之一。当反应物料一定时,若高温持续时间越长,表明反应放热量越大, 反应进行得越彻底。同时,反应器内高温持续时间对试剂中Al Cl3,Ti Cl3含量也将带来一定程度影响。图7为不同高温持续时间条件下制备所得低价钛除钒试剂中Ti Cl3与Al Cl3含量变化情况。
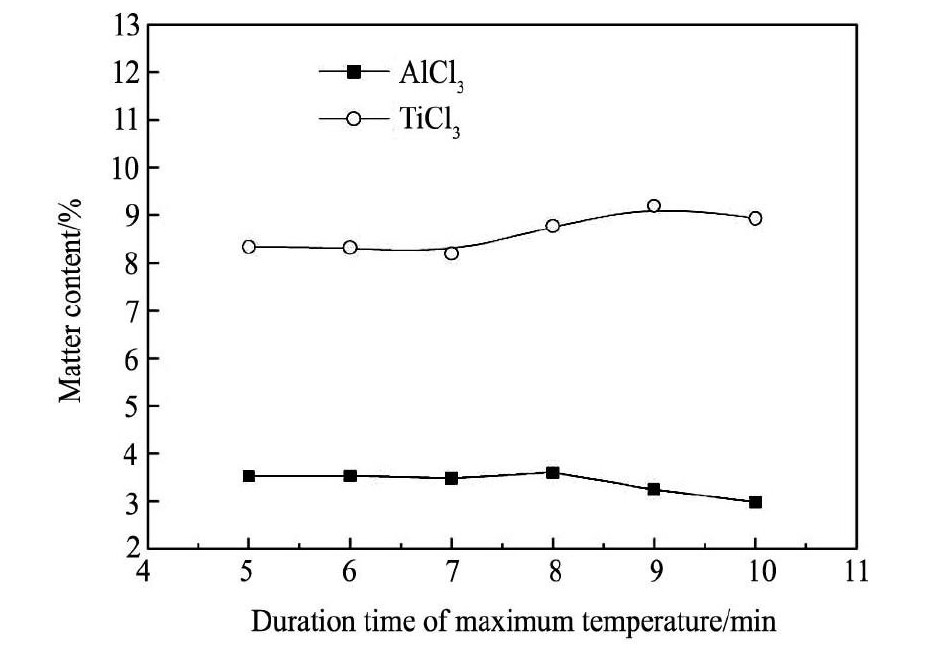
图7 高温持续时间对除钒试剂中 Al Cl3,Ti Cl3含量影响 Fig.7Effect of duration time of maximum temperature on Al Cl3and Ti Cl3contents in vanadium removing reagent
图7结果表明: 除钒试剂中Ti Cl3含量随着高温持续时间的延长而增加,Al Cl3含量随其延长而减少。与高温持续5 ~7 min相比,持续8 ~10 min时, 除钒试剂中Ti Cl3含量较高,表明高温持续时间越长除钒试剂中Ti Cl3含量越高,且其含量在8%~ 10% 的理想值内; 当高温持续时间大于9 min时,除钒试剂中Al Cl3含量均低于3. 5% 。因此,高温持续时间在8 ~10 min之间时,除钒试剂制备效果较好。
2. 5工艺优化验证实验通过探索实验结果分析得出除钒试剂制备过程的优化工艺参数,列于表3。
图8为优化工艺参数条件下除钒试剂制备过程最高温度变化图。由图8结果可知: 优化工艺参数后,除钒试剂制备过程中反应最高温度均大于131 ℃ ,平均温度为132. 4 ℃ ,表明反应释放热量充分,反应顺利进行。
图9为优化工艺参数后制备所得除钒试剂中Ti Cl3与Al Cl3含量情况。
由图9可知: 优化工艺参数条件下制备所得除钒试剂矿浆中Ti Cl3含量较稳定,其变化范围为8. 24% ~ 9. 24% ,平均含量为8. 93% ; Al Cl3含量维持在2. 67%~ 3. 68% 之间,结果理想。
表3 除钒试剂制备过程优化后工艺参数 Table 3 Optimized parameters of vanadium removing reagent preparation process 下载原图

表3 除钒试剂制备过程优化后工艺参数 Table 3 Optimized parameters of vanadium removing reagent preparation process
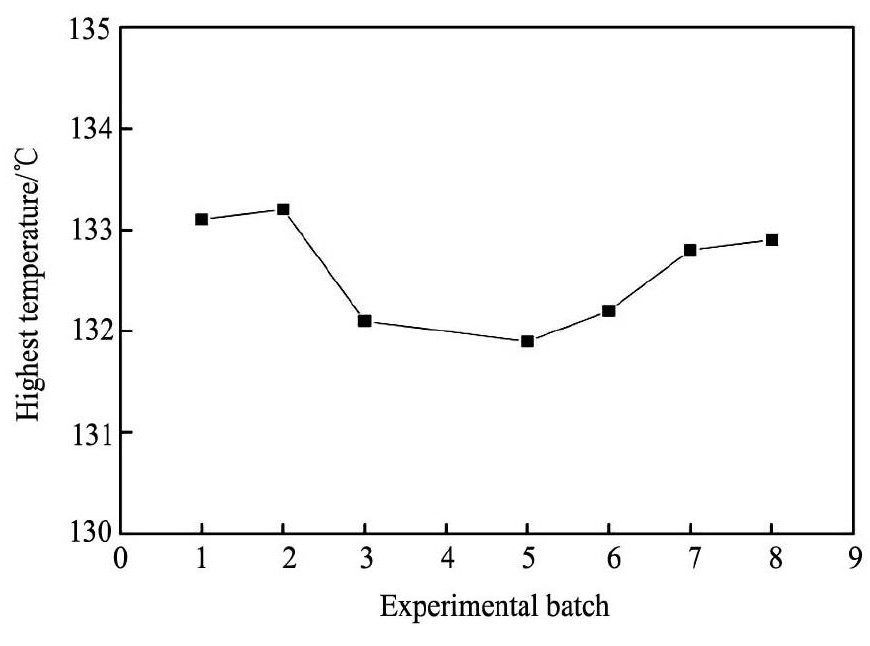
图8 优化工艺参数后反应最高温度 Fig.8 Hightest temperature after optimizing parameters

图9 除钒试剂中 Ti Cl3与 Al Cl3含量变化图 Fig.9 Ti Cl3and Al Cl3contents in vanadium removing reagent
2. 6除钒试剂的应用为考察优化工艺参数后制备所得除钒试剂矿浆的除钒效果,开展了除钒试剂的应用实验研究。实验在蒸馏釜中进行,控制蒸馏釜温度为140 ℃,平均每吨粗Ti Cl4中加入70 ~ 80 kg除钒试剂进行除钒作业,实验条件及结果列于表4。
表4结果表明: 当粗Ti Cl4中VOCl3含量在0. 0963% ~ 0. 1116% 之间时,采用优化工艺参数后制备所得除钒试剂的除钒效果较好。通过蒸馏釜中的除钒操作,可使粗Ti Cl4中VOCl3含量降低至0. 0003% ,满足国家标准中一级精Ti Cl4对VOCl3含量要求,同时也满足海绵钛后续生产工艺需要。
表4 除钒试剂的应用结果 Table 4 Application results of vanadium removing reagent ( %) 下载原图
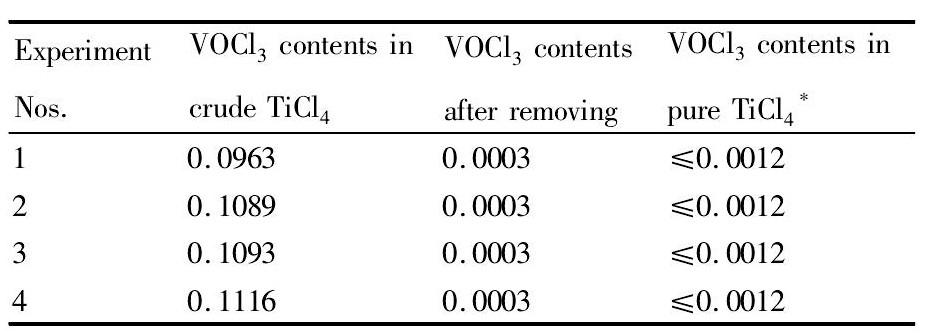
* Chinese National Standard
表4 除钒试剂的应用结果 Table 4 Application results of vanadium removing reagent ( %)
3结论
1. 热力学分析结果表明: 温度为25 ~ 140 ℃ 时,Al粉与精Ti Cl4能够在通氯条件下反应生成低价钛除钒试剂。温度为90 ~ 150 ℃ 时能使溶于粗Ti Cl4中的VOCl3转变为不溶于Ti Cl4的VOCl2沉淀除去。
2. 铝粉悬浮液中铝含量为30 ~ 35 g・L- 1,Cl2浓度为85%~ 90% 、停止通氯温度为105 ℃、反应器内最高温度持续时间为8 ~ 10 min是制备除钒试剂的较优工艺参数。
3. 优化工艺参数后制备所得除钒试剂质量稳定,Ti Cl3含量为8. 24% ~ 9. 24% 、Al Cl3含量2. 67% ~ 3. 68% 。除钒试剂的除钒效果好,可使粗Ti Cl4中VOCl3含量由0. 1116% 降低至0. 0003% 。