文章编号:1004-0609(2014)11-2813-08
高倍率锂离子电池正极材料LiCo0.9Ni0.05Mn0.05O2的合成及电化学性能
曹景超,胡国荣,彭忠东,杜 柯,曹雁冰
(中南大学 冶金与环境学院,长沙 410083)
摘 要:以碳酸氢铵为沉淀剂采用共沉淀法合成球形Co0.9Ni0.05Mn0.05CO3前驱体,以碳酸盐前驱体和Li2CO3为原料,在空气中通过固相反应制备出LiCo0.9Ni0.05Mn0.05O2正极材料,研究烧结温度对产物结构及电化学性能的影响。采用扫描电镜(SEM)、X射线衍射(XRD)和光电子能谱(XRS)分别表征样品的形貌、结构和元素价态。结果表明:不同烧结温度下合成产物的性能差别很大,较适合的合成温度为900 ℃;在3.0~4.5 V电压范围内,LiCo0.9Ni0.05Mn0.05O2显示出较好的倍率性能;在25 ℃测试条件下,材料在0.2C、0.5C、1C、5C和10C时的放电比容量分别为181.6、178.3、173.9、167.8和157.1 mA・h/g。
关键词:锂离子电池;正极材料;碳酸氢铵;共沉淀
中图分类号:TM12.9 文献标志码:A
Synthesis and electrochemical properties of LiCo0.9Ni0.05Mn0.05O2 cathode material with high rate capability for lithium ion batteries
CAO Jing-chao, HU Guo-rong, PENG Zhong-dong, DU Ke, CAO Yan-bing
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
Abstract: The spherical precursor of metal carbonate, Co0.9Ni0.05Mn0.05CO3, was prepared by co-precipitation method using NH4HCO3 as precipitating agent. LiCo0.9Ni0.05Mn0.05O2 was prepared by solid-state reaction method in air using Co0.9Ni0.05Mn0.05CO3 and Li2CO3 as starting materials. The effects of sintering temperature on the structure and electrochemical properties of the product were studied. The morphology and structure of LiCo0.9Ni0.05Mn0.05O2 were characterized by SEM and XRD, respectively. The valence state of transition metal was determined by XPS. The results show that sintering temperature has a critical role in the performance of the product and the suitable sintering temperature is 900 ℃. LiCo0.9Ni0.05Mn0.05O2 exhibits good cycle performance and high rate capability within the voltage range of 3.0-4.5 V. At 25 ℃, the initial discharge capacity are 181.6, 178.3, 173.9, 167.8 and 157.1 mA・h/g at 0.2C, 0.5C, 1C, 5C and 10C, respectively.
Key word: lithium-ion battery; cathode material; ammonium bicarbonate; co-precipitation
锂离子电池具有工作电压高、比能量高、容量大、自放电小、循环性能好和使用寿命长等优点,已成为移动电话、笔记本电脑等便携式电子设备的理想电源[1-4]。目前,商业化用的最广的锂离子电池正极材料是LiCoO2,但是,因为钴资源匮乏,且在常规充放电压范围内(3.0~4.3 V)容量发挥受到限制,仅为理论容量的一半左右(140 mA・h/g)[5]。最近,以通式为LiCo1-2xNixMnxO2的一系列层状高钴正极材料成为众多科学工作者的研究对象。ZENG等[6]研究了Li[NiyMnyCo(1-2y)]O2(y=0.05)结构变化,证明该材料在电化学过程中的稳定性,为后期工作者提供了理论基础。SAADOUNE等[7]研究了LiCo0.8Ni0.1Mn0.1O2在脱嵌过程中材料的结构稳定性,其可逆容量达到180 mA・h/g,但其循环性能有待改善。同时,BENTALE等[8]研究了LiCo0.6Ni0.2Mn0.2O2在2.7~4.3 V条件下不同倍率的电化学性能,但是没有研究材料在较高截止充电电压(电压大于4.3 V)下材料的性能。MAHMOUD等[9]通过燃烧法合成了LiCo2/3Ni1/6Mn1/6O2材料,在充电电压为2.7~4.6 V时,材料的放电比容量达到199 mA・h/g,循环50周后容量衰减到150 mA・h/g;在充电范围2.7~4.5 V内,0.05C倍率下首次放电容量达到178 mA・h/g,但是材料的循环和倍率性能仍需要很大的改善。在LiCo1-2xNixMnxO2系列材料中,由于Mn以Mn4+形式存在,在电化学充放电过程中为非活性状态,过多Mn的掺入导致材料的放电比容量降低[7]。Ni2+在充放电过程中尤其是在电压大于4.4 V时可以释放出更高的容量,这主要是因为Ni2+释放两个电子被氧化成Ni4+,但是Ni2+(r=0.69 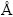 )和Li+(r=0.76
)和Li+(r=0.76 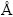 )离子半径差别不大,在高温烧结时容易出现阳离子混排,Ni含量越高,阳离子混排越严重,导致材料的结构稳定性变差[10]。在此,以碳酸氢铵为沉淀剂采用共沉淀法制备了球形前驱体Co0.9Ni0.05Mn0.05CO3,再将前驱体与Li2CO3混合,通过高温煅烧的方法得到了高倍率性能的LiCo0.9Ni0.05Mn0.05O2正极材料,研究了烧结温度对材料性能的影响,并用XRD和SEM对结构和形貌进行了分析。
)离子半径差别不大,在高温烧结时容易出现阳离子混排,Ni含量越高,阳离子混排越严重,导致材料的结构稳定性变差[10]。在此,以碳酸氢铵为沉淀剂采用共沉淀法制备了球形前驱体Co0.9Ni0.05Mn0.05CO3,再将前驱体与Li2CO3混合,通过高温煅烧的方法得到了高倍率性能的LiCo0.9Ni0.05Mn0.05O2正极材料,研究了烧结温度对材料性能的影响,并用XRD和SEM对结构和形貌进行了分析。
1 实验
1.1 材料制备
以CoSO4・7H2O(纯度99.0%,浙江华友钴业生产)、NiSO4・6H2O(纯度99.0%,吉林吉恩镍业股份有限公司生产)和 MnSO4・H2O(纯度99.0%,湖南佳飞新材料有限公司生产)配制成浓度为1.5 mol/L离子混合溶液,其中Co2+、Ni2+、Mn2+摩尔比为18:1:1。同时配制3 mol/L碳酸氢铵溶液。在容积为50 L的反应釜中加入以10 L碳铵溶液和5 L去离子水作为底液,用蠕动泵分别将金属混合溶液和碳酸氢铵溶液连续输入到反应釜中。整个进料过程中温度控制在45 ℃,pH值为8.0,搅拌速度400 r/min。待金属混合液滴加完毕后继续搅拌2 h,将反应得到的沉淀物经去离子水洗涤3次,过滤后在80 ℃真空干燥箱内干燥24 h,最终得到前驱体Co0.9Ni0.05Mn0.05CO3。
按物质的量比1.01:1称取Li2CO3(纯度99.5%,四川天齐锂业生产)和上述前驱体,混合均匀后放入马弗炉中焙烧,在空气气氛下以2 ℃/min的升温速度焙烧20 h,自然冷却至室温,即可得到LiCo0.9Ni0.05Mn0.05O2正极材料。然后将产品粉碎、研磨,并用孔径149 μm的筛子过筛。
1.2 实验仪器
采用日本Rigaku公司生产Minflex型的X射线自动衍射仪对产物的结构进行测试,实验条件如下: Cu Kα辐射;管电压为40 kV;管电流为250 mA;扫描速度为10 (°)/min;扫描角度2θ为10°~80°;步长为0.02°;采用日本JEOL公司JSM-5600LV型扫描电子显微镜对产物的颗粒大小和表面形貌进行观察。采用英国Malvern公司生产的Microplus激光粒度分析仪对样品进行测定。
1.3 电池组装与测试
将样品与乙炔黑、PVDF粘结剂按质量比8.5:1.5:1均匀混合,再加入适量有机溶剂N-甲基吡咯烷酮(NMP)继续研磨至黑色糊状物质。将糊状物均匀涂在铝箔上,再置于60 ℃的烘箱中干燥1~2 h,之后置于120 ℃烘箱中真空干燥24 h,然后轧制成正极片。以金属锂为对负极,Celgard 2400多孔聚乙烯膜为隔膜,1 mol/L LiPF6的EC、DMC和EMC(体积比1:1:1)的混合溶液为电解液,在水和氧含量均小于1×10-6的充满氩气的手套箱(上海米开罗那机电技术有限公司生产,Universal 2440/750)中组装成扣式实验电池,用电池测试系统(武汉市金诺电子有限公司生产,LAND CT2001A)对扣式电池进行在恒温25 ℃下进行充放电测试,电压范围为3.0~4.5 V。
2 结果与讨论
2.1 前驱体的形貌与结构
图1所示为采用碳酸氢铵为沉淀剂以共沉淀法合成的碳酸盐Co0.9Ni0.05Mn0.05CO3前驱体的SEM像。从图1可以看出,前驱体二次颗粒呈规整球形、且由细微的一次颗粒紧密团聚而成。颗粒的平均粒径约为15 μm。
图2所示为合成的Co0.9Ni0.05Mn0.05CO3前驱体的XRD谱。从图2可以看出,合成的前驱体的XRD谱中的主峰与CoCO3的主峰位置相吻合,而与MnCO3和NiCO3的主峰位置有所偏差,主要是因为材料中钴含量较高,而锰和镍的含量较低。整体谱中并未形成杂峰,说明得到了碳酸盐结构的前驱体。
2.2 正极材料LiCo0.9Ni0.05Mn0.05O2的性能
2.2.1 LiCo0.9Ni0.05Mn0.05O2样品的形貌分析

图1 前驱体Co0.9Ni0.05Mn0.05CO3的SEM像
Fig. 1 SEM images of Co0.9Ni0.05Mn0.05CO3 precursor
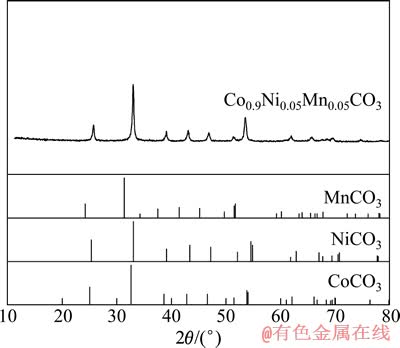
图2 Co0.9Ni0.05Mn0.05CO3的XRD谱
Fig. 2 XRD patterns of obtained Co0.9Ni0.05Mn0.05CO3
图3所示为不同温度下合成LiCo0.9Ni0.05Mn0.05O2 样品的SEM像。从图3可以看出,在配锂高温烧结后,不规则的LiCo0.9Ni0.05Mn0.05O2一次颗粒长大并紧密地团聚成二次球形颗粒。相比于前驱体,LiCo0.9Ni0.05Mn0.05O2的表面变得粗糙,这主要是由于前驱体经过锂化后生成的不规则一次单晶颗粒堆垛造成的。观察样品的一次颗粒可以看出,800 ℃下合成材料的一次颗粒粒径最小,平均粒径小于1 μm,在850 ℃下合成的样品一次颗粒略有长大,当温度升到950 ℃时,一次颗粒的平均粒径约为2 μm。说明随着温度的升高,一次颗粒略有长大,温度的升高较大程度上促进了晶粒的生长。一般认为颗粒过大会导致锂离子在固相中扩散距离增加,颗粒中心的部分活性物质难以脱嵌锂,从而导致容量下降和倍率性能变差。
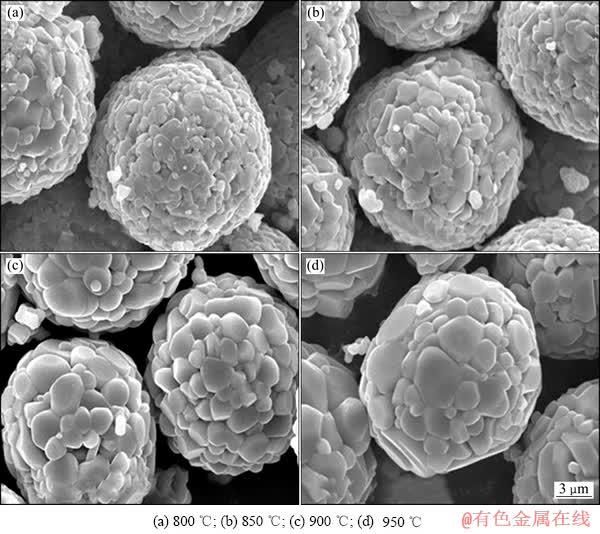
图3 不同温度下合成LiCo0.9Ni0.05Mn0.05O2的SEM像
Fig. 3 SEM images of LiCo0.9Ni0.05Mn0.05O2 materials synthesized at different temperatures
2.2.2 LiCo0.9Ni0.05Mn0.05O2样品的结构
图4所示为800、850、900和950 ℃下反应20 h 合成的LiCo0.9Ni0.05Mn0.05O2样品的XRD谱。从图4中可以看出,该正极材料的XRD谱可以归属为空间群为 型的α-NaFeO2型层状结构。对比不同温度下合成材料的XRD谱可发现,各衍射峰的强度和尖锐程度受烧结温度影响。800 ℃时,合成的样品已具有纯相LiCo0.9Ni0.05Mn0.05O2的层状结构,但衍射峰强度稍弱。且随着合成温度的升高,产物的结晶度加强。900 ℃时,合成的样品的(006)和(102)以及(018)和(110)的两组峰的分裂明显,表明在此条件下合成的材料具有良好的层状结构[11]。
型的α-NaFeO2型层状结构。对比不同温度下合成材料的XRD谱可发现,各衍射峰的强度和尖锐程度受烧结温度影响。800 ℃时,合成的样品已具有纯相LiCo0.9Ni0.05Mn0.05O2的层状结构,但衍射峰强度稍弱。且随着合成温度的升高,产物的结晶度加强。900 ℃时,合成的样品的(006)和(102)以及(018)和(110)的两组峰的分裂明显,表明在此条件下合成的材料具有良好的层状结构[11]。
LiCo0.9Ni0.05Mn0.05O2具有与LiCoO2类似的层状结构,过渡金属离子(Co,Ni,Mn)占据3b位置,氧原子占据6c位置,3a位置上的Li+与3b位置上的Ni2+由于离子半径相近,在高温下容易发生交错占据,产生阳离子混排[11-13]。对比图4中在950 ℃下合成的材料的XRD谱与800、850和900 ℃下合成的材料的XRD谱可以发现,在950 ℃下合成的材料的XRD谱产生微小的杂质峰,这可能是由Li+和Ni2+在高温下发生阳离子混排导致。
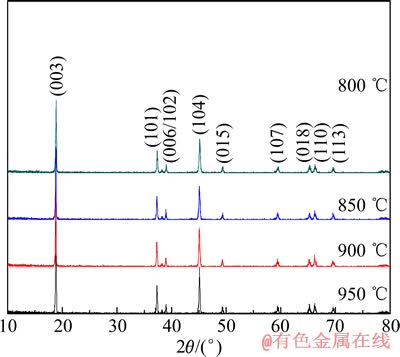
图4 不同温度下保温20 h合成LiCo0.9Ni0.05Mn0.05O2样品的XRD谱
Fig. 4 XRD patterns of LiCo0.9Ni0.05Mn0.05O2 samples synthesized at different temperatures for 20 h
由图4的XRD谱可计算出样品的晶胞参数(a和c)、c/a值以及I003/I104强度比,各样品的具体数据见表1。从表1可以看出,在各温度条件下合成的样品的晶胞参数c/a 值均大于理想的立方密堆积结构的c/a 值(4.899)[14],这表明各样品均已具有较为完整的层状结构。I003/I104值可以用来衡量材料中的阳离子混排程度[15],其值越大,阳离子混排程度越小,一般认为其值大于1.2时,形成的层状结构较好[16]。温度从800 ℃升高到900 ℃时,晶胞参数a、c、c/a和I003/I104逐渐增大(见表1)。这表明,随着合成温度的升高,晶格应力减小,微晶尺寸增大。但是,当合成温度升至950 ℃时,相应的晶胞参数又有所下降,这可能是由温度过高引起阳离子混排造成的。
表1 不同温度下反应20 h合成的LiCo0.9Ni0.05Mn0.05O2的晶胞参数及强度比值
Table 1 Lattice parameters and I003/I104 of LiCo0.9Ni0.05Mn0.05O2 samples synthesized at different temperatures for 20 h

图5所示为900 ℃保温20 h合成的LiCo0.9Ni0.05Mn0.05O2样品中Co、Ni、Mn和O的XPS谱。从图5可以看出,Co 2p3/2和Co 2p1/2 结合能分别为780.3和795.6 eV,这与之前报道的LiCoO2[17]的性能很接近,这说明在高温煅烧过程中,Co2+完全氧化成Co3+。元素Ni的2p3/2结合能为855.6 eV,与OSWALD等[18]报道的Ni(OH)2中Ni的接近,说明在LiCo0.9Ni0.05Mn0.05O2中,Ni以Ni2+形式存在。而Mn 2p3/2和Mn 2p1/2的结合能分别为642.5和653.8 eV,它和文献[19]中报道的MnO2中Mn4+的大小一致,都与MnO2标准XPS衍射谱相符[20],说明Mn是以Mn4+形式存在。非活性Mn4+在LiCo0.9Ni0.05Mn0.05O2起到支撑骨架的作用,提高了材料结构的稳定性。
2.2.3 LiCo0.9Ni0.05Mn0.05O2样品的电化学性能
图6(a)所示为在800、850、900和950 ℃条件下保温20h合成的LiCo0.9Ni0.05Mn0.05O2样品在电压范围3.0~4.5 V内0.2C时的首次充放电曲线。从图6(a)中可以看出,随着合成温度从800 ℃升高到900 ℃,初次放电比容量由162.4 mA・h/g提高到182.6 mA・h/g,说明随着温度的升高,晶体结构更加完整,但是当温度到达950 ℃时,初次放电比容量却下降到170.4 mA・h/g,分析样品的XRD谱可知,温度过高,材料中Ni2+和Li+发生阳离子混排影响了材料的电化学性能,因此,放电比容量下降。图6(b)所示为不同温度下合成的LiCo0.9Ni0.05Mn0.05O2样品循环曲线。从图6(b)中可以看出,800、850和900 ℃温度下材料具有较好的循环性能,50个循环后,容量保持率分别高达95.9%、95.2%和97.5%。温度为950℃时,材料循环性能明显下降,50个循环后容量保持率仅为91.7%。这可能是因为一定范围内提高合成温度有助于晶体的发育和规整,而过高的合成温度将造成Li和O的挥发及晶体分解。综上所述,900℃为本实验范围内的最佳合成温度。
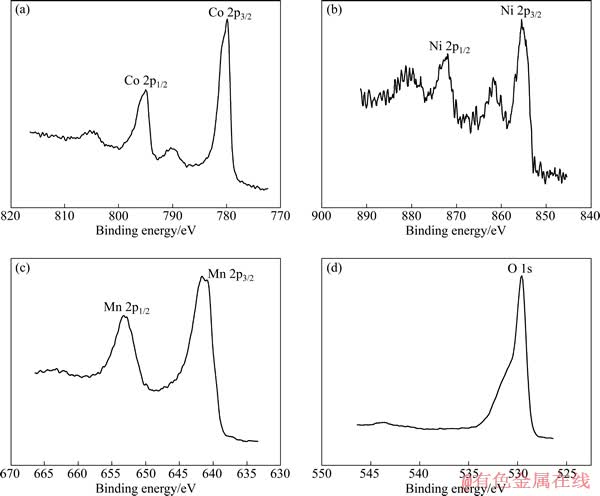
图5 LiCo0.9Ni0.05Mn0.05O2样品中元素Co、Ni、Mn和O的XPS谱
Fig. 5 XPS spectra of Co, Ni, Mn and O in LiCo0.9Ni0.05Mn0.05O2
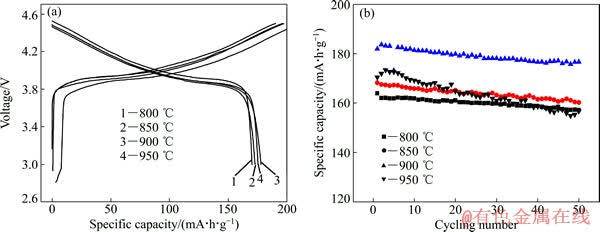
图6 不同温度下合成LiCo0.9Ni0.05Mn0.05O2样品在0.2C、电压范围3.0~4.5 V时的首次充放电曲线和循环
Fig. 6 First charge-discharge curves (a) and cycle performance (b) of LiCo0.9Ni0.05Mn0.05O2 samples synthesized at different temperatures with 0.2C between 3.0-4.5 V
倍率性能是锂离子电池正极材料的关键性指标[21]。为了研究LiCo0.9Ni0.05Mn0.05O2正极材料的倍率性能,选用在900 ℃下合成的材料为代表。图7(a)反应了900 ℃合成材料在不同倍率下的首次充放电容量。从图中可以看出,900 ℃合成材料在0.2C、0.5C、1C、5C和10C下充电比容量分别为182.5、180.7、174.3、169.4和159.9 mA・h/g,首次放电比容量分别181.6、178.6、173.2、167.6和157.1 mA・h/g,对应的库仑效率分别为99.5%、98.8%、99.3%、98.8%和98.2%;相对于0.2C下的放电比容量,0.5C、1C、5C和10C的相对容量保持率分别达到98.3%、95.4%、92.3%和86.5%,显示出较好的倍率性能。图7(b)所示为倍率循环图,电池的充放电制度为首先在0.2C下充放10周,然后依次在0.5C、1C、5C和10C下充放10周,最后在返回小倍率0.2C充放。从图7(b)中可以看出,即使在10C的电流密度下放电10周,材料仍保持较好的循环性能。最后的10次小倍率(0.2C)充放电仍能保持较高的容量(170 mA・h/g以上),且循环10次后,并没有明显的衰减,表明经历10C倍率下充放电过程并没有破坏材料的层状结构。
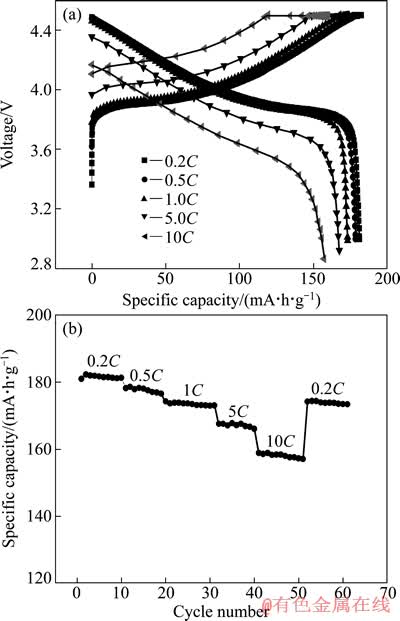
图7 900 ℃合成Li/LiCo0.9Ni0.05Mn0.05O2在不同倍率下的充放电曲线与循环
Fig. 7 Initial charge-discharge (a) and cycle number (b) curves at various current densities of LiCo0.9Ni0.05Mn0.05O2 prepared at 900 ℃
为了进一步研究LiCo0.9Ni0.05Mn0.05O2在高倍率下结构的稳定性,测试了材料不同倍率下的循环性能。如图8所示。由图8可以看出,0.2C、0.5C、5C和10C的首次放电比容量分别为181.6、178.6、167.6和157.1 mA・h/g,循环50周后的容量分别为176.6、171.8、160.4和136.5 mA・h/g,容量保持率分别为97.8%、96.2%、95.7%和86.9%。LiCo0.9Ni0.05Mn0.05O2之所以在大倍率放电保持良好的结构稳定性,原因主要如下:1) 由于非活性Mn4+的掺入,在电化学过程中未参与化学反应,而是起到支撑结构框架的作用;2) 材料具有规整球形二次颗粒,小的一次颗粒紧密团聚在一起,有利于锂离子的快速扩散。

图8 LiCo0.9Ni0.05Mn0.05O2在不同倍率下的循环性能
Fig. 8 Cycle performance of LiCo0.9Ni0.05Mn0.05O2 with various current densities
3 结论
1) 通过共沉淀法制备了前驱体Co0.9Ni0.05Mn0.05CO3,再将前驱体与Li2CO3混合,通过高温煅烧的方法得到了LiCo0.9Ni0.05Mn0.05O2正极材料。通过XRD、SEM、XPS及电化学性能测试分析表明,合成温度对LiCo0.9Ni0.05Mn0.05O2材料的晶体结构、电化学性能有着明显的影响。
2) LiCo0.9Ni0.05Mn0.05O2正极材料中Mn以Mn4+形式存在,在结构中起到支撑骨架作用,有利于提高材料结构的稳定性。
3) 选取较小镍、锰取代量的LiCo0.9Ni0.05Mn0.05O2作为研究对象,以提高材料的循环和倍率性能。通过电化学测试结果得出:当充电截止电压达到4.5 V时仍具有良好的倍率和循环性能,0.2C、0.5C、5C和10C首次放电比容量分别181.6、178.6、167.6和157.1 mA・h/g,循环50周后的容量分别为176.6、171.8、160.4和136.5 mA・h/g,容量保持率分别为97.8%、96.2%、95.7%和86.9%。
REFERENCES
[1] 张 宝, 张 明, 李新海, 王志兴, 郭华军, 彭文杰. 锂离子电池正极材料LiCo0.1Ni0.45Mn0.45O2合成及电化学性能[J]. 中南大学学报: 自然科学版, 2008, 39(1): 75-79.
ZHANG Bao, ZHANG Ming, LI Xin-hai, WANG ZHi-xing, GUO Hua-jun, PENG Wen-jie. Synthesis and electrochemical properties of LiCo0.1Ni0.45Mn0.45O2 cathode material for lithium ion batteries[J]. Journal of Central South University: Science and Technology, 2008, 39(1): 75-79.
[2] 朱伟雄, 李新海, 王志兴, 郭华军. 锂离子电池富锂材料Li[Li0.2Ni0.2Mn0.6]O2的制备及掺杂改性[J]. 中国有色金属学报, 2013, 23(4): 1047-1052.
ZHU Wei-xiong, LI Xin-hai, WANG Zhi-xing, GUO Hua-jun. Synthesis and modification of Li-rich cathode Li[Li0.2Ni0.2Mn0.6]O2 for Li-ion batteries[J]. The Chinese Journal of Nonferrous Metals: 2013, 23(4):1047-1052.
[3] HAO Qin, XU Cai-xia, JIA Su-zhen. Improving the cycling stability of LiCoO2 at 4.5V through surface modification by Fe2O3 coating[J]. Electrochimca Acta, 2013, 113: 439-445.
[4] 杜 柯, 黄 霞, 胡国荣, 彭忠东. 高容量正极材料Li[Li0.2Ni0.2Mn0.6]O2的合成及电化学性能[J]. 中国有色金属学报, 2012, 22(4): 1202-1208.
DU Ke, HUANG Xia, HU Gong-rong, PENG Zhong-dong. Synthesis and electrochemical properties of Li[Li0.2Ni0.2Mn0.6]O2 as high capacity cathode material[J]. The Chinese Journal of Nonferrous Metals, 2012, 22(4): 1202-1208.
[5] CHO J, KIM G. Enhancement of thermal stability of LiCoO2 by LiMn2O4 coating[J]. Electrochem Solid-State Lett, 1999, 2: 253-255.
[6] ZENG Dong-li, CABANA J, YOON W S, GERY C P. Investigation of the structure changes in Li[NiyMnyCo(1-2y)]O2(y=0.05) upon electrochemical lithium deintercalation[J]. Chem Mater, 2010, 22: 1209-1219.
[7] SAADOUNE I, LABRINI M, YAHYA M, ALMAGGOUSSI A, EHRENBERG H. LiNi0.1Mn0.1Co0.8O2 electrode material: Structure changes upon lithium electrochemical extraction[J]. Electrochim Acta, 2010, 55: 5180-5185.
[8] BENTALEB Y, SAADOUNE I, KENZA M, SAADI L, FUJIMOTO K, ITO S. On the LiNi0.2Mn0.2Co0.6O2 positive electrode material[J]. Journal of Power Sources, 2010, 195: 1510-1515.
[9] MAHMOUD A, SAADOUNE I, AMARILL J M. On the LiCo2/3Ni1/6Mn1/6O2 positive electrode material[J]. Electrochim Acta 2011, 56: 4081-4086.
[10] WHITFIELD P S, DAVIDSON I J, CRANSWICK L M D. Investigation of possible superstructure and cation disorder in the lithium battery cathode material LiMn1/3Ni1/3Co1/3O2 using neutron and anomalous dispersion powder diffraction[J]. Solid State Ionics, 2005, 176(5/6): 463-471.
[11] 王希敏, 王先友, 易四勇, 曹俊琪. 层状锂离子电池正极材料LiNi0.8Co0.1Mn0.1O2的制备及性能[J]. 过程工程学报, 2007, 7(4): 817-821.
WANG Xi-min, WANG Xian-you, YI Si-yong, CAO Jun-qi. Synthesis and characteristics of layered LiNi0.8Co0.1Mn0.1O2 cathode material for lithium rechargeable batteries[J]. The Chinese Journal of Process Engineering, 2007, 7(4): 817-821.
[12] 马全新, 孟军霞, 杨 磊, 曹 文. 锂离子电池正极材料LiNi0.5Co0.2Mn0.3O2的制备及电化学性能[J]. 中国有色金属学报, 2013, 23(2): 456-462.
MA Quan-xin, MENG Jun-xia, YANG Lei, CAO Wen. Preparation of Li-ion battery cathode material LiNi0.5Co0.2Mn0.3O2 and its electrochemical performances[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(2): 456-462.
[13] 赵军峰. 三元系锂离子电池正极材料的制备与研究[D]. 长沙: 中南大学, 2011.
ZHAO Jun-feng. Preparation and study of the performance of lithium-nickel-cobalt-manganese oxides cathode material for lithium-ion batteries[D]. Changsha: Central South University, 2011.
[14] 叶 茂, 周 震, 卞锡奎, 阎 杰. 电解Co-Ni-Mn合金制备LiCo1/3Ni1/3Mn1/3O2正极材[J]. 无机化学学报, 2006, 22(11): 2006-2010.
YE Mao, ZHOU Zhen, BIAN Xi-kui, YAN Jie. Structual and electrochemical properties of LiCo1/3Ni1/3Mn1/3O2 cathode material by electrolysis of Co-Ni-Mn alloy[J]. Chinese Journal of Inorganic Chemistry, 2006, 22(11): 2006-2010.
[15] KIM Y, KIM H S, MARTIN S W. Synthesis and electrochemical characteristics of Al2O3-coated LiNi1/3Co1/3- Mn1/3O2cathode materials for lithium ion batteries[J]. Electrochim Acta, 2006, 52: 1316-1322.
[16] LUZ C H, WANG H C. Microemulsion-mediated synthesis and electrochemical characterization of nanosized LiNi0.25Co0.5- Mn0.25O2 powders[J]. Electrochemical Society, 2005, 152(6): C341-C347.
[17] DUPIN J C, GONBEAU D, MOUDDEN H B. XPS analysis of new lithium cobalt oxide thin-films before and after lithium deintercalation[J]. Thin Solid Films, 2001, 384: 23-32.
[18] OSWALD S,  W. XPS depth profile analysis of non-stroichiometric NiO films[J]. Surface and Interface Analysis, 2004, 36: 17-22.
W. XPS depth profile analysis of non-stroichiometric NiO films[J]. Surface and Interface Analysis, 2004, 36: 17-22.
[19] TSAI Y W, LEE J F, LIU D G. In-situ X-ray absorption spectroscopy investigations of a layered LiNi0.65Co0.25Mn0.1O2 cathode material for rechargeable lithium batteries[J]. Journal of Materials Chemistry, 2004 14: 958-965.
[20] GALAKHOV V R, KOROTIN M A, OVECHKINA N A, KURMAEV E Z, GORSHKOV E Z, GORSHKOV V S, KELLERMAN D G, BARTKOWSKI S, NEUMANN M. Electronic structure of LiMnO2: X-ray emission and photoelectron spectra and band structure calculations[J]. J Eur Phys, 2000, 14: 281-286.
[21] 黄 果, 杨顺毅, 雷钢铁, 黄友元, 岳 敏, 胡社军, 任建国, 侯贤华. Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2)正极材料的喷雾干燥法合成及电化学性能[J]. 中国有色金属学报, 2014, 24(3): 725-732.
HUANG Guo, YANG Shun-yi, LEI Gang-tie, HUANG You-yuan, YUE Min, HU She-jun, REN Jian-guo, HOU Xian-hua. Spray drying synthesis and electrochemical performance of Li(1+x)Ni0.166Co0.166Mn0.667O(2.175+x/2) cathode materials[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(3): 725-732.
(编辑 龙怀中)
基金项目:国家自然科学基金资助项目(50604018);中央高校基本科研业务费资金资助项目(2012QNZT018)
收稿日期:2014-06-27;修订日期:2014-09-20
通信作者:胡国荣,教授,博士;电话:0731-88830474;E-mail:hgrhsj@263.net