���±�ţ�1004-0609(2007)07-1172-05
M�ͱ���������������ܽ�-�����Ʊ���ᾧ����
���1, 2�����1
(1. ɽ����ѧ ����Һ̬�ṹ�����Ŵ��Խ������ص�ʵ���ң����� 260061��
2. ɽ����ͨѧԺ ��ľ����ϵ������ 250023)
ժ Ҫ�� �Ի�ѧ�����ȵ����ᱵ����������������Ϊԭ�ϲ����ܽ�-���������Ʊ�M�ͱ������������壬ͨ��XRD��TEM�Ȳ����ֶα�������Ľᾧ���Լ��۽ṹ�����о���Ӧ�����Լ��ս��¶ȡ�����ʱ��Ծ����ߴ��Ӱ�죬��������������ƽ�������ߴ�Ϊ40~70 nm���ս��¶�����Ӱ��ᾧ���̡������ߴ缰��ֲ����ս��¶�Ϊ800 �棬����ʱ��Ϊ0.5 h���������γɵķ�������ʰ�״�����ij���ԼΪ150~200 nm��ֱ��ԼΪ30~50 nm��
�ؼ��ʣ�M�ͱ������壻�ܽ�-�������գ��ᾧ���ԣ��ս�
��ͼ����ţ�O 614.23���� ���ױ�ʶ�룺A
Preparation and crystalline properties of M-type barium ferrite nanopowder by sol-gel process
SUN Chang1, 2, SUN Kang-ning1, 2
(1. Key Laboratory of Liquid Structure and Heredity of Materials, Ministry of Education,
Shandong University, Ji��nan 250061, China;
2. Department of Civil Engineering, Shandong Jiaotong University, Ji��nan 250023, China)
Abstract: M-type barium ferrite (BaFe12O19) nanopowders were synthesized by a sol-gel process. The crystalline properties and morphologies of the powders were characterized by means of X-ray diffraction (XRD) and transmission electron microscope (TEM). The reaction mechanism and the effects of calcinations temperature and calcinations time on grain size were studied. The results show that M-type barium ferrite powders with the average grain size range of 40-70 nm can be prepared at 800 �� and the calcinations temperature has obvious influence on crystalline process, the particle size and its distribution. The as-prepared samples obtained after heat-treatment at 800 �� for 0.5 h exhibit that the rod-like particles have a length of about 150-200 nm and a diameter of about 30-50 nm.
Key words: M-type barium ferrite; sol-gel process; crystalline property; calcination
M�ͱ�������(BaFe12O19)���ж��ص�������ѧ���ʣ���һ����Ҫ��Ӳ�Ų��ϣ����㷺Ӧ���ڸ��ܶȴż�¼ý�顢�����塢��ɫ��ʾ�������ռ�������[1-5]��M�ͱ�������ʸ߱��ʹŻ�ǿ��(Ms =70 Am2/kg������)��ǿ�����������[6-7]�����Ǿ�ϵ�����廹����Ƭ״�ṹ��Ƭ״�ṹ����������ѵĽṹ��Ϊ��þ���������ܵ�M�ͱ������壬�����Ʊ����ձ������Ʊ�M�ͱ���������壬���绯ѧ�������������¹�̬��Ӧ��ˮ�ȷ����ܽ�-��������[2, 8-14]���ܽ�-�������վ��з���ˮƽ���ʻ�ϡ��ϵ͵��ȴ����¶ȡ������Ʊ��������ͱ�Ĥ���������ƣ���ˣ��ܽ�-�������ճ���������������������-�մɺ��մɷ��塣���Ʊ��������������о��У���������[15]����������Ϊǰ���壬�õ�������Ϊ30~80 nm, ��ȱ��ʹŻ�ǿ��Ms=60.61 Am2/kg, ������Hc=382.7 kA/m ��M�ͱ������塣�������[16]�������������ܽ����������ڼ�������Ϊ60 ��/h������850 ��������£��������Ҫ����Ϊ���Ǵ�Ǧʯ�ͱ�������BaFe12O19�������ߴ�Ϊ50 nm�����о��˱���������������������ܵ�Ӱ�졣����ƽ��[17]����һ�ֻ�ѧ����װ�����Ծ�(����ϩ-��-��ϩ��)�齺����Ϊģ��, �����ᴼ�����, ���ھ��Ҷ���ˮ��Һ�еõ��ı�������ǰ���������ģ�������ϣ��γɾ�(����ϩ-��-��ϩ��)/��������ǰ����˿����������ӣ��������Ӿ�750 ����ȴ������ɻ��������ΪBaFe12O19�ı���������������Ӧ����[18]Ӧ���ܽ�-���������Ʊ����ױ������壬��ȱ��ʹŻ�ǿ��Ms=70.12 A��m 2/kg��������Hc=31.26��103 A/m����ƽ��[19]�����ܽ�-�������Ʊ����ӱ����ӵ��������Ǿ��������壬�����Ҵ���ɢ��ϡŨ����������ԭ���������ºܺõع۲쵽��������������ƽ������ԼΪ52.68 nm��
�������������ܽ�-�������գ�ʹ�û�ѧ�����ȵ����ᱵ����������������Ϊԭ�ϣ����ò�ͬ���ս��ƶ��Ʊ���ͬ�����ߴ��M�ͱ������������塣ʹ��X����������(XRD��RIGAKUD/Max-A)����羵(TEM��HITACHI-2500)��������Ľᾧ�������۽ṹ����̽���Ʊ��ͱ���M�ͱ�����������Ͼ���һ����ָ�����塣
1 ʵ��
1.1 �Լ�������
ʵ�����õ��Լ���Ҫ�У�Ba(NO3)2��6H2O�����������������ӻ�ѧ�Լ�����Fe(NO3)3��9H2O��������������и�����ѧ�Լ�����������(C6H8O7��H2O),�������������Ͼ���ɽ���Ź�˾��������NH3��H2O��Ũ��25%~28%�����������ൺ������ѧ�Լ�������������ˮ��ʵ�������ơ�
��Ҫ������FA2004N�͵�����ƽ���Ϻ����ܿ�ѧ��������˾��������������WCJ-802�ͣ�����̩�ؽ������ߵ糧��ˮԡ������Ҧ�ж����繤��������DZF-6050����ո����䣬�Ϻ���Ѹʵҵ����˾ҽ���豸���������豸��SX2-8-13��ʽ����¯�������е�¯���쳧��
1.2 ����
�����ܽ�-���������Ʊ�M�ͱ������壬��Ӧ������Ľ�������������Ba(NO3)2?6H2O ��Fe(NO3)3?9H2O������ϳɲ������£���һ����ѧ������ȳ�ȡ���ᱵ����������n(���ᱵ)?n(������)=1?12���ֱ�������������Һ�У�����������������ӵ�Ħ����Ϊ1?1�������Ӻ�õ���һ���Ļ����Һ������Һ�е���һ�����İ�ˮ����pHֵΪ7����Ž���2 h���������ϻ�12 h���������Һ����ˮԡ����80 ��ˮԡ3 h�γ��ܽ���Ȼ���������������120 �� ����1~2 dֱ���γɸ������������������ս�¯�У�210 �� ����3 hȥ�������е��л��ɷ֡��ֱ���600��800��900��1 100��1 300 ���½������ա���¯��ȴ����Ʒȡ������ĥ����44 ��mɸ���á�
1.3 ���Է���
����X����������(XRD, RIGAKUD/Max-A)�Ժϳɵķ�������������������ѹ60 kV����������40 mA��ɨ�跽ʽ��10?~70?��Χ������0.02?��Cu��Ka����(��=0.154 05 nm)��ͨ����羵(TEM, HITACHI- 2500)�۲�ϳɷ��������ò��
2 ���������
2.1 ������XRD����
ͼ1��ʾΪ�ڲ�ͬ�ս��¶����Ʊ��ı�����������XRD�ס���ͼ 1���Կ�����600 ��ʱ������������Ǧ�-Fe2O3 ��������������BaCO3 ��a-Fe2O3�����ս��¶�Ϊ800 ��ʱ���������������û�з��֦�-Fe2O3��a-Fe2O3 �� BaCO3 �࣬��Ӧ�γɵ�һ�ġ���M�ͱ������塣���ھ���ṹ�ĸ����ԣ�һ�����ֱ���γɵ�һ��M�ͱ������壬��Ӧ�����г�����Fe2O3 ��BaCO3 ��BaFe2O4 �м�����֡�M�ͱ���������800 �� ��ʼ�γɣ���û�з������մɹ��պϳ��г�����BaFe2O4 �ͱ�����������������м����-Fe2O3 ��BaCO3�ij��������ڱ�����������γɣ���Ϊ��-Fe2O3 Ϊ�����⾧ʯ�ṹ���仯ѧ���ӱ���ʽΪFe(Fe5/3��1/3)O4 �������������ӿ�λ����ṹͬ����������ӱ���ʽ�е�Fe6O82+ ���ƣ����Ԧ�-Fe2O3��BaCO3 ��Ӧ�������ڽϵ��ս��¶����γɵ�һ�ı��������ࡣ��a-Fe2O3 �����ڽṹ��û���������ƣ�Ҫ��ȫת��ɵ�һ�ı�����������Ҫ�ϸߵ��ս��¡���[20]�����������������ܽ�-�������Ʊ����ױ������������ܻ���Ϊ
C6H8O7+ 2NH3��H2O��C6H6O7(NH) 2+2H2O
C6H6O7(NH) 2+Ba2+��BaC6H6O7(NH) 2+ 2H+
C6H6O7(NH) 2+2Fe3+��Fe2(C6H6O7(NH) 2) 3+ 6H+
��������Fe2O3+CaCO3
Fe2O3+CaCO3��BaFe12O19+CO2��
ͼ2��ʾΪ���ս��¶�Ϊ800 �� ʱ��ͬ����ʱ�����Ʊ��ı�����������XRD�ס���ͼ���Կ���XRD���г���������ǿ���б仯�⣬����û�з����仯����ˣ�ͨ������ʱ��Ա���������γɵ�Ӱ�죬�����ܽ�-������������Խ϶̵ı���ʱ���¿��Եõ��������壬�����ù�̬��Ӧ������ͬ��������ȴ��Ҫ�����ı���ʱ�䡣
ͼ3��ʾΪ�ս��¶ȷֱ�Ϊ800��1100��1 300 �汣��5 h�������Ʊ��ķ����XRD�ס�����һ��
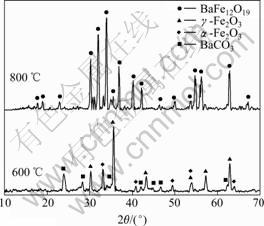
ͼ1 ����0.5 h ��ͬ�ս��¶����Ʊ��ı�����������XRD��
Fig.1 XRD patterns of barium ferrite at different temperatures for 0.5 h
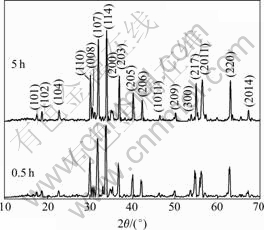
ͼ2 �ս��¶�Ϊ800 ��ʱ��ͬ����ʱ�����Ʊ��ı�����������XRD��
Fig.2 XRD patterns of barium ferrite calcined at 800 �� for different holding time

ͼ3 ����5 h��ͬ�ս��¶����Ʊ��ı�������ķ����XRD��
Fig.3 XRD patterns of barium ferrite at different temperatures for 5 h
�����˵�������ľ����ԽϺã��ᾧ�Ⱥܸߡ���XRD������֪���ϳɵķ����Ǿ��������ͽṹ�ĵ�һ��ı������塣����XRD���ݣ����ݹ�ʽ

ͼ4��ʾΪ������ʱ��Ϊ5 hʱ�������徧�������ս��¶ȵı仯����ͼ���Կ����������¶ȵ�����a���ֵ���٣���1 100 ���a���ֵ��ԼΪһ��ֵ����c���ֵ�����¶ȵ����������ߣ�1 100 ���c���ֵ��ԼΪһ��ֵ����˵����800 ��ʱ�γɽ��������ľ�һ�ṹ��

ͼ4 ����5 h��ͬ�ս��¶����Ʊ��ı����������ľ������仯����
Fig.4 Lattice parameters of barium ferrite at different temperatures for 5 h
���־����Ľṹ�����¶ȸ���1 100 ��ʱ�γɽ����Ƶľ����ṹ����ͼ 3�ó��ķ��������һ�¡�
������������ƽ�������ߴ���Ը���Scherrer��ʽ����õ���

ʽ�� ��Ϊ����X���߲���(��=0.154 05 nm)����Ϊ����������ǣ���iΪX���������İ�߿����������(114)�����İ�߿���ͼ 5��ʾΪ������������ƽ�������ߴ����ս��¶ȵĹ�ϵ���ߡ���ͼ��������ؿ�����ʵ���Ʊ��ķ���ƽ�������ߴ�Ϊ40~70 nm�������ս��¶ȵ�����ƽ�������ߴ������ӡ�
2.2 ������TEM����
ͼ6��ʾΪ�ս��¶�Ϊ800 �桢����ʱ��Ϊ0.5 hʱ�Ʊ��ı�������������羵��Ƭ����ͼ���Կ�
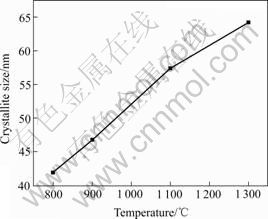
ͼ5 ��������������ƽ�������ߴ����ս��¶ȱ仯������
Fig.5 Mean grain size of barium ferrite as function of calcination temperature
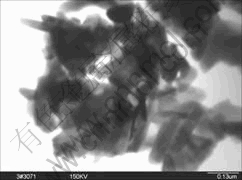
ͼ6 �ս��¶�800 ��ʱ����0.5 h �Ʊ��ı�����������TEM��
Fig.6 TEM micrograph of barium ferrite calcined at 800 �� for 0.5 h
�����ڸ��������γɵķ�������ֳʰ�״������Լ150~200 nm��ֱ��ԼΪ30~50 nm�����ڿ��������������ã��ֿ��Ծۼ���Ⱥ��һЩ���װ���˲��ܱ��۲쵽��M�ͱ��������������Ǿ�ϵ���ᾧʱ��c�᷽��������������c�᷽���϶������дӶ����ְ�״��̬�������TEM��ӳ�������һ�¡�
3 ����
1) �Ʊ���M�ͱ�������ƽ�������ߴ�Ϊ40~70 nm���ս��¶���800 �����ϡ�
2) �ս��¶�Ϊ800 �桢����ʱ��Ϊ0.5 h���������Ʊ��ķ���������ְ�״������Լ150~200 nm��ֱ��Լ30~50 nm��
3) ͨ���ı��ս��¶ȿ��Կ��ƾ�����������Ʊ��ʺϲ�ͬʵ��Ӧ�á���ͬ�����ߴ�Ĵ��������塣
REFERENCES
[1] Pullar R C, Bhattacharya A K. Crystallisation of hexagonal M- ferrites from a stoichiometric sol-gel precursor, without formation of the ��-BaFe2O4 intermediate phase[J]. Materials Letters, 2002, 57(3): 537-542.
[2] Mali A, Ataie A. Structural characterization of nano-crystalline BaFe12O19 powders synthesized by sol-gel combustion route[J]. Scripta Materialia, 2005, 53(9): 1065-1070.
[3] Zhang H J, Wu M Z, Yao X, Zhang L Y. Complex permittivity, permeability, and microwave absorption of barium ferrite by citrate sol-gel process[J]. Rare Metals, 2003, 22(2): 125-130.
[4] ������, ������, �� ��. �������峬ϸ��ĩ���Ʊ�[J]. ��ɳ������ѧѧ��(��Ȼ��ѧ��), 2006, 3(2): 86-90.
ZENG Ai-xiang, ZHOU Qiong-hua, ZHOU Yi. Preparation of ultra fine BaFe12O19 powder[J]. Journal of Changsha University of Science and Technology (Natural Science), 2006, 3(2): 86-90.
[5] Mishra D, Anand S, Panda R K, Das R P. Studies on characterization, microstructures and magnetic properties of nano-size barium hexa-ferrite prepared through a hydrothermal precipitation�Ccalcination route[J]. Materials Chemistry and Physics, 2004, 86(1): 132-136.
[6] Kojima H. Fundamental properties of hexagonal ferrites with magnetoplumbite structure, ferromagnetic materials[M]. Netherlands: North-Holland, 1982: 305-391.
[7] Braun P B. The crystal structures of a new group of ferromagnetic compounds[J]. Philips Res Rep, 1957, 12: 491-548.
[8] Hong Y K, Jung H S. New barium ferrite particles: Spherical shape[J]. Journal of Applied Physics, 1999, 85(8): 5549-5551.
[9] Kaneko Y, Iyi N, Kurashima K, Matsumoto T, Fujita T, Kitamura K. Hexagonal-structured polysiloxane material prepared by sol-gel reaction of aminoalkyltrialkoxysilane without using surfactants[J]. Chemistry of Materials, 2004, 16(18): 3417-3423.
[10] ������, ����Ϊ. M���������������״���չ[J]. ���Բ��ϼ�����, 2001, 32(1): 27-32.
LIU Xian-song, DU You-wei. Present states and recent advances in M-type ferrites[J]. Journal of Magnetic Materials and Devices, 2004, 16(18): 3417-3423.
[11] �ܿ�ʡ, �� ��, ������, ����, �ƿ���. La0.8Sr0.2- Mn1-yFeyO3�������������Ļ���[J]. �й���ɫ����ѧ��, 2006, 6(5): 753-757.
ZHOU Ke-sheng, WANG Da, YIN Li-shong, KONG De-ming, HUANG Ke-long. Electromagnetic properties and loss mechanism of La0.8Sr0.2Mn1-yFeyO3 in microwave band[J]. The Chinese Journal of Nonferrous Metals, 2006, 6(5): 753-757.
[12] Wang J, Wu Y, Zhu Y, Wang P Q. Formation of rod-shaped BaFe12O19 nanoparticles with well magnetic properties[J]. Materials Letters, 2007, 61(7): 1522-1525.
[13] Qiu J, Gu M. Crystal structure and magnetic properties of barium ferrite synthesized using GSPC and HEBM[J]. Journal of Alloys and Compounds, 2006, 415(1/2): 209-212.
[14] SUN Chang, SUN Kang-ning. Preparation and microwave absorption properties of Ce-substituted lithium ferrite[J]. Solid State Communications, 2007, 141(5): 258-261.
[15] ������, �� Ӣ, �� ��, �� ��. ��������-�ܽ�ǰ�����Ʊ�����������о�[J]. �������Ͽ�ѧ�빤��, 2006, 29(3): 37-41.
WANG Yan-li, HUANG Ying, YAN Li, HUANG Fei. Barium ferrite prepared with two kinds of sol-gel precursor[J]. Ordnance Material Science and Engineering, 2006, 29(3): 37-41.
[16] ������, �� ��. ��������Ŀ������������������о�[J]. ͬ�ô�ѧѧ��(��Ȼ��ѧ��), 2006, 34(2): 225-228.
ZHANG Yan-qing, ZHANG Xiong. Effect of particle size on microwave absorption property of barium ferrite[J]. Journal of Tongji University (Natural Science), 2006, 34(2): 225-228.
[17] ����ƽ, �ٽ���. ��ѧ����װ���Ʊ�����������������[J]. ������ѧѧ��, 2006, 22(2): 189-192.
GAN Zhi-ping, GUAN Jian-guo. Chemical self-assembly route to fabricate hollow barium ferrite submicrospheres[J]. Acta Phys-Chim Sin, 2006, 22(2): 189-192.
[18] �� Ӣ, ������, ���㶫, �� ��, �ܡ���. �Ʊ����ն����ױ����������ɹ��̵�Ӱ��[J]. ������ҵ��ѧѧ��, 2005, 23(2): 193-196.
HUANG Ying, WANG Qi-jie, WANG Guang-dong, HUANG Fei, XIONG Jia. A better preparation process on formation of BaFe12O19 nanoparticles[J]. Journal of Northwestern Polytechnical University, 2005, 23(2): 193-196.
[19] ��ƽ, �� ��. �������������ԭ�������������������ܵ��о�[J]. ��������ѧ��, 2005, 24(3): 14-17.
ZHUO Chang-ping, ZHANG Xiong. Atomic force microscopic analysis and microwave properties of nano-scale M-type barium hexaferrite[J]. Journal of Instrumental Analysis, 2005, 24(3): 14-17.
[20] Zhong W, Ding W, Zhang N, Du Y, Yan Q, Hong J. Key step in synthesis of ultrafine BaFe12O19 by sol-gel technique[J]. Journal of Magnetism and Magnetic Materials, 1997, 168(1/2): 196-202.
(�༭������Ⱥ)
������Ŀ��������Ȼ��ѧ����������Ŀ(30540061, 50672051)
�ո����ڣ�2006-09-30�������ڣ�2007-05-21
ͨѶ���ߣ���������ڣ���ʿ���绰��0531-88392439; E-mail: sunkangning@sina.com