文章编号:1004-0609(2011)06-1409-06
TiB2合成反应机理的优势区相图分析
马爱琼,蒋明学
(西安建筑科技大学 材料科学与工程学院,西安 710055)
摘 要:以TiO2、B2O3、C为原料,采用碳热还原法合成TiB2粉末。通过热力学分析,绘制Ti-C-O、B-C-O系统的优势区相图和TiO2-B2O3-C系统的优势区相图叠加图,从优势区相图的角度研究碳热还原法合成TiB2的反应机理。结果表明:在Ti-C-O系统中,随着反应温度的升高,TiO2被碳还原的先后顺序为TiO2→Ti4O7→Ti3O5→Ti2O3,其中中间产物Ti4O7和Ti3O5最容易出现,也是较稳定的。在B-C-O系统中,随着碳热还原反应的进行,B2O3被C还原生成B2O2,B2O2进一步被碳还原生成B4C。碳热还原TiO2和B2O3合成TiB2的反应机理如下:在1 200~ 1 300 ℃温度下,TiO2被C还原成中间产物Ti3O5;在1 250~1 300 ℃温度范围,B2O3被C还原生成中间气相产物B2O2;当还原反应温度达到1 300 ℃以上时,中间产物Ti3O5与B2O2一起被C还原生成TiB2。
关键词:TiB2;优势区相图;碳热还原法;反应机理
中图分类号:TQ174 文献标志码:A
Predominace area phase diagram analysis about
synthetic reaction mechanism of TiB2
MA Ai-qiong, JIANG Ming-xue
(School of Material Science and Engineering, Xi’an University of Architecture and Technology, Xi’an 710055, China)
Abstract: Using TiO2, B2O3 and C as raw material, TiB2 powder was synthesized by carbothermal reduction. The predominance area phase diagram (PAPD) of Ti-C-O system and B-C-O system were plotted by thermodynamic analysis. In addition, the superposition of predominance area phase diagram of TiO2-B2O3-C system was achieved. The reaction mechanism of synthesizing TiB2 by carbothermal reduction was studied from the standpoint of predominance area phase diagram (PAPD). The results show that in Ti-C-O system, with reaction temperature rising, TiO2 was reduced according to following subsequence: TiO2→Ti4O7→Ti3O5→Ti2O3. In these intermediate products, Ti4O7 and Ti3O5 appear easily. In B-C-O system, along with carbothermal reduction happening, B2O3 is reduced to revert B2O2 while B2O2 is further reduced by carbon to revert B4C. The reaction mechanism of synthesizing TiB2 by carbothermal reducing TiO2 and B2O3 can be decripted by the following reactions: at reduction temperature area of 1 200-1 300 ℃ and 1 250-1 300 ℃, TiO2 and B2O3 are reduced by carbon to revert intermediate products Ti3O5 and B2O2, respectively, when the reduction temperature reaches above 1 300 ℃, the intermediate products Ti3O5 and B2O2 are together reduced by carbon to form product TiB2.
Key words: TiB2; predominance area phase diagram; carbothermal reduction; reaction mechanism
硼化钛(TiB2)是一种新型的多功能材料,它具有高强度、高硬度、耐高温、耐酸碱腐蚀、耐磨损以及良好的导电性和导热性等优点,广泛用于制备金属陶瓷、切削工具、模具、熔炼金属用坩埚,作为复合材料的增强相。尤其是硼化钛具有优良的导电性和不与金属铝液及冰晶石反应的特点,用于制备铝电解槽的阴极,具有极大的开发价值和应用前景[1-4],近年来受到极大的关注。但是,到目前为止,TiB2材料并没有获得大规模的工业应用,其中一个关键的原因在于TiB2原料价格昂贵,生产成本过高。因此,制备原料来源广、价格低廉、纯度高、粒度小、粒度分布窄的硼化钛粉末是目前研究的焦点[5-9]。与自蔓延高温合成法相比,以钛白粉、氧化硼、炭粉为原料,采用碳热还原法制备TiB2具有这方面的原料成本低、来源广、合成简单等优点,是目前工业上生产TiB2的主要方法,有望降低TiB2材料的生产成本,扩大TiB2材料的应用范围。
在TiB2粉末合成过程中,为了得到合适的粉末,对反应机理的充分理解是十分必要的。研究碳热还原TiO2与B2O3合成TiB2的反应机理,不仅有助于理解TiB2粉末合成反应的本质、合成反应中所出现的物相、合成反应的传质机理,且对采用碳热还原法制备其它金属陶瓷粉末也有指导意义。
优势区相图(Predominance area phase diagram, PAPD)是一种包括化学反应体系的广义相图,近几年来,在无机材料中, 特别是在陶瓷中的应用逐渐增多,主要是因为非氧化物如硼化物和碳化物等材料在合成过程中均有气体参加,应用优势区相图易于确定体系中凝聚相与气体和温度的关系,并进一步明确合成反应顺序与机理。本文作者通过对Ti-C-O和B-C-O系统进行热力学分析[10-12],绘制了相应系统的优势区相图,并通过对Ti-C-O和B-C-O系统优势区相图的叠加,得到了TiO2-B2O3-C系统的优势区相图叠加图,并在此基础上分析碳热还原TiO2和B2O3合成TiB2的反应机理。
1 实验
将TiO2粉末(纯度为99.95%,平均粒径为1.75 μm)、B2O3粉末(纯度为98.8%,平均粒径为2.62 μm)、石墨粉(纯度为99.49%,平均粒径为0.5 μm)按1?2?5.5(摩尔比)放入尼龙球磨罐中以蒸馏水混合,以刚玉为研磨介质,其中料、球和水的质量比为1?5?1.5,湿磨24 h后,取出料浆,在烘箱中进行110 ℃、24 h干燥,过88 μm筛。
将3%无水乙醇和0.2%的糊精(质量分数)加入到粉料中,搅拌碾压均匀,用内径为d 38 mm的模具,在20 MPa的压力下压制成d 38 mm×35 mm的圆柱形试样。将压制好的生坯试样在烘箱中进行110 ℃、24 h干燥。
将制备好的试样置于ZT-50-20Y真空碳管炉内,对炉内抽真空至50 Pa以下,并充氩气洗炉2~3次,最后,在抽真空的条件下加热至设定合成温度,反应温度分别设定为900、1 000、1 100、1 200、1 300、 1 400和1 450 ℃。升温速度平均为10 ℃/min,在合成温度下保温3 h,并定时记录炉内温度和压力变化情况,在合成反应结束后,以15 ℃/min的降温速率迅速冷却至室温。
采用日本理学公司生产的D/MAX-2400型X射线衍射仪对合成试样进行XRD分析,采用美国FEI公司生产的Quanta 200型扫描电子显微镜对试样进行SEM分析。
2 结果与分析
2.1 对TiB2合成反应机理的优势区相图分析
2.1.1 Ti-C-O系优势区相图
在Ti-C-O系中,所存在的化学反应如下所示,利用文献[10-12]所提供的热力学数据,可求得各反应相应的?G~T关系:
4TiO2(s)+C(s)=Ti4O7(s)+CO(g) (1)
3TiO2(s)+C(s)=Ti3O5(s)+CO(g) (2)
2TiO2(s)+C(s)=Ti2O3(s)+CO(g) (3)
TiO2(s)+C(s)=TiO(s)+CO(g) (4)
TiO2(s)+2C(s)=Ti(s)+2CO(g) (5)
经热力学计算,反应方程式(1)~(5)的吉布斯自由能(?G)与温度(T)的关系如图1所示。
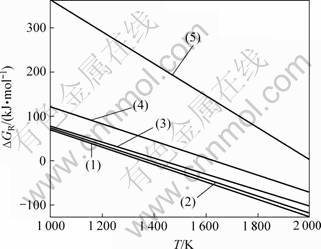
图1 反应方程式(1)~(5)的吉布斯自由能与温度的关系
Fig.1 Relaitionship between Gibbs free energy of reactions (1)-(5) and temperature
在此基础上,进一步绘制了在温度为1 000~2 000 K范围内时,TiO2的各还原产物稳定存在区域图(优势区相图)如图2所示。由图2可知,仅当CO分压较低时,单质Ti与TiO才有可能稳定存在,而碳热还原反应气氛为还原性气氛,在此条件下,单质钛难以稳定存在,通过这一分析,可以初步排除生成TiB2是通过TiO2还原为单质Ti的反应步骤。由图1和2可知,随着温度逐渐升高,TiO2的逐级还原的先后顺序为TiO2→Ti4O7→Ti3O5→Ti2O3→TiO→Ti。在1 000~2 000 K的温度范围内,在TiO2的碳热还原反应中,最容易得到的物相分别是Ti4O7和Ti3O5,这与WELHAM[13-14]的分析吻合。
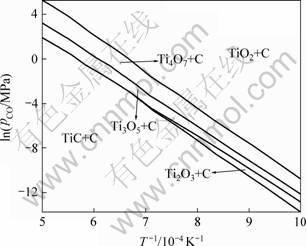
图2 Ti-C-O系统的优势区相图
Fig.2 Predominance area phase diagram in Ti-C-O system
2.1.2 B-C-O系统的优势区相图
相比Ti-C-O系统的反应,在B-C-O系统中的反应要简单一些。SINHA等[15]在研究碳热还原B2O3制备B4C的过程中发现,发生在B-C-O系统的主要反应为
2B2O3(l)+ 7C(s)→B4C(s)+6CO(g) (6)
除此之外,在B-C-O系统内,B2O3被碳还原,还可能发生如下反应:
B2O3(l)+3C(s)=2B(s)+3CO(g) (7)
B2O3(l)+C(s)=B2O2(g)+CO(g) (8)
5B2O3(l)+B4C(s)=7B2O2(g)+CO(g) (9)
B2O3(l)+3B4C(s)=14B(s)+3CO(g) (10)
2B2O2(g)+5C(s)=B4C(s)+4CO(g) (11)
B2O2(g)+2C(s)=2B(s)+2CO(g) (12)
B2O2(g)+2B4C(s)=10B(s)+2CO(g) (13)
B2O2(g)=2BO(g) (14)
由以上反应式可见,在B-C-O系统中,包括有复杂的气相组成,如B2O2(g)、BO(g)和CO等,这些气相对凝聚态产物B4C和单质B的生成有何影响,尚没有详细的研究,为此,本文作者通过热力学计算,绘制B-C-O系统的优势区相图(见图3)。由图3可知,随着碳热还原反应的进行,B2O3被C还原生成B2O2,B2O2进一步被碳还原生成B4C。随着还原反应的逐渐进行,对反应体系中CO的分压要求越来越高。仅当反应体系中CO分压极低时,生成单质B才可能实现。可以推断,在碳热还原B2O3时,B4C更容易生成,而单质B的生成来自于B4C和B2O2进一步被C还原,在碳热还原反应中,B2O3被C还原生成的B2O2气相是B-C-O系统中的一种重要的气相反应物。

图3 B-C-O系统的优势区相图
Fig.3 Predominance area phase diagram in B-C-O system
2.1.3 TiO2-B2O3-C系统的优势区相图
由于Ti-B-C-O系所涉及的物相组成比较复杂,直接绘制Ti-B-C-O系的优势区相图缺乏部分热力学数据。而采用碳热还原法合成TiB2时,是以TiO2、B2O3和C为原料,为阐明碳热还原法合成TiB2的反应机理,本文作者在绘制Ti-C-O系和B-C-O系优势区相图的基础上,通过对Ti-C-O和B-C-O系统优势区相图的叠加,得到了TiO2-B2O3-C系统的优势区相图(见图4)。
图中实线区域为B-C-O系统中各物相的稳定存在区域,虚线区域为Ti-C-O系统中各物相的稳定存在区域。由图4可见,Ti-C-O系统和B-C-O系统有部分重叠区域,随着CO分压的降低,这些区域分别是B2O3- TiO2-C、B2O2-Ti4O7-C、B2O2-Ti3O5-C和B2O3-Ti3O5- B4C,其中B2O2-Ti3O5-C和B2O3-Ti3O5-B4C重叠面积最大,根据前面讨论B-C-O系统的优势区相图。由图3还可见,重叠区域内的B4C也是由B2O2还原而来,根据这一结论并结合图4可以判断,在TiO2-B2O3-C系统中,碳热还原合成TiB2的反应可能通过如下反应发生:
B2O3(l)+C(s)=B2O2(g)+CO(g) (15)
4TiO2(s)+C(s)=Ti4O7(s)+CO(g) (16)
3Ti4O7(s)+C(s)=4Ti3O5(s)+CO(g) (17)
Ti3O5(s)+3B2O2(g)+11C(s)=3TiB2(s)+11CO(g) (18)
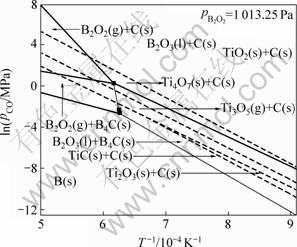
图4 TiO2-B2O3-C系统的优势区相图
Fig.4 Diagram of stability relations of phases in TiO2-B2O3-C system
从图4可知,单质B与 TiO2的还原产物之间没有明显的重叠区域,且B2O3被还原为单质B仅在极低的CO分压下才可能发生,因此,从热力学分析的角度,可以证明在TiB2的合成过程中,单质B参与反应的可能性不大,而B2O2应是合成反应中B的前驱体。
2.2 合成试样的XRD分析
以TiO2、B2O3和C粉为原料,通过碳热还原法合成TiB2在不同温度下的反应产物,其XRD谱如图5所示。由图5可知,随着反应温度的升高,当反应温度达到1 100 ℃时,金红石开始被碳还原,并在此温度下,还原产物为Ti4O7和Ti6O11;1 200 ℃的反应产物为Ti3O5、Ti4O7和Ti5O9,其中Ti4O7的衍射峰逐渐减弱,而Ti3O5的衍射峰逐渐增强,Magneli相Ti6O11被Ti5O9所代替,这表明Ti6O11和Ti5O9只在一定温度范围内稳定存在,在其它温度下仍会转变为Ti3O5和Ti4O7。在此温度下,没有检测到与B2O3相关的物相存在,这与B2O3为非晶态物质有关;1 300 ℃的还原
产物为Ti3O5、Ti2O3、C和TiB2,在此温度下,TiB2的生成量很少,而Ti4O7已完全被Ti3O5所代替。同时,少量的Ti3O5被进一步还原生成Ti2O3;1 400 ℃的反应产物仍然为Ti3O5、Ti2O3和TiB2,但是,TiB2的生成量增加,衍射峰逐渐增强,而Ti3O5的衍射峰逐渐减弱,这表明,在此温度下,TiB2的生成主要源自Ti3O5的还原及与B2O2气相的反应;当温度升高至1 450 ℃时,反应产物已完全是单一的TiB2相。这与图4对TiO2-B2O3-C系统的优势区相图分析结果一致。

图5 不同温度下合成产物的XRD谱
Fig.5 XRD patterns of synthesized products at different temperatures
由XRD分析结果可见,随着合成反应温度的升高,TiO2的还原先后顺序依次为
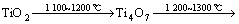
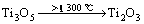
这与图2对Ti-C-O系统的优势区相图分析结果是一致的。XRD分析表明,TiB2的生成反应温度开始于1 300 ℃左右,随着反应温度的升高,TiB2的生成量逐渐增加。当反应温度达到1 450 ℃时,TiB2的生成反应已趋于完成。
由于所用原料B2O3为非晶态,XRD分析难以检测到其存在与否,为了阐明在900~1 450 ℃温度范围内,B2O3的含量变化规律,对以上反应试样在经过110 ℃、24 h干燥后,将样品密封保存。利用B2O3在甲醇溶液中溶解性好的特点,采用甲醇溶解法将样品充分溶入甲醇溶液,经过滤干燥后,分别称量试样溶解前后的质量变化,并由此计算样品中B2O3的含量变化规律,如图6所示。
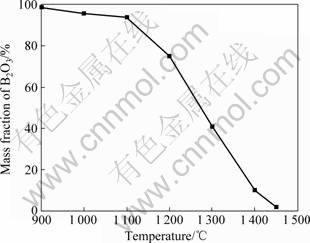
图6 不同温度反应后试样中的B2O3含量
Fig.6 B2O3 content in sample after reaction at different temperatures
由图6可见,当反应温度为900 ℃时,试样中的B2O3基本没反应,这表明,在此反应温度下,B2O3的碳热还原反应没有开始,且当反应温度为900 ℃时,B2O3几乎没有挥发损失;随着温度升高,当反应温度在1 000~1 100 ℃范围内时,B2O3的含量变化不明显,这与随着温度升高,少量B2O3升华挥发有关,这表明,在1 100 ℃之前,B2O3的碳热还原反应没有开始。随着反应温度继续升高,当反应温度为1 200~1 300 ℃时,与1 100 ℃反应后产物中B2O3含量相比,B2O3含量下降较明显,由图3对B-C-O系统的优势区相图分析可知,这一现象的出现与以下原因有关:一是由于B2O3的碳热还原反应开始,反应生成B2O2气相,导致试样中B2O3含量下降;二是由于还原生成的B2O2作为硼源,参与到合成TiB2的反应中。这一结果与图4对TiO2-B2O3-C系统的优势区相图分析结果完全吻合。随着反应温度的继续升高,B2O2不断参与到合成TiB2的反应中,因此,试样中游离B2O3的含量逐渐下降。由图6可见,当反应温度为1 450 ℃时,试样中游离B2O3的含量已接近为零,这表明,在此温度下,合成TiB2的反应已基本进行完全,这一分析结果与XRD分析结果一致。
2.3 TiB2粉末的形貌
图7所示为合成产物的SEM像。由图7(a)可见,当反应温度为1 100 ℃时,合成TiB2的反应并没有开始,从图中仍可见到片状的石墨颗粒,不规则形状的B2O3颗粒及少量尚未完全发育完整的三斜状Ti4O7晶粒,这表明,在此条件下,TiO2的还原反应刚刚开始,此时的还原产物为三斜晶Ti4O7晶粒;当温度升高到1 450 ℃时,如图7(b)所示,合成TiB2的反应已经完成,产物为基本发育完整的六方短柱状TiB2晶粒,在TiB2晶粒中存在大大小小的孔洞,这进一步证实,在合成TiB2的反应中,存在气相传质机理,在反应中有B2O2和CO等气体释放。

图7 不同温度合成产物的SEM像
Fig.7 SEM images of product synthesized at different temperatures: (a) 1 100 ℃; (b) 1 450 ℃
2.4 碳热还原法合成TiB2的反应机理
通过以上对碳热还原法合成TiB2反应体系的优势区相图分析并结合XRD和SEM分析可知,在碳热还原TiO2和B2O3合成TiB2时,反应机理由以下3个连续步骤组成:
Ⅰ:
Ⅱ:
Ⅲ: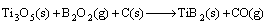
在碳热还原TiO2与B2O3合成TiB2的反应过程中,B2O2(g)气相和Ti3O5(s)分别是形成TiB2的前驱体,在反应过程中存在气相传质机理。
3 结论
1) 在Ti-C-O系统中,随着反应温度的升高,TiO2被碳还原的先后顺序为TiO2→Ti4O7→Ti3O5→Ti2O3,其中中间产物Ti4O7和Ti3O5最容易出现,也比较稳定。
2) 在B-C-O系统中,随着碳热还原反应的进行,B2O3被C还原生成B2O2,B2O2进一步被碳还原才生成B4C。
3) 碳热还原TiO2和B2O3合成TiB2的反应机理应为C将TiO2还原为中间产物Ti3O5,B2O3被C还原生成中间气相产物B2O2,随后中间产物Ti3O5与B2O2一起逐渐被C还原生成TiB2。
REFERENCES
[1] 向 新, 秦 岩. TiB2及其复合材料研究进展[J]. 陶瓷学报, 1999, 20(2): 112-117.
XIANG Xin, QIN Yan. Development of research on TiB2 and its composites[J]. Journal of Ceramics, 1999, 20(2): 112-117.
[2] LU L, LAI M O, WANG H Y. Synthesis of Titanium diboride TiB2 and Ti-Al-B metal matrix composites[J]. Journal of Materials Science, 2000, 35: 241-248.
[3] 刘业翔. 铝电解槽惰性阳极与可湿润型阴极的研究与开发进展[J]. 轻金属, 2001, 5: 26-29.
LIU Ye-xiang. The study development of aluminum reduction cells with inert anode and wettable cathodes[J]. Light Metal, 2001, 5: 26-29.
[4] 陈肇友. ZrB2和TiB2质耐火材料[J]. 耐火材料, 2000, 34(4): 224-229.
CHEN Zhao-you. ZrB2 and TiB2 refractories[J]. Refractory, 2000, 34(4): 224-229.
[5] 王化章, 汤 啸, 杨建红. 氯化物熔体中电化学合成硼化钛[J]. 中国有色金属学报, 1997, 7(2): 34-38.
WANG Hua-zhang, TANG Xiao, YANG Jian-hong. Electrochemical synthesis TiB2 in chloride molten salts[J]. The Chinese Journal of Nonferrous Metals, 1997, 7(2): 34-38.
[6] 张廷安, 杨 欢, 牛丽萍. 镁热还原自蔓延高温合成硼化钛微粉的动力学[J]. 中国有色金属学报, 2001, 11(4): 567-570.
ZHANG Ting-an, YANG Huan, LIU Li-ping. Kinetics of preparation of titanium boride by SHS[J]. The Chinese Journal of Nonferrous Metals, 2001, 11(4): 567-570.
[7] KANG S H, KIM D J. Synthesis of nano-titanium diboride powders by carbothermal reduction[J]. Journal of the European Ceramic Society, 2007, 27: 715-718.
[8] BRUCE N B, JACK W, LACKEY. Process-structure-reflectance correlations for TiB2 films prepared by chemical vapor deposition[J]. Journal of the American Ceramic Society, 1999, 82(3): 503-512.
[9] DARREN A H, MARC A M. Consolidation of combustion- synthesized titanium diboride- based materials[J]. Journal of the American Ceramic Society, 1995, 78(2): 375-381.
[10] 叶瑞伦. 无机材料物理化学[M]. 北京: 中国建筑工业出版社, 1986: 132-134.
YE Rui-lun. Physical chemistry of inorganic materials[M]. Beijing: Chinese Building Industry Press, 1986: 132-134.
[11] 陆佩文. 无机材料科学基础[M]. 武汉: 武汉理工大学出版社, 1996: 144-145.
LU Pei-wen. Inorganic materials science foundation[M]. Wuhan: Wuhan University of Technology Press, 1996: 144-145.
[12] 叶大伦, 胡建华. 实用无机物热力学数据手册[M]. 北京: 冶金工业出版社, 2002: 1049-1060.
YE Da-lun, HU Jian-hua. Inorganic thermodynamic data manual[M]. Beijing: Metallurgical Industry Press, 2002: 1049-1060.
[13] WELHAM N J. Formation of nanometric TiB2 from TiO2[J]. Journal of the American Ceramic Society, 2000, 83(5): 1290-1292.
[14] WELHAM N J. Mechanical enhancement of the carbothermic formation of TiB2[J]. Metallurgical and Materials Transactions, 2000, 31(1): 283-289.
[15] SINHA A, MAHATA T, SHARMA B P. Carbothermal route for preparation of boron carbide powder from boric acid-citric gel precursor[J]. Journal of Nuclear Materials, 2002, 301: 165-169.
(编辑 李艳红)
基金项目:陕西省教育厅自然科学专项科研基金资助(09JK532);陕西省重点学科建设专项资金资助项目
收稿日期:2010-05-05;修订日期:2010-10-28
通信作者:马爱琼,副教授,博士;电话:029-82205798;E-mail: maaiqiong@xauat.edu.cn