NiPO4/LiNiPO4离子筛盐湖提锂热力学分析
来源期刊:稀有金属2016年第10期
论文作者:陈浩 何利华 刘旭恒
文章页码:1045 - 1052
关键词:Me-Ni-P-H2O系;NiPO4/LiNiPO4;盐湖提锂;热力学;
摘 要:基于锂离子电池充放电过程的可逆氧化还原反应原理,提出利用NiPO4/LiNiPO4电极对盐湖卤水进行锂镁分离的思路。运用同系线性规律对Me(Li,Na,K,Mg)-Ni-P-H2O中NiPO4,Ni3(PO4)2,LiNiPO4,Na NiPO4,KNiPO4,Mg0.5NiPO4的标准吉布斯自由能进行了估算。在热力学计算的基础上绘制了298.15 K时,Me(Li,Na,K,Mg)-Ni-P-H2O系的φ-p H图,讨论了NiPO4对盐湖卤水中主要金属离子(Li+,Na+,K+,Mg2+)的选择性吸附行为。结果表明:水溶液中存在LiNiPO4,Na NiPO4,KNiPO4的稳定区,还原电位(vs SHE)分别为0.2379,-0.0291,0.0209 V,不存在Mg0.5NiPO4的稳定区。在实际盐湖卤水(Mg/Li质量比为67)离子浓度条件下,NiPO4/LiNiPO4电极对仍具有良好的选择性提锂功能。而天然卤水的p H一般在7左右,表明此时无需添加酸或碱来调节卤水的p H,这与节能减排和环境保护的理念不谋而合,不断重复脱嵌锂过程即可从盐湖卤水中选择性提取锂。
网络首发时间: 2016-06-22 08:23
稀有金属 2016,40(10),1045-1052 DOI:10.13373/j.cnki.cjrm.xy15020602
陈浩 何利华 刘旭恒
中南大学冶金与环境学院
基于锂离子电池充放电过程的可逆氧化还原反应原理,提出利用NiPO_4/LiNiPO_4电极对盐湖卤水进行锂镁分离的思路。运用同系线性规律对Me(Li,Na,K,Mg)-Ni-P-H_2O中NiPO_4,Ni_3(PO_4)_2,LiNiPO_4,Na NiPO_4,KNiPO_4,Mg_(0.5)NiPO_4的标准吉布斯自由能进行了估算。在热力学计算的基础上绘制了298.15 K时,Me(Li,Na,K,Mg)-Ni-P-H_2O系的φ-p H图,讨论了NiPO_4对盐湖卤水中主要金属离子(Li~+,Na~+,K~+,Mg~(2+))的选择性吸附行为。结果表明:水溶液中存在LiNiPO_4,Na NiPO_4,KNiPO_4的稳定区,还原电位(vs SHE)分别为0.2379,-0.0291,0.0209 V,不存在Mg_(0.5)NiPO_4的稳定区。在实际盐湖卤水(Mg/Li质量比为67)离子浓度条件下,NiPO_4/LiNiPO_4电极对仍具有良好的选择性提锂功能。而天然卤水的p H一般在7左右,表明此时无需添加酸或碱来调节卤水的p H,这与节能减排和环境保护的理念不谋而合,不断重复脱嵌锂过程即可从盐湖卤水中选择性提取锂。
Me-Ni-P-H2O系;NiPO4/LiNiPO4;盐湖提锂;热力学;
中图分类号: TF826.3
作者简介:陈浩(1990-),男,湖北天门人,硕士研究生,研究方向:有色金属冶金与材料制备;E-mail:chenhao8688@126.com;;刘旭恒,副教授;电话:0731-88830476;E-mail:liuxuheng@csu.edu.cn;
收稿日期:2015-02-10
基金:国家自然科学基金联合项目(U1407137)资助;
Chen Hao He Lihua Liu Xuheng
School of Metallurgy and Environment,Central South University
Abstract:
NiPO_4/LiNiPO_4 electrode was selected to separate lithium and magnesium from salt lake brine based on the principle of reversible redox reaction in lithium ion battery during charging and discharging process. The standard Gibbs free energies of NiPO_4,Ni_3( PO_4)_2,LiNiPO_4,Na NiPO_4,KNiPO_4 and Mg0. 5NiPO_4 in Me( Li,Na,K,Mg)-Ni-P-H_2 O system were estimated by congeneric linearity rule. The φ-p H diagrams of Me( Li,Na,K,Mg)-Ni-P-H_2 O system at 298. 15 K were plotted and the selectivity of adsorption of main metal ions( Li~+,Na~+,K~+,Mg~(2 +)) by NiPO_4/LiNiPO_4 in brine were discussed according to thermodynamic calculation. The results showed that LiNiPO_4,Na NiPO_4 and KNiPO_4 could exist steadily in aqueous solution and the reduction potentials( vs SHE) were0. 2379,- 0. 0291,0. 0209 V,respectively,while the stable region of Mg_(0. 5)NiPO_4 did not exist in the studied range. Under the condition of real brine concentration,in which the mass ratio of Mg/Li was as high as 67,the calculation result showed that NiPO_4/LiNiPO_4 electrode still presented favorable selective adsorption characteristics. The p H of brine was generally about 7,indicating that there was no need to add acid or base to adjust p H,which coincided with the concept of energy saving and environmental protection. Lithium could be extracted from salt lake brine selectively by repeating the process.
Keyword:
Me-Ni-P-H2O system; NiPO4/LiNiPO4; lithium extraction; thermodynamics;
Received: 2015-02-10
锂离子电池被誉为“21世纪的清洁能源”,其快速发展使锂及其化合物的应用越来越受到重视
为了解决高镁锂比盐湖卤水镁锂分离的难题,文献
考虑到盐湖卤水成分复杂,如西台吉乃尔盐湖老卤中存在大量的与Li+同族的Na+,K+以及和Li+处于对角线位置的Mg2+
1 Me(Li,Na,K,Mg)-Ni-P-H2O体系热力学计算
1.1 相关热力学数据估算
虽然已有Li Ni PO4材料成功制备的报道
利用表1中查到的铁、镍化合物的ΔfGΘ298.15数据,以铁化合物的ΔfGΘ298.15(Fe)为横坐标,镍化合物的ΔfGΘ298.15(Ni)为纵坐标进行线性拟合,所得结果如图1所示。由图1可知,铁、镍化合物的ΔfGΘ298.15数据几乎落在一条直线上,其线性方程为:ΔfGΘ298.15(Ni)=0.96537ΔfGΘ298.15(Fe)+28.370,线性相关系数R2=0.99906。将Fe PO4,Fe3(PO4)2,Li Fe PO4,Na FePO4,KFe PO4和Mg0.5Fe PO4的ΔfGΘ298.15代入方程即可求得Ni PO4,Ni3(PO4)2,Li Ni PO4,Na Ni PO4,KNi PO4,Mg0.5Ni PO4的ΔfGΘ298.15分别为-1115.506,-2331.767,-1436.772,-1380.298,-1405.668和-1325.330 k J・mol-1。
1.2 热力学平衡计算
金属-水系中存在水解-中和、氧化-还原、水解-中和与氧化-还原共存3类反应。基于热力学基本原理
表1 Fe,Ni相关化合物在298.15 K下的热力学数据Table 1Thermodynamic data of compounds containing Fe,Ni at 298.15 K(k J・mol-1) 下载原图
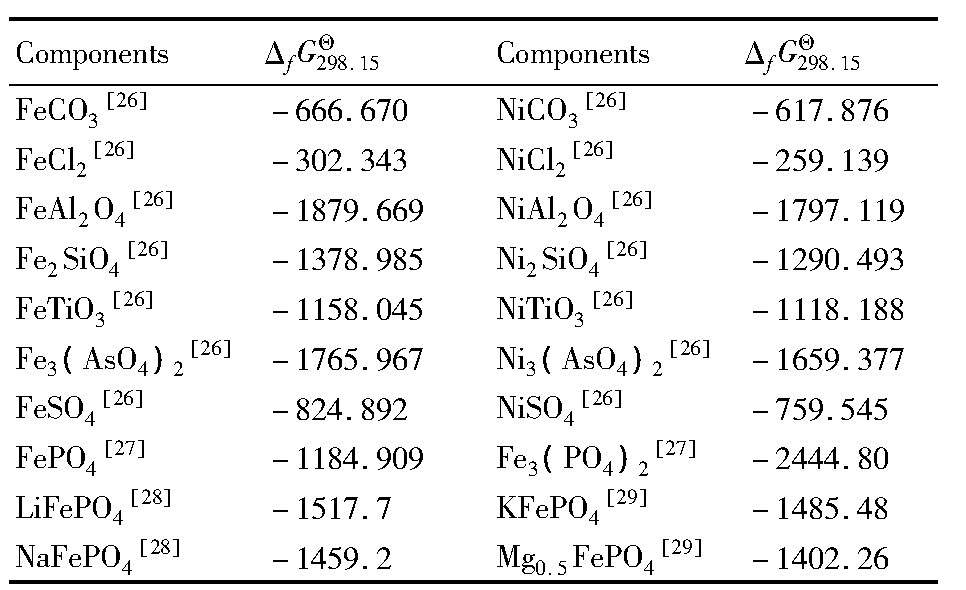
表1 Fe,Ni相关化合物在298.15 K下的热力学数据Table 1Thermodynamic data of compounds containing Fe,Ni at 298.15 K(k J・mol-1)
图1 Fe盐与Ni盐的ΔfGΘ298.15间的同系线性关系Fig.1Linearity relation ofΔfGΘ298.15between iron compounds and nickel compounds
2 分析与讨论
2.1 Ni-P-H2O系和Li-Ni-P-H2O系φ-p H图分析
Ni PO4和Li Ni PO4在水溶液中稳定存在是其应用于盐湖提锂的先决条件。因此,本文先对其在水溶液中的稳定性进行考察。以离子浓度代替活度,设定体系中各离子浓度均为0.1 mol・L-1,根据表3中的φ-p H关系式,绘制相应的φ-p H图,如图2,3所示。
表2 Ni,Li,Na,K,Mg离子及相关化合物在298.15 K下的热力学数据Table 2 Thermodynamic data of ions and compounds contai-ning Ni,Li,Na,K and Mg at 298.15 K(k J・mol-1) 下载原图

表2 Ni,Li,Na,K,Mg离子及相关化合物在298.15 K下的热力学数据Table 2 Thermodynamic data of ions and compounds contai-ning Ni,Li,Na,K and Mg at 298.15 K(k J・mol-1)
表3 Ni-P-H2O系、Li-Ni-P-H2O系、Na-Ni-P-H2O系、K-Ni-P-H2O系以及Mg-Ni-P-H2O系中各反应在298.15 K下的反应式及φ-p H计算式Table 3φ-p H formula of equilibrium reactions in Ni-P-H2O,Li-Ni-P-H2O,Na-Ni-P-H2O,K-Ni-P-H2O and Mg-Ni-P-H2O systems at 298.15 K 下载原图

表3 Ni-P-H2O系、Li-Ni-P-H2O系、Na-Ni-P-H2O系、K-Ni-P-H2O系以及Mg-Ni-P-H2O系中各反应在298.15 K下的反应式及φ-p H计算式Table 3φ-p H formula of equilibrium reactions in Ni-P-H2O,Li-Ni-P-H2O,Na-Ni-P-H2O,K-Ni-P-H2O and Mg-Ni-P-H2O systems at 298.15 K
由图2可知,在水的稳定区内,三价Ni主要以Ni PO4的形式存在,二价Ni以Ni2+,Ni3(PO4)2和Ni(OH)2的形式存在。在3.948<p H<10.908的范围内,Ni3(PO4)2在水溶液中都可以稳定存在,当p H<3.948或p H>10.908时,Ni3(PO4)2以Ni2+或Ni(OH)2的形式存在。
对比图2和3可知:当在Ni-P-H2O体系中引入Li+后,热力学计算条件下Ni3(PO4)2不再存在,取而代之以更大稳定区域的Li Ni PO4相,Ni2+,Ni(OH)2的稳定区也有较大部分被Li Ni PO4侵占,在3.885<p H<13.009的范围内,Li Ni PO4在水溶液中都可以稳定存在;当p H<3.885时,Li Ni PO4会溶解到酸性溶液中,Ni以Ni2+形式存在;而当p H>13.009时,Li Ni PO4也不能稳定存在,Ni以Ni(OH)2形式存在。由此可知,控制合适的p H和电位,Ni PO4和Li Ni PO4都能在水溶液中稳定存在。
图2 Ni-P-H2O系φ-p H图([Ni]=[P]=0.1 mol・L-1)Fig.2φ-p H diagram of Ni-P-H2O system([Ni]=[P]=0.1mol・L-1)
图3 Li-Ni-P-H2O系φ-p H图([Li]=[Ni]=[P]=0.1 mol・L-1)Fig.3φ-p H diagram of Li-Ni-P-H2O system([Li]=[Ni]=[P]=0.1 mol・L-1)
对比图2和3还可以得知:由于Li+的加入,在水溶液中,高电位和高p H条件下,出现了Ni(OH)3的稳定区。由图3中的线1可知,在p H为3.885~13.009的范围内,当体系电位φ≤0.2379V(vs SHE,以下所有电位均是相对于标准氢电极)时,Ni PO4中Ni3+将被还原为Ni2+,而体系中存在Li+,此时Ni3(PO4)2不能稳定存在,将转化为更加稳定的Li Ni PO4。由此可知,在中性条件下,只需将体系的氧化还原电位调至0.2379 V以上,Li Ni PO4将会分解为Ni PO4并释放出Li+,若将氧化还原电位调至0.2379 V以下,Ni PO4又会与Li+结合生成Li Ni PO4。从热力学的角度分析,通过控制体系的氧化还原电位,可使水溶液中的Li+在电极材料中可逆嵌入/脱出,这为采用Ni PO4/Li NiPO4进行盐湖提锂奠定了理论基础。
2.2 Me-Ni-P-H2O(Me=Na,K,Mg)系φ-p H图分析
由于盐湖卤水中不仅存在Li+,还存在大量的与Li+同族的Na+,K+以及处于对角线位置的Mg2+,其化学性质非常相似,极有可能对Ni PO4选择性提锂造成干扰,因此有必要研究杂质离子对Ni PO4离子筛提锂过程的影响。假设Na+,K+,Mg2+嵌入Ni PO4晶格中后会形成Na Ni PO4,KNiPO4,Mg0.5Ni PO4,分别将0.1 mol・L-1的Na+,K+,Mg2+引入Ni-P-H2O系中,绘制出Na-Ni-P-H2O系、K-Ni-P-H2O系、Mg-Ni-P-H2O系,具体如图4~6所示。
由图4和5可知,Na-Ni-P-H2O,K-Ni-P-H2O与Li-Ni-P-H2O系比较类似,Ni3(PO4)2的稳定区也不存在。对Na-Ni-P-H2O,在5.389<p H<10.750的范围内,二价Ni主要以Na Ni PO4的形式存在。当体系的还原电位φ<-0.0291V,Na Ni PO4可转变为Ni PO4。而在K-Ni-P-H2O系中,5.11<p H<11.17的范围内,二价Ni主要以KNi PO4的形式存在,Ni PO4与KNi PO4之间相互转化的电位为0.0209 V。而由图6可以知道,由于Mg HPO4・3H2O,Mg3(PO4)2,Mg(OH)2的溶度积非常小,在Mg-Ni-P-H2O系中会出现Mg HPO4・3H2O,Mg3(PO4)2,Mg(OH)2的固相。与图3~5相比,最大不同在于该体系中没有Mg0.5Ni PO4的稳定区域,表明热力学计算条件下Mg0.5Ni PO4无法在该体系中稳定存在,换言之,Mg2+不能进入Ni PO4晶格生成Mg0.5Ni PO4,Ni PO4/Li Ni PO4具有显著的锂镁分离性能。
图4 Na-Ni-P-H2O系φ-p H图([Na]=[Ni]=[P]=0.1mol・L-1)Fig.4φ-p H diagram of Na-Ni-P-H2O system([Na]=[Ni]=[P]=0.1 mol・L-1)
图5 K-Ni-P-H2O系φ-p H图([K]=[Ni]=[P]=0.1mol・L-1)Fig.5φ-p H diagram of K-Ni-P-H2O system([K]=[Ni]=[P]=0.1 mol・L-1)
图6 Mg-Ni-P-H2O系φ-p H图([Mg]=[Ni]=[P]=0.1mol・L-1)Fig.6φ-p H diagram of Mg-Ni-P-H2O system([Mg]=[Ni]=[P]=0.1 mol・L-1)
对比图3~5可知,虽然Na Ni PO4和KNi PO4均可在水的稳定区域存在,但Li Ni PO4的稳定区大于Na Ni PO4和KNi PO4的稳定区,且转变成Ni PO4时所需的电位各不相同,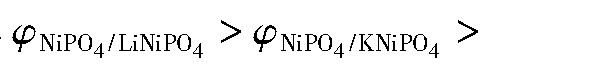
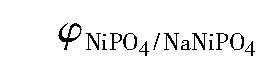
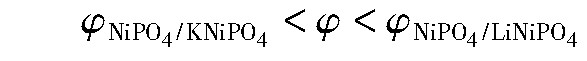
2.3 实际浓度φ-p H叠加图分析
由于以上计算均假定Li+,Na+,K+,Mg2+浓度为0.1 mol・L-1,而实际的盐湖卤水中Li+浓度较低,Na+,Mg2+,K+浓度较高。从表3可知,体系的电位与离子浓度密切相关,为了考察实际盐湖卤水中各种离子的影响,现以如表4所示的西台吉乃尔盐湖卤水中主要阳离子的浓度
由图7可知,当Mg2+浓度达到0.6 mol・L-1时(此时Mg/Li质量比高达67),Mg0.5Ni PO4仍不能在水溶液中稳定存在,Li Ni PO4的稳定区仍然比Na Ni PO4和KNi PO4的稳定区大。比较图7中的1,2,3线可知:在较高的氧化还原电位(φ=0.207V)下,Ni PO4被还原为Li Ni PO4,而生成Na Ni PO4和KNi PO4所需的还原电位更负,分别为0.071,0.0387 V;当p H≥4.058时,Ni2+不再稳定,与Li+结合转化为Li Ni PO4;Na Ni PO4和KNi PO4也表现出类似的现象,只是p H略有不同,分别在p H≥4.822和p H≥5.009时发生转化。上述结果表明,与Na+,K+相比,Li+更容易在电极材料中嵌入/脱出,针对实际的盐湖卤水,电极材料仍具有良好的选择性提锂性能。
表4 西台吉乃尔盐湖地表湖水部分离子组成Table 4Partial composition of lake water in West Salt Lake Taijnar(g・L-1) 下载原图

表4 西台吉乃尔盐湖地表湖水部分离子组成Table 4Partial composition of lake water in West Salt Lake Taijnar(g・L-1)
图7 Li-Ni-P-H2O系、Na-Ni-P-H2O系、K-Ni-P-H2O系φ-p H叠加图Fig.7φ-p H diagram of Li-Ni-P-H2O,Na-Ni-P-H2O,K-Ni-P-H2O system
([Li]=0.03 mol・L-1,[Na]=5 mol・L-1,[K]=0.2 mol・L-1,[Ni]=[P]=0.1 mol・L-1)
由图7还可知,在中性条件下,控制体系的电位0.071 V<φ<0.207 V,即可使卤水中的Li嵌入到Ni PO4中生成Li Ni PO4,而天然卤水的p H一般在7左右,表明此时无需添加酸或碱来调节卤水的p H,这与节能减排和环境保护的理念不谋而合;再调节体系的氧化还原电位φ>0.207 V,使Li NiPO4中的Li脱出到溶液中同时得到Ni PO4;不断重复上述过程,即可从盐湖卤水中选择性提取锂。
3 结论
1.运用同系线性规律对Me(Li,Na,K,Mg)-Ni-P-H2O中Ni PO4,Ni3(PO4)2,Li Ni PO4,Na Ni PO4,KNi PO4,Mg0.5Ni PO4的标准吉布斯自由能进行了估算。绘制了298.15 K、离子浓度0.1 mol・L-1的Ni-P-H2O系、Li-Ni-P-H2O系、Na-Ni-P-H2O系、K-Ni-P-H2O系以及Mg-Ni-P-H2O系φ-p H图,结果表明:水溶液中存在Ni PO4,Li Ni PO4,Na Ni PO4,KNi PO4的稳定区,不存在Mg0.5Ni PO4的稳定区;生成Li N-i PO4,Na Ni PO4,KNi PO4的还原电位(vs SHE)分别为0.2379,-0.0291,0.0209 V。
2.根据西台吉乃尔盐湖卤水中的实际离子浓度,绘制出Me(Li,Na,K,Mg)-Ni-P-H2O系叠加φ-p H图,结果表明:在Mg/Li质量比高达67的情况下,Ni PO4/Li Ni PO4电极对仍然具有良好的选择性提锂功能。
3.提出采用Ni PO4/Li Ni PO4进行盐湖卤水提锂的思路:在天然卤水原始p H值条件下,控制体系的电位0.071 V<φ<0.207 V使Ni PO4发生嵌锂反应生成Li Ni PO4;通过调节体系的电位φ>0.207 V,Li Ni PO4发生脱锂反应得到含锂的纯溶液和Ni PO4;不断重复该过程即可实现从盐湖卤水中选择性提取锂。
参考文献
[14] B Ueli X,Wenjiao.Exploitation of Lithium in Brines by Hsus Method[M].Amsterdam,2001.62.

