文章编号:1004-0609(2008)S1-0199-08
RbCl-H2O二元系和RbCl-RbNO3-H2O三元系作用浓度计算模型
郭汉杰1,杨学民2,赵伟洁1,焦晋沙1
(1. 北京科技大学 冶金与生态工程学院,北京 100083;
2. 中国科学院 过程工程研究所 多相复杂系统国家重点实验室, 北京 100080)
摘 要:利用离子-分子共存理论建立温度为298.15 K时强电解质水溶液二元系RbCl-H2O和三元系RbCl-RbNO3-H2O作用浓度计算热力学模型。热力学模型计算的以纯物质为标准态、以摩尔分数为浓度单位的RbCl-H2O二元系各组元作用浓度经过转换系数转换后,与文献报道的以无限稀为标准态、以质量摩尔浓度为浓度单位的组元活度吻合良好。RbCl-RbNO3-H2O三元系的RbCl和RbNO3转换后的作用浓度与文献报道的活度在总离子强度为0.01、0.05、0.1、0.5、1.0、1.5、2.0、3.0和3.5 mol/kg时均良好吻合。这说明基于离子-分子共存理论建立的作用浓度计算热力学模型能反映强电解质水溶液RbCl-H2O和RbCl-RbNO3-H2O的结构特性;且组元的作用浓度在计算的浓度单位内严格遵守质量作用定律。
关键词:RbCl-H2O;RbCl-RbNO3-H2O;作用浓度;活度;离子-分子共存理论;转换系数
中图分类号:TQ 013.1 文献标识码:A
Calculating models of mass action concentrations for RbCl-H2O binary system and RbCl-RbNO3-H2O ternary system
GUO Han-jie 1, YANG Xue-min 2, ZHAO Wei-jie 1, JIAO Jin-sha 1
(1. School of Metallurgical and Ecological Engineering, University of Science and Technology Beijing,Beijing 100083, China;
2. State Key Laboratory of Multiphase Complex System, Institute of Process Engineering, Chinese Academy of Sciences,Beijing 100080, China)
Abstract: Thermodynamic models of calculating mass action concentrations of components in RbCl-H2O binary and RbCl-RbNO3-H2O ternary strong electrolyte aqueous solutions were developed based on the ion and molecule coexistence theory at 298.15 K. A transformation coefficient is needed to compare calculated mass action concentration with reported activity because they are obtained at different standard state and concentration unit. The results show that transformation coefficients between calculated mass action concentrations and reported activities of the same components change in a very narrow range. The transformed mass action concentrations of components in RbCl-H2O binary system are in good agreement with reported activities. The transformed mass action concentrations of RbCl and RbNO3 in RbCl-RbNO3-H2O ternary solution are in good agreement with reported activities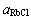 and
and 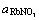 with different constant total ionic strengths as 0.01, 0.05, 0.1, 0.5, 1.0, 1.5, 2.0, 3.0 and 3.5 mol/kg, respectively. All those results mean that the developed thermodynamic model of strong electrolyte aqueous solutions can reflect structural characteristics of RbCl-H2O binary and RbCl-RbNO3-H2O ternary strong electrolyte aqueous solutions and the mass action concentration also strictly follows mass action law.
with different constant total ionic strengths as 0.01, 0.05, 0.1, 0.5, 1.0, 1.5, 2.0, 3.0 and 3.5 mol/kg, respectively. All those results mean that the developed thermodynamic model of strong electrolyte aqueous solutions can reflect structural characteristics of RbCl-H2O binary and RbCl-RbNO3-H2O ternary strong electrolyte aqueous solutions and the mass action concentration also strictly follows mass action law.
Key words: RbCl-H2O; RbCl-RbNO3-H2O; mass action concentration; activity; coexistence theory; transformation coefficient
________________
20世纪80年代张鉴教授提出的离子-分子共存理论在以二元金属熔体[1]、二元冶金炉渣[2]、三元金属熔体[3-4]、三元冶金炉渣[5-6]和多元熔渣[7-8]为代表的熔体中得到良好应用。电解质水溶液的热力学参数,如活度和活度系数,在生化过程[9-12]、工业生产过程[13]、湿法冶金、环境化学和地球化学[14]等领域有重要而广泛的应用。为了预测活度和活度系数数据不全的电解质水溶液组元的活度和其结构本质,研究电解质水溶液作用浓度的热力学模型和方法是十分必要的。
电解质水溶液由离子、简单分子和复杂分子组成。因此依据离子-分子共存理论计算的组元作用浓度与活度一样能反映出电解质水溶液中各组元的反应能力。在离子-分子共存理论成功应用于二元电解质水溶液体系KCl-H2O、CsCl-H2O、NaCl-H2O、BaCl2- H2O[15],NaBr-H2O、LiNO3-H2O、HNO3-H2O、KF- H2O[16],三元电解质水溶液体系NaCl-KCl-H2O[17]和NaClO4-NaF-H2O[18]的基础上,为了进一步拓展离子-分子共存理论预报电解质水溶液组元反应能力的适用性,本文作者依据三元系强电解质水溶液作用浓度通用热力学模型[17]建立了RbCl-RbNO3-H2O三元系作用浓度的热力学模型。为了便于描述三元系RbCl- RbNO3-H2O中各组元的性质,本文作者以二元系强电解质水溶液作用浓度通用热力学模型[15-18]为依据,建立了RbCl-H2O二元系各组元作用浓度热力学模型。
利用本研究建立的RbCl-RbNO3-H2O三元系作用浓度热力学模型,计算了工作温度为298.15 K时RbCl-RbNO3-H2O三元系中RbCl和RbNO3的作用浓度,并与文献报道的总离子强度为0.01、0.05、0.1、0.5、1.0、1.5、2.0、3.0 和3.5 mol/kg时的活度进行了比较。由于作用浓度和活度的标准态和浓度单位不同,为了便于比较,需定义不同标准态和浓度单位的活度和作用浓度间的转换系数。
1 作用浓度的计算热力学模型
1.1 假设
强电解质水溶液共存理论基本假设如下:
1) 电解质溶液由电离得到的简单离子(Na+、Ca2+、Mg2+、Cl-、Br-、F-等)和H2O、水合盐等分子组成。其中电离得到的正、负离子在溶液中各占一个结构单元;
2) 简单离子和水分子生成水合盐分子时进行动态平衡反应;
3) 水溶液的结构单元在研究的成分范围内具有连续性;
4) 水溶液内部各组元间的化学反应服从质量作用定律。
1.2 RbCl-H2O二元系作用浓度计算模型
1.2.1 结构单元和计算模型
研究表明[19],温度为298.15 K时RbCl在水中完全电离,且RbCl和H2O不能生成水合盐。因此RbCl-
H2O水溶液的结构单元为Rb+、Cl-和H2O分子。配制溶液时RbCl的摩尔数为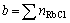 ,H2O的摩尔数为
,H2O的摩尔数为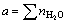 ;平衡后溶液中各组元摩尔数分别为x=
;平衡后溶液中各组元摩尔数分别为x=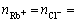 nRbCl,
nRbCl,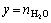 ;平衡后电解质溶液的组元作用浓度分别为 N1=NRbCl,
;平衡后电解质溶液的组元作用浓度分别为 N1=NRbCl,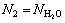 ;
;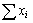 为配制溶液时组元i的摩尔分数,
为配制溶液时组元i的摩尔分数,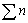 为平衡后溶液组
为平衡后溶液组
元的总摩尔数。RbCl-H2O二元系中溶质和溶液的质量平衡为
b=x, a=y, 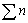 =2x+y (1)
=2x+y (1)
RbCl和H2O的作用浓度Ni分别为
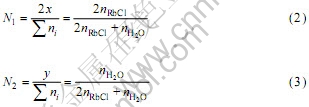
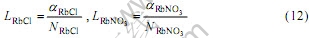
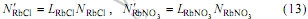
根据体系中总摩尔分数为1的原则,可得下式:
N1+N2=1 (4)
因此,式(2)~(3)为可计算组元作用浓度Ni的RbCl-H2O二元系热力学模型。
计算得到的作用浓度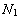 是以纯物质为标准态以摩尔分数为浓度单位,而文献报道的电解质水溶液各组元的活度系数通常以无限稀溶液为标准态以摩尔分数为浓度单位。因此,必须进行不同标准态的换算,以便相互比较。转换系数LRbCl和转换后的作用浓度
是以纯物质为标准态以摩尔分数为浓度单位,而文献报道的电解质水溶液各组元的活度系数通常以无限稀溶液为标准态以摩尔分数为浓度单位。因此,必须进行不同标准态的换算,以便相互比较。转换系数LRbCl和转换后的作用浓度
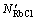 为
为
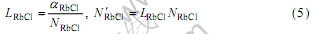
1.2.2 计算结果和分析
利用热力学模型计算的温度为298.15 K时RbCl- H2O二元系组元RbCl转换后的作用浓度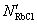 和文献报道[20]的实测活度αRbCl的比较如图1所示,计算得到水的作用浓度NH2O与摩尔分数的关系如图2所示。从图1中可看出,RbCl-H2O二元系计算的RbCl转换后作用浓度
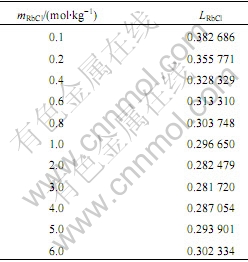
和文献报道[20]的实测活度αRbCl的比较如图1所示,计算得到水的作用浓度NH2O与摩尔分数的关系如图2所示。从图1中可看出,RbCl-H2O二元系计算的RbCl转换后作用浓度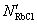 和其实测活度αRbCl[20]吻合较好。RbCl-H2O二元系中RbCl的质量摩尔浓度在0.1~6.0 mol/kg范围变化时作用浓度和活度的转换系数LRbCl如表1所列。从表1可看出RbCl的转换系数LRbCl较守常,平均值为0.311 635。因此,计算的作用浓度可反映RbCl在RbCl-H2O二元系溶液的反应能力。可以推论,本研究中建立的RbCl-H2O二元系水溶液热力学模型的假设是合理可信的,该模型也反映了RbCl二元水溶液的结构本质。
和其实测活度αRbCl[20]吻合较好。RbCl-H2O二元系中RbCl的质量摩尔浓度在0.1~6.0 mol/kg范围变化时作用浓度和活度的转换系数LRbCl如表1所列。从表1可看出RbCl的转换系数LRbCl较守常,平均值为0.311 635。因此,计算的作用浓度可反映RbCl在RbCl-H2O二元系溶液的反应能力。可以推论,本研究中建立的RbCl-H2O二元系水溶液热力学模型的假设是合理可信的,该模型也反映了RbCl二元水溶液的结构本质。
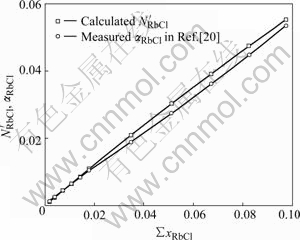
图1 RbCl-H2O二元系RbCl的作用浓度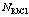 和实测活度aRbCl的比较
和实测活度aRbCl的比较
Fig.1 Comparison of transformed mass action concentration 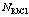 with reported activity aRbCl of RbCl
with reported activity aRbCl of RbCl
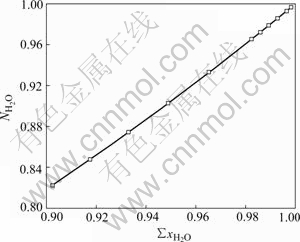
图2 H2O的作用浓度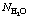 和摩尔分数的关系
和摩尔分数的关系
Fig.2 Relationship between calculated mass action concentra- tion 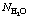 and mole fraction of H2O in RbCl-H2O binary solution
and mole fraction of H2O in RbCl-H2O binary solution
表1 RbCl-H2O二元系溶液RbCl的作用浓度和活度的转换系数
Table 1 Transformation coefficients between calculated mass action concentrations and reported activities of RbCl in RbCl-H2O solutions
1.3 RbCl-RbNO3-H2O三元系作用浓度计算模型
1.3.1 结构单元和计算模型
研究表明[19],温度为298.15 K时RbCl和RbNO3在水中可完全电离,且均不和水分子生成水合盐。根据离子-分子共存理论,RbCl-RbNO3-H2O水溶液的结构单元为Rb+、Cl-、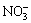 离子和H2O分子。配制溶液时RbCl和RbNO3的摩尔数为
离子和H2O分子。配制溶液时RbCl和RbNO3的摩尔数为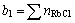 ,
,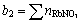 ,H2O的摩尔数为
,H2O的摩尔数为 ;平衡后溶液各组元摩尔数为
;平衡后溶液各组元摩尔数为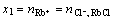 ,x2=
,x2=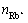 =
= 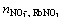 ,
,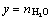 ;平衡后溶液各组元的作用浓度为N1=NRbCl,
;平衡后溶液各组元的作用浓度为N1=NRbCl,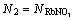 ,
,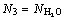 ;
;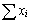 为配制溶液时组元i的摩尔分数;
为配制溶液时组元i的摩尔分数;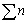 为平衡后溶液各组元的总摩尔数。根据质量作用定律,RbCl-RbNO3-H2O三元系中溶质和溶质的质量平衡为
为平衡后溶液各组元的总摩尔数。根据质量作用定律,RbCl-RbNO3-H2O三元系中溶质和溶质的质量平衡为
b1=x1,b2=x2,a=y,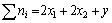 (6)
(6)
RbCl、RbNO3和H2O的作用浓度Ni分别为

根据体系中总摩尔分数为1的原则,可得下式:
N1+N2+N3=1 (11)
为了比较溶质的作用浓度和活度,RbCl和RbNO3的转换系数LRbCl和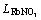 以及转换后的作用浓度
以及转换后的作用浓度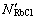 和
和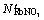 定义如下:
定义如下:
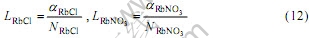
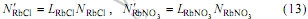
式(8)~(10)为可计算RbCl-RbNO3-H2O三元系各组元作用浓度Ni的热力学模型。
1.3.2 计算结果和分析
文献[21]给出了总离子强度I在0.01~3.5 mol/kg范围内RbNO3离子强度分数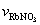 分别为0、0.2、0.4、0.6和0.8的RbCl-RbNO3-H2O三元系中RbCl和RbNO3实测活度和水的活度。式中 总离子强度I定义为
分别为0、0.2、0.4、0.6和0.8的RbCl-RbNO3-H2O三元系中RbCl和RbNO3实测活度和水的活度。式中 总离子强度I定义为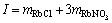 ,RbNO3的离子强度分数
,RbNO3的离子强度分数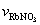 定义为
定义为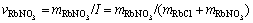 。为了便于比较,本研究中也按I和
。为了便于比较,本研究中也按I和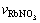 计算了RbCl-RbNO3-H2O三元系各组元的作用浓度,计算结果与实测活度[21]的对比如图3(a)~3(r)所示。从图3(a)~3(r)可看出,转换后的作用浓度
计算了RbCl-RbNO3-H2O三元系各组元的作用浓度,计算结果与实测活度[21]的对比如图3(a)~3(r)所示。从图3(a)~3(r)可看出,转换后的作用浓度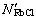 、
、 与实测的活度值[21]αRbCl,
与实测的活度值[21]αRbCl,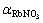 吻合很好。由表2给出的转换系数
吻合很好。由表2给出的转换系数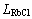 和
和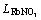 可知,不同总离子强度I时,RbCl和RbNO3的转换系数均较守常。H2O的作用浓度NH2O也以不同的总离子强度I列在表2。结合图3和表2可知,RbCl-RbNO3-H2O三元系溶液中各组元的活度和计算得到的作用浓度良好吻合,因此离子-分子共存理论可成功应用于该水溶液体系。
可知,不同总离子强度I时,RbCl和RbNO3的转换系数均较守常。H2O的作用浓度NH2O也以不同的总离子强度I列在表2。结合图3和表2可知,RbCl-RbNO3-H2O三元系溶液中各组元的活度和计算得到的作用浓度良好吻合,因此离子-分子共存理论可成功应用于该水溶液体系。
应强调的是,Rb+为RbCl-RbNO3-H2O三元系中组元RbCl和RbNO3的共有离子,本研究中开发的计算该三元系组元作用浓度的热力学模型并未考虑来自不同组元Rb+的交互作用;虽然计算的作用浓度与实测活度值良好吻合,但对共有离子Rb+的作用还应进一步研究;转换后的作用浓度和实测活度值良好吻合表明,依据质量作用定律建立的RbCl-RbNO3-H2O三元系热力学模型反映了该三元水溶液的结构特性;计算得到的组元质量作用浓度和文献报道的实测活度存在一定的误差,这主要是由于两者采取的标准态不同所致,通过以纯物质为标准态、以摩尔分数作浓度单位的活度测定可望减少这一误差。
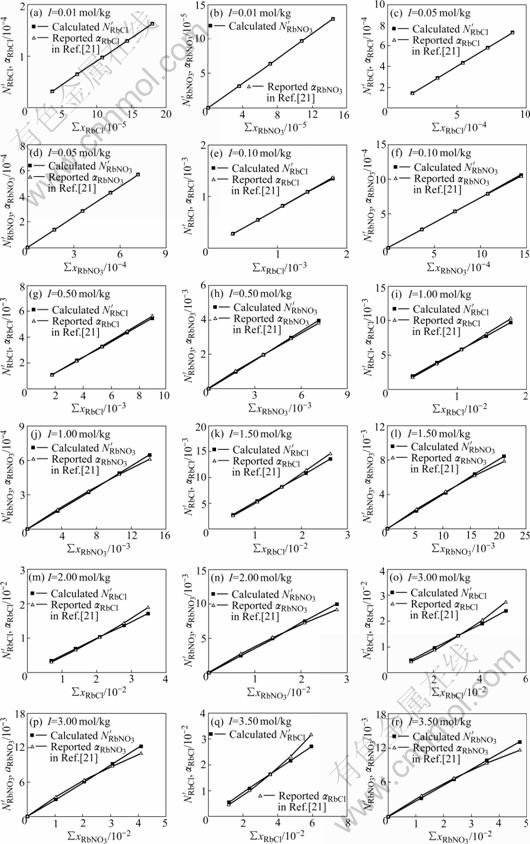
图3 RbCl-RbNO3-H2O三元系组元RbCl和RbNO3的作用浓度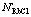 、
、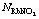 和实测活度值αRbCl、
和实测活度值αRbCl、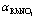 在不同总离子强度时的比较
在不同总离子强度时的比较
Fig.3 Comparison of mass action concentrations 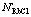 and
and 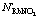 with reported activities αRbCl and
with reported activities αRbCl and 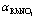 of RbCl and NbNO3 in RbCl-RbNO3-H2O ternary solution with different total ionic strengths (I)
of RbCl and NbNO3 in RbCl-RbNO3-H2O ternary solution with different total ionic strengths (I)
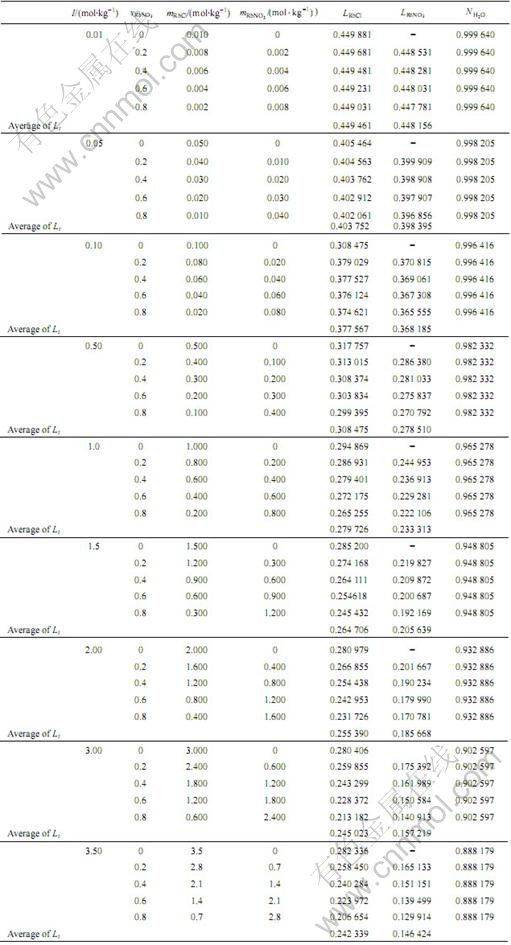
表2 RbCl-RbNO3-H2O三元水溶液体系中不同总离子强度和RbNO3离子强度分数条件下RbCl和RbNO转换系数及H2O的作用浓度
Table 2 Transformation coefficients LRbCl and 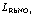 in range of total ionic strength from 0.01 mol/kg to 3.5mol/kg with different ionic strength fractions of RbNO3,
in range of total ionic strength from 0.01 mol/kg to 3.5mol/kg with different ionic strength fractions of RbNO3, 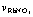 and calculated mass action concentration of H2O in RbCl-RbNO3-H2O ternary solution
and calculated mass action concentration of H2O in RbCl-RbNO3-H2O ternary solution
2 结论
1) 计算得到的RbCl-H2O二元系和RbCl-RbNO3- H2O三元系强电解质水溶液各组元的作用浓度和文献报道的活度吻合很好,因此,本研究中提出的RbCl- H2O二元系和RbCl-RbNO3-H2O三元系组元作用浓度的热力学模型可以预测组元的活度,即反应能力。
2) 质量作用定律和离子-分子共存理论不仅适用于RbCl-H2O二元系强电解质水溶液,而且能成功应用于RbCl-RbNO3-H2O三元系强电解质水溶液。
3) 计算得到的作用浓度和实测活度之间有少量误差,该问题可望通过以纯物质为标准态、以摩尔分数为浓度单位进行实测活度研究而解决。
REFERENCES
[1] ZHANG J. Calculation model of mass action concentrations for Mg-Al, Sr-Al and Ba-Al melts and determination of their thermodynamic parameters [J]. Journal of Iron and Steel Research International, 2003, 10(2): 5-9.
[2] 张 鉴. CaO-SiO2渣系的作用浓度的计算模型[J]. 北京钢铁学院学报, 1988, 10(4): 412-421.
ZHANG Jian. Calculation model of mass action concentrations CaO-SiO2 slag system [J]. Journal of University of Science and Technology Beijing, 1988, 10(4): 412-421.
[3] ZHANG J. Calculation model of mass action concentrations for Ag-Au-Cu melts [J]. Rare Metals, 2002, 21(1): 43-47.
[4] ZHANG J. Application of the annexation principle to the thermodynamic property study of ternary metallic melts In-Bi-Cu and In-Sb-Cu [J]. Journal of University of Science and Technology Beijing, 2002, 9(3): 170-176.
[5] 张 鉴, 袁伟霞. CaO-Al2O3-SiO2熔渣作用浓度计算模型[J]. 北京科技大学学报, 1995, 17(5): 418-423.
ZHANG Jian, YUAN Wei-xia. Calculation model of mass action concentrations CaO-Al2O3-SiO2 slag system [J]. Journal of University of Science and Technology Beijing, 1995, 17(5): 418-423.
[6] 张 鉴. FeO-Fe2O3-SiO2渣系的作用浓度计算模型[J]. 北京钢铁学院学报, 1988, 10(1): 1-6.
ZHANG Jian. Calculation model of mass action concentrations FeO-Fe2O3-SiO2 slag system [J]. Journal of University of Science and Technology Beijing, 1988, 10(1): 1-6.
[7] 张 鉴. FeO-MnO-MgO-SiO2 渣系和铁液间锰的平衡[J]. 北京科技大学学报, 1992, 14(5): 496-501.
ZHANG Jian. Manganese equilibrium between FeO-MnO-MgO- SiO2 slags and molten iron [J]. Journal of University of Science and Technology Beijing, 1992, 14(5): 496-501.
[8] ZHANG J. Application of the coexistence theory of slag structure to multi-component slag systems [C]// Proceedings of 4th International Conference On Molten Slags and Fluxes. Sendai: Sendai International Center, The Iron and Steel Institute of Japan, 1992: 244-249.
[9] CHAN C K, HA Z Y, CHOI M Y. Study of water activities of aerosols of mixtures of sodium and magnesium salts [J]. Atmospheric Environment, 2000, 34(28): 4795-4803.
[10] HA Z Y, CHAN C K. The water activities of MgCl2, Mg(NO3)2, MgSO4, and their mixtures [J]. Aerosol Sci Technol, 1999, 31(2/3): 154-169.
[11] PRUPPACHER H R, KLETT J D. Microphysics of clouds and precipitation [M]. Holland: Reidel Publishing Company, 1978.
[12] MOLINA M J, ZHANG R, WOOLDRIDGE P J, et al. Physical chemistry of the H2SO4/HNO3/H2O system: implications for polar stratospheric clouds [J]. Science, 1993, 261(5127): 1418-1423.
[13] GOKCEN N A. Determination and estimation of ionic activities of metal salts in water [R]. Report of Investigations No.8372, U.S. Department of the Interior, Bureau of Mines, 1979.
[14] GUENDOUZI M E, DINANE A. Determination of water activities, osmotic and activity coefficients in aqueous solutions using the hygrometric method [J]. J Chem Thermodynamics, 2000, 32(3): 297-310.
[15] 郭汉杰, 赵伟洁, 杨学民. 基于共存理论的二元系强电解质水溶液作用浓度通用热力学模型[J]. 过程工程学报, 2007, 7(2): 347-353.
GUO Han-jie, ZHAO Wei-jie, YANG Xue-min. A universal thermodynamic model of calculating mass action concentration of components in strong electrolyte binary aqueous solutions [J]. The Chinese Journal of Process Engineering, 2007, 7(2): 347-353.
[16] GUO H J, ZHAO W J, YANG X M. Calculating models of mass action concentrations for NaBr(aq), LiNO3(aq), HNO3(aq), and KF(aq) binary solutions [J]. Journal of University of Science and Technology Beijing, 2007, 14(3): 204-211.
[17] ZHAO W J, GUO H J, YANG X M. A universal thermodynamic model of calculating mass action concentrations for components in ternary strong electrolyte aqueous solution and its application in NaCl-KCl-H2O system [J]. Journal of University of Science and Technology Beijing, 2008, 15(3): 1-7.
[18] 赵伟杰. 电解质水溶液作用浓度的热力学模型[D]. 北京: 北京科技大学, 2007.
ZHAO Wei-jie. Thermodynamic model of mass action concentrations in electrolyte aqueous solutions [D]. Beijing: University of Science and Technology Beijing, 2007.
[19] DONALD D W, WILLIAM H E, VIVIAN B P, PICHARD H S, IVA H, SYLVIA M B, KENNETH L C, RALPH L N. NBS化学热力学性质表[M]. 刘天和, 赵梦月, 译. 北京: 中国标准出版社, 1998.
DONALD D W, WILLIAM H E, VIVIAN B P, PICHARD H S, IVA H, SYLVIA M B, KENNETH L C, RALPH L N. The NBS tables of chemical thermodynamic properties [M]. LIU Tian-he, ZHAO Meng-yue, transl. Beijing: Chinese Standards Press, 1998.
[20] РАБИНОВИЧ В А, ХАВИН З Я. 简明化学手册[M]. 尹承烈, 译. 北京: 化学工业出版社, 1983: 651-659.
РАБИНОВИЧ В А, ХАВИН З Я. Concise handbook of chemistry [M]. YIN Chen-lie, transl. Beijing: Chemical Industry Press, 1983: 651-659.
[21] ZHANG J, HUANG Y, XIA S P. Experimental determination and prediction of activity coefficients of RbCl in aqueous (RbCl+RbNO3) mixture at T=298.15 K [J]. The Journal of Chemical Thermodynamics, 2005, 37: 1162-1167.
______________________________
基金项目:“十一五”国家重点图书和国家科学技术著作出版基金资助项目
通讯作者:杨学民,博士;电话:010-82622893;E-mail: yangxm71@home.ipe.ac.cn
(编辑 何学锋)