п®АлЧУөзіШМјёәј«ЦРұЯФөМјј°ұнГжМјФӯЧУә¬БҝөДАнВЫјЖЛг
ХЕЎЎұҰЈ¬№щ»ӘҫьЈ¬АоРВәЈЈ¬НхЦҫРЛЈ¬ЕнОДҪЬ
(ЦРДПҙуС§ ТұҪрҝЖС§Ул№ӨіМС§ФәЈ¬әюДП іӨЙіЈ¬410083)
ХӘЎЎТӘЈәНЁ№эАнВЫ·ЦОцУлјЖЛгөГөҪұЯФөМјј°ұнГжМјФӯЧУә¬БҝөДұнҙпКҪЎЈ·ЦОцБЛКҜД«Оўҫ§Ҫб№№УліЙјьМШХчЈ¬СРҫҝБЛКҜД«Оўҫ§ЦРұЯФөМјФӯЧУУл»щЖҪГжМјФӯЧУөДөз»ҜС§МШРФЎЈҪб№ыұнГчЈәұЯФөМјФӯЧУұИ»щЖҪГжМјФӯЧУёьТЧУЪУлЖдЛыФӯЧУ»т»щНЕРОіЙҪПОӘОИ№МөДБӘҪУЈ¬өз»ҜС§·ҙУҰ»оРФҪПёЯЈ»ФЪКЧҙОідөз№эіМЦРЈ¬ұЯФөМјФӯЧУёҪҪьөзҪвЦКөД·ЦҪвУлSEIДӨіЙДӨ·ҙУҰЛЩ¶ИҪПҝмЈ¬УРАыУЪРОіЙБӘҪУҪПОӘҪфГЬөДSEIДӨЈ»ҪЁБўБЛҪфГЬ¶СЖцөДХэБщАвЦщҝЕБЈДЈРНЈ¬НЖөјіцАнПлКҜД«ЦРұЯФөМјФӯЧУј°ұнГжМјФӯЧУә¬БҝУлОўҫ§ІОКэЎўҝЕБЈіЯҙзЦ®јдөД№ШПөКҪЎЈНЁ№эТэИлККөұТтЧУЈ¬РЮХэБЛКөјККҜД«ҝЕБЈУлАнПлКҜД«ФЪҪб№№ЎўРОГІЎўҝЧП¶ВКөИ·ҪГжөДІоұрЈ¬өГөҪөДұнҙпКҪҝЙККУГУЪКҜД«ЎўОЮ¶ЁРОМјј°ёДРФМјөИ¶аЦЦМјІДБПМјФӯЧУә¬БҝөДјЖЛгЎЈ
№ШјьҙКЈәп®АлЧУөзіШЈ»ёәј«Ј»МјЈ»КҜД«
ЦРНј·ЦАаәЕЈәTM912.9 ОДПЧұкК¶ВлЈәA ОДХВұаәЕЈә1672-7207(2007)02-0251-05
Theoretical calculation of fraction of carbon atoms on surface and
edge for carbon anode of lithium ion battery
ZHANG Bao, GUO Hua-jun, LI Xin-hai, WANG Zhi-xing, PENG Wen-jie
(School of Metallurgical Science and Engineering, Central South University, Changsha 410083, China)
Abstract: The fractions of carbon atoms on the surface and edge were obtained by theoretical analysis and calculation. The electrochemical characteristics of carbon atoms on the edge and basal plane were determined by analyzing structure of graphite crystal and bond of different carbon atoms. The results show that the atoms on the edge are more active for electrochemical reactions and tend to form stable bond with other atoms and groups. In the initial charge, the electrolyte decomposition and formation of solid electrolyte interface (SEI) on the edge are faster, and tighter SEI is formed there. A hexagonal close-packed model for graphite particle was developed. The fraction of carbon atoms on the surface and edge was derived in expression of crystallographic parameters and particle size. The practical graphite particle and the ideal graphite have some difference in structure, appearance and micro-cavity, which may cause the fractions of surface carbon and edge carbon change, and some correctional factors have been introduced to revise the difference. The revised expression is suitable for calculation on fraction of carbon atoms of carbon materials such as graphite, disordered carbon and modified carbon.
Key words: lithium ion battery; anode; carbon; graphite
Мјёәј«ІДБПөДСРҫҝКЗДҝЗ°п®АлЧУөзіШСРҫҝЦРЧоОӘ»оФҫөДБмУтЦ®Т»Ј¬п®АлЧУөзіШМјёәј«ІДБПЦЦАа·ұ¶аЈ¬ёчЦЦМјІДБПөДЗ¶п®МШРФІоұрҪПҙу[1-5]ЎЈМјІДБПөДөз»ҜС§РФДЬУлЖдҪб№№УРәЬЗҝөДПа№ШРФ[6-11]Ј¬ҪшТ»ІҪ¶ФЖдҪб№№ёшіцҫ«И·өДұнХчЈ¬ІўҪТКҫХвЦЦПа№ШРФЈ¬¶ФПЦУРІДБПөДёДҪшәНРВІДБПөД·ўПЦТвТеЦШҙуЈ¬ө«ДҝЗ°ЙРОҙјыөҪХв·ҪГжөДОДПЧұЁөАЎЈ
ұҫСРҫҝҙУМјІДБПөД»щұҫҪб№№өҘФӘЎӘЎӘ МјБщФӘ»·іц·ўЈ¬ёщҫЭКҜД«өДҪб№№МШХчЈ¬·ЦОцКҜД«Оўҫ§ЦРІ»Н¬О»ЦГМјФӯЧУөДөз»ҜС§»оРФЈ¬НЖөјұЯФөМјФӯЧУј°ұнГжМјФӯЧУә¬БҝУлКҜД«Оўҫ§»тҝЕБЈөДҪб№№УлМШРФІОКэөД№ШПөКҪЈ¬ТФЖЪ№№ЦюБӘПөМјІДБПөДҪб№№ЎўМШРФУлөз»ҜС§РФДЬөДЗЕБәЈ¬ОӘәуРшМҪЛч¶аЦЦМјёәј«ІДБПј°ёДРФМјІДБПөДЗ¶п®ЧчУГ»ъАнМṩАнВЫ»щҙЎәНТАҫЭЎЈ
1 КҜД«өДҪб№№ј°І»Н¬О»ЦГМјФӯЧУөДөз»ҜС§»оРФ
МјО»УЪФӘЛШЦЬЖЪұнЦРөДөЪ¶юЦЬЖЪөЪЛДЦчЧеЈ¬МјФӯЧУөДөзЧУЕЕІјОӘ1s22s22p2ЎЈФЪКҜД«ЦРЈ¬МјФӯЧУөД1ёц2s№мөАУл2ёц2p№мөА(2pxУл2py)ФУ»ҜРОіЙ3ёцөИН¬өДsp2ФУ»Ҝ№мөАЈ¬·ЦұрЦёПтХэИэҪЗРОөД3ёцҪЗЈ¬БнНвТ»ёцОҙІОјУФУ»ҜөД2pz№мөАФтУлҙЛИэҪЗРОөДЖҪГжҙ№ЦұЎЈөұРн¶аМјФӯЧУФЪН¬Т»ЖҪГжДЪПа»ҘҪУҪь¶шҪбәПКұЈ¬ЛьГЗТЧУЪІЙУГФУ»Ҝ№мөАЈ¬ұЛҙЛјд(ЖҪГж·ҪПт)ТФ3ёц№ІјЫјьРОіЙБщҪЗ»·РОНшЧҙҪб№№(ИзНј1(a)әН(b)ЛщКҫ)ЎЈРн¶аЖҪРжѻэөДҙуЖ¬НшЧҙМе·ЦЧУНЁ№э·¶өВ»ӘБҰ(·ЦЧУјь)ҪбәПЖрАҙЈ¬РОіЙБЛКҜД«өДҫ§МеҪб№№[12]ЎЈ
КҜД«ІгУлІгЦ®јдөДПа¶ФО»ЦГУР2ЦЦЕЕБРРОКҪЈ¬Тт¶шРОіЙ2ЦЦКҜД«ҫ§МеЈәТ»ЦЦКЗБщ·Ҫҫ§ПөКҜД«Ј¬ПаБЪөДБҪ»щГжПа»ҘҙнҝӘЈ¬ЙПІг»щГжөД1ёцМјФӯЧУҙҰУЪПВІг»щГжөДБщҪЗРОНшёсөДЦРСлЈ¬Гҝёф1ІгЈ¬МјФӯЧУөДО»ЦГПаН¬Ј¬іЙОӘABABABЎӯЎӯөДИэО¬ҝХјдУРРтЕЕБР(ИзНј1(b)ЛщКҫ)[12-13]Ј»БнТ»ЦЦКЗБвГжМеҫ§ПөКҜД«Ј¬ІгУлІгЦ®јдөДҪбәПіКABCABCЎӯЎӯЦШөюЈ¬БвГжМеҫ§ПөКҜД«КөјКЙПКЗТ»ЦЦУРИұПЭөДКҜД«Ј¬ФЪёЯОВПВҝЙЧӘ»ҜОӘБщ·Ҫҫ§ПөКҜД«ЎЈҙу¶аКэөДМмИ»КҜД«УлИЛФмКҜД«ОӘБщ·Ҫҫ§ПөКҜД«ЎЈ
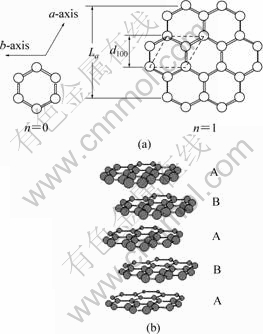
(a)carbon plane; (b)hexagonal crystallite
Нј1 КҜД«Оўҫ§Ҫб№№КҫТвНј
Fig.1 Schematic diagram for structure of graphite crystallite
ёщҫЭМјФӯЧУөДҪб№№КҫТвНј(Нј1)Ј¬КҜД«Оўҫ§ұнГжөДМјФӯЧУҝЙ·ЦОӘ2Аа[14-15]ЈәО»УЪКҜД«Оўҫ§ІаГжөДұЯФөМјФӯЧУЈ¬ТФј°О»УЪКҜД«Оўҫ§ЙППВұнГжЦРөДДЪІгМјФӯЧУ(ұҫСРҫҝіЖЦ®ОӘ»щЖҪГжМјФӯЧУ)ЎЈУЙУЪ»·ҫіј°іЙјьЗйҝцөДІ»Н¬Ј¬»щЖҪГжМјФӯЧУУлұЯФөМјФӯЧУөДөз»ҜС§РФЦКІоұрәЬҙуЈә
a. ұЯФөМјФӯЧУЦРУРІҝ·ЦМјФӯЧУУлПаБЪМјФӯЧУРОіЙ№ІјЫјьөДКэДҝОӘ2Ј¬ФЪНј1өДДЈРНЦРіЙјьКэОӘ2өДМјФӯЧУФЪұЯФөМјФӯЧУЦРөДұИАэОӘ(n+1)/(2n+1)Ј¬ХвР©МјФӯЧУөДsp2ФУ»Ҝ№мөАЙПЙРҙжФЪ1ёцОҙіЙјьөзЧУЈ¬Тт¶шФЪәПККөДМхјюПВТЧУлЦЬО§өДЖдЛьФӯЧУ»т»щНЕИзСхЎўЗвЎўфЗ»щЎўфИ»щөИ·ўЙъ·ҙУҰіЙјьЈ¬¶ш»щЖҪГжДЪөДМјФӯЧУУЙУЪsp2ФУ»Ҝ№мөАЙПөДөзЧУҫщТСУлПаБЪөДМјФӯЧУРОіЙ№ІјЫјьЈ¬ЛьГЗЦ»ДЬТФ·ЦЧУјьөДЧчУГБҰУлЖдЛы·ЦЧУБӘҪУЈ¬јҙұЯФөМјФӯЧУУлЖдЛыФӯЧУЎў·ЦЧУЎўАлЧУөДЧчУГБҰҪПЗҝЈ¬БӘҪУҪПОӘОИ№МЈ»
b. ұЯФөМјФӯЧУУЙУЪЖдіЙјьөДІ»ұҘәНРФЈ¬ТЧУЪОьёҪЖдЛыФӯЧУЎў·ЦЧУ»тАлЧУЈ¬ТтҙЛЈ¬ФЪУҰУГМјІДБПЧчөзј«КұЈ¬ЖдЛыФӯЧУЎў·ЦЧУ»тАлЧУТЧҙУұЯФөМјФӯЧУёҪҪь»сөГ»тК§ИҘөзЧУ¶ш·ўЙъөз»ҜС§·ҙУҰЈ¬јҙұЯФөМјФӯЧУөДөз»ҜС§·ҙУҰ»оРФҪПёЯЎЈ
ТтҙЛЈ¬О»УЪКҜД«Оўҫ§ұнГжөДұЯФөМјФӯЧУҫЯУРұИ»щЖҪГжМјФӯЧУёЯөГ¶аөДөз»ҜС§»оРФЈ¬ФЪКЧҙОідөз№эіМЦРЈ¬ұЯФөМјФӯЧУёҪҪьөДSEIДӨіЙДӨ·ҙУҰЛЩ¶ИҪПҝмЈ¬¶шЗТУРАыУЪРОіЙБӘҪУҪПОӘҪфГЬөД№ММе-өзҪвЦКЦРјдПа(SEI)ДӨЎЈ
2 АнПлКҜД«ҝЕБЈЦРұЯФөМјФӯЧУј°ұнГжМјФӯЧУә¬БҝөДјЖЛг
јЩЙиАнПлКҜД«МјІгКЗУЙМјБщФӘ»·°ҙХХНј1·ҪКҪҫщФИ·ўХ№іЙХэБщұЯРОЈ¬КҜД«Оўҫ§КЗУЙmІгХэБщұЯРОөДМјІг¶СХ»РОіЙөДХэБщАвЦщЈ¬ФтУРЧйіЙКҜД«Оўҫ§өДМјІгөД¶юО¬іЯҙз[15]Јә

КҜД«Оўҫ§өД¶СХ»әс¶ИОӘ

КҜД«Оўҫ§ЦРГҝТ»МјІгЦРөДұЯФөМјФӯЧУКэОӘ

КҜД«Оўҫ§ЦРmІгМјІгөДұЯФөМјФӯЧУКэОӘ
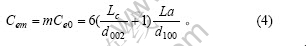
Оўҫ§ЦРГҝТ»МјІгЦР°ьә¬өДМјФӯЧУКэОӘ
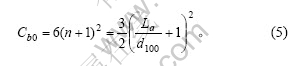
јЩЙиХэБщАвЦщөДКҜД«Оўҫ§ҪфГЬ¶С»эРОіЙХэБщАвЦщөДКҜД«ҝЕБЈЎЈКҜД«ҝЕБЈөЧГжөД¶ФҪЗПЯіӨОӘDЈ¬ёЯОӘHЎЈФтУРКҜД«ҝЕБЈёЯ¶И·ҪПтОўҫ§ІгКэОӘ

КҜД«ҝЕБЈЦРГҝТ»Оўҫ§ІгЦР°ьә¬өДОўҫ§КэОӘКҜД«ҝЕБЈөЧГжөДГж»эУлКҜД«Оўҫ§¶юО¬·ҪПтөДГж»эЦ®ұИЈә
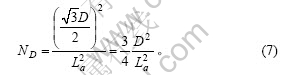
ГҝТ»ІгКҜД«Оўҫ§ІгөДБщМхұЯЙП°ьә¬өДОўҫ§КэОӘ

ГҝТ»ұЯФөОўҫ§УР2ёцІаГжО»УЪҝЕБЈөДНвІаЈ¬Оўҫ§ГҝІаөДұЯФөМјФӯЧУКэОӘCem/6Ј¬ФтКҜД«ҝЕБЈЦРГҝТ»Оўҫ§ІгЦРұЯФөМјФӯЧУКэОӘ

Ҫ«КҪ(4)ј°(8)ҙъИлКҪ(9)Іў»ҜјтөГ
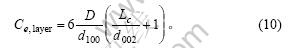
ёщҫЭКҪ(10)ј°КҪ(6)Ј¬КҜД«ҝЕБЈІаГжұЯФөМјФӯЧУКэОӘ

ёщҫЭКҪ(7)ј°КҪ(9)Ј¬ҝЕБЈЙППВ2ёцөЧГжЦРөДМјФӯЧУКэОӘ

ұҫОДЧчХЯИПОӘЈ¬ЙППВБҪөЧГжөДМјІгЦРЈ¬ёчОўҫ§ұЯФөөДМјФӯЧУТІКЗКҜД«ҝЕБЈЦРөДТ»ЦЦұЯФөМјФӯЧУЈ¬ёщҫЭКҪ(3)ј°КҪ(7)Ј¬УР

КҜД«ҝЕБЈЦРЙППВөЧГж2ёцМјІгЦРЦЬұЯЙПөДұЯФөМјФӯЧУјИ°ьАЁФЪКҪ(11)Ј¬УЦ°ьАЁФЪКҪ(12)әН(13)ЦРЈ¬УЙКҪ(3)ј°(8)ҝЙјЖЛгіцХвІҝ·ЦМјФӯЧУКэОӘ

ФтКҜД«ҝЕБЈЦРөДұЯФөМјФӯЧУКэОӘ
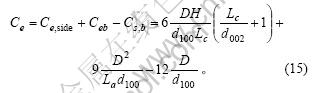
КҜД«ҝЕБЈЦРұнГжМјФӯЧУКэОӘ

ёщҫЭКҪ(2)Ўў(5)Ўў(6)әН(7)өГКҜД«ҝЕБЈЦРМјФӯЧУөДЧЬКэОӘ

¶ФУЪКҜД«ІДБПЈ¬D?LaЈ¬H?LcЈ¬La?d100Ј¬Lc?d002Ј¬№ККҪ(15)әН(16)ЦРөЪ3По(¶ФУҰУЪCs,b)УлЗ°2ПоПаұИҝЙТФәцВФЈ¬Хв2КҪј°КҪ(17)ҝЙ·Цұрјт»ҜОӘ

өЪ2По¶ФУҰУЪЙПЎўПВөЧГжОўҫ§ұЯҪзЙПөДұЯФөМјФӯЧУЎЈ

КҜД«ҝЕБЈЦРЧЬөДМјФӯЧУКэОӘЈә
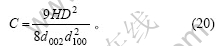
ФтұЯФөМјФӯЧУФЪКҜД«ҝЕБЈұнГжМјФӯЧУЦРөДұИАэОӘ

ұнГжМјФӯЧУФЪКҜД«ҝЕБЈЧЬөДМјФӯЧУЦРЛщХјөДұИАэОӘ

ТФЙПОӘАнПлКҜД«ЦРөДЗйРОЈ¬ФЪКөјКөДКҜД«ҝЕБЈЦРЈ¬Ри¶ФХвР©ұнҙпКҪҪшРРТ»Р©РЮХэЎЈ
3 КөјККҜД«ҝЕБЈЦРұЯФөМјФӯЧУј°ұнГжМјФӯЧУә¬БҝөДРЮХэ
ФЪАнПлКҜД«өДНЖөј№эіМЦРЈ¬Ҫ«КҜД«ҝЕБЈНвРОЧчОӘХэБщАвЦщҪшРРҙҰАнЎЈКВКөЙПЈ¬КҜД«ҝЕБЈөДөЧГжҝЙДЬОӘёчЦЦёчСщөД¶аұЯРОЎЈФЪХвАпЈ¬ПИјЩЙиКҜД«ҝЕБЈНвРООӘФІЦщМе»тХэЛДАвЦщЈ¬ЗТКҜД«ҝЕБЈөДМе»эәНёЯ(H)І»ұдЈ¬УЙҙЛұИҪПЖдРОЧҙұд»Ҝ¶ФұЯФөМјФӯЧУәНұнГжМјФӯЧУә¬БҝөДУ°ПмЎЈУЙУЪКҜД«ҝЕБЈөДМе»эј°ёЯ¶ИІ»ұдЈ¬ЖдөЧГж»эТаұЈіЦІ»ұдЈ¬ЙППВөЧГжөДұЯФөМјФӯЧУј°БҪөЧГжЦРөДМјФӯЧУКэГ»УРұд»ҜЈ¬ФтКҪ(18)Ј¬(19)Ј¬(21)әН(22)·ЦұрРЮХэОӘ

¶ФУЪЗ°ГжјЩЙиөДФІЦщМеәНХэЛДАвЦщРОЧҙөДКҜД«ҝЕБЈЈ¬ҰБ·ЦұрФјОӘ0.952әН1.075ЎЈҝЙТФИПОӘЈ¬КҜД«ҝЕБЈөДҪШГжФҪҪУҪьУЪФІРОЈ¬ҰБФҪРЎЈ¬ҪШГжРОЧҙұвЖҪЎўАвҪЗН»іц»тіКПЦБЛ°ј¶аұЯРОКұЈ¬ҰБҪПҙуЎЈ
УЙУЪКҜД«Оўҫ§ҙуРЎІ»Т»ЦВј°¶С»эіМ¶ИІ»ИзАнПлЧҙҝцПВДЗГҙҪфГЬЈ¬КҜД«ҝЕБЈЦР»бІъЙъРн¶аОўҝЧЈ¬ЖдЦРУР·вұХКҪөДЈ¬ТІУРТ»¶ЛҝӘҝЪөДЈ¬ЙхЦБҙжФЪНЁҝЧЎЈө«¶ФКҜД«»Ҝ¶ИҪПёЯөДМјІДБПАҙЛөЈ¬НЁҝЧөДҝЙДЬРФҪПРЎЎЈ¶ФУЪТ»¶ЛҝӘҝЪөДОўҝЧЈ¬Ц»ТӘҝЧҫ¶Чг№»ҙуЈ¬К№өГИЬјБ·ЦЧУј°ИЬјБ»ҜАлЧУДЬ№»ҪшИлЈ¬ЖдҝЧұЪөДМјФӯЧУЧчУГУлҝЕБЈНвұнГжөДМјФӯЧУТ»СщЎЈН¬КұЈ¬З°Гж¶ФКҜД«ҝЕБЈІаГжРОЧҙөДРЮХэ¶ФОўҝЧДЪұЪН¬СщУРР§Ј¬ФтКҪ(23)Ј¬(24)әН(20)ҝЙРЮХэОӘ

УЙУЪКҜД«ҝЕБЈЦРөДұЯФөМјФӯЧУCeУлұнГжМјФӯЧУCfТФПаН¬ұИАэ(S/S0)ФцјУЈ¬ТтҙЛЈ¬ұЯФөМјФӯЧУФЪұнГжМјФӯЧУөДұИАэPeІ»ұдЈ¬УлКҪ(25)ПаН¬Ј¬¶шұнГжМјФӯЧУФЪЧЬөДМјФӯЧУЦРөДұИАэPfФтұдОӘ

ФЪЗ°ГжөДНЖөјЦРЈ¬јЩЙиБЛЧйіЙКҜД«ҝЕБЈөДёчОўҫ§өД»щЖҪГжҫщЖҪРРУЪЙППВөЧГжЎЈ¶ФУЪКөјКөДКҜД«ҝЕБЈЈ¬УЙУЪКҜД«Оўҫ§Ц®јдөДО»ҙн»тИЎПтІ»Н¬Ј¬ЛщУРөДКҜД«Оўҫ§өД»щЖҪГжІў·ЗЖҪРРУЪН¬Т»ЖҪГжЎЈТтҙЛЈ¬ұҫОДЧчХЯМбіцТФПВөДјёөгјЩЙиЈәa. Т»ПөБР»щЖҪГжПа»ҘЖҪРРөДКҜД«Оўҫ§ЧйіЙТ»ёцКҜД«ОўФӘ(ОўРЎөҘФӘ)Ј¬КҜД«ҝЕБЈФтКЗУЙРн¶аИЎПтІ»Н¬өДКҜД«ОўФӘ№№іЙЈ¬ЖдЦРО»УЪКҜД«ұнГж(°ьАЁНвұнГжәНОўҝЧДЪұЪ)өДКҜД«ОўФӘУРNёцЈ»b. ТФХэБщАвЦщАҙұнХчКҜД«ОўФӘ(КөјКРОЧҙУлХэБщАвЦщЦ®јдөДІоұрҝЙТФНЁ№эРОЧҙТтЧУАҙРЮХэ)Ј¬NёцКҜД«ОўФӘөДөЧГжХэБщұЯРОөД¶ФҪЗПЯіӨј°АвЦщөДёЯ·ЦұрОӘDiәНHiЈ»c. КҜД«ОўФӘО»УЪКҜД«ұнГжөДІаГжГж»эХјёГКҜД«ОўФӘІаГж»эөДұИАэ·ЦКэОӘAiЈ¬О»УЪКҜД«ұнГжөДЙППВөЧГжГж»эХјёГКҜД«ОўФӘЙППВөЧГж»эөДұИАэ·ЦКэОӘBi(i=1Ј¬2Ј¬3Ј¬ЎӯЈ¬N)Ј¬ФтКҜД«ҝЕБЈЦРөДұЯФөМјФӯЧУј°ұнГжМјФӯЧУ·ЦұрОӘХвNёцКҜД«ОўФӘөД¶ФУҰЦөЦ®әНЎЈТтҙЛЈ¬КҪ(23)әН(24)ұдОӘ

ҝЕБЈЦРЧЬөДМјФӯЧУКэҝЙұнКҫОӘ

ёщҫЭLcәНLaөД¶ЁТеј°КҪ(4)Ј¬ФтУР

КҪЦРЈәLc?d002Ј¬ЙПКҪҝЙјт»ҜОӘ
 (37)
(37)
Ҫ«КҪ(31)~(37)УлКҪ(18)~(22)ҪшРРұИҪПҝЙЦӘЈ¬ФЪКөјКөДЗйРОЦРЈ¬DәНHөДОпАнТвТе·ЦұрОӘ¶ФУҰУЪҪфГЬ¶СЖцөДХэБщАвЦщКҜД«ҝЕБЈДЈРНЦРөДөЧГж¶ФҪЗПЯј°ёЯ¶ИөДУРР§ЦөЈ¬ЗТУР

ұЯФөМјФӯЧУј°ұнГжМјФӯЧУә¬БҝөДұнҙпКҪЧоіхКЗУЙАнПлКҜД«өДХэБщАвЦщОўҫ§ДЈРНј°ҪфГЬ¶С»эРОіЙХэБщАвЦщөДКҜД«ҝЕБЈДЈРННЖөјіцАҙөДЈ¬ө«КЗІ»ДС·ўПЦЈ¬ҫӯ№эТ»ПөБРРЮХэәуЈ¬ёГұнҙпКҪН¬СщККУГУЪКҜД«»ҜіМ¶ИҪПөНөДМјІДБПТФј°ОЮ¶ЁРОМјІДБПЦРМјФӯЧУә¬БҝөДјЖЛгЈ¬Ц»КЗёчұнҙпКҪЦРРЮХэПөКэөДИЎЦөІ»Н¬ЎЈ
4ЎЎҪбЎЎВЫ
a. КҜД«Оўҫ§ЦРұЯФөМјФӯЧУТЧУлЖдЛыФӯЧУ»т»щНЕРОіЙҪПОӘОИ№МөДБӘҪУЈ¬өз»ҜС§·ҙУҰ»оРФҪПёЯЎЈ
b. ҪЁБўБЛАнПлКҜД«өДХэБщАвЦщОўҫ§ДЈРНј°ҪфГЬ¶СЖцөДХэБщАвЦщҝЕБЈДЈРНЈ¬НЖөјіцАнПлКҜД«ЦРұЯФөМјФӯЧУј°ұнГжМјФӯЧУә¬БҝөДјЖЛ㹫КҪЎЈ
c. ·ЦОцБЛКөјККҜД«ҝЕБЈУлАнПлКҜД«Ц®јдҪб№№өДІоұ𣬶ԼЖЛ㹫КҪҪшРРБЛТ»ПөБРөДРЮХэЈ¬ІўҪ«ЖдНЖ№гөҪЖдЛыМјІДБПМјФӯЧУә¬БҝөДјЖЛгЎЈ
ІОҝјОДПЧЈә
[1] Katsunori Y, Atsushi Y, Yoshinori K, et al. Carbon hybrids graphite-hard carbon and graphite-coke as negative electrode materials for lithium secondary batteries charge/discharge characteristics[J]. J Electrochem Soc, 2002, A149(7): A804-807.
[2] Guo Hua-jun, Li Xin-hai, Wang Zhi-xing, et al. Effect of lithium or aluminum substitution on the characteristics[J]. Rare Metals, 2003, 22(4): 280-284.
[3] Hongyu W, Masaki Y, Takeshi A, et al. Characterization of carbon-coated natural graphite as a lithium ion battery anode material[J]. J Electrochem Soc, 2002, A149(4): 499-503.
[4] Wu Y P, Rahm E, Holze R. Carbon anode materials for lithium ion batteries[J]. Journal of Power Sources, 2003, 114: 228-236.
[5] Guo Hua-jun, Li Xin-hai, Wang Zhi-xing, et al. Si-doped composite carbon as anode of lithium ion batteries[J]. Transactions of Nonferrous Metals Society of China, 2003, 13(5): 1062-1065.
[6] Michael E S, Henri W, Felix J, et al. Purely hexagonal graphite and the influence of surface modifications on its electrochemical lithium insertion properties[J]. J Electrochem Soc, 2002, A149(8): 960-966.
[7] Jung Y, Suh M C, Shim S C, et al. Lithium insertion into disordered carbons prepared from organic polymers[J]. J Electrochem Soc, 1998, A145(9): 3123-3129.
[8] Wang S, Yata S, Nagano J, et al. A new carbonaceous material with large capacity and high efficiency for rechargeable Li-ion batteries[J]. J Electrochem Soc, 2000, A147(7): 2498-2502.
[9] Shin R M, Takahiro H, Michiya T, et al. Reduction of irreversible capacities of amorphous carbon materials for lithium ion battery anodes by Li2CO3 addition[J]. Carbon, 2004, 42: 837-842
[10] GUO Hua-jun, LI Xin-hai, WANG Zhi-xing, et al. Mild oxidation treatment of graphite anode for Li-ion batteries[J]. J Cent South Univ Technol, 2005, 12(1): 50-54.
[11] Inagaki M. Textures in carbon materials[J]. New Carbon, 1999, 14(2): 1-13.
[12] АоКҘ»Ә. МјәНКҜД«ЦЖЖ·(ЙП)[M]. ұұҫ©: ТұҪр№ӨТөіц°жЙз, 1983.
LI Sheng-hua. Products of Carbon and Graphite (I)[M]. Beijing: Press of Metallurgical Industry, 1983.
[13] АоКҝПН, ТҰ ҪЁ, БЦ¶ЁәЖ. КҜД«[M]. ұұҫ©: »ҜС§№ӨТөіц°жЙз, 1991
LI Shi-xian, YAO Jian, LIN Ding-hao. Graphite[M]. Beijing: Press of Chemical Industry, 1991
[14] Chung G C; Jun S H; Lee K Y, et al. Effect of surface structure on the irreversible capacity of various graphitic carbon electrodes[J]. J Electrochem Soc, 1999, A146(5): 1664-1671.
[15] Zaghib K, Nadeau G, Kinoshita K. Effect of graphite particle size on irreversible capacity loss[J]. J Electrochem Soc, 2000, A147(6): 2110-2115.
КХёеИХЖЪЈә2006-06-12
»щҪрПоДҝЈә№ъјТЧФИ»ҝЖС§»щҪрЧКЦъПоДҝ(50302016); ЦР№ъІ©Кҝәу»щҪрЧКЦъПоДҝ(2005037698)
ЧчХЯјтҪйЈәХЕ ұҰ(1971-)Ј¬ДРЈ¬ҪӯЛХнмнфИЛЈ¬І©КҝәуЈ¬ҙУКВІДБПј°өз»ҜС§СРҫҝ
НЁС¶ЧчХЯЈәХЕ ұҰЈ¬ДРЈ¬І©КҝәуЈ»өз»°Јә0731-8836357Ј»E-mail: zhangb@qianlong.com