���¹��෴Ӧ/ˮ�ȷ��ϳ�LiMn0.4Fe0.6PO4/C���ϵ��۽ṹ����绯ѧ����
���1, 2���1��������3���ܺ���1, 2��Ҧ���1������2��������1
(1. ���ϴ�ѧ ���Ͽ�ѧ�빤��ѧԺ������ ��ɳ��410083��
2. ����ʡ��Դ���ܲ����������о��������� ��ɳ��410083��
3. ��ұ��«����ɫ������������˾������ ��«����125003)
ժҪ����Li2CO3��MnCO3��FeC2O4��2H2O��NH4H2PO4Ϊԭ�ϣ����õ��¹��෴Ӧ/ˮ�ȷ��Ʊ�LiMn0.4Fe0.6PO4/C���ϡ�����XRD��SEM��TEM��LiMn0.4Fe0.6PO4/C�ľ���ṹ����ò�Լ�����������ò���б����������ú�����ŵ�ʵ�����绯ѧ���ܽ������ۡ��о������������400 �洦��4 h��ɻ�þ���ṹ��LiMPO4(MΪFe��Mn)����ͳ���෨�͵��¹��෴Ӧ/ˮ�ȷ��ϳɵ�LiMn0.4Fe0.6PO4���Ͼ�Ϊ��һ�����ʯ�ṹ������������ε�̼���ɵ��¹��෴Ӧ/ˮ�ȷ��ϳɵIJ��Ͽ�������Ϊ100 nm���ң��绯ѧ������������0.1C(CΪ��ŵ��������)�µ��״ηŵ�����Ϊ157 mA��h/g���Ǵ�ͳ���෨�ϳɲ�Ʒ��1.07����0.5C��ѭ��50������������133 mA��h/g���ң��Ǵ�ͳ���෨�ϳɲ�Ʒ��1.21����
�ؼ��ʣ�LiMn0.4Fe0.6PO4�����෴Ӧ��ˮ�Ⱥϳɣ��绯ѧ����
��ͼ����ţ�TM912 ���ױ�־�룺A ���±�ţ�1672-7207(2013)09-3612-07
Microstructure and electrochemical characteristics of LiMn0.4Fe0.6PO4/C composites by low temperature solid-state reaction/hydrothermal synthesis
LI Jian1, 2, YANG Jun1, LI Liangdong3, ZHOU Hongming1, 2, YAO Shuheng1, YANG Liang2, FANG Zhenqi1
(1. School of Materials Science and Engineering, Central South University, Changsha 410083, China;
2. Hunan Zhengyuan Institute for Energy Storage Materials and Devices, Changsha 410083, China;
3. China Metallurgical Group Corporation, Huludao 125003, China)
Abstract: The olivine type LiMn0.4Fe0.6PO4 was synthesized via the low temperature solid-state reaction combined with hydrothermal synthesis from Li2CO3, FeC2O4��2H2O, MnCO3 and NH4H2PO4. The product from the low temperature solid-state reaction was studied. The structure, particle size and surface morphology of these cathode active materials were investigated by XRD, SEM and TEM. Electrochemical characteristics of the composites were evaluated using galvanostatic charge/discharge tests. The results show that olivine LiMPO4 (M=Fe,Mn) is obtained after the raw materials are fired at 400 ��for 4 h. All Li(Mn0.4Fe0.6)PO4 samples are simple pure olive-type phase with a conductive, thin web of carbon surrounding them. The composite synthesized via the low temperature solid-state reaction/hydrothermal synthesis has homogeneous particles of size 100 nm, an initial discharge capacity of 157 mA��h/g at 0.1C and a specific capacity of about 133 mA��h/g after 50 times cycling at 0.5 C rate. They are 1.07 times and 1.21 times of the products from the traditional solid-state, respectively.
Key words: LiMn0.4Fe0.6PO4; solid-state reaction; hydrothermal synthesis; electrochemical properties
�����������ǶԸɾ����ʵľ�ס�����Ϳɳ���ʹ�õ���Դ������ٽ����������Ƶ���������ϵͳ����ӵ�صķ�չ���Է�չ�ɱ��͡���ȫ�ȶ��������ܶȸߡ������ܶȸߵ�﮵���������������ͳLiCoO2��LiNiO2��LiMn2O4��Ϊ����﮵�������ȵ�[1]��Padhi��[2-3]��1997���LiFePO4�����˱����������˹��ʵ绯ѧ������ʯ�ṹLiFePO4�Ĺ�ע��LiFePO4���Ͼ��а�ȫ�ȶ�������������(170 mA��h/g)����ŵ��������仯С��ѭ�����ܺõ��ŵ㣬���ǣ������е��ӵ絼��̫�͡��������ɢϵ��С��Ӱ��缫���ϵ绯ѧ���ܵ�����ȱ��[4-5]����LiFePO4���Ͻ��е�����ϰ������������������Ʊ����ײ��ϣ��������ӵ絼�ʣ���������ӵ���ɢ�̣�ΪLiFePO4��ҵ���춨�˻�����LiMnPO4ͬ���������ʯ�ṹ�����������ܶ�Ϊ701 W��h/kg����LiFePO4��586 W��h/kg ���ߣ���λ�����е��Һ��ϵ���ȶ��绯ѧ���������ܻ�õ���������ܶ�[3]�����ǣ�LiMnPO4�ĵ��ӵ�����(��1.0��10-10 S/cm)��LiFePO4(1.8��10-9 S/cm)���ͣ�ʹ����ѻ������ĵ绯ѧ����[6]�����⣬LiMnPO4�ڳ�ŵ�����У�����Mn3+��Jahn-TellerЧӦ��LiMnPO4��MnPO4�ת��������仯�������ı���Ӧ��������Ӱ�������ŵ�����[7]����ĿǰΪֹ�������л�ÿ�����������120 mA��h/g ��LiMnPO4����[1, 7-10]����Fe��Mn����魽ṹ��4cλ�ù���ʱ�����Ի�ýϸߵĿ����������뵥һ��LiFePO4������ȣ���ص������ܶ�Ҳ���õ����[3, 11-21]����ˣ���������Li(MnyFe1-y)PO4���о��ѳ�Ϊ�о��ȵ�֮һ��Ŀǰ���㷺�����Ʊ�Li(MnyFe1-y)PO4/C�ķ����й��෨[3, 11-14]���ܽ�-������[19-21]�ȡ�Ȼ�������ô�ͳ�����Ʊ���LiMnyFe1-yPO4��Ʒ��Mn��Fe�����ʵ����ȴ���1:2ʱ����������١�Shin��[15-18]���ù��෨�Ʊ���LiMn0.4Fe0.6PO4/C��0.1C(CΪ��ŵ籶��)�µķŵ�������Ϊ145 mA��h/g���ң�Mi��[14]���ù��෨�Ʊ���LiMn0.6Fe0.4PO4/C��0.1C�µķŵ�����Ϊ143 mA��h/g����ͳ���෨�¶ȳ�����һ�����������Li(MnyFe1-y)PO4��������ƫ���ҷֲ������ȣ�Ӱ����Mn3+/Mn2+�����������ߣ�ʹ���ò��ϵ�����ƫ�͡��ڵ����������ܹ����Ϳ��������ȣ������ϵĽᾧ�Ȳ��ߣ��Ҵ������Ե����ʳɷ֣�Ӱ����ϵ�ѭ�����ܡ�Ȼ�����Ե������մ�����IJ��Ͻ���ˮ�ȴ������ܹ�ʵ�ֵ�����߲��ϵĽᾧ�ȣ�ͬʱ����һ�ȶ��ĸ�ѹ���»��������ڿ����ij��������ڵõ���������ϸС��Li(MnyFe1-y)PO4����Ŀǰ��û���ⷽ������ױ�������������ѡ��y=0.4�����õ��¹��෴Ӧ/ˮ�ȷ��Ʊ��߽ᾧ�ȵ� LiMn0.4Fe0.6PO4/C�����봫ͳ���෨�Ʊ��IJ����ڽṹ����ò�͵绯ѧ���ܵȷ�����бȽϡ�
1 ʵ�鲿��
1.1 ���ϵ��Ʊ�
��Li2CO3��MnCO3��FeC2O4��2H2O��NH4H2PO4��Li��Mn��Fe��P�����ʵ�����Ϊ1:0.4:0.6:1���ϣ�ͬʱ�����������Ϊ18%������(���LiMn0.4Fe0.6PO4���������)������ˮ�Ҵ�Ϊ���ʾ�������ĥ���Ϻ�ֳ�2�ݣ�һ���������������400 ������4 h������700 ������18 h����ȴ��õ�LiMn0.4Fe0.6PO4/C���ϣ���ΪLMFP1����һ���������������400 ������4 hʹ֮�ֽ⣬��ȴ�õ��м��������ĥ����180 �滷����ˮ�ȴ���24 h��Ȼ����700 ����ArΪ������������3 h���õ�LiMn0.4Fe0.6PO4/C���ϣ���ΪLMFP2��
1.2 ���ϱ���
����METTLER TOLEDO TGA/SDTA851e���ȷ����ǶԻ��ԭ�Ͻ������ط����������¶ȷ�ΧΪ50~850 �棬��������Ϊ10 ��/min����������Ϊ�����
����Dmax-2500VB X��������(XRD)�Բ��Ͻ��о��ͽṹ������������ѹΪ40 kV����������Ϊ250 mA��ɨ�跶ΧΪ10��~80�㣬ɨ���ٶ�Ϊ8 (��)/min��
����Sirion 200�ͳ�����ɨ�������������Ʒ�Ŀ�����ò���й۲죬����HEM-2100F/UHR�߷ֱ��������������Ʒ�Ŀ������۽ṹ���й۲졣
1.3 �绯ѧ���ܲ���
�����Ʊ��Ļ������ʰ�������m(LiMn0.4Fe0.6PO4): m(��Ȳ��):m(PVDF)=8:1:1���ϡ��������ĥ��Ϻ���N-��������ͪ(NMP)Ϊ�ܼ���������Ⱥ�Ϳ�������ϣ�����ո������к�ɣ�ѹƬ�Ƶ�����Ƭ���Խ����ƬΪ���缫Ƭ��1 mol/L LiPF6̼����ϩ��(EC)-̼�������(DMC)(�����1:1)Ϊ���Һ���۱�ϩ��Ĥ(Celgard2400)Ϊ��Ĥ����װ��R2032��ť�۵�ء�����������˾������CT-2008W�͵�����ܲ����ǶԵ�صij�ŵ����ܽ��в��ԣ������¶�Ϊ���£���ѹ��ΧΪ2.5~4.5 V����������Ϊ0.1C��0.5C�������Ϻ�������˾������CHI-660A�绯ѧ����վ�Ե�ؽ���ѭ���������ߵIJ��ԣ���ѹ��ΧΪ2.5~4.5 V��ɨ���ٶ�Ϊ0.1 mV/s��
2 ���������
ͼ1��ʾΪ���ԭ�ϵ�TG/DTA���ߣ�ͼ2��ʾΪԭ����400 ������4 h���XRD��ͼ����ͼ1��֪���ϳ�LiMn0.4Fe0.6PO4��50~425 ��������ʧ�����47.5%����425 ���Ժ����������ʧ����������180 ���230 �洦����2�����ȷ壬�ֱ���NH4H2PO4�ķֽ��FeC2O4��2H2Oʧȥ�ᾧˮ�й�[22]����425 ��������û�����������ȷ壬����Ӧ���������һ�����٣������Li2CO3��MnCO3��FeC2O4�����˷ֽⷴӦ������NH4H2PO4�ķֽ������˸��Ϸ�Ӧ����230~425 ����447 �洦����2�����Եķ��ȷ塣
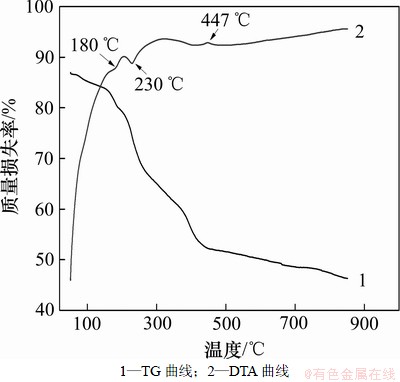
ͼ1 �Ʊ�LiMn0.4Fe0.6PO4���ϵ�ǰ�������������/�Ȳ�( TG/DTA)����
Fig.1 TG and DTA curves of precursors composed of Li2CO3, FeC2O4��2H2O, MnCO3 and NH4H2PO4
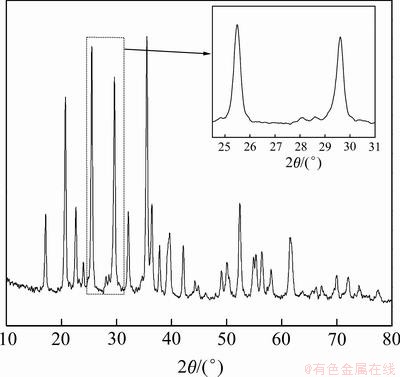
ͼ2 ��400 ������4 h������Ʒ��XRDͼ��
Fig.2 XRD pattern of sample fired at 400 �� for 4 h
��ˣ��ںϳ�LiMn0.4Fe0.6PO4�Ĺ����У���Ӧ��ķֽ��Լ�����Ӧ��֮�䷢���Ļ�ѧ��Ӧ��Ҫ������425 ��ǰ����230~425 ���������ʯ�ṹLiMPO4�������ɣ���425 ���Ժ���ϵ�ڷ����ķ�Ӧ��Ҫ�����ʯ�ṹLiMPO4����ṹ���γɺ;��������йء����⣬��ͼ2��֪��ԭ����400 �����յõ������ʯ�ṹ��LiMPO4������27�㣼2�ȣ�29�㴦����2��С�����ʷ壬���������ΪLi4(P2O7)��Mn2P2O7������һ��������֤������/�Ȳ��������Լ��Է�Ӧ���̵����ۡ�
ͼ3��ʾΪ��ƷLMFP1��LMFP2��XRD��ͼ����ͼ3�ɼ���2��������ͼ�еķ�λ����LiFePO4 (Pnma)�ı���һһ��Ӧ����û�з������Ե����ʷ壬˵��LiMn0.6Fe0.4PO4��Fe��Mn��ͬռ���ھ���ṹ��4cλ�á�ͨ����XRDͼ���м���õ�LiMn0.6Fe0.4PO4�ľ�������Ϊ��a=6.047 7��10-10 m��b=10.384 0��10-10 m��c=4.715 0��10-10 m������[2]����LiFePO4�ľ�������Ϊ��a=6.008 0��10-10 m��b=10.324 0��10-10 m��c=4.694 0��10-10 m����˵����LiFePO4�в���Mnʹ����ľ�������a��b��c����ͼ����û�з���̼�������λ����Ҫ������̼�ĺ����ͣ��������νṹ�����ø��¹��෨�����¹��෴Ӧ/ˮ�ȷ����ܵõ�����LiMn0.6Fe0.4PO4��
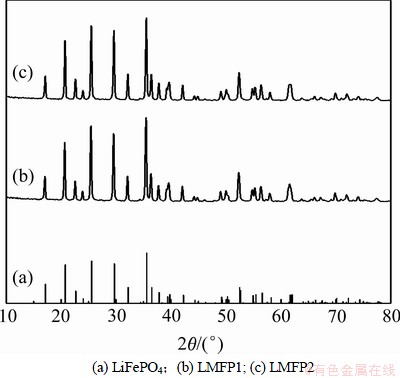
ͼ3 ��ƷLMFP1��LMFP2��XRD��ͼ�Լ�LiFePO4�ı���ͼ
Fig.3 Standard pattern of LiFePO4 and XRD pattern of LMFP1 and LMFP2
ͼ4��ʾΪLMFP1��LMFP2��Ʒ��SEM��TEMͼ�����У�ͼ4(a)��4(b)��ʾ�ֱ�ΪLMFP1��LMFP2��SEMͼ��ͼ4(c)��4(d)��ʾ�ֱ�ΪLMFP1��LMFP2��TEMͼ��ͼ4(e)��4(f)��ʾ�ֱ�Ϊͼ4(e)��4(f)���������HR-TEMͼ��
��ͼ4(a)��4(b)���Կ�����LMFP1�������Ȳ�һ����100~500 nm֮�䣬���ҿ�����ò���������봫ͳ�����Ʊ���LMFP1��ȣ����õ��¹��෴Ӧ��ˮ�ȷ������Ʊ���LMFP2����ϸС��Ϊ100 nm���ң���ò�������ڵ��¹��෴Ӧ�����У�ԭ�Ϸ����ֽ⣬���Ӧ�γ������ʯ�ṹ��LiMPO4���ˣ�Ϊ����LiMPO4�����Ŀ����γɴ�������������ˮ�ȷ�Ӧ�����У���Ӧ����Χ��һ��ѹ���µĻ�����ֹ�˿����������γɾ�һϸС��������Ҫ��������ͼ4(c)��4(d)�ɼ���LMFP1��LMFP2�����������ϴ���һ�����ʡ����νṹ��̼(��ͼ�еĺ�ɫ��ͷ��ʾ)����Ҳ���ڱ���⻬�ֵط��⻬�Ŀ�������ͼ4(e)��4(f)���Կ���������⻬�Ŀ�����Χ���ܰ���һ��̼��̼������ĺ��Ϊ7 nm���ң�̼������Ϳ��������ε�̼��֤��LiMn0.4Fe0.6PO4���ϵĵ��ӵ���������

ͼ4 LMFP1��LMFP2��Ʒ��SEM��TEMͼ
Fig.4 SEM��TEM images of samples of LMFP1and LMFP2
Ϊ�˿���LMFP1��LMFP2��������(25 ��)�ĺ������ŵ����ܣ������ϳɵ�LiMn0.4Fe0.6PO4��Ϊ��������������װ�ɶ��缫ʵ���أ���0.1C�ĵ������г䡢�ŵ�õ����״γ�ŵ�������ͼ5��ʾ����ͼ5�ɼ���LMFP1��LMFP2���״ηŵ������ֱ�Ϊ146 mA��h/g��157 mA��h/g��2����Ʒ�ij�����߾�����2����λƽ̨���ֱ���3.5 V��4.0 V������ͬ����2����Ʒ�ķŵ�������3.4 V��3.9 V��������2����λƽ̨�����ʱ��LMFP1��2����λƽ̨����LMFP2�ĸߣ����ŵ�ʱȴ�෴����˵��LMFP1�ڳ�ŵ�����е缫������LMFP2�����أ�LMFP1�ĸߵ�λ�ŵ�ƽ̨�̣��½��ٶȿ죬˵���ŵ����Mn3+/Mn2+������ܲ���������û�еõ�����ͷš�
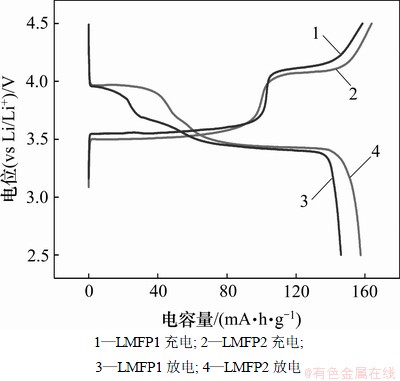
ͼ5 �����£�LMFP1��LMFP2��Ʒ��0.1C�����µ��״γ�ŵ�����
Fig.5 Charge-discharge curves of lithium cells with LMFP1 and LMFP2 as cathode material at 0.1C rate at 25 ��
ͼ6��ʾΪLMFP1��LMFP2��Ʒ��0.1 mV/s��ɨ�������µ�ѭ����������ͼ����ͼ6�ɼ���LMFP1��LMFP2��������2��������ԭ�壬��3.5 V�����ķ���������Ƕ�ѹ�����Fe3+/Fe2+��Եķ�Ӧ��4.0 V�����ķ���������Ƕ�ѹ�����Mn3+/Mn2+��Եķ�Ӧ���������ŵ�ʱFe3+/Fe2+��Mn3+/Mn2+��Եij�ŵ�ƽ̨���Ӧ��LMFP1��LMFP2��Fe��ϼ����ҷ�������������뻹ԭ���ĵ�λ��ֱ�Ϊ0.63 V��0.43 V����Mn������Ӧ�ķ������С���������뻹ԭ���ĵ�λ��ֱ�Ϊ0.33 V��0.30 V�����⣬LMFP2��Fe������������뻹ԭ������Լ�Mn������������뻹ԭ���������LMFP1��Fe��������ԭ�����������ȣ�Mn��������������Դ��ڻ�ԭ���������˵��LMFP2��Fe3+/Fe2+��Mn3+/Mn2+��Ӧ�Ŀ����Ա�LMFP1�еĿ����Ժã�LMFP1��Fe3+/Fe2+��Է�Ӧ�Ŀ����Ա�Mn3+/Mn2+�Ŀ����Ժá�Yamada��[13]���Ʊ���LixMnyFe1-yPO4 (0��x��1��0��y��1)��ͼ��ʾ��LiMn0.4Fe0.6PO4����Ƕ﮵Ĺ����У�Fe3+/Fe2+���֮���ת�����ڵ���ת�䣬Mn3+/Mn2+���֮���ת����������ת�䣻����ת�䷴Ӧ�����Ժã�����ת��ή�ͷ�Ӧ�Ŀ����ԣ��Ӷ�Ӱ���˵缫���ϵĵ绯ѧ����[23]������������ʯ�ṹLiMPO4����ɢϵ��С�����������ز��ϵ绯ѧ���ܳ�ַ��ӵ���Ҫ���ء����ô�ͳ���෨�Ʊ���LMFP1����һ�ο����ϴ֣��ڵ�س�ŵ�����и����ײ���������ʹ���ϵ绯ѧ��Ӧ�Ŀ����Խ�һ�����ͣ���ˣ�LMFP2�ij�ŵ�Ч�ʱ�LMFP1�ĸߣ�LMFP1��LMFP2��Fe3+/Fe2+������Ӧ�ij�ŵ�Ч�ʱ�Mn3+/Mn2+�ĸߣ�������LMFP1�����ֵø�������(��ͼ5��ʾ)��

ͼ6 LMFP1��LMFP2��Ʒ��0.1 mV/s�µ�ѭ����������
Fig.6 Normalized cyclic voltammagram of lithium cells LMFP1 and LMFP2 as cathode material at 0.1 mV/s
Ϊ�˿��������������µij�ŵ�ѭ���������ܣ���ʵ������0.5C�½���50�γ�ŵ�ѭ�����ԣ�ͼ7��ʾΪLMFP1��LMFP2ѭ�����ܱȽ�ͼ����ͼ7���Կ�����LMFP1��LMFP2��0.5C�µ��״ηŵ������ֱ�Ϊ127��143 mA��h/g����2����������������ѭ���������в�����������˥�����٣�LMFP1ѭ��50�κ�����������110 mA��h/g ���ң�˥����13.4%��LMFP2ѭ��50�κ�����������133 mA��h/g���ң���˥����7%����˵��LMFP2�ĸ߱���ѭ�����ܱ�LMFP1�ĺá�LMFP2���������ĵ绯ѧ���ܣ�����Ϊ���ȡ�ϸС�ľ�������������ӵ���ɢ·�̣����㵼��̼��İ�������˲��ϵĵ��ӵ���������
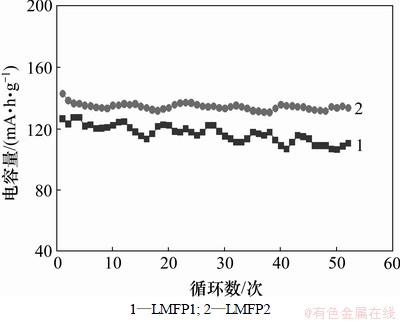
ͼ7 �����£�LMFP1��LMFP2��Ʒ����0.5C�����µķŵ�������ѭ�������Ĺ�ϵ����
Fig.7 Cycle performance of lithium cells with LMFP1 and LMFP2 as cathode materials at 0.5C rate at 25 ��
3 ����
(1) ��Li2CO3��MnCO3��FeC2O4��2H2O��NH4H2PO4Ϊԭ�ϣ����ô�ͳ�ĸ��¹��෨�͵��¹��෴Ӧ��ˮ�ȷ�Ӧ���ϵķ����Ʊ��˸߽ᾧ���ܵ�LiMn0.4Fe0.6PO4/C���ϣ�����LiMn0.4Fe0.6PO4����PnmaȺ��
(2) �ϳ�LiMn0.4Fe0.6PO4�Ĺ����з�Ӧ��ķֽ��Լ�����Ӧ��֮�䷢���Ļ�ѧ��Ӧ��Ҫ������425 ��ǰ����400 �洦��4 h�����о���ṹ��LiMPO4���ɣ�������������Li4(P2O7)��Mn2P2O7��
(3) ����ͳ���෨�õ��IJ�Ʒ��������ò�����������ȷֲ������ȣ�Ϊ100~500 nm��̼����Ч���ã�0.1C�������ŵ���״ηŵ�����Ϊ146 mA��h/g, 0.5C�������ŵ��״ηŵ�����Ϊ127 mA��h/g��ѭ��50�κ�������������110 mA��h/g ���ң�˥����13.4%�����¹��෴Ӧ��ˮ�ȷ�Ӧ���ϵķ����ϳɵIJ��Ͽ�����ò�����������ֲַ����ȣ���������Ϊ100 nm���ң�̼����Ч���ã��绯ѧ����������0.1C�½��г�ŵ�ʵ���״ηŵ�����Ϊ157 mA��h/g��0.5C�µ��״ηŵ�����Ϊ143 mA��h/g��ѭ��50������������133 mA��h/g ���ң���˥����7%��
�ο����ף�
[1] Yonemura M, Yamada A, Takei Y. Comparative kinetic study of olivine LixMPO4 (M=Fe, Mn)[J]. Journal of the Electrochemical Society, 2004, 151(9): A1352-A1356.
[2] Padhi A, Najundaswamy K, Goodenough J. Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J]. Journal of the Electrochemical Society, 1997, 144: 1188-1194.
[3] Yamada A, Kudo Y, Liu K Y. Reaction mechanism of the olivine-type LixMn0.6Fe0.4PO4(0��x��1)[J]. Journal of the Electrochemical Society, 2001, 148(7): A747-A754.
[4] Wang Y, Wang Y, Hosono E. The design of a LiFePO4/carbon nano-composite with a core-shell structure and its synthesis by an in situ polymerization restriction method[J]. Angewandte Chemie International Edition, 2008, 47(39): 7461-7465.
[5] Choi D, Kumta P N. Surfactant based sol-gel approach to nanostructured LiFePO4 for high rate Li-ion batteries[J]. Journal of Power Sources, 2007, 163(2): 1064-1069.
[6] Delacourt C, Laffont L, Bouchet R. Toward understanding of electrical limitations (electronic, ionic) in LiMPO4 (M=Fe, Mn) electrode materials[J]. Journal of Electrochemical Society, 2005, 152(5): A913-A921.
[7] Drezen T, Kwon N, Bowen P. Effect of particle size on LiMnPO4 cathodes[J]. Journal of Power Sources, 2007, 174(2): 949-953.
[8] Daiwon C, Donghai W, Bae I T. LiMnPO4 nanoplate grown via solid-state reaction in molten hydrocarbon for Li-ion battery cathode[J]. Nano Letters, 2010, 10(8): 2799-2805.
[9] Wang D, Buqa H, Michael Crouzet M. High-performance, nano-structured LiMnPO4 synthesized via a polyol method[J]. Journal of Power Sources, 2009, 189(1): 624-628.
[10] Drezen T, Kwon N H, Bowen P. Effect of particle size on LiMnPO4 cathodes[J]. Journal of Power Sources, 2007, 174(2): 949-953.
[11] ������, Ī����, ����. ����ӵ����������LiFe1-2xMnxMgxPO4/C�ĵ绯ѧ�����о�[J]. ���ܲ���, 2010, 41(2): 208-210.
KANG Cairong, MO Xiangyin, DING Yi. Electrochemical properties of LiFe1-2xMnxMgxPO4/C cathode material as lithium ion batteries[J]. Journal of Functional Materials, 2010, 41(2): 208-210.
[12] л��, ������. ����ӵ����������LiMnyFe1-yPO4���Ʊ��������о�[J]. ������ѧ��, 2006, 21(3): 591-598.
XIE Hui, ZHOU Zhentao. Synthesis and performances of LiMnyFe1-xPO4 as cathode materials for lithium-ion batteries[J]. Journal of Inorganic Materials, 2006, 21(3): 591-598.
[13] Yamada A, Kudo Y, Liu K Y. Phase diagram of Lix(MnyFe1-y)PO4(0��x, y��1)[J]. Journal of the Electrochemical Society, 2001, 148(10): 1153-1158.
[14] Mi C H, Zhang X G, Zhao X B, et al. Synthesis and performance of LiMn0.6Fe0.4PO4/nano-carbonwebs composite cathode[J]. Materials Science and Engineering B, 2006, 129(1/2/3): 8-13.
[15] Shin Y J, Kim J K, Cheruvally G. Li(Mn0.4Fe0.6)PO4 cathode active material: Synthesis and electrochemical performance evaluation[J]. Journal of Physics and Chemistry of Solids, 2008, 69(5/6): 1253-1256.
[16] Kope M, Yamada A, Kobayashi G. Structural and magnetic properties of Lix(MnyFe1-y)PO4 electrode materials for Li-ion batteries[J]. Journal of Power Sources, 2009, 189(2): 1154-1163.
[17] Lee K T, Lee K S. Electrochemical properties of LiFe0.9Mn0.1PO4/Fe2P cathode material by mechanical alloying[J]. Journal of Power Sources, 2009, 189(1): 435-439.
[18] Baek D H, Kim J K, Shin Y J. Effect of firing temperature on the electrochemical performance of LiMn0.4Fe0.6PO4/C materials prepared by mechanical activation[J]. Journal of Power Sources, 2009, 189(1): 59-65.
[19] Dominko R, Bele M, Gaberscek M. Porous olivine composites synthesized by sol�Cgel technique[J]. Journal of Power Sources, 2006, 153(2): 274-280.
[20] Nam K W, Yoon W S, Zaghib K. The phase transition behaviors of Li1 -xMn0.5Fe0.5PO4 during lithium extraction studied by in situ X-ray absorption and diffraction techniques[J]. Electrochemistry Communications, 2009, 11(10): 2023-2026.
[21] Yao J, Bewlay S, Konstantionv K. Characterization of olivine-type LiMnxFe1-xPO4 cathode materials[J]. Journal of Alloys and Compounds, 2006, 425(1/2): 362-366.
[22] Wang D, Li H, Wang Z, et al. New solid-state synthesis routine and mechanism for LiFePO4 using LiF as lithium precursor[J]. Journal of Solid State Chemistry, 2004, 177(12): 4582-4587.
[23] Hashambhoy A M, Whitacre J F. Li Diffusivity and phase change in LiFe0.5Mn0.5PO4: A comparative study using galvanostatic intermittent titrationand cyclic voltammetry[J]. Journal of the Electrochemical Society, 2011, 158(4): A390-A395.
(�༭ �²ӻ�)
�ո����ڣ�2012-09-25�������ڣ�2012-12-05
������Ŀ�����ҿƼ�֧�żƻ���Ŀ(2009BAE71B04)������ʡ�Ƽ��ƻ���Ŀ(2010FJ4061)����ɳ�пƼ��ƻ���Ŀ(K1201039-11)
ͨ�����ߣ����(1969-)���У������۶��ˣ���ʿ�������ڣ���������Դ�����о����绰��0731-88877173��E-mail: ziliao2000@126.com