文章编号:1004-0609(2012)05-1488-09
低品位氧化铜矿氨-硫酸铵体系过硫酸铵氧化浸出
刘志雄1, 2,尹周澜1,胡慧萍1,陈启元1
(1. 中南大学 化学化工学院,长沙 410083;2. 吉首大学 化学化工学院,吉首 416000)
摘 要:以过硫酸铵为氧化剂,研究低品位氧化铜矿在氨-硫酸铵体系氧化浸出工艺。讨论氨/铵离子摩尔比、总氨浓度,氨、硫酸铵和过硫酸铵的浓度,反应温度,液固比,反应时间和搅拌速度等操作条件对铜浸出的影响。结果表明:在92.8%的矿样粒径小于0.045 mm,氨、硫酸铵和过硫酸铵浓度分别为2.4、1.8和0.100 mol/L,浸出时间为90 min,温度为30 ℃,液固比(mL/g)为5:1,搅拌速度为500 r/min时的优化条件下,低品位铜矿的铜浸出率达87.7%。
关键词:低品位氧化铜矿;氧化浸出;氨-硫酸铵;过硫酸铵
中图分类号:TF803.21 文献标志码:A
Oxidative leaching of low-grade copper ore in ammonia-ammonium sulfate solution with ammonium persulfate
LIU Zhi-xiong1, 2, YIN Zhou-lan1, HU Hui-ping1, CHEN Qi-yuan1
(1. School of Chemistry and Chemical Engineering, Central South University, Changsha 410083, China;
2. College of Chemistry and Chemical Engineering, Jishou University, Jishou 416000, China)
Abstract: The oxidative leaching of low-grade copper ore was investigated in the ammonia-ammonium sulfate solution with ammonium persulfate. The effects of different parameters on the leaching of copper, including ammonia-to- ammonium ion ratio, total ammonia concentration, concentrations of ammonia, ammonium sulfate and ammonium persulfate, temperature, liquid-to-solid ratio and stirring speed, were investigated. The result shows that the optimal conditions for the leaching of low-grade copper ore with a copper extraction 87.7% are the particle sizes of 92.8% of sample finer than 0.045 mm, the concentrations of ammonia, ammonium sulfate and ammonium persulfate are 2.4, 1.8 and 0.100 mol/L, respectively, leaching time 90 min, temperature 30 ℃, liquid-to-solid ratio (mL/g) 5:1, stirring speed 500 r/min.
Key words: low-grade copper ore; oxidative leaching; ammonia-ammonium sulfate; ammonium persulfate
火法炼铜作为冶炼硫化铜矿的传统技术,生产了世界上70%~80%的金属铜[1]。因为过度开采铜矿资源,使得铜矿日益减少和贫化。目前,复杂多金属伴生铜矿、低品位氧化铜矿及硫氧混合铜矿急需开发利用,同时鉴于社会对环境保护要求的提高,传统的火法炼铜面临挑战[2-3]。目前,湿法冶金技术发展迅速且相关研究日渐活跃,对于铜、钴、镍的硫化矿、低品位矿和硫氧混合矿的湿法冶金的方法主要有高压氨浸法、氧压浸出法、氧化焙烧还原氨浸法和氯化浸出法等[4-10],这些方法在处理不同的矿物各有优势。氧化氨浸为一种新兴的湿法冶金技术[11-14],即在氨性溶液中添加氧化剂用以氧化硫化矿,促进有价金属元素的溶解。氧气是研究最多又便宜的氧化剂[12],高温高压下氧化氨浸主要在浸出高品位的硫化矿和低品位贵金属的硫化物具有一定的优势,但其高温高压的苛刻条件,对设备耐温耐压性能提出了较高的要求,同时高温操作所需能耗较高,因此设备投资和生产成本相应地增加;非贵金属低品位复杂硫氧混合矿采用高温有氧氨浸时,虽然金属的浸出率可能比常温有氧氨浸要高,但高温氧化浸出的生产成本高,因此,采用高温有氧的氧化氨浸处理非贵金属低品位含硫化物的氧化矿,其优势得不到体现;另外,常温常压下有氧的氧化氨浸一般生产周期长,且硫化矿浸出效果欠佳[5]。
BING?L等[15]研究了含孔雀石氧化铜矿在氨-碳酸铵体系中的浸出行为,刘维等[16]研究了孔雀石在铵-氯化氨-乙二胺体系中的溶解热力学行为,孙锡良 等[17]研究了复杂氧化铜矿在氨性溶液中浸出技术条件和动力学行为,但这些学者均没有对低品位氧化铜矿中的硫化矿在氨性溶液的浸出进行研究。因此,常温常压下浸出难选含硫化物的低品位的氧化铜矿是氨性浸出的难点,其中氧化剂的选择是关键。
云南省汤丹低品位氧化铜矿为中国大型的氧化铜矿,贮量达115×105 t,是一座高碱性脉石的难选铜 矿,矿石平均品位0.75% , 氧化率在70%以上,结合率30%左右。矿石中碱性脉石含量很高(w(CaO+ MgO)>40%),铜矿物中孔雀石和硅孔雀石的比例在70%以上,其余为次生硫化铜矿(斑铜矿等)。刘维等[18]研究了汤丹低品位氧化铜矿在氨-氯化铵体系中浸出动力学行为,但是其中的硫化物(斑铜矿)基本未浸出。
REED等[19]报道过硫酸盐在碱性环境中氧化浸出金属,其在中性或碱性溶液中还原电势为
 →
→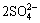 ,E0=+2.01 V (1)
,E0=+2.01 V (1)
实验结果表明浸出周期短,且浸出效果好,其主要原因是过硫酸盐氧化能力强,氧化能力与pH值无关,不随pH值的变化而改变。
虽然采用氨-硫酸铵溶液体系氧化铜矿浸出曾有研究,但常温常压下以过硫酸盐为氧化剂,氧化浸出含硫化物的低品位氧化铜矿未有报道。本文作者尝试常温常压下在氨-硫酸铵体系中以过硫酸铵为氧化
剂,氧化浸出含硫化矿的低品位氧化铜矿,希望有效地解决硫化铜矿浸出问题。
1 实验
1.1 试验原料
汤丹低品位氧化铜矿的铜矿物绝大部分呈极细网脉状或显微网脉状,呈现于脉石的晶粒界面、晶粒间隙、解理面和裂纹中, 网脉的宽度小至0.015~0.002 mm[20], 因此汤丹低品位氧化铜矿矿样需要破碎,研磨成细粒才能实现铜矿从脉石中剥离。试验用矿样经破碎、磨细、筛分后,粒度如表1所列。矿样粒度分析表明:92.8%矿物粒度小于0.045 mm。
矿样的化学组成分析和XRD谱分别如表2和图1所示。由表2可知,氧化钙和氧化镁二者的质量分数超过40%,而铜含量(质量分数)仅为0.77%;因矿物中铜含量太低以至XRD无法观测到矿物中的铜物相,XRD分析表明脉石主要为白云母、方解石、白云石和石英等矿物。
表1 总矿样粒度分布
Table 1 Distribution of sample granularity

表2 矿样的化学组成
Table 2 Chemical analysis of sample (mass fraction, %)

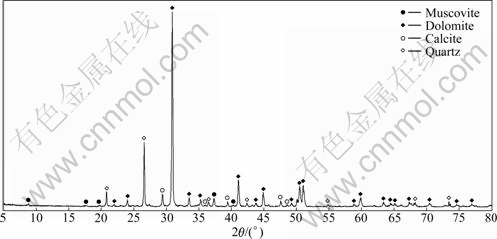
图1 矿样的XRD谱
Fig. 1 XRD pattern of sample
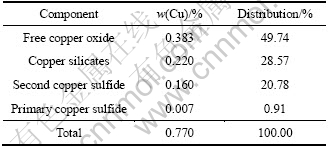
矿样的SEM-EDS图、化学物相组成及EDS的元素分析分别如图2、表3和表4所示。同时,通过偏光显微镜观测证实,矿样铜物相以孔雀石为主,其次是硅孔雀石,再次之是斑铜矿,分别对应于自由氧化铜、硅酸铜和次生硫化铜矿(见表3)。EDS 2和3的元素分析分别与硅孔雀石(CuSiO3)和斑铜矿分子式的元素理论值接近,表明EDS 2和3中铜矿物分别为硅孔雀石和斑铜矿;EDS 1中氧元素分析含量与孔雀石分子式理论值相比明显偏小,但是EDS 1中铜和碳元素含量与理论值相近,可以认为EDS 1的矿物是以孔雀石为主。因此,EDS元素分析(见表4)也证实了铜物相与偏光显微镜所观测的结果一致。
1.2 试验装置
试验装置主要包括一台电子恒温水浴锅,机械搅拌器和一个1000 mL的四口圆底烧瓶,四口瓶分别用于安装冷凝器、机械搅拌器、水银温度计和一个便于取样的橡胶塞。另外还有抽滤设备和干燥箱等。

图2 矿样的SEM像及相应的EDS谱
Fig. 2 SEM images and EDS spectra of samples (white parts, containing copper minerals): (a), (b) Malachite and its analysis of EDS1; (c), (d) Chrysocolla and its analysis of EDS2; (e), (f) Bornite and it analysis of EDS3
表3 矿样的化学物相组成
Table 3 Chemical phase composition of sample
1.3 试验方法
在反应圆底烧瓶中加入氨、硫酸铵和过硫酸盐浓度一定的500 mL溶液,同时加热和搅拌,待所需温度和搅拌速度达到设定值,将矿样投入反应瓶;间隔一定的反应时间从反应瓶中取5 mL反应液,过滤、用原子吸收光谱分析滤液的铜离子浓度;同时补加 5 mL新鲜浸出剂于反应瓶,以维持反应溶液体积恒定。反应完毕,抽滤分离固液,用蒸馏水洗涤滤饼,将滤饼在恒温110 ℃下干燥8 h。
2 结果与讨论
2.1 浸出机理
孔雀石和硅雀石各自的溶解机理如反应式(2)和(3)
Cu2(OH)2CO3+6NH4OH+2(NH4)2SO4?
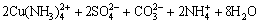 (2)
(2)
CuSiO3×H2O+2NH4OH+(NH4)2SO4?
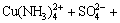 SiO2?+4H2O (3)
SiO2?+4H2O (3)
PARK等[5]和REILLY及SCOTT[21]的研究表明:在氨氧溶液硫化矿中,硫元素最终被氧化为硫酸根离子。FURMAN等[22]提出了碱性环境中过硫酸盐的分
解机理如反应式(4)~(7):
 2H2O
2H2O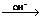
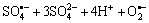 (4)
(4)
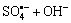 →
→ (5)
(5)
 →O2+OH- (6)
→O2+OH- (6)
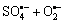 →
→ (7)
(7)
联立反应式(4)~(7)可得碱性条件下过硫酸盐分解方程为
 2H2O
2H2O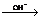
 O2+4H+ (8)
O2+4H+ (8)
反应式(8)表明 在氨溶液中可进行如下分解:
在氨溶液中可进行如下分解:
 4NH3+2H2O?
4NH3+2H2O? O2+4NH4+ (9)
O2+4NH4+ (9)
斑铜矿在氨氧体系如式(10)进行溶解反应:
2Cu5FeS4 + 18.5O2 + 36NH3 + H2O + 2(NH4)2SO4→
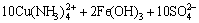 (10)
(10)
因此,联立反应式(9)和(10)可得斑铜矿在含过硫酸盐的氨-硫酸铵溶液中的溶解机理:
Cu5FeS4 +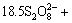 55NH3+19H2O+(NH4)2SO4?
55NH3+19H2O+(NH4)2SO4?
 (11)
(11)
2.2 氨/铵离子摩尔比和总氨浓度对铜浸出率的影响
在总氨浓度6 mol/L、反应时间4 h、液固比(mL/g) 5:1、反应温度30 ℃、搅拌速度为500 r/min条件下,研究了不同氧化剂下氨/铵离子摩尔比对铜浸出率的影响,结果见图3。
从图3可知:氨/铵离子摩尔比在0.5~2.0之间,不论是否添加氧化剂,铜浸出率的曲线都呈现一个平缓的“台阶”,主要是氨和硫酸铵形成的缓冲溶液pH值变化小,有利于铜与氨形成可溶性铜氨配位物,为常规浸出(未加氧化剂)和氧化浸出应用提供了较大的空间;当氨/铵离子摩尔比为5:7时, 常规浸出和以过硫酸钠、过硫酸钾、过硫酸铵为氧化剂氧化浸出的铜浸出率分别为75.9%、85.5%、85.9%和 86.5%;当其它条件相同时,氧化浸出比常规浸出的铜浸出率高,在氨/铵摩尔比为5:7时,氧化浸出的铜浸出率比常规浸出的高9%以上,据反应式(11)浸出机理分析,主要是斑铜矿被过硫酸盐氧化而溶解;3种过硫酸盐均能促进铜的浸出,但其中以过硫酸铵的效果好,同时遵循少引入杂质离子的原则,确定过硫酸铵作为氧化浸出剂。后续试验确定氨/铵离子摩尔比为5:7,以过硫酸铵为氧化剂,研究总氨浓度对铜浸出率的影响。
表4 矿样的EDS元素分析
Table 4 EDS elements analysis of sample

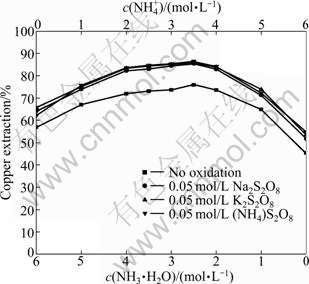
图3 不同氧化剂条件下氨/铵离子摩尔比对铜浸出率的影响
Fig. 3 Effect of ammonia/ammonium ion mole ratio on copper extraction at different oxidants
在过硫酸铵0.05 mol/L、液固比(mL/g) 5:1、搅拌速度500 r/min、反应温度30 ℃的条件下,保持氨/铵离子摩尔比为5:7,研究总氨浓度对铜浸出率的影响(见图4)。从图4可知:铜浸出率随总氨浓度的增大而增大,总氨浓度较低时,随着总氨浓度的增加,铜浸出率增大明显,总氨浓度较高时,铜浸出率增加幅度变小;氨/铵离子摩尔比一定时,随着总氨浓度的增大,氨和铵离子的浓度都随之相应地增大,此时铜的浸出率随氨和铵离子浓度的增大而增大;不同总氨浓度下,铜浸出率均随时间的延长而增大,浸出60 min后,铜浸出率变化不明显;浸出90 min后,总氨浓度为5、6和7 mol/L时,铜的浸出率分别为85.5%、86.5%和86.6%。从能耗和浸出剂消耗两方面考虑,选择反应时间90 min,总氨浓度6 mol/L,此时氨和硫酸铵浓度分别为2.4和1.8 mol/L,因此拟定以此两种浓度进行后续试验。
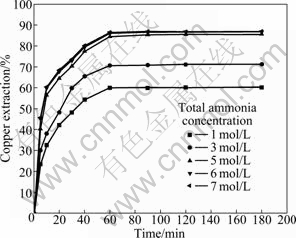
图4 总氨浓度对铜浸出率的影响
Fig. 4 Effect of total ammonia concentration on copper extraction
2.3 搅拌速度对铜浸出率的影响
在反应温度30 ℃、反应时间90 min、液固比(mL/g) 5:1,氨、硫酸铵和过硫酸铵浓度分别为2.4、1.8和0.050 mol/L的条件下,研究了搅拌速度对铜浸出率的影响,结果如图5所示。由图5可知:铜的浸出率随搅拌速度增大而提高,当搅拌速度达到400 r/min后,铜的浸出率无明显变化,同时观察到矿粒较均匀地悬浮于浸出液。当搅拌速度超400 r/min时,搅拌速度作为浸出过程中的可变因素可以不予考虑,因此,后续的试验拟定搅拌速度为500 r/min,以消除搅拌速度对浸出过程的影响。

图5 搅拌速度对铜浸出率的影响
Fig. 5 Effect of stirring speed on copper extraction
2.4 氨和硫酸铵浓度对铜浸出率的影响
在过硫酸铵0.05 mol/L、液固比(mL/g) 5:1、搅拌速度500 r/min、反应温度30 ℃的条件下,分别研究了氨和硫酸铵浓度对铜浸出率的影响,结果如图6所示。

图6 氨和硫酸铵浓度对铜浸出率的影响
Fig. 6 Effects of concentrations of ammonia and ammonium sulfate on copper extraction: (a) Ammonia concentration; (b) Ammonium sulfate concentration
在硫酸铵浓度为1.8 mol/L时,研究了氨浓度对铜浸出率的影响试验结果,如图6(a)所示。由图6(a)可知:不同氨浓度下铜浸出率随浸出时间的延长而增加;同时铜浸率随氨浓度的增加而增加,当氨浓度较低时,铜浸出率的增加幅度大;当氨浓度超过2.0 mol/L时,铜浸出率的增加幅度明显变小;当氨浓度为2.4和3.0 mol/L时,反应90 min后,铜浸出率分别为86.5%和86.7%,二者的浸出率相差不大。鉴于高浓度氨易挥发,因此后续试验氨浓度确定为2.4 mol/L。
在氨浓度为2.4 mol/L时,研究了不同硫酸铵浓度对铜浸出率的影响,如图6(b)所示。由图6(b)可知:不同硫酸铵浓度对铜浸出率的影响与氨浓度的影响相类似,即随浸出时间的延长,铜浸出率增加;当硫酸铵浓度较低时,铜浸出率的增加幅度较大;当硫酸铵浓度超过1.8 mol/L时,铜浸出率的增大幅度变小;当硫酸铵浓度为1.8、2.4和3.0 mol/L时,反应90 min后,铜浸出率分别为86.5%、86.7%和86.8%。在实际操作过程中,由于硫酸铵的溶解度随温度的变化大,高浓度的硫酸铵在低温时易结晶析出,不利后续操作,同时硫酸铵浓度为1.8和3.0 mol/L时,铜浸出率相差只有0.3%;同时过硫酸铵浓度为0.05 mol/L,其浓度远小于硫酸铵的浓度1.8 mol/L,可忽略过硫酸铵的铵离子作用。因此综合考虑选择硫酸铵的浓度为1.8 mol/L。
综上所述,后续试验氨和硫酸铵的浓度分别确定为2.4和1.8 mol/L。
2.5 过硫酸铵浓度对铜浸出率的影响
在氨和硫酸铵分别为2.4和1.8 mol/L、液固比(mL/g) 5:1、搅拌速度500 r/min,反应温度30 ℃的条件下,研究了过硫酸铵浓度对铜浸出率的影响,结果如图7所示。
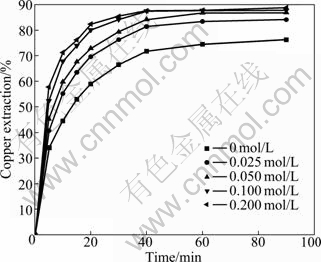
图7 过硫酸铵浓度对铜浸出率的影响
Fig. 7 Effect of ammonium persulfate concentration on copper extraction
由图7可知:在不同浓度的过硫酸铵溶液中; 铜浸出率随着时间的延长而增加;在试验浓度内,铜浸出率随过硫酸铵浓度的增加而增大;在未加过硫酸铵氧化剂的常规浸出中,铜浸出率低,其主要原因是无氧化剂作用时,氧化铜矿中的斑铜矿矿物无法氧化和溶解浸出,过硫酸盐的添加可以氧化和促进溶解斑铜矿,有利于铜的浸出;当过硫酸铵浓度增加到0.100 mol/L时,继续增加过硫铵浓度,反应结束时,铜浸出率增加不明显;过硫酸铵浓度为0.100和0.200 mol/L时,浸出90 min后,铜浸出率分别为87.7%和87.8%。因此,后续试验确定过硫酸铵的浓度为0.100 mol/L。
2.6 液固比对铜浸出率的影响
在氨、硫酸铵和过硫酸铵浓度分别为2.4、1.8和0.100 mol/L,搅拌速度500 r/min,反应温度30 ℃的条件下,研究了液固比对铜浸出率的影响,结果如图8所示。由图8可知:随浸出时间的延长,铜浸出率相应的增加,浸出60 min后,继续延长时间,浸出率增大不明显;液固比增大时,铜浸出率也随之增大,即单位质量矿样的浸出剂量增大,有利于铜的浸出;液固比(mL/g)增大到5:1时,继续增大液固比,浸出结束时,铜浸出率几乎相同。因此,确定浸出的液固比(mL/g)为5:1。
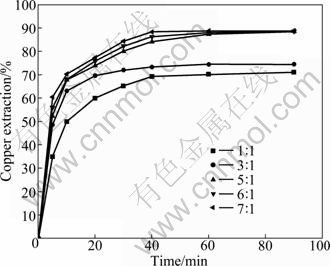
图8 液固比对铜浸出率的影响
Fig. 8 Effect of liquid-to-solid ratio on copper extraction
2.7 温度对铜浸出率的影响
在氨、硫酸铵和过硫酸铵分别为2.4、1.8和0.100 mol/L,液固比5:1,搅拌速度500 r/min的条件下,考察了温度对铜浸出率的影响,结果如图9所示。
由图9可知:提高温度可缩短浸出时间,50 ℃时,浸出40 min后,铜浸出率达86.7%;浸出90 min后,30、40和50 ℃的铜浸出率分别为87.7%、87.8%和87.8%;温度的升高,不仅增大了能耗,同时也增大了氨的挥发性,增加氨的消耗,且恶化操作环境。因此温度选择30 ℃较宜。
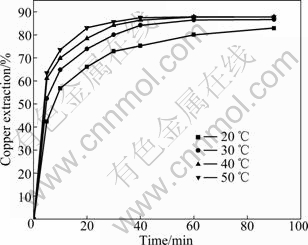
图9 温度对铜浸出率的影响
Fig. 9 Effect of temperature on copper extraction
综合上述可得低品位氧化铜矿浸出的较佳条件如下:92.8%矿样粒度小于0.045 mm,氨、硫酸铵和过硫酸铵浓度分别为2.4、1.8和0.100 mol/L,浸出时间为90 min,温度为30 ℃,液固比为5:1,搅拌速度为500 r/min。在此条件下,铜的浸出率达87.7%。
2.8 浸出渣分析
浸出渣的EDS元素分析和SEM-EDS图分别如表5和图10所示。浸出前矿样表面显微结构呈粗糙和多孔状(见图2),但是浸出渣的显微结构呈现不同的表面。浸出渣中没有观测到孔雀石,说明孔雀石全部溶解。对比浸出前矿样EDS2(见图2(d))和浸出渣EDS4 (图10(b)和表5))可知,硅孔雀石部分溶解。由图10(a) 可知,硅孔雀石的浸出渣表面不如浸出前粗糙和多孔,氨浸过程中,析出的二氧化硅吸附在硅孔雀石的表面, 阻止了硅孔雀石的进一步溶解;对比浸出前矿样EDS3 (见图2(f))和浸出渣EDS5(见图10(d))可知,斑铜矿几乎全部氧化溶解。由图10(c)可知,浸出渣源自斑铜矿的氧化, 斑铜矿浸出渣的表面虽然呈现粗糙与多孔状,但是有部分的针状物出现,证实了斑铜矿发生了氧化和溶解。矿样浸出前后铜墙铁壁的化学物相组成分析的结果如表6所列,证实了斑铜矿被过硫酸所氧化,溶解于氨-硫酸铵溶液。
表5 浸出渣的EDS元素分析
Table 5 EDS element analysis of leaching residue
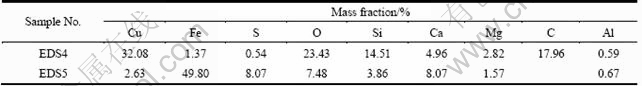

图10 浸出渣的SEM像及相应的EDS谱
Fig. 10 SEM images and EDS spectra of leaching residue (white parts, containing copper minerals): (a), (b) Leaching residue of chrysocolla and its analysis of EDS4; (c), (d) Leaching residue of bornite and its analysis of EDS5
表6 矿样浸出前后铜的化学物相组成
Table 6 Chemical phase composition of copper in samples before and after leaching

3 结论
1) 以过硫酸铵为氧化剂,研究了含硫化物的低品位氧化铜矿在氨-硫酸铵溶液中的氧化浸出行为,矿物浸出前后的化学物相定量分析和SEM-EDS半定量分析表明,斑铜矿经过硫酸盐氧化,基本上溶解于氨-硫酸铵溶液。
2) 浸出低品位氧化铜矿的较佳条件是92.8%矿样粒径小于0.045 mm,氨、硫酸铵和过硫酸铵浓度分别为2.4、1.8和0.100 mol/L,浸出时间为90 min,温度为30 ℃,液固比(mL/g)为5:1,搅拌速度为500 r/min。在较佳浸出条件下,铜的浸出率达87.7%。
3) 在氨-硫酸铵体系,孔雀石能全部溶解浸出,硅孔雀石部分溶出。
REFERENCES
[1] 范兴祥, 彭金辉, 黄孟阳, 张世敏, 张利波. 浸出黄铜矿的新工艺研究[J]. 矿冶工程, 2005, 25(3): 58-62.
FAN Xing-xiang, PENG Jin-hui, HUANG Meng-yang, ZHANG Shi-min, ZHANG Li-bo. Study on innovative process of leaching of chalcopyrite [J]. Ming and Metallurgical Engineering, 2005, 25(3): 58-62.
[2] QIU Ting-shieng, NIE Guang-hua, WANG Jun-feng, CUI Li-feng. Kinetic process of oxidative leaching of chalcopyrite under low oxygen pressure and low temperature [J]. Transactions of Nonferrous Metals Society of China, 2007, 17(2): 418-422.
[3] 王海北, 蒋开喜, 张邦胜, 王玉芳, 林江顺, 王 春. 新疆某复杂硫化铜矿低温低压浸出工艺研究[J]. 有色金属, 2004, 56(3): 52-56.
WANG Hai-bei, JIANG Kai-xi, ZHANG Bang-sheng, WANG Yu-fang, LIN Jiang-shun, WANG Chun. A novel hydrometallurgical process with low temperature and pressure for complicated copper concentration from Xinjiang of China [J]. Nonferrous Metals, 2004, 56(3): 52-56.
[4] JIN B, YANG X, SHEN Q. Kinetics of copper dissolution during pressure oxidative leaching of lead-containing copper matte [J]. Hydrometallurgy, 2009, 96(1/2): 56-61.
[5] PARK K H, MOHAPATRA D, REDDY B R, NAM C W. A study on the oxidative ammonia-ammonium suphate leaching of a complex (Cu-Ni-Co-Fe) matte [J]. Hydrometallurgy, 2007, 96(1/2): 164-171.
[6] 杨俊奎, 徐 斌, 杨大锦. 复杂铜精矿氧压浸出综合回收工艺[J]. 矿冶工程, 2011, 31(1): 73-80.
YANG Jun-kui, XU Bin, YANG Da-jin. Comprehensive recovery of oxygen pressure leaching for complex Cu concentrate [J]. Ming and Metallurgical Engineering, 2011, 31(1): 73-80.
[7] 徐志峰, 李 强, 王成彦. 复杂硫化铜矿热活化-加压浸出工艺[J]. 中国有色金属学报, 2010, 20(12): 2412-2418.
XU Zhi-feng, LI Qiang, WANG Cheng-yan. Heat activation pretreatment and pressure leaching of complex copper sulfide ores [J]. The Chinese Journal of Nonferrous Metals, 2010, 20(12): 2412-2418.
[8] 《有色金属提取冶金手册》编辑委员会. 有色金属提取冶金手册铜镍[M]. 北京: 冶金工业出版社, 2000: 433-441.
Edition Committee of Non-ferrous Metal Extraction Metallurgy Handbook. Copper-nickel of non-ferrous metal extraction metallurgy handbook [M]. Beijing: Metallurgical Industry Press, 2000: 433-441.
[9] EKMEKYAPAR A, ?OLAK S, ALKAN M. Dissolution kinetics of an oxidezed copper ore in water saturated by chlorine [J]. J Chem Tech Biotechnol, 1998, 43(3): 195-204.
[10] ?OLAK S, ALKAN M, KOCAKERIM M M. Dissolution kinetics of chalcopyrite containing pyrite in water saturated with chlorine [J]. Hydrometallurgy, 1987, 18(2): 183-193.
[11] RAO K S, RAY H S. A new look at characterization and oxidative ammonia leaching behavior of multimetal sulphides [J]. Minerals Engineering, 1998, 11(11): 1011-1024.
[12] BELL S L, WELCH G D, BENNETT P G. Development of ammoniacal lixiviants for the in-situ leaching of chalcopyrite [J]. Hydrometallurgy, 1995, 39(1/3): 11-23.
[13] GHOSH M K, DAS R P, BISWAS A K. Oxidative ammonia leaching of sphalerite: Part I. Noncatalytic kinetics [J]. International Journal of Mineral Processing, 2002, 66(1/4): 241-254.
[14] HALPERN J, MILANTS H, WILES D R. Kinetics of the dissolution of copper in oxygen-containing solutions of various chelating agents [J]. Journal of the Electrochemical Society, 1959, 106(8): 647-650.
[15] BING?L D, CANBAZO?L M, AYDI?AN S. Dissokution kinetics of malachite in ammonia/amminiun carbonate leaching [J]. Hydrometallurgy 2005, 76(1/2): 55-62.
[16] LIU Wei, TANG Mo-tang, TANG Chao-bo, HE Jing, YANG Sheng-hai, YANG Jian-guang. Thermodynamics of solubility of Cu2(OH)2CO3 in ammonia-ammonium chloride-ethylene- diamine(En)-water system [J]. Transactions of Nonferrous Metals Society of China, 2010, 20(2): 336-343.
[17] SUN Xi-liang, CHEN Bai-zhen, YANG Xi-yun, LIU You-yuan. Technological conditions and kinetics of leaching copper from complex copper oxide ore [J]. Journal of Central South University of Technology, 2009, 16(6): 936-941.
[18] LIU Wei, TANG Mo-tang, TANG Chao-bo, HE Jing, YANG Sheng-hai, YANG Jian-guang. Dissolution kinetics of low grade complex copper ore in ammonia-ammonium chloride solution [J]. Transactions of Nonferrous Metals Society of China, 2010, 20(5): 910-917.
[19] REED W A, GARNOV Y A, RAO L, NASH K L, BOND A H. Oxidative alkaline leaching of Americium from simulated high-level nuclear waste sludges [J]. Separation Science and Technology, 2005, 40(5): 1029-1046.
[20] 刘殿文, 张文彬, 方建军, 库建刚. 试论东川汤丹难选氧化铜矿的工艺矿物学特征及可选性[J]. 云南冶金, 2003, 32(3): 7-8.
LIU Dian-wen, ZHANG Wen-bin, FANG Jian-jun, KU Jian-gang. A discussion on mineralogical characteristics and washability of oxide copper ore in Tangdan mine [J]. Yunnan Metallurgy, 2003, 32(3): 7-8.
[21] REILL I G, SCOTT D S. The leaching of cupric sulfide in ammonia [J]. Ind Eng Chem, Process Des Dev, 1976, 15(1): 60-67.
[22] FURMAN O S, TEEL A L, WATTS R J. Mechanism of base activation of persulfate [J]. Environmental Science Technology, 2010, 44(16): 6423-6428.
(编辑 何学锋)
基金项目:国家基础研究重点资助项目(2007CB13601);湖南省教育厅资助项目(10C1095)
收稿日期:2011-06-03;修订日期:2011-10-14
通信作者:尹周澜,教授,博士;电话:0731-88877364;传真:0731-88879616;E-mail: yzllxh@gmail.com