����ˮ��Һ������п��þ��Ԫ��������ϵ�Ľᾧ��Ϊ
��Դ�ڿ����й���ɫ����ѧ��2020���7��
�������ߣ������� ��־�� κ�� ���˱� ��F͢ ����ӡ ����
����ҳ�룺1691 - 1703
�ؼ��ʣ���������������п������þ���ܽ�ȣ��ᾧ���¶�
Key words��ferrous sulfate; zinc sulphate; magnesium sulfate; solubility; crystallization; temperature
ժ Ҫ��ͨ���о�FeSO4-ZnSO4-MgSO4-H2SO4��ϵ��п������þ�Ľᾧ��Ϊ�����첻ͬ������Ũ�����¶ȶ���������������п������þ�ᾧ��Ӱ�졣��������������¶ȵ����ߣ���������������п������þ���ܽ�Ƚ��ͣ��ı��ʼ��Һ���������ӵ�Ũ�ȣ����������ļ��罵������(160~180 ��)���ֲ��䣻����п�����������Ĵ������������þ�Ľᾧ�ʣ�����þ�����������Ĵ����������п�Ľᾧ�ʣ�����160 ��ʱ������п������þ�Ĵ�����������������ᾧ�ʣ�����170 ��ʱ������п������þ�Ĵ��ڽ������������ᾧ�ʡ�
Abstract: The effects of different sulfate concentrations on the crystallization of ferrous sulfate, zinc sulfate and magnesium sulfate were investigated through investigating the crystallization behavior of zinc, iron and magnesium in FeSO4-ZnSO4-MgSO4-H2SO4 system. The results show that the solubility of ferrous sulfate, zinc sulfate and magnesium sulfate decreases with the increase of temperature. When the concentration of ferrous ions in the initial solution is changed, the sharp decrease interval of ferrous sulfate (160-180 ��) remains unchanged. The presence of zinc sulfate and ferrous sulfate increases the crystallization rate of magnesium sulfate, the presence of magnesium sulfate and ferrous sulfate increases the crystallization rate of zinc sulfate. When the temperature is lower than 160 ��, the presence of zinc sulfate and magnesium sulfate increases the crystallization rate of ferrous sulfate, when the temperature is higher than 170 ��, it decreases the crystallization rate of ferrous sulfate.
DOI: 10.11817/j.ysxb.1004.0609.2020-37596
�������־�ң�κ �ƣ����˱���F͢������ӡ���� ��
(����������ѧ ұ������Դ����ѧԺ������ 650093)
ժ Ҫ��ͨ���о�FeSO4-ZnSO4-MgSO4-H2SO4��ϵ��п������þ�Ľᾧ��Ϊ�����첻ͬ������Ũ�����¶ȶ���������������п������þ�ᾧ��Ӱ�졣��������������¶ȵ����ߣ���������������п������þ���ܽ�Ƚ��ͣ��ı��ʼ��Һ���������ӵ�Ũ�ȣ����������ļ��罵������(160~180 ��)���ֲ��䣻����п�����������Ĵ������������þ�Ľᾧ�ʣ�����þ�����������Ĵ����������п�Ľᾧ�ʣ�����160 ��ʱ������п������þ�Ĵ�����������������ᾧ�ʣ�����170 ��ʱ������п������þ�Ĵ��ڽ������������ᾧ�ʡ�
�ؼ��ʣ���������������п������þ���ܽ�ȣ��ᾧ���¶�
���±�ţ�1004-0609(2020)-07-1691-12���� ��ͼ����ţ�TF813���� ���ױ�־�룺A
����ȫ����п��ҵ�Ŀ��ٷ�չ������п��Դ���ϼ��٣�Ϊ����п��Դ�г�����Ҫ����Ʒλ������������ʺ����ߵĸ���п������Դ�Ŀ����������ܵ�пұ����ҵ�����ӣ��ر������п��Ŀ�������������ȫ��Ĺ�ע�������ϵĸ�����п����Դ��п�Ĵ����ߴ�700��t[1-4]��п�������Ѿ���Ϊʪ����п������һ���ձ���ڵ���Ҫ���⣬���Ź��һ�������Խ��Խ�ϸ�ʪ����п�����г������յ�ѡ��������Ҫ[5-6]������ں�п������Һ��ʵ��п���ĸ�Ч�����Լ������м۽�������Դ�������Ѿ���Ϊ����ʪ����п��ҵ���ȵ�����[3]��Ŀǰ��ʪ����п��ҵ�ڹ�ҵ���Ѿ��ɹ�Ӧ�õij��������лƼ��������������ͳ�����[7]��
�Ƽ������������������ϴ������������������ã�ͬʱ���к���п��ͭ����������������ӣ����������ȶ���������������������[8-9]��V.M.������Ӫ�ɱ��ߣ�E.Z.����ϡɢ��������ʧ�ʸߣ�������Ѵ�ʱ����������������ӿ�����©����ɻ�����Ⱦ���Ҵ����м۽��������ʵ͵�����[10-11]�����֮�£���Ȼ��������Ͷ�ʼ�ά�����ýϸߺͲ���Ҫ���Ϊ�ϸ��dz��������������٣������ߵ��ŵ㣬���������ܳ�Ϊˮ����ҵ������ҵ��ԭ�ϻ������� ��[12]������ȫ������Խ��Խ�ϸ���ʹп��ҵ���������ȹ̻��ķ������߿��������ij�������[13]����Ŀǰ���еij��������г���������������DZ����Ϊ�����ij�������[14]�����ڳ����ļ���Ҫ��ߣ�Ŀǰ������������Ӫ�Ĺ�˾�����ձ�����ұ�������й�����������ɽп��ұ������˾��
Ϊ�˱�֤���õij������������������¶Ȳ�����180 �棬����������180 ��Ĵ�ˮ���ܽ��Ϊ3.43 g/L[15]���ڳ��������IJ�����������������������п������þ�����ᾧ[6]������ᾧ����ָ��[16]�����ͳ������ڳ�����ѹ���£��������һ���佺��ǿ�����ž������������ͳ»�ʱ����ӳ��������������Ž���ǿ�ȵ��������������ξ��������ɸ��ڽṸ���Ṹ���������������ܽ�������������Һ������Ũ�Ƚϸߺ������������������⡣����������⣬��������ͨ���о�������FeSO4-ZnSO4- MgSO4-H2SO4��ϵ�������εĽᾧ��Ϊ��̽����������������þ������п֮��Ľᾧ���ɣ�Ϊ�����������������ܽ���������������ʽ��͵������ṩ���ۻ�����
1 ʵ��
1.1 ʵ�鷽��
�÷�����FeSO4��7H2O��MgSO4��7H2O��ZnSO4��7H2O����Fe2+Ũ��Ϊ30 g/L����ͬŨ�ȵ�����п������þ��Һ�����������ҺpHֵΪ3(���ݳ�����������գ��ڶ����к�Һ(����ǰҺ)��pHά����4���ң�Ϊ��ʹ�о�����Һ�ӽ�ʵ����Һ����ȣ�����ֹ����ˮ�⣬ͬʱΪȷ��������Һ��ʵ�������ͽ����ʵ����Һ��ʵ����ָ�����壬������Һ��pHֵά����3����)������2L-GSH��ѹ��(����Ϊ1Gr18Ni9Ti-TA20)��Ϊ��Ӧ��������1 L���ƺõ���Һ�����ѹ���ڣ����ӹ����豸�����ѹ���������ԣ�������뵪��(��99.2%)�������ų��Ի����ȫ�ĵ�����Χ�����ڸ�����ѹΪ1.6 MPa�������Ȳ����裬����ת��Ϊ300 r/min���ﵽ���趨��ʵ������ʱ������ʵ����������ȡ����ȡ��Һ������ɰо����װ�ù��˺��棬������Һ�и������ӵ�Ũ�ȡ�
1.2 ��������
����EDTA�ζ����ͻ���ԭ�����չ���(WFX-110B)����п���ӵ�Ũ�ȣ������ظ���صζ�������Fe2+���ӵ�Ũ�ȣ����û���ԭ�����չ�������þ���ӵ�Ũ�ȡ����������͵�����ұ���о�Ժ�������Ԫ�صĺ�������֤����֤ʵ�����ݵ�ȷ�ԡ�Fe2+��Mg2+��Zn2+�Ľᾧ�ʼ��㹫ʽΪ
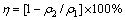 (1)
(1)
ʽ�У���ΪFeSO4��ZnSO4��MgSO4�Ľᾧ�ʣ�%��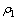 Ϊ��ʼ��Һ��Fe2+��Zn2+��Mg2+��Ũ�ȣ�g/L��
Ϊ��ʼ��Һ��Fe2+��Zn2+��Mg2+��Ũ�ȣ�g/L��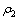 Ϊȡ��Һ��Fe2+��Zn2+��Mg2+��Ũ�ȣ�g/L(ÿ��ȡ��С��5 mL����֤��Һ��������Ա仯)��
Ϊȡ��Һ��Fe2+��Zn2+��Mg2+��Ũ�ȣ�g/L(ÿ��ȡ��С��5 mL����֤��Һ��������Ա仯)��
1.3 ʵ��ԭ��
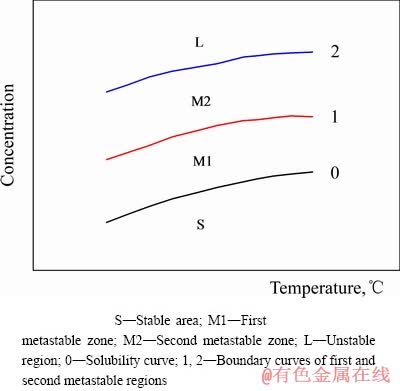
ͼ1 ��Һ״̬ͼ[17]
Fig. 1 Solution state diagram[17]
��ķ˹���о�����[17]����Һͨ���ɴ����ȶ�̬������̬�Ͳ���̬3��״̬(��ͼ1)�����ȶ�������Һ��ҺŨ��С�ڻ�����ܽ�ȣ��ᾧ���ܷ������ڵ�һ���ȶ����������ϲ��ܾ���ɺˣ��ᾧ���̲��ܷ������ڵڶ����ȶ��������Է��ɺ˵Ŀ��ܣ����ɺ˲���ͬʱ���Ϸ��������˵��γɺ;���ij�����Ҫʱ�������ܷ������ڲ��ȶ������ᾧ���Ͽ�ʼ��
BRUHN��[18]�о�����������������ˮ�е��ܽ�������¶ȵ������ܽ�Ȳ������ӣ�����55~65 ��֮��ﵽ���ֵ�����¶ȼ������ߣ��ܽ�Ȼ�Ͻ��͡�HASEGAWA��[15]�о���ͬ�¶Ⱥ�����Ũ���������������ܽ�����¶ȵĹ�ϵ(��ͼ2)������þ������п���ܽ��������������ˮ�е��ܽ�������Ƶ����ԣ�����þ��Լ70 ��ʱ�ܽ�ȴﵽ���ֵ�����¶ȼ�������ʱ������þ���ܽ�Ƚ����Ͻ��ͣ�����þ���ܽ�����¶ȵĹ�ϵ(��ͼ3)[19]������п���ܽ����55~65 ��֮��ﵽ���ֵ�����¶ȼ������ߣ�����п���ܽ�Ȼ�Ͻ��ͣ�����п���ܽ�����¶ȵĹ�ϵ(��ͼ4)[20]����ͼ5[18]��6[21]��֪�������¶ȵ�����ZnSO4��FeSO4��MgSO4���ܽ�Ƚ��ͣ��ڸ�����ˮ��Һ��ZnSO4��FeSO4��MgSO4�Ľᾧ��������ҪΪһˮ�����Ρ���������漵�[22]������[23]�����о�������п������þ����ʱ��������ͬ������ص��¸��������β������ڶ�Ԫ��������ϵ�м�������ı������εĽᾧ���ֻ࣬�ı������ε��ܽ�ȡ�
HASEGAWA��[15]�о�����������Ԫ��ϵFeSO4-ZnSO4-H2SO4��FeSO4-MgSO4-H2SO4�У�������ȵ����ӣ������������ܽ�����ߡ������һ���������£�������Һ��п���Ӻ�þ����Ũ�ȵ����ߣ������������ܽ����֮���ͣ�����ԪϵFeSO4-ZnSO4- MgSO4-H2SO4�У�������ȵ����ӣ������������ܽ����֮���ߡ������һ���������£�п��þ���ӵļ��뽵���������������ܽ�ȡ�
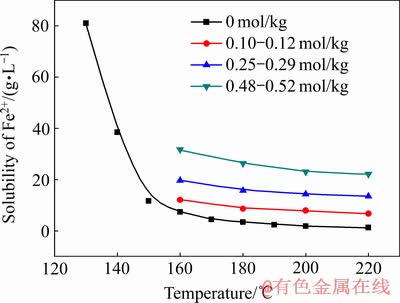
ͼ2 ���������ڲ�ͬ����Ũ���µ��ܽ�����¶ȵĹ�ϵ[15]
Fig. 2 Relationship between solubility of ferrous sulfate and temperature at each sulfuric acid concentration[15]
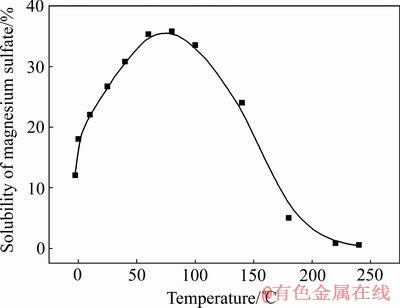
ͼ3 ����þ���ܽ�����¶ȵĹ�ϵ[19]
Fig. 3 Relationship between solubility and temperature of magnesium sulfate[19]
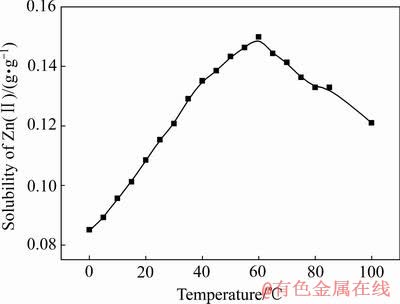
ͼ4 ����п���ܽ�����¶ȵĹ�ϵ[20]
Fig. 4 Relationship between solubility of zinc sulfate and temperature[20]
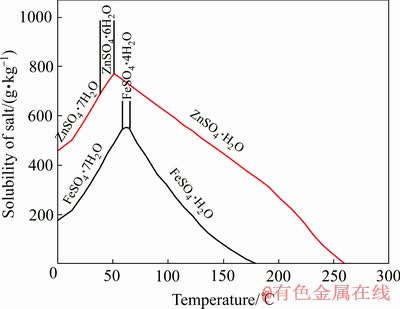
ͼ5 ZnSO4/FeSO4-H2O��ϵ�ܽ��ͼ[18]
Fig. 5 Solubility diagram of ZnSO4/FeSO4-H2O system[18]
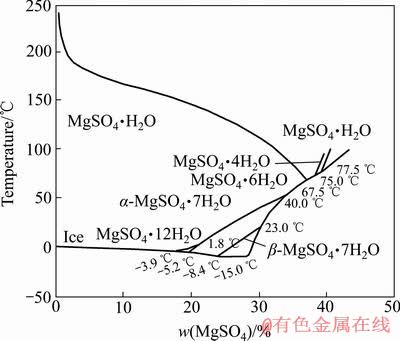
ͼ6 MgSO4-H2O��ϵ�ܽ��ͼ[21]
Fig. 6 Solubility diagram of MgSO4-H2O system[21]
���������ǰҺ��������п����������������þ������������������¶ȸߴ�180~200 �棬��ͼ1��2��3��4��֪���ڴ��¶����䣬����п����������������þ���ܽ�Ƚϵͣ�����ǰҺ���ڲ��ȶ�����ڶ����ȶ�������Һ������п����������������þ�ᷢ�����½ᾧ��Ӧ(��ʽ(2)~(4))��Ϊ�ˣ���������ͨ���о�FeSO4-ZnSO4-MgSO4-H2SO4��ϵ�ڸ���ˮ��Һ�еĽᾧ��Ϊ��̽����������������þ������п֮��Ľᾧ���ɣ�Ϊ���������Һ������Ũ�Ƚϸߡ�������������ķ��ܻ������������ʽ��͵������ṩ���ۻ�����
Zn2++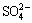 +xH2O=ZnSO4��xH2O (2)
+xH2O=ZnSO4��xH2O (2)
Fe2++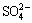 +xH2O=FeSO4��xH2O (3)
+xH2O=FeSO4��xH2O (3)
Mg2++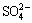 +xH2O=MgSO4��xH2O (4)
+xH2O=MgSO4��xH2O (4)
2 ���������
2.1 FeSO4-H2SO4��ϵ�����������Ľᾧ��Ϊ
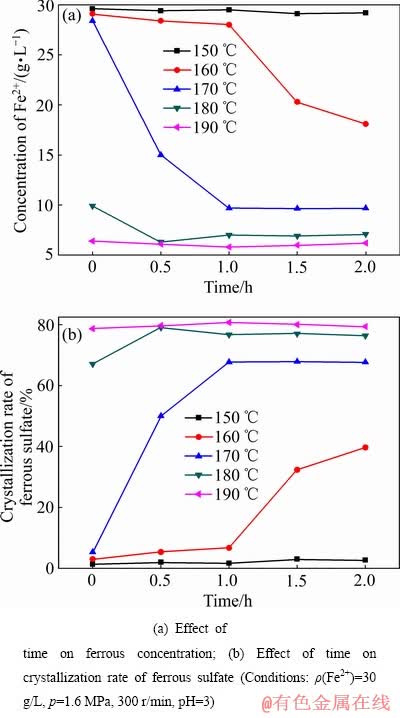
ͼ7 ������ϵ�½ᾧʱ������������ᾧ��Ӱ��
Fig. 7 Effect of crystallization time on crystallization of ferrous sulfate under high temperature system
��ͬ��Ӧ�¶��½ᾧʱ�������������Ӱ������ͼ7����ͼ7(a)��(b)��֪����150 ��ʱ�����Žᾧʱ����ӳ�����Һ����������Ũ�Ⱥ����������Ľᾧ�ʱ��ֺ㶨����ʱ����Һ�����ȶ������ߵ�һ���ȶ�������Һ�������������ܽᾧ����������������Һ����160~170 ��ʱ�����Žᾧʱ����ӳ�����Һ����������Ũ�Ƚ��ͺ����������Ľᾧ��������������Һ���ڵڶ����ȶ�������Һ�е����������ijɺ��뾧�峤����Ҫ�ϳ���ʱ�������ɡ������¶ȵ����ߣ������������ܽ�Ƚ��ͣ���Һ�ļ������Ͷ�����(���ޱ��Ͷ���ָ��������Һ�ɲ��Է��ɺ�ת���Է��ɺ�״̬�Ľ��ޣ���Ӧͼ1�еĵ�һ���ȶ����������ߣ���Һ������������Ũ������¶��¼��ޱ��Ͷ�֮��Ϊ�������Ͷȣ��ǽᾧ���̵��ƶ���[24])�����������Ľᾧ�ƶ������ӣ���������������Ľᾧ�ʣ���1 h���¶���160 ��������170 ��ʱ�����������Ľᾧ����6.67%������67.67%�����¶�Ϊ180~190 ��ʱ����Һ���ڲ��ȶ����������������ٽᾧ���ܿ�ﵽ�ᾧ-�ܽ�ƽ�⣻��180 ���190 ��ʱ���ᾧʱ����0 h�ӳ���2 hʱ�����������Ľᾧ�ʷֱ������9.33%(��67%������76.33%)��0.66%(��78.67%����79.33%)��
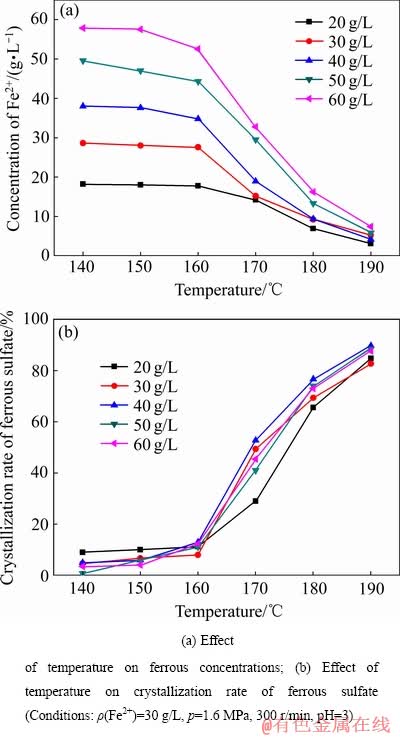
ͼ8 ��ͬ��������Ũ�����¶ȶ����������ᾧ��Ӱ��
Fig. 8 Effect of temperature on crystallization of ferrous sulfate under different ferrous sulfate concentrations
��ͬ��������Ũ�����¶ȶ����������ᾧ��Ӱ������ͼ8����ͼ8(a)��(b)��֪�����¶ȵ���160 ��ʱ����Һ�������������������ᾧ��������������Һ����140~160 ��ʱ����Һ���ڵڶ����ȶ��������������ļ������ͶȽ�С���������������ɺ��Ҿ��������С�����ᾧ��Ӧ��һ����̬���̣��ɺ˺;��峤���������������巵����һ������Ĺ��̣���С�ľ���;����������ܣ����¶�160 ��ʱ�����������Ľᾧ����߽���13%�����¶���160 ��������180 ��ʱ�������������ܽ�ȼ��罵�ͣ���Һ���ڲ����������������ļ��������������ӣ��������������ɺ˺���������������ٳ���������������ʼ������Ũ��Ϊ40 g/Lʱ����Һ�¶���160 ��������180 ��ʱ�����������Ľᾧ����13%������76.625%��HASEGAWA��[15]���о����������������ڴ�ˮ���ܽ�ȵļ����С����Ϊ130~150 �档��ʵ���о����Ϊ160~180�棬������Ϊ��ʵ��������Һ��pHԼΪ3(�������pH)����HASEGAWA��[15]�о������������ڴ�ˮ��Һ�С�������ȵ����ӣ���Һ�����������ӵ�Ũ�����ӣ���Ӧ5���ҽ��У���Һ���������Ũ�Ƚ��ͣ������������ܽ�����ӣ��������������ܽ�ȼ��罵��������130~150 ��������160~180 �棬��20~60 g/L�ķ�Χ�����������ܽ�ȵļ��罵������(160~180 ��)���ֲ��䡣
H++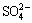 =
=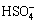 (5)
(5)
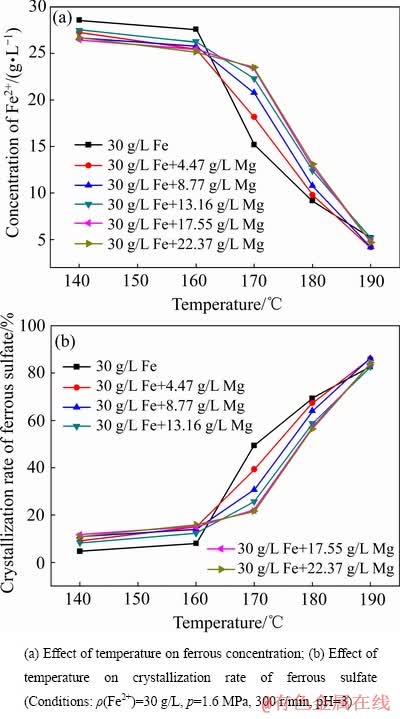
2.2 FeSO4-ZnSO4-H2SO4��ϵ�������εĽᾧ��Ϊ
������ϵ��FeSO4��ZnSO4�������ö������νᾧ�ʵ�Ӱ������ͼ9��ʾ����ͼ9��֪�������¶ȵ����ߣ���������������п�Ľᾧ����֮���ߣ�BRUHN��[18]���ܸ���[20]���о����������¶ȸ���65 ��ʱ�������¶ȵ����ߣ���������������п���ܽ�Ȳ��Ͻ��͡����������Ĵ������������п�ᾧ�ʣ����¶ȵ���160 ��ʱ������п�Ĵ�����������������Ľᾧ�ʣ����¶ȸ���170 ��ʱ������п�Ĵ��ڽ��������������ᾧ�ʣ����¶ȵ���160 ��ʱ������п��������������ʱ����Һ�������Ũ�����ӣ���Һ��п���Ӻ��������ӵ���Ũ��Ҳ���ӣ���ͬ����ЧӦ��п���Ӻ��������ӽ���H+�Ļ��[11]��H+�Ļ�Ƚ��ͣ������ڷ�Ӧʽ(5) ���ҽ��У���Һ�����������Ũ�����ӣ��ٽ���Ӧ(2)��(3)���ҽ��У����������п�����������Ľᾧ�ʡ���ͼ9������a��֪�����¶�Ϊ����170 ��ʱ�������������ܽ�ȼ��罵�ͣ���Һ�д��ڴ����������������壬����������п�Ǿ���ɺˣ��ٽ�����п�ᾧ��BRUHN��[18]���о���֪�������µ�250 ��֮�䣬�����������ܽ�ȵ�������п���ܽ�ȣ���Һ���д�������п���ӣ�п����������ͬ��[22, 25]ȡ��FeSO4��xH2O�еIJ�����ԭ�ӣ��������������Ľᾧ�ʽ��Ͷ�����п�Ľᾧ�����(��ͼ9�е�����b��d)�������¶ȵ����ߣ���������������п���ܽ�Ƚ��ͣ���Һ���������п���ӵ�Ũ�Ƚ��͡�ͬ����ЧӦ������ͬ������ü�������������������������п�ᾧ����Ӱ�졣
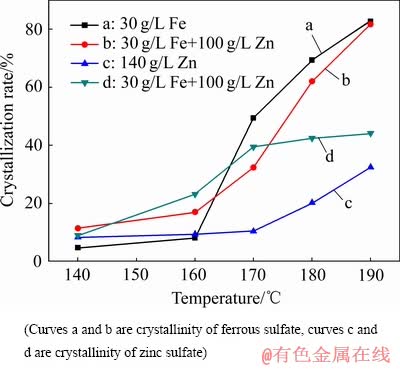
ͼ9 ������ϵ��FeSO4��ZnSO4�������ö������νᾧ�ʵ�Ӱ��
Fig. 9 Effect of interaction between FeSO4 and ZnSO4 on sulfate crystallization rate under high temperature system
��ͬ����пŨ�����¶ȶ�����п�����������ᾧ��Ӱ������ͼ10��ͼ11����ͼ10(a)��(b)��ͼ11(a)��(b)��֪�����¶ȵ���160 ��ʱ������п���ӵ�Ũ����������п�����������Ľᾧ����ߣ���п���Ӵﵽ120 g/Lʱ������п�Ľᾧ����ߣ���Һ�е�п���Ӽ�����������п�Ľᾧ�ʽ��͡���ʼп����Ũ��Խ�ߣ�����ͬ���¶��£���Һ������п�ļ������Ͷ����ߣ�����п�Ľᾧ����ߡ���������п���ܽ�ȸ��������������ܽ�ȣ���������пŨ�ȵ����ӣ���Һ�������������Ũ�����ӣ���������ʽ(3)���ҽ��У�ͬʱ��ͬ����ЧӦ��п����Ũ�����ӽ�����H+�Ļ��[11]�������ڷ�Ӧ(5)���ҽ��У���Һ����������ӣ��ٽ���Ӧ(3)���ҽ��У�������������Ľᾧ�ʶ�����������п�Ľᾧ�ʡ�
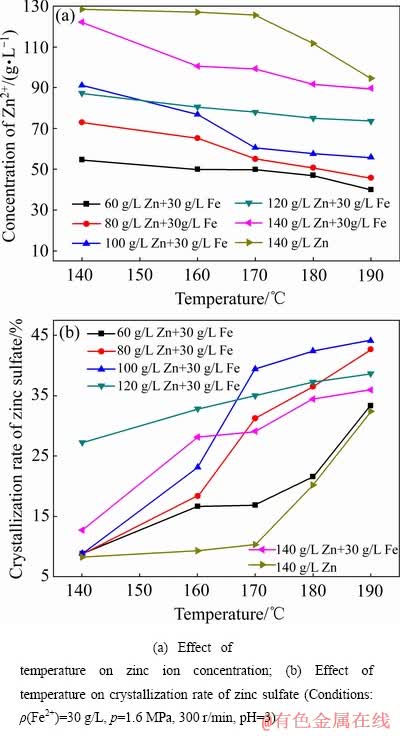
ͼ10 ��ͬ����пŨ�����¶ȶ�����п�ᾧ��Ӱ��
Fig. 10 Effect of temperature on crystallization of zinc sulfate under different zinc sulphate concentration
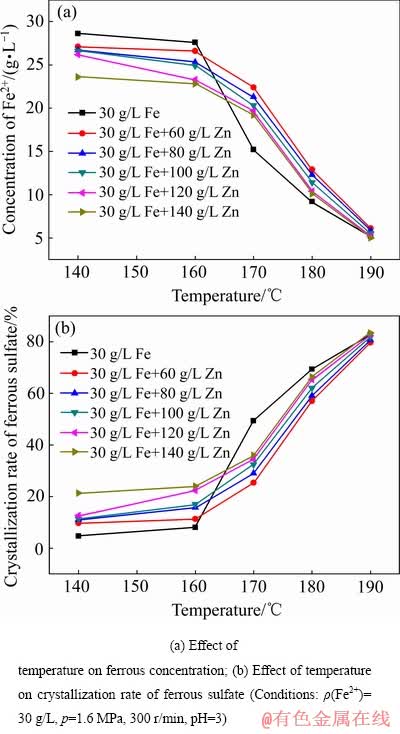
ͼ11 ��ͬ����пŨ�����¶ȶ����������ᾧ��Ӱ��
Fig. 11 Effect of temperature on crystallization of ferrous sulfate under different zinc sulphate concentration
���¶ȸ���160 ��ʱ����Һ�е������������������п�Ľᾧ�ʶ���Һ�е�����п���������������Ľᾧ�ʣ������µ�������������������п���Ӱ�����(��ͼ10(b)��ͼ11(b))�������¶ȵ����ߣ������������ܽ�ȼ��罵�ͣ���Һ�����������������ӣ���Һ�е���������������Ϊ���ˣ��ٽ�����п�Ľᾧ���������п�Ľᾧ�ʣ�ͬʱ����Һ�����ɵ�п����������ͬ��ȡ��FeSO4��xH2O�еIJ�����ԭ�ӣ����������п�Ľᾧ�ʶ����������������Ľᾧ�ʡ������¶ȵ����ӣ�����п�������������ܽ�Ƚ��ͣ�����п�����������Ĵ����ᾧ����Һ�������ƶ����������п����Ũ�Ƚ��ͣ�����ͬ������ü���������������п�����������ᾧ�������á����¶�Ϊ170 ��ʱ����ʼп����Ũ��Ϊ140 g/Lʱ������81.43 g/L����������ʱ(Fe2+Ũ��Ϊ30 g/L)������п�Ľᾧ�������25.7%(��10.3%������36%)�������¶�Ϊ190 ��ʱ������п�Ľᾧ�ʽ�������3.55%(��32.41%������35.96%)�����¶�Ϊ170 ��ʱ����ʼ��������Ũ��Ϊ30 g/Lʱ������247.7 g/L (Zn2+Ϊ100 g/L)����пʱ�����������Ľᾧ�ʽ�����17%(��49.33%������32.33%)�������¶�Ϊ190 ��ʱ�����������Ľᾧ�ʽ�����1%(��82.67%����81.67%)��
FeSO4-ZnSO4-H2SO4��ϵ�У���ʼ��������Ũ��Ϊ30 g/L���¶�Ϊ140~190 ��֮�䡢п����Ũ��Ϊ60~140 g/L�ķ�Χ�ڣ����������Ĵ������������п�Ľᾧ�ʣ����¶ȵ���160 ��ʱ������п�Ĵ�����������������Ľᾧ�ʣ����¶ȸ���170 ��ʱ������п�Ĵ��ڽ��������������Ľᾧ�ʡ�
2.3 FeSO4-MgSO4-H2SO4��ϵ�������εĽᾧ��Ϊ
������ϵ��FeSO4��MgSO4�������ö������νᾧ�ʵ�Ӱ�������ͼ12����ͼ12��֪�������¶ȵ����ߣ���������������þ�Ľᾧ�����ߣ����������Ĵ������������п�Ľᾧ�ʣ����¶ȵ���160 ��ʱ������þ�Ĵ�����������������Ľᾧ�ʣ����¶ȸ���170 ��ʱ������þ�Ĵ��ڽ��������������Ľᾧ�ʣ����¶ȵ���160 ��ʱ������þ��������������ʱ����Һ�������Ũ�����ӣ�����Һ��þ���Ӻ��������ӵ���Ũ�����ӣ�����ͬ����ЧӦ��þ���Ӻ��������ӽ���H+�Ļ��[11]��H+�Ļ�Ƚ��ͣ������ڷ�Ӧʽ(5)���ҽ��У���Һ�����������Ũ�����ӣ��ٽ���Ӧ(3)��(4)���ҽ��У��������������������þ�Ľᾧ�ʡ����¶ȸ���170 ��ʱ����Һ�д��ڴ����������������壬����������þ��ײ�ɺˣ��������þ�Ľᾧ�ʡ���Ӣ�̵�[19]�о��������¶�Ϊ180 ��ʱ������þ���ܽ��Ϊ250 g/kg(��Һ��þ���ӵ�Ũ��Ϊ50 g/kg)������þ���ܽ�ȸ��������������ܽ�ȡ���Һ�е������ƶ���þ����������ͬ��[24]ȡ��FeSO4��xH2O�еIJ�����ԭ�ӣ��������������Ľᾧ�ʽ��Ͷ�����þ�Ľᾧ�����(��ͼ12�е�����b��c)�������¶ȵ����ߣ���������������þ�ܽ�Ƚ��ͣ���Һ���������þ���ӵ�Ũ�Ƚ��͡�ͬ����ЧӦ������ͬ������ü�������������������þ�ᾧ�������ý��͡�
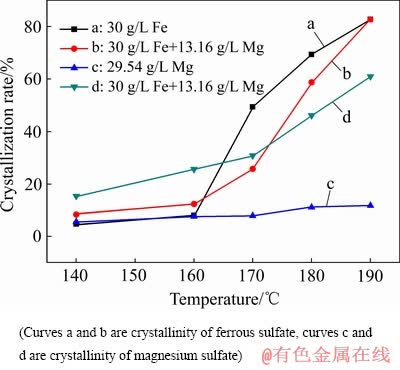
ͼ12 ������ϵ��FeSO4��MgSO4�������ö������νᾧ�ʵ�Ӱ��
Fig. 12 Effect of interaction between FeSO4 and MgSO4 on sulfate crystallization rate under high temperature system
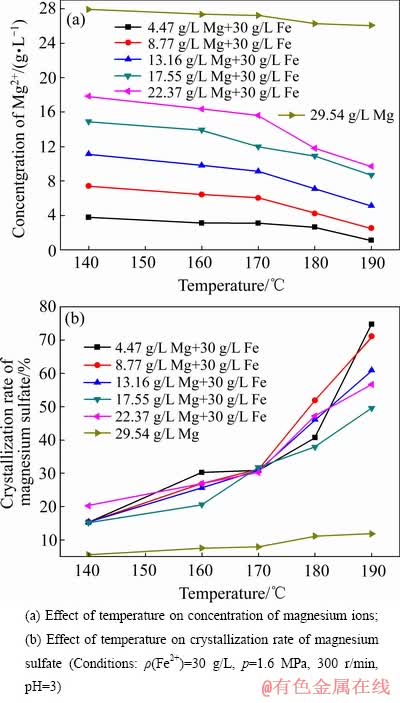
ͼ13 ��ͬ����þŨ�����¶ȶ�����þ�ᾧ��Ӱ��
Fig. 13 Effect of temperature on crystallization of magnesium sulfate under different concentrations of magnesium sulfate
ͼ14 ��ͬ����þŨ�����¶ȶ����������ᾧ��Ӱ��
Fig. 14 Effect of temperature on crystallization of ferrous sulfate at different concentrations of magnesium sulfate
��ͬþ����Ũ�����¶ȶ�����þ�����������ᾧ��Ӱ����ͼ13��14��ʾ����ͼ13(a)��(b)��ͼ14(a)�� (b)��֪������Һ��Zn2+Ũ��Ϊ29.54 g/L���¶���170 ��������190 ��ʱ������þ�Ľᾧ����7.85%������11.78%����Ӣ�̵�[19]�о��������¶�Ϊ180 ��ʱ������þ���ܽ��Ϊ250 g/kg(��Һ��þ���ӵ�Ũ��Ϊ50 g/kg)������140~190 ���¶����䣬����þ��Һ���ڵڶ����ȶ������ȶ�����������þ��Һ�ļ������ͶȽ�С������þ�Ľᾧ�ƶ���С���ᾧ����ʱ��̣���Һ�ܿ�ﵽ�ᾧ-�ܽ�ƽ��[22]����ͼ13��14��֪�����������Ĵ������������þ�Ľᾧ�ʣ�������160 ��ʱ������þ�Ĵ�����������������Ľᾧ�ʣ�������170 ��ʱ������þ�Ĵ��ڽ��������������Ľᾧ�ʡ���������þŨ�ȵ����ӣ���Һ���������Ũ�����ӣ�ͬʱ����Һ���������Ӻ�þ���ӵ���Ũ�����ӣ��������Ӻ�þ���ӵ�ͬ����ЧӦ������H+�Ļ��[11]��H+�Ļ�Ƚ��ͣ������ڷ�Ӧʽ(5)���ҽ��У���Һ�����������Ũ�����ӣ��ٽ���Ӧ(3)��(4)���ҽ��У��������������������þ�Ľᾧ�ʡ����¶ȸ���170 ��ʱ�������������ܽ�ȼ��罵�ͣ���Һ�д����������������������������þ��ײ�ɺˣ��������þ�Ľᾧ�ʡ�ͬʱ����Һ�������ƶ���þ����������ͬ�������ȡ���������������в�����ԭ�ӣ����������þ�Ľᾧ�ʶ����������������Ľᾧ�ʡ������¶ȵ���������þ�������������ܽ�Ƚ��ͣ�����þ�����������Ĵ����ᾧ����Һ�������ƶ���þ���ӡ��������Ӻ��������Ũ�Ƚ��ͣ�����ͬ������ü�������������������þ�ᾧ����Ӱ�������
FeSO4-MgSO4-H2SO4��ϵ�У���ʼ��������Ũ��Ϊ30 g/L���¶�Ϊ140~190 ��֮�䡢þ����Ũ��Ϊ4.47~22.37 g/L�ķ�Χ�ڣ����������Ĵ������������þ�Ľᾧ�ʡ����¶ȵ���160 ��ʱ������þ�Ĵ�����������������Ľᾧ�ʣ����¶ȸ���170 ��ʱ������þ�Ĵ��ڽ��������������Ľᾧ�ʡ�
2.4 FeSO4-ZnSO4-MgSO4-H2SO4��ϵ�������εĽᾧ��Ϊ
������ϵ��FeSO4��ZnSO4��MgSO4�������ö������νᾧ�ʵ�Ӱ������ͼ15��ʾ���Ա�ͼ15�е�����a��b��c��d��֪����140~190 ��֮�䣬��FeSO4-ZnSO4-H2SO4��ϵתΪFeSO4-ZnSO4- MgSO4-H2SO4ʱ����������������п�Ľᾧ�ʽ��͡���Һ������þ��Ũ�����ӣ���Һ��þ���ӵ�Ũ�����ӣ���þ���Ӹ���ȡ���������������е���ԭ�ӣ�������������������þ�Ľᾧ�ʽ��ͣ��Ա�ͼ15�е�����b��c��f��g��֪����140~170 ��֮��ʱ����FeSO4-ZnSO4- H2SO4��ϵתΪFeSO4-ZnSO4-MgSO4-H2SO4ʱ����������������þ�Ľᾧ����ߣ���170~190 ��֮��ʱ����������������þ�Ľᾧ�ʽ��ͣ����¶ȵ���170 ��ʱ����������п����Һ���������Ũ�����ӣ���Һ���������Ũ�����Ӵٽ���Ӧ(3)��(4)���ҽ��У��������������������þ�Ľᾧ�ʣ����¶ȸ���170 �棬��������п����Һ��п���ӵ�Ũ�����ӣ�п����������ͬ������ã�ȡ�����������������в�������ԭ�Ӷ�������þ���ӵ�����ͬ���ã�������������������þ�Ľᾧ�ʽ��͡�
��ͬп���Ӻ�þ����Ũ�����¶ȶ�����п������þ�����������ᾧ��Ӱ������ͼ16��ʾ��
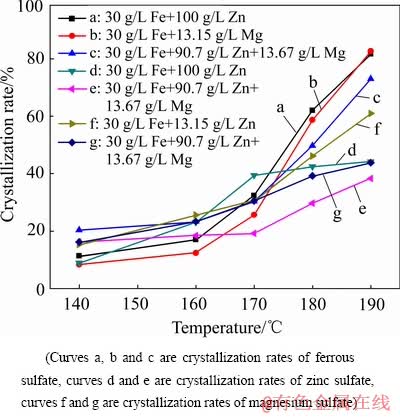
ͼ15 ������ϵ��FeSO4��ZnSO4��MgSO4�������ö������νᾧ�ʵ�Ӱ��
Fig. 15 Effect of interaction between FeSO4, ZnSO4 and MgSO4 on sulfate crystallization rate under high temperature system
��ͼ16(a)��(a��)��֪�������¶ȡ���������þ�������������ٽ�����п�ᾧ�������¶ȵ����ߣ�����п���ܽ�Ƚ��ͣ�����п�Ľᾧ����ߡ���������þ������������ͬʱҲ�����˴��������������Һ���������Ũ�����ӡ�����ͬ����ЧӦ��þ���Ӻ������ӵļ��뽵����H+�Ļ�ȣ������ڷ�Ӧ(5)���ҽ��У�������Һ�������Ũ�ȵ����ӣ�����������Ӵٽ���Ӧ(2)���ҽ��У����������п�Ľᾧ�ʡ����¶ȸ���170 ��ʱ�����������Ĵ����ᾧ����Һ�е�����������������������п��ײ�ɺˣ��������п�Ľᾧ�ʣ�ͬʱ��Һ�������ƶ���п����������ͬ�������ȡ�����������ᾧ�в��������Ӷ���������п�Ľᾧ����ߡ����¶�Ϊ190 ��ʱ���������Ũ��2.14 mol/L(140 g/L Zn)������2.56 mol/L(122.5 g/L Zn+3.63 g/L Mg+ 30 g/L Fe)ʱ������п�Ľᾧ����32.41%������45.19%��
��ͼ16(b)��(b��)��֪�������¶ȡ�����п�����������ļ�������������þ�Ľᾧ�������¶ȵ���������þ���ܽ�Ƚ��ͣ����������þ�Ľᾧ�ʡ���������п������������ͬʱҲ�����˴��������������Һ���������Ũ�����ӡ�����ͬ����ЧӦ��п���Ӻ������ӵļ��뽵����H+�Ļ�ȣ������ڷ�Ӧ(5)���ҽ��У�������Һ�������Ũ�����ӣ��������Ũ�����Ӵٽ���Ӧ(4)���ҽ��У�����þ�Ľᾧ�����ӡ����¶�Ϊ190 ��ʱ�����������Ľᾧ�ʸ���70%����Һ�д����������������壬��Һ������������������������þ��ײ�ɺˣ��������þ�Ľᾧ�ʣ�����Һ������þ����������ͬ�������ȡ���������������в��������Ӷ���������þ�Ľᾧ����ߡ����¶�Ϊ190 ��ʱ���������Ũ��1.234 mol/L(30 g/L Mg)������2.56 mol/L (122.5 g/L Zn+3.63 g/L Mg+30 g/L Fe)ʱ������þ�Ľᾧ����11.78%������44.35%��
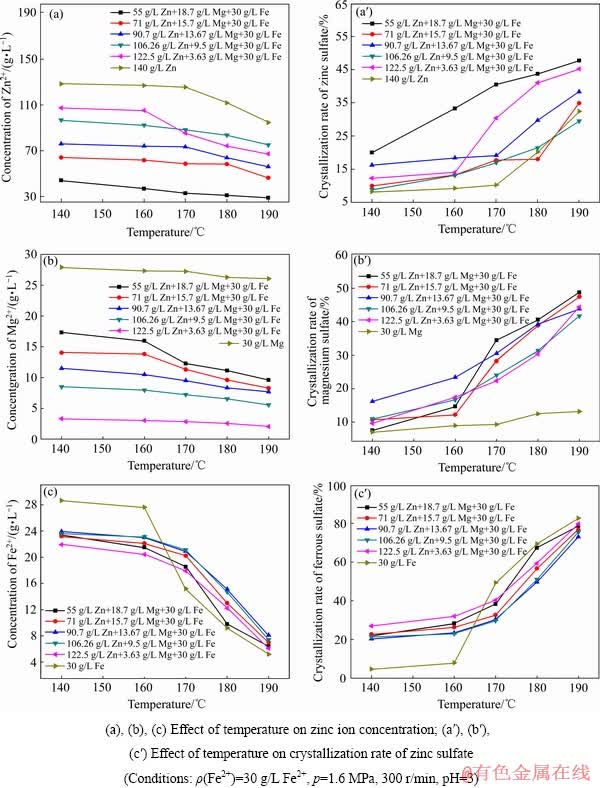
ͼ16 ��ͬ����п������þŨ�����¶ȶ�����п������þ�����������ᾧ��Ӱ��
Fig. 16 Effect of temperature on crystallization of zinc sulfate((a), (a��)), magnesium sulfate((b), (b��)) and ferrous sulfate((c), (c��)) at different concentrations of zinc sulfate and magnesium sulfate
��ͼ16(c)��(c��)��֪�����¶�С�ڻ����160 ��ʱ����������п������þ��������������Ľᾧ�ʡ����¶�С��160 ��ʱ����������������п������þ���ܽ�Ƚϴ��������������ܽ�����������п������þʹ��Һ�е������Ũ�����ӣ�����ͬ����ЧӦ��п���Ӻ�þ���ӵļ��뽵����H+�Ļ�ȣ������ڷ�Ӧ(5)���ҽ��У���Һ����������ӣ��ٽ���Ӧ(3)���ҽ��У���������������Ľᾧ�ʣ���Ӧ�¶�Ϊ170~190 ��ʱ����������п������þ���������������Ľᾧ�ʡ������¶ȵ���������п������þ�����������ᾧ��Ӱ����������¶ȸ���170 ��ʱ�����������Ĵ����ᾧ��������п������þ���ܽ�ȸ��������������ܽ�ȣ���Һ�������ƶ���п���Ӻ�þ����������ͬ��ȡ���������������еIJ����������ӣ��������������Ľᾧ�ʽ��ͣ������¶ȵ���������п������þ���ܽ�Ƚ��ͺ���������������Ϊ���ˣ��ٽ�����п������þ�ᾧ����Һ�������ƶ���п���Ӻ�þ���Ӽ��٣�����ͬ������ü���������п������þ�����������ᾧ��Ӱ����������¶�Ϊ170 ��ʱ������122.5 g/L��п���Ӻ�3.63 g/L��þ����ʱ�����������Ľᾧ����49.33%����40.33%�����¶�Ϊ190 ��ʱ�����������Ľᾧ����82.67%����79.67%��
FeSO4-ZnSO4-MgSO4-H2SO4��ϵ�У���ʼ��������Ũ��Ϊ30 g/L���¶�Ϊ140~190 ��֮�䣬����Һ����Ԫ��ϵFeSO4-ZnSO4-H2SO4��FeSO4-MgSO4-H2SO4תΪFeSO4-ZnSO4-MgSO4-H2SO4��ϵʱ�����������п������þ�ĵĽᾧ�ʣ����¶ȵ���160 ��ʱ����������������ĵĽᾧ�ʣ����¶ȸ���170 ��ʱ�����������������ĵĽᾧ�ʡ�
3 ����
1) FeSO4-H2SO4��ϵ�У���ʼ��������Ũ��Ϊ30 g/L���¶�Ϊ150 ��ʱ����Һ���ڵ�һ���ȶ�������160~170 ��ʱ����������Һ���ڵڶ����ȶ�������180~190 ��ʱ����Һ���ڲ��ȶ������ı��ʼ����������Ũ�����������ܽ�ȵļ��罵������(160~180 ��)���ֲ��䡣
2) FeSO4-ZnSO4-H2SO4��ϵ�У���ʼ��������Ũ��Ϊ30 g/L���¶�Ϊ140~190 ��֮�䡢п����Ũ��Ϊ60~140 g/L�ķ�Χ�ڣ����������Ĵ������������п�Ľᾧ�ʣ����¶ȵ���160 ��ʱ������п�Ĵ�����������������Ľᾧ�ʣ����¶ȸ���170 ��ʱ������п�Ĵ��ڽ��������������Ľᾧ�ʡ�
3) FeSO4-MgSO4-H2SO4��ϵ�У���ʼ��������Ũ��Ϊ30 g/L���¶�Ϊ140~190 �桢þ����Ũ��Ϊ4.47~22.37 g/L�ķ�Χ�ڣ����������Ĵ������������þ�Ľᾧ�ʣ����¶ȵ���160 ��ʱ������þ�Ĵ�����������������Ľᾧ�ʣ����¶ȸ���170 ��ʱ������þ�Ĵ��ڽ��������������Ľᾧ�ʡ�
4) FeSO4-ZnSO4-MgSO4-H2SO4��ϵ�У���ʼ��������Ũ��Ϊ30 g/L���¶�Ϊ140~190 ��֮�䣬��Һ����Ԫ��ϵFeSO4-ZnSO4-H2SO4��FeSO4-MgSO4-H2SO4תΪFeSO4-ZnSO4-MgSO4-H2SO4��Ԫ��ϵʱ�����������п������þ�ĵĽᾧ�ʣ����¶ȵ���160 ��ʱ����������������ĵĽᾧ�ʣ����¶ȸ���170 ��ʱ�����������������ĵĽᾧ�ʡ�
5) ���ó�������������Һ(30 g/L)ʱ����ֹ���������������ᾧ�����������������ʵ�����������������巵�ܻ�����������������������ķ����������������¶�Ϊ170~180 �桢п����Ũ��Ϊ80~100 g/L��þ����Ũ��С��15.7 g/LΪ�ˡ�
REFERENCES
[1] PARKER R H. An introduction to chemical metallurgy [M].Oxford: Pergamon Press Ltd, 1978: 263-318.
[2] �� ��, �� ��, ����־, �ƿ���, ������, ��͢��. ��ѹ���������ϵ��������������[J]. �й���ɫ����ѧ��, 2017, 27(3): 655-665.
TIAN Lei, LIU Yan, L�� Guo-zhi, TANG Jun-jie, ZHAO Qiu-yue, ZHANG Ting-an. Gas holdup in pressure agitation leaching system[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(3): 655-665.
[3] ������, �����, κ ��, ��־��, ���˱�, �� ��, ��˸��. ʪ����п�����г��������ɼ��������ת��[J]. �й���ɫ����ѧ��, 2017, 27(10): 2145-2153.
WANG Yi-zhao, LI Cun-xiong, WEI Chang, DENG Zhi-gan, LI Xing-bin, FAN Gang, YI Shuo-wen. Production of hematite and conversion of adsorption S in zinc hydrometallurgy process[J]. The Chinese Journal of Nonferrous Metals, 2017, 27(10): 2145-2153.
[4] ������, �����, ������. ��ɫ���������Դ�Ŀ������ӹ�����[M]. ����: ����ʡ�Ƽ�������, 2000: 247-252.
WANG Ji-kun, FENG Gui-lin, XU Xiao-jun. Development and processing technology of nonferrous metal mineral resources[M]. Kunming: Yunnan science and Technology Press, 2000: 247-252.
[5] ZHANG Fan, WEI Chang, DENG Zhi-gan, LI Xing-bin, LI Cun-xiong. Reductive leaching of indium-bearing zinc residue in sulfuric acid using sphalerite concentrate as reductant[J]. Hydrometallurgy, 2016, 161: 102-106.
[6] ������, �� ��, ��־��, κ ��, �챱ƽ, ţ ��. п������Ũ�ȶԳ���������Ӱ��[J]. ��ɫ��������, 2017, 7(6): 54-57.
HU Zhi-run, LUO Jia, DENG Zhi-gan, WEI Chang, ZHU Bei-ping, NIU Hui. Effects of zinc and iron concentration on iron-removing by hematite precipitation[J]. Nonferrous Metals Engineering, 2017, 7(6): 54-57.
[7] �� ��, ��־��, κ ��, �����, ���˱�. ���ó�����ȥ��������п�����Һ�е���[J]. �й���ɫ����ѧ��, 2014, 24(9): 2387-2392.
YANG Fan, DENG Zhi-gan, WEI Chang, LI Cun-xiong, LI Xing-bin. Iron-removal by hematite from leaching liquor of high iron sphalerite[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(9): 2387-2392.
[8] Ԭ����, �����, ��ٻٻ. ʪ����п�������յ���״��չ��[J]. ����ۺ�����, 2011(2): 30-32.
YUAN Fang-qin, WU Ke-ming, DING Qian-qian, KE Xing. Status and prospect of technology for iron removal in zinc hydrometallurgy[J]. Multipurpose Utilization of Mineral Resources, 2011(2): 30-32.
[9] �¼���, ������, ��־��. ʪ��ұ�������ķ�����Ӧ��[M]. ����: ұ��ҵ������, 1991: 93-103.
CHEN Jia-yong, YU Shu-qiu, WU Zhi-chun. Separation and application of iron in hydrometallurgy[M]. Beijing: Metallurgical Industry Press, 1991: 93-103.
[10] ������. Ǧпұ��ѧ[M]. ����: ��ѧ������, 2003: 328-349.
PENG Qiu-rong. Metallurgy of lead and zinc[M]. Beijing: Science Press, 2003: 328-349.
[11] �� ��, ��־��, κ ��, ���˱�, ��ΰ��, ������. ������п�����������п���Ӻ�þ���ӵ�Ӱ�켰���ڻ���[J]. �й���ɫ����ѧ��, 2014, 24(11): 2906-2913.
YANG Fan, DENG Zhi-gan, WEI Chang, LI Cun-xiong, QIU Wei-jia, ZHU Ru-long. Effect and existence mechanism of zinc ion and magnesium ion in iron removal from high iron sphalerite by hematite process[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(11): 2906-2913.
[12] �� ��, ������, �� ��, �۽���, ����ɽ, �����E, ½ҵ��. п����Һ������ֱ��ˮ�����������̽��[J].�й���ɫұ��, 2012, 41(4): 80-85.
YUE Ming, SUN Ning-lei, ZOU Xing, SHAO Jian-chun, LIU Jin-shan, WANG Kui-ting, LU Ye-da. The discussion on hydrolysis precipitation of ferric oxide directly from ferric-ion rich zinc leachate[J]. China Nonferrous Metallurgy, 2012, 41(4): 80-85.
[13] Von ROPENACK A. Hematite-the solution to a disposal problem-an example from the zinc industry[J]. Iron Control in Hydrometallurgy, 1986, 11(12): 730-741.
[14] �ų���, �� ��. �������������ʪ����п�����е�Ӧ��[J]. ������ɫ����, 2014, 30(2): 39-41.
ZHANG Cheng-song, ZHAO Ting. Application of the hematite process for removing iron in the zinc hydrometallurgical production[J]. Hunan Nonferrous Metals, 2014, 30(2): 39-41.
[15] HASEGAWA F, TOZAWA K, NISHIMURA T. Solubility of ferrous sulfate in aqueous solutions at high temperatures[J]. Journal of the Mining and Materials Processing Institute of Japan, 1996, 112(12): 879-884. (in Japanese)
[16] ������. �ؽ���ʪ��ұ����̸�þ�ᾧ�Ļ�����ػ�ѧ�о�[D]. ��ɳ: ���ϴ�ѧ, 2010: 1-3.
WANG Wen-lei. Removing calcium and magnesium form heavy metal hydrometallurgical process based on phase chemistry[D]. Changsha: Hunan University, 2010: 1-3.
[17] E. B����ķ˹��. ��ѧ��ҵ�еĽᾧ[M]. ����, Ҷ����, ��. ����: ��ѧ��ҵ������, 1984: 3-97.
HAMSKY E B. Crystallization in chemical industry[M]. GU Tao, YE Tie-lin, transl. Beijing: Chemical Industry Press, 1984: 3-97.
[18] BRUHN B, GERLACH J, PAWLEK F. Solubilities of salts and gasses in water[J]. Journal of Inorganic and General Chemistry, 1965, 337: 68-79. (in German)
[19] ��Ӣ��, �����. ��������ѧ�����ֲ�[M]. ����: ������ѧ������, 1993: 573-574.
LIANG Ying-jiao, CHE Yin-chang. Handbook for thermodynamic data of inorganic substances[M]. Shenyang: Northeastern University Press, 1993: 573-574.
[20] �ܸ���. ��ˮ����п�ᾧ�����о�[D]. ���: ����ѧ, 2017: 7-18.
ZHOU Fu-li. Study on the crystallization process of zinc sulfate heptahydrate[D]. Tianjin: Tianjin University, 2017: 7-18.
[21] M.E.����. ���ι���ѧ[M]. ����: ��ѧ��ҵ������, 1982: 153-155.
������������������ M E. Inorganic salt processing technology[M]. Beijing: Chemical Industry Press, 1982: 153-155.
[22] �����, �����, �� ��, ���ȹ�, ������. ��Ԫ��ϵ MgSO4-FeSO4-H2O ����ƽ���о�[J]. ��ѧ����, 2017, 45(1): 36-39.
ZHANG Yu-jie, ZHU Jia-wen, CHEN Kui, FAN Xian-guo, ZHOU Xiao-kui. Metastable phase equilibrium in the aqueous ternary system MgSO4-FeSO4-H2O[J]. Chemical Engineering, 2017, 45(1): 36-39.
[23] �� ��, ������. ֲ�ﲹ���� ���� ��������þ�����ε�̽��[J]. ɽ������, 2002, 22(4): 10-12.
SUN Hong, JING Yong-feng. Plants iron supplies��Mixture of iron and magnesium protosulfate[J]. Shanxi Chemical Industry, 2002, 22(4): 10-12.
[24] ������. ����þ��Һ���½ᾧ���ɵ��о�[D]. ����: ������ѧ, 1999: 11-16.
ZHANG Li-qing. Study on high temperature crystallization of magnesium sulfate solution[D]. Shenyang: Northeastern University, 1999: 11-16.
[25] �� ��. ����ѧ����[M]. ����: ������ѧ������, 2004: 97-100.
QIN Shan. Basis fundamentals of crystallography[M]. Beijing: Peking University Press, 2004��97-100.
LIU Hui-yang, DENG Zhi-gan, WEI Chang, LI Xing-bin, LI Min-ting, WANG Chang-yin, ZENG Tao
(Faculty of Metallurgical and Energy Engineering, Kunming University of Science and Technology, Kunming 650093, China)
Abstract: The effects of different sulfate concentrations on the crystallization of ferrous sulfate, zinc sulfate and magnesium sulfate were investigated through investigating the crystallization behavior of zinc, iron and magnesium in FeSO4-ZnSO4-MgSO4-H2SO4 system. The results show that the solubility of ferrous sulfate, zinc sulfate and magnesium sulfate decreases with the increase of temperature. When the concentration of ferrous ions in the initial solution is changed, the sharp decrease interval of ferrous sulfate (160-180 ��) remains unchanged. The presence of zinc sulfate and ferrous sulfate increases the crystallization rate of magnesium sulfate, the presence of magnesium sulfate and ferrous sulfate increases the crystallization rate of zinc sulfate. When the temperature is lower than 160 ��, the presence of zinc sulfate and magnesium sulfate increases the crystallization rate of ferrous sulfate, when the temperature is higher than 170 ��, it decreases the crystallization rate of ferrous sulfate.
Key words: ferrous sulfate; zinc sulphate; magnesium sulfate; solubility; crystallization; temperature
Foundation item: Project(2018YFC1900402) supported by the National Key Research and Development Plan of China; Projects(51804146, 51964029, 51564030, 51664030, 51664029) supported by the National Natural Science Foundation of China
Received date: 2019-07-26; Accepted date: 2020-04-28
Corresponding author: DENG Zhi-gan; Tel: +86-15925127947; E-mail: dengzhigan83@163.com
(�༭ ����)
������Ŀ�������ص��з��ƻ�������Ŀ(2018YFC1900402)��������Ȼ��ѧ����������Ŀ(51804146��51964029��51564030��51664030��51664029)
�ո����ڣ�2019-07-26�������ڣ�2020-04-28
ͨ�����ߣ���־�ң���ʦ����ʿ���绰��15925127947��E-mail��dengzhigan83@163.com

